磁共振成像诊断肛瘘误诊或漏诊分析
刘卫英, 邵志红, 刘 梦, 王 帅
(1. 上海市静安区市北医院放射科,上海 200435; 2. 同济大学附属第十人民医院放射科,上海 200072)
肛瘘是指沟通肛管或直肠与肛周皮肤之间的异常通道,是临床常见疾病之一,尤其是男性患者。术后复发率高是肛瘘治疗主要的问题[1-2],尤其是复杂性肛瘘,其原因可能在于对肛周括约肌累及的程度、肛瘘内口或细小分支瘘管的认识不足等。MRI是诊断肛瘘的主要影像学检查方法。有关MRI在肛瘘诊断中的应用文献报道较多,但针对其误诊或漏诊病例的分析报告相对少见。本研究通过收集68例肛瘘患者的临床及术前影像资料,对比手术记录,分析MRI假阳性或假阴性病例,以提高MRI对肛瘘诊断的准确性。
1 资料与方法
1.1 一般资料
回顾性收集2018年6月1日至2019年6月30日在上海市静安区市北医院接受肛瘘手术治疗患者的临床及术前MRI资料。入选标准: MRI检查在术前1周内完成;MRI扫描序列完整,图像质量符合评判要求;手术明确为肛瘘,且术中记录完整。依据入选标准,共计68例肛瘘患者纳入研究,其中男性59例,女性9例,年龄18~65岁。临床症状主要表现为肛周肿痛、肛门附近瘘口或伴有脓性分泌物,9例曾有过肛瘘或肛周脓肿手术史。
1.2 MRI扫描方法及序列
所有患者均采用Philips Multiva 1.5T磁共振扫描。采用体部相控阵线圈,检查前患者无须肠道准备,未放置肠道标记物。扫描序列见表1。扫描快速,定位像后,先扫描正中线矢状位T2加权成像(T2WI),从而判断肛管结构相对位置,随后以肛管为轴定位,扫描垂直于肛管的斜轴位T1加权成像(T1WI)及T2抑脂像(T2WI_SPAIR),扫描平行于肛管的斜冠位T2WI及T2WI_SPAIR。68例患者中,29例扫描了斜轴位弥散加权成像(DWI),采用单次激发SE-EPI序列,扩散敏感梯度b值为0和600s/mm2;17例扫描了斜轴位增强后T1抑脂像,采用增强后快速T1高分辨力各向同性容积激发(CE THRIVE_FS)序列,对比剂选用Gd-DTPA,注射速率为2mL/s。
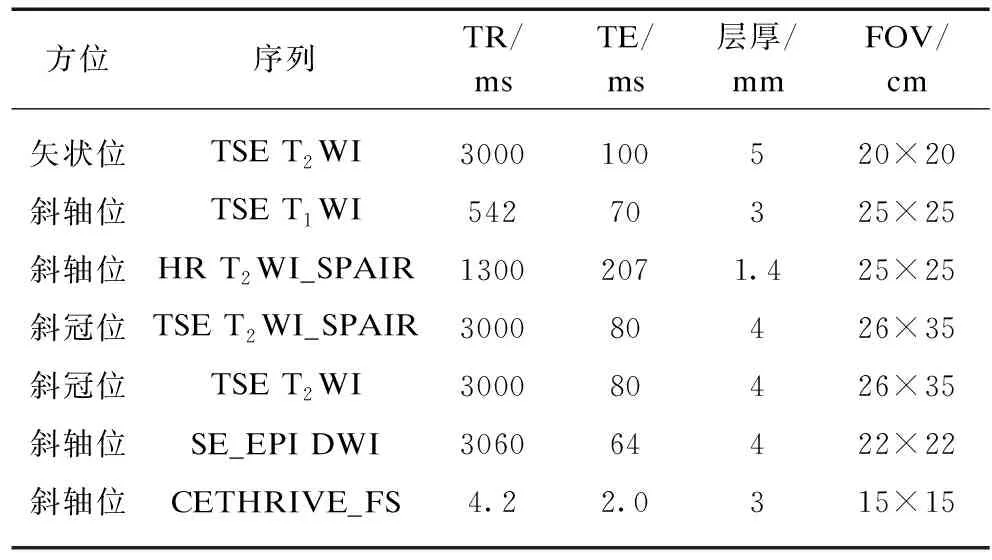
表1 磁共振各扫描序列及参数Tab.1 MRI scan sequence and parameters
1.3 MRI观察指标
MRI图像由2名经过培训的影像医师采用双盲法分析,如有分歧则协商解决。MRI观察指标主要包括: 肛瘘主瘘管的走形,并依据Parks分型分为浅表型、括约肌间型、穿括约肌型、括约肌上型以及括约肌外型;判断内口的位置,内口定位采用截石位钟表定位法;判断有无支管形成、支管的走形,有无伴发脓肿,脓肿的形态、大小、边缘以及邻近内外括约肌的信号特征。
术中记录指标主要包括相对应的主瘘管及其Parks分型,瘘管内口的位置、是否存在支管形成或伴发脓肿。
将MRI表现与术中结果对照,计算MRI诊断肛瘘的准确性,分析假阳性或假阴性病例。
2 结 果
2.1 术中记录
68例肛瘘患者中,依据主瘘管及其Parks分型,其中浅表瘘有9例,括约肌间瘘37例,穿括约肌瘘14例,括约肌上瘘5例,括约肌外瘘3例。手术共发现主瘘管68个,内口74个,合并脓肿27例,发现支管27个。
2.2 术前MRI表现
与手术结果对照,68例患者中,MRI对主瘘管及其Parks分型检出率为94.1%(64/68);瘘管内口检出率为70.9%(56/74),其中5例假阳性,18例假阴性;脓肿检出率为100%(27/27),支管检出率为70.0%(21/27),3例假阳性,6例假阴性,见表2。
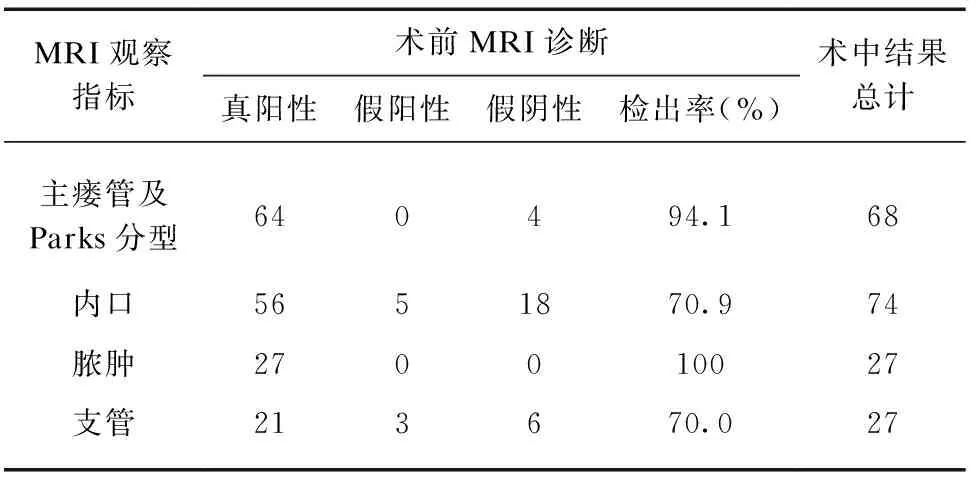
表2 肛瘘术前MRI指标与手术结果对照Tab.2 Comparison of MRI findings and surgical results
MRI对于肛瘘的主瘘管及Parks分型具有较高的诊断准确性。MRI主瘘管表现为连接肛管直肠与肛周皮肤的条形异常信号,T1WI呈等低信号,与周围组织分界不清,T2WI、T2WI_SPAIR、DWI呈稍高信号(图1A、1B;图2A、2B),走形多扭曲不规则,有时管壁呈条形低信号;内口表现为肛管内括约肌内或直肠壁内与主瘘管相连的点状、条状异常信号,T2WI_SPAIR呈稍高信号(图1C);支管表现为瘘管分支,发自主瘘管向周围延伸出现盲端或达皮肤表面的条状、管状、线状异常信号,T2WI_SPAIR、DWI呈稍高信号图(图1A、1B);合并脓肿表现为类圆形或片状不规则异常信号,T1WI呈低信号,T2WI_SPAIR呈高信号,DWI呈高信号,周围组织常伴有炎性改变,T2WI_SPAIR呈稍高信号。
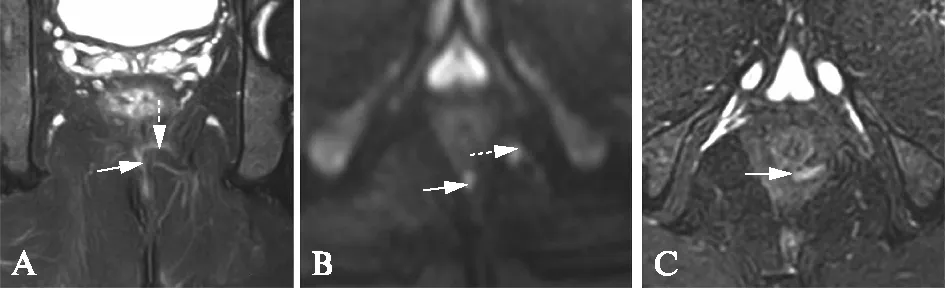
图1 括约肌上型肛瘘Fig.1 A suprasphincteric fistulaA: 主瘘管及分支瘘管,T2WI_SPAIR呈高信号,边缘模糊,主瘘管走形于括约肌与提肛肌之间;B: 主瘘管及分支瘘管,弥散加权成像(DWI)呈高信号;C: 内口,主瘘管与内括约肌相连处,T2WI_SPAIR稍高信号
主瘘管4例假阴性,对照手术结果显示,其中3例瘘管中液体含量少,常规T2WI_SPAIR无法清楚、明确地显示,1例病灶处于慢性静止期,缺乏典型的瘘管T2WI高信号特征。
内口的检出率为70.9%,对照手术结果显示,5例假阳性中,3例由于黏膜呈皱缩状态,皱缩的黏膜在T2WI_SPAIR也呈高信号,从而将其误认为内口;2例由于肛管周围血管T2WI_SPAIR也呈条状或点状高信号,与肛瘘内口信号类似而被误认为肛瘘内口。18例假阴性中,13例患者由于内外括约肌炎性水肿,内外括约肌在T2WI及T2WI_SPAIR上呈稍高信号、等信号,与内口的高信号无法辨别,见图2。5例患者由于内口闭塞而呈假阴性。
支管的检出率为70.0%,对照手术结果发现,主要原因在于细小分支(图2B、2C),另外扫描层厚较厚,支管一般多扭曲走形、延伸,难以单纯在一个方位显示,同时部分细小的血管被误认为支管。
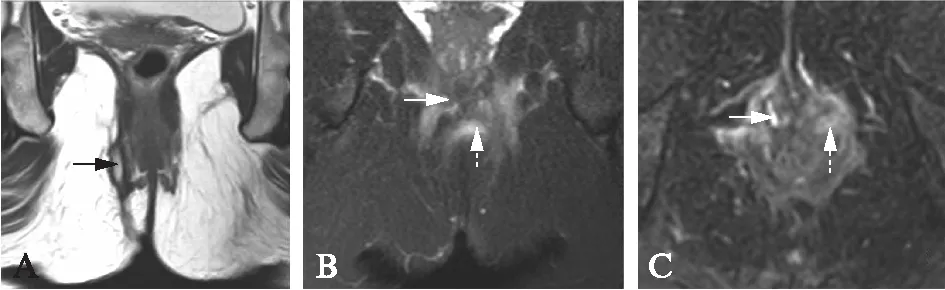
图2 穿括约肌型肛瘘Fig.2 A trans-sphincteric fistulaA: 主瘘管位于外括约肌外侧缘,T2WI呈高信号;B: 主瘘管向右下方走形,上缘可见细小分支瘘管形成,T2WI_SPAIR呈高信号,边缘模糊,周围软组织肿胀;C: 主瘘管内口周围括约肌肿胀,T2WI_SPAIR呈稍高信号,与内口无法区分
3 讨 论
肛瘘是临床上常见疾病之一。肛瘘临床诊断容易,但是术后复发率高,是肛肠外科面临的棘手问题,尤其是复杂性肛瘘。影像学检查的主要目的是在术前准确查找内口的位置,显示肛瘘的内口及与肛门括约肌的关系;发现支管及判断肛周肌肉的受累范围,显示瘘管的走形及其分支,帮助肛肠外科医生准确定位,以便为肛肠外科医师术式的选择提供参考[3-4]。
MRI具有良好的软组织分辨率及空间分辨率,可以多参数、多方位成像,是诊断肛瘘的主要影像学检查方法[5-7]。在临床实际工作中,复杂性瘘管涉及周围组织较多且内口位置较深、分支较多,漏诊及误诊时有发生,假阳性有可能误导手术,对患者肛肠生理功能造成过度伤害,假阴性会遗漏病灶导致肛瘘复发。
对于肛瘘误诊及漏诊的原因,首先是完善的检查序列。T2WI矢状位用于扫描准确定位,帮助诊断医师判断瘘管的位置;很多文献[8]报道证实了T2抑脂序列在肛瘘诊断中的重要性,斜冠位及斜轴位的T2抑脂序列有利于检出活动性瘘管及内口、外口、支管。斜冠位T2WI及斜轴位T1WI主要用于肛瘘的准确分型。DWI有利于分支瘘管显示,增强T1抑脂序列有利于内口的诊断。缺乏完善的MRI检查序列有可能导致误诊或漏诊。
由于肛瘘的准确诊断需要明确主瘘管的准确位置、内口数及其位置、瘘管与内外括约肌的关系、肛提肌的完整性,是否伴发脓肿等,所以要求影像科医师具备一定的盆底解剖知识。而多数影像医师对于盆底结构不重视,并且盆底的某些细节结构尚存在一定争议,导致肛瘘的准确描述与影像诊断有一定难度。这也是导致肛瘘误诊及漏诊的一大原因。
部分学者提出MRI增强扫描对检出瘘管及支管、内口的重要性。杨烁慧等[9]比较增强T1WI_SPAIR与平扫MRI对肛瘘的诊断性能,显示增强T1WI_SPAIR发现瘘管、内口、分支和脓腔的准确率高于T1WI及T2WI_SPAIR序列。增强T1WI_SPAIR除了能显示含脓液较多的瘘管及分支外,同时由于炎性组织的强化[10],也有利于显示细小的或处于非活动期含脓液较少的瘘管和分支,进一步弥补了T2WI_SPAIR等主要依赖于脓液成像的不足。张莲等[11]比较T2WI脂肪抑制(FS)序列、质子加权预饱和脂肪抑制(PDW PFS)序列与增强T1WI FS序列对肛瘘瘘管诊断价值的差异,结果显示,3种扫描序列对主瘘管(包括脓肿)的诊断正确率分别为96.7%、97.8%、97.8%,差异无统计学意义(P>0.05)。对瘘管分支、多发细小瘘管诊断正确率3种序列均为95.7%,差异也无统计学意义(P>0.05)。Baik等[12]认为虽然T1WI FS增强能更直观地显示瘘管,但在诊断的准确性上与T2WI FS无明显差异。本研究认为这可能与肛周疾病活动性有关。临床上以肛周疾病活动性指数判断疾病活动度,Present等[13]提出以5分为阈值将患者进行分组,评分≤5的归入缓解期组,>5则纳入活动期组。因此,建议对于临床上判定缓解期组的患者若无MRI造影剂禁忌者,应将MRI增强扫描作为肛瘘的常规检查序列。本研究仅部分患者采用了增强扫描序列,也可能是导致内口与支管误诊或漏诊的原因。
现在多数学者强调薄层扫描对于肛瘘诊断的重要性[14-15],薄层T2抑脂像可以沿着瘘管连续查找内口,同时可进行多平面重建后处理,提高了对瘘管诊断的准确性。张芳等[14]利用薄层扫描的三维超长回波链采集FSE(3D CUBE T2WI)抑脂序列观察复杂性肛瘘,结果显示常规MRI T2WI抑脂序列联合3D CUBE T2WI抑脂序列对肛瘘分型诊断明显优于常规MRI T2WI抑脂序列;对肛瘘瘘管支数和内口数目的显示也优于常规MRI T2WI抑脂序列。韩金花等[15]用超薄快速三维容积T1加权脂肪抑制成像技术(liver acceleration volume acquisition, LAVA)增强技术联合常规序列,探讨超薄LAVA增强与常规T1WI增强在复杂性肛瘘内口及分型中的应用价值,结果显示超薄LAVA增强技术在内口、分型诊断的灵感度、特异度、阳性预测值及阴性预测值较常规T1WI增强明显提高。
DWI在显示内口、主管与支管上也有显著的临床价值[16-17]。陈均等[18]报道常规序列联合DWI因小血管扩散不受限,能有效区分局部走形的血管影与分支瘘管,其诊断支管的灵敏度和阳性预测值均增加。唐晓雯等[19]报道DWI序列中肛周脂肪、蜂窝织炎区域及血管因背景抑制效果呈相对低信号,与高信号瘘管及脓腔对比明显,能有效区分肛周脓肿与蜂窝织炎。Yoshizako等[20]报道表观弥散系数(apparent diffusion coefficient, ADC)值在PIA和NIA瘘管中存在显著性差异(P=0.0019),因此认为DWI有助于评价肛瘘的活动性。肛周血管一般呈对称分布,渐进性延伸,但正常人群解剖也有不少非对称、非连续血管[21]。对于细小的,特别是低位的瘘管,由于肛周血管丰富,常规序列很容易漏诊。本研究仅部分患者增扫了DWI序列,也可能是导致支管误诊或漏诊的原因。
此外,龚志刚等[22]比较PDW PFS与T2WI_SPAIR对于肛瘘内口及瘘管的诊断,结果表明T2WI_SPAIR常常由于脂肪抑制不均匀,解剖细节显示较差,部分瘘管的走行及内口的显示不及PDW PFS。通过与手术结果对照,PDW PFS对内口及瘘管的显示优于T2W SPAIR序列。
总之,MRI诊断肛瘘误诊或漏诊主要表现在内口或支管的检出。提高MRI对于肛瘘诊断的准确性,需要影像医师对盆底解剖结构的正确认识,完善的MR扫描序列。增强MR扫描有利于脓液少或非活动性瘘管的检出,有利于分辨瘘管内口;DWI有利于检出支管及低位细小瘘管;薄层扫描,有利于提高内口、支管的检出率。

