硅胶鼓室支撑片用于中耳手术的安全性验证
魏兴梅冯国栋陈龙云王晓喆高志强*
1中国医学科学院北京协和医学院北京协和医院耳鼻喉科(北京100730)
2中国医学科学院北京协和医学院北京协和医院病理科(北京100730)
对于中耳黏膜病变严重的患者,中耳术后鼓室粘连会造成鼓室含气腔减小,从而影响中耳振动,导致听力不佳[1,2]。有研究证明硅胶材料用于鼓室成形术中可有效防止鼓室粘连[3,4],医用硅胶材料理化性质稳定,具有惰性、无毒性的特点,对人体组织反应小,并且可长久存在,耐老化,起到支撑和阻隔的作用[3-6]。目前医用硅胶材料已广泛用于医疗卫生领域,包括可长期留置的人工肺、人工脑膜、乳房假体、鼻梁假体、人工心脏瓣膜、人工耳蜗电极等[7],经多年临床应用显示产品性能稳定。目前未见国内外专用于中耳手术防止粘连的硅胶产品,也未见其安全性、有效性的系列研究。另外由于中耳腔的特殊生理功能,其通过咽鼓管与外界相通,内耳圆窗膜的渗透作用等,硅胶材料的应用是否会导致感染或加重炎症,甚至影响内耳功能,尚未见有研究报道。北京协和医院设计并委托上海威宁整形制品有限公司(III类医疗器械生产资格证号:20000284)加工生产硅胶片。通过动物实验验证鼓室硅胶支撑片的安全性。由于豚鼠听觉灵敏且与人类听力水平相近,耳道宽、短、直,鼓膜面积较大[8],便于手术操作,我们选用豚鼠为实验动物,通过将硅胶片植入中耳腔观察鼓膜、鼓室情况及鼓室黏膜炎症和测试听力情况以验证该产品的安全性。本研究经过北京协和医院实验动物福利伦理委员会批准(编号:XHDW-2019-006)。
1 方法
1.1 实验动物与麻醉
使用豚鼠(雄性,12-14周,重约350g)为实验动物,动物由北京维通利华实验动物有限公司提供,动物数量为18只。使用异氟烷(瑞沃德生命科技有限公司,深圳,中国)吸入麻醉(诱导5%,流量5ml,维持1.5%,流量1ml)。
1.2 实验材料
实验所用的硅胶材料委托上海威宁整形制品有限公司加工生产,原材料皆来自于美国Nusil公司的MED-47系列,经精炼制胶,压模成型加工制成。产品大小为10×10×1mm,动物实验中根据需要裁剪至合适大小。
1.3 听力测试方法
麻醉生效后,清理双侧耳道后测试双耳听力。使用 RZ6(BioSigRZ ,Tucker-Davis Technologies,USA)系统测试听性脑干反应(Auditory Brainstem Response,ABR)并记录。测试方法如下:使用针刺电极,记录电极位于颅底正中,同侧乳突部位为参考电极,对侧乳突为负极,极间电阻<5kΩ。通过声场耳机位于测试侧给声,刺激声为Click声。自80dB SPL开始,以10dB递减,接近阈值时以5dB递减;能检测到的反应最低水平即为反应阈值(图1)。
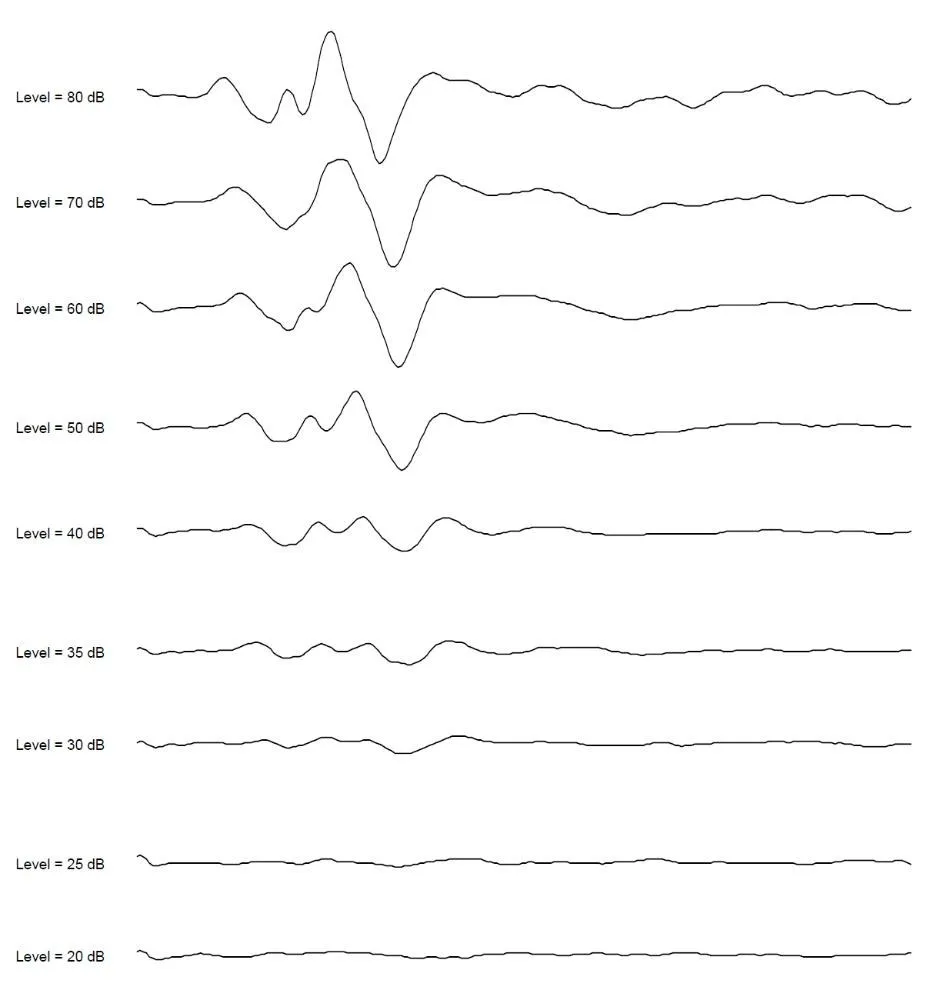
图1 听性脑干反应测试结果示例。此例中30dB SPL为听力阈值Fig.1 An example of recorded auditory brainstem response trace of a guinea pig.In this example,the hearing threshold is 30dB SPL.
1.4 手术过程
测完听力后,选择左侧为实验侧。左耳向上,去除耳周毛发并进行耳周及耳道消毒,耳内镜(Karl Storz,Tuttlingen,Germany)辅助下暴露鼓膜,于鼓膜后下象限制作穿孔,然后在相应的鼓岬黏膜使用尖针划伤,面积约2×2mm,于划伤部位放置硅胶片,使硅胶片覆盖划伤的黏膜(图2)。同法将右侧制作鼓膜穿孔,但不放置硅胶片。术后每天肌注抗生素(阿莫西林克拉维酸钾12.5ml/kg,一天两次)预防感染。4周后,全麻下再次观察鼓膜像和进行ABR阈值测试,然后处死动物取出听泡,观察鼓室内情况(图3)。
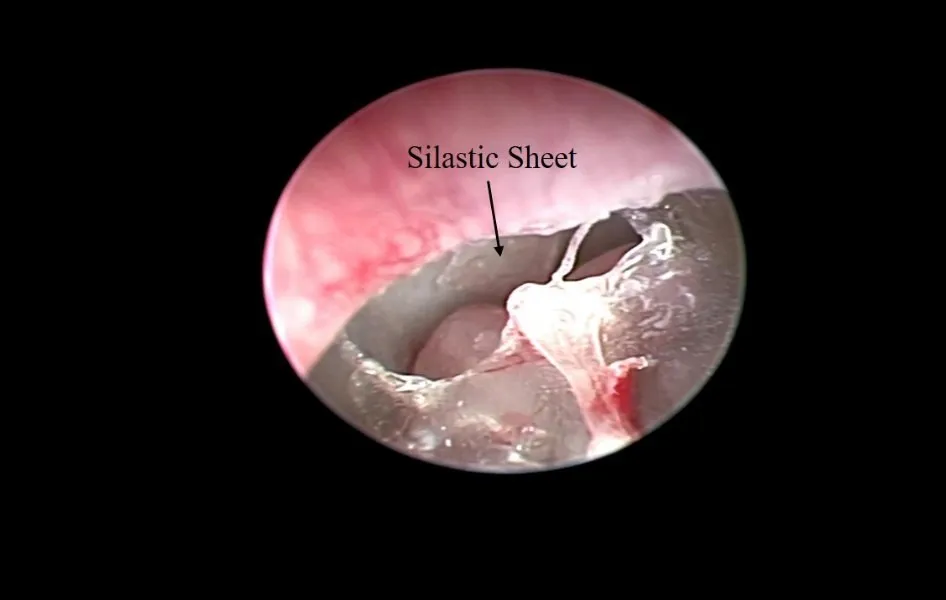
图2 硅胶片置于划伤的鼓岬黏膜表面Fig.2 The picture of silastic sheet put on the abraded mucosa of middle ear
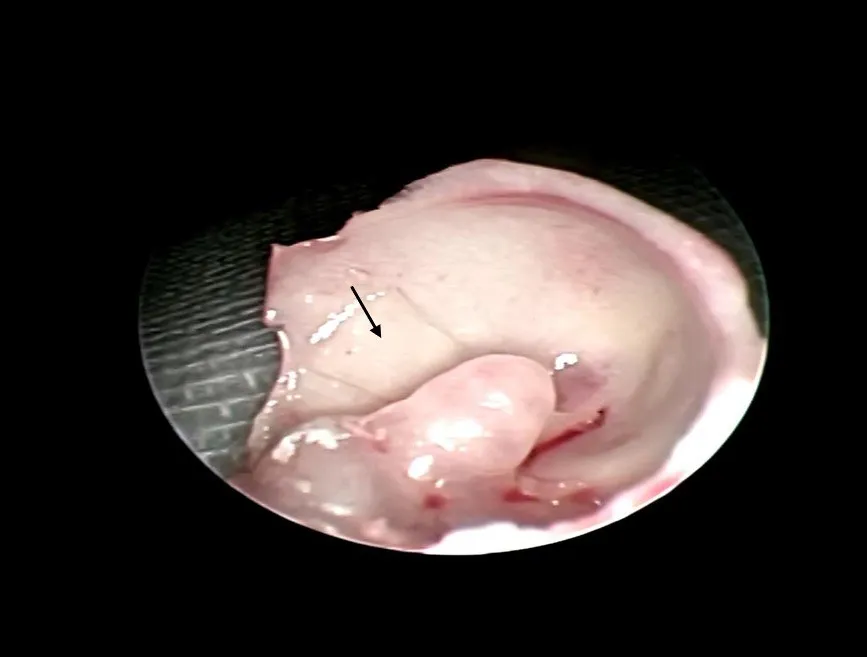
图3 豚鼠离体的听泡标本。黑色箭头所指为硅胶片Fig.3 The isolated tympanic bullas of a guinea pig.The arrow points to silastic sheet
1.5 病理情况
取出划伤部位的黏膜及骨质固定于4%的福尔马林中24h,然后进行脱钙、石蜡包埋、切片和H&E染色。然后光镜下对中耳黏膜根据炎性反应、纤维化程度和黏膜厚度进行分级和评分(图4)。
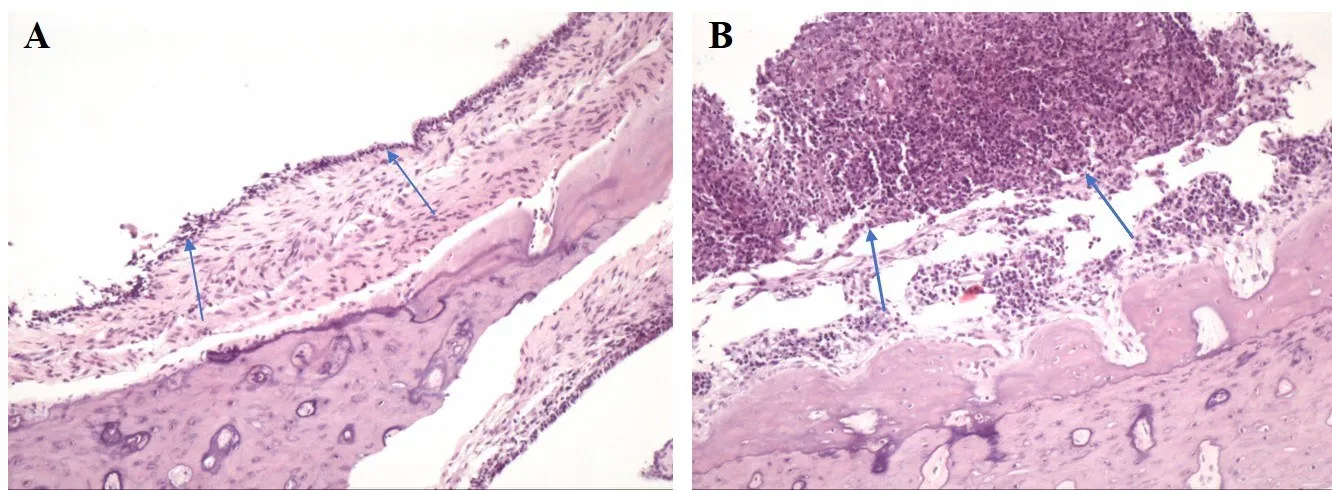
图4 中耳黏膜病理切片所见。A.炎性反应较轻的中耳黏膜示意,黏膜较薄。箭头所指为炎性反应。H&E染色,放大10倍;B.炎性反应较重的中耳黏膜示意,黏膜较厚。箭头所指为炎性反应。H&E染色,放大10倍。Fig.4 A.Example with mild inflammation of mucosa in middle ear.The mucosa is thinner.B.Example with severe inflammation of mucosa in middle ear.The mucosa is thicker.Arrow points to inflammation react.H&E stain,×10
1.6 统计分析
使用SPSS 24.0(IBM,Armonk,NY)对数据进行统计学分析。使用配对T检验分别比较实验侧和对照侧的术前术后听力变化,独立样本T检验比较术前术后双侧听力有无差异。使用卡方检验比较实验组和对照组鼓膜、中耳情况和中耳黏膜的炎症、纤维化和黏膜厚度的区别。以P<0.05为差异有统计学意义。
2 结果
2.1 鼓膜和中耳黏膜情况
术后4周,耳内镜下所见显示实验侧有一只动物存在小穿孔,其余鼓膜皆完整(图5)。取下听泡后,打开鼓膜见实验侧和对照侧各有一只存在少量鼓室积液(图6),其余鼓室内皆无积液及异常渗出。所有标本皆未见化脓、感染及粘连的发生。卡方检验显示试验组和对照组的鼓膜情况(χ2=1.029,P=1)和鼓室内情况(χ2=0,P=1)均无统计学差异(P>0.05)。

图5 术后4周所见鼓膜像。A.鼓膜愈合完整,箭头所指为制作穿孔处;B.鼓膜未完全愈合的1例鼓膜像,见为边缘性干穿孔。Fig.5 The tympanic membrane(TM)images four weeks after surgery.A.The TM was intact,and the arrow points to the place where the perforation was made.B.The one with a little perforation left.
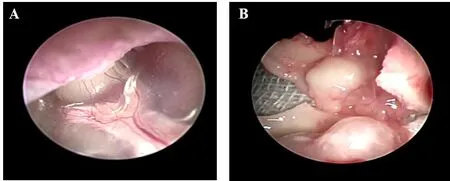
图6 存在中耳积液的样本。A.鼓膜像可见鼓室内存在积液;B.打开听泡见黏膜表面有渗出。Fig.6 The one with middle ear effusion.A.The tympanic membrane shows there was liquid in the middle ear.B.When the tympanic bulla was open, there was effusion on the mucosa.
2.2 听力结果
实验侧术前平均听力为27.22±6.00 dB SPL,术后平均听力为30.28±5.55 dB SPL,对照侧术前平均听力为26.94±6.22 dB SPL,术后平均听力为27.22±7.12 dB SPL。配对T检验显示实验侧术前术后听力无显著性差异(T=0.102,P=1.355>0.05),对照侧术前术后听力无显著性差异(T=0.193,P=0.920>0.05)。独立样本T检验显示术前两组的听力均无统计学差异(T=0.546,P=0.589>0.05),术后两组的听力均无统计学差异(T=-0.804,P=0.427>0.05)。
2.3 病理结果
中耳黏膜的炎性反应、纤维化程度和黏膜厚度如表1所示。卡方检验显示两者无显著性差异(P>0.05)。
3 讨论
中耳黏膜状态是影响中耳手术听力预后最重要的因素之一[9,10],已有研究表明约10%的传导性听力下降是由粘连性中耳炎导致[11]。为了预防中耳粘连,曾有多种材料应用于临床。例如曾有石蜡[12]、丝线[13]用于预防鼓室粘连,但由于易产生异物反应及影响听力被废用;后发展出的高分子塑料制品,由于太薄易被纤维组织机化而卷曲,并且异物反应比硅胶材料高,而逐渐被硅胶材料所取代[14]。后来使用的可吸收新型材料对于黏膜病变较轻的患者尚有一定作用,但对于黏膜病变严重的患者由于可吸收材料在短期内被吸收不能起到较长时间的阻隔作用而效果不佳[3,5]。所以硅胶材料由于其惰性、无毒性、不易卷曲且可长期起到阻隔作用而显示出一定的优势,显示出良好的应用前景[15,16]。临床上常用的乳房假体、鼻梁假体手术已经证明本研究所用硅胶产品的原材料、加工生产及消毒工艺和环境同该公司生产的目前市场上所用的乳房、鼻梁假体等一致,已经临床证实其安全性[17,18]。但由于中耳腔的特殊结构及传声的重要功能,其在中耳腔中的安全性研究未见报道,主要解决问题:1、由于中耳与外界相通的结构,异物的存在是否会导致感染或炎症加重的机会增加?2、是否会导致内耳功能损伤?
本实验统计学验证两组鼓膜愈合及中耳腔检查并无统计学差异,显示硅胶片没有影响鼓膜愈合和中耳腔黏膜的恢复。听力测试结果证明实验侧和对照侧术前术后听力均不存在差异,术后中耳黏膜炎性反应、纤维化程度和黏膜厚度两组亦无差异,显示硅胶片未影响听力,未加重中耳黏膜的炎性反应,未造成内耳毒性。这一结果与大部分前期文献报道结果相同。例如,1968年,Paparella等[14,19]报道在猫和松鼠猴的鼓室内植入硅胶材料并行鼓室成形术,经过2-4个月后观察鼓室内情况,无明显异物反应,且有助于鼓室含气腔的形成;1992年,Ng和Linthicum等[19]对6具植入硅胶的尸头进行研究,其最长植入时间可达21年,所有标本均有相对正常的中耳黏膜,均未见异物反应。术后两组听力未见差异,提示无内耳功能损伤。
但与有些学者报道的结果不同,例如黄德亮等[21]报道120耳粘连性中耳炎的治疗疗效,发现当时采用硅胶隔离物来预防粘连没有达到理想的目标,部分病例出现了鼓膜穿孔、中耳感染,不得不经穿孔取出硅胶片才使炎症反应得以控制。考虑可能与当时所用硅胶的原材料及加工工艺有关。医用硅胶加工过程中的物理、化学和生物性能需达到相关标准,并且通过试验证明植入品对人体无毒、不会引起组织炎症反应,副产物不会向重要器官迁移,材料未老化等方可临床应用[22,23]。若使用质地不纯或工业用有毒的硅酮类,可引起局部组织无菌性坏死;若清洗、灭菌不彻底,可造成异物反应,甚至植入时将指纹、棉纱纤维或粉尘带入都有可能造成异物反应[24]。即使严格按照良好的生产方法进行加工,每批产品仍必须进行一系列的短期试验,以确保植入物的无毒性和安全性,此外还必须消除可能引起的污染因素,因此需要有效的净化室[24]。例如,与血液接触的硅橡胶制品应在100级(每立方英尺空气中0.3μm大小的杂质粒子不超过100个)的净化室内进行加工,不植入体内的制品,通常是在10000级的净化室内制作[25]。
本实验结果有1例实验侧存在鼓膜小穿孔,穿孔为一干洁的穿孔,无感染征象,考虑穿孔是由于操作时靠近鼓膜边缘,从而需要更多的时间愈合;实验侧和对照侧各有一例发现鼓室内存在少量积液,存在积液的样本病理也证实其炎症反应较其他样本更为严重,考虑积液可能是由于操作造成的创伤未完全愈合。

表1 炎性反应,纤维化程度和黏膜厚度的分级以及实验侧和对照侧的比较。Table 1 The grading of inflammation,fibrosis and mucosal thickness as well as the comparison between test and control groups
改善硅胶片的性状将有可能提高产品的性能。如2016年,Jang等[26]通过豚鼠动物实验验证加入地塞米松-海藻酸钠的硅胶片较传统硅胶片可减轻中耳黏膜炎症反应,尽管尚未见相关产品上市,但毫无疑问,这是一个通过改进硅胶性状和成分进而提升其治疗效果的极有意义的探索。但是这一产品复杂的加工工艺和毒性验证过程是应该考虑的。
本研究的局限性在于,由于目前尚无成熟可靠的中耳炎动物模型建立,与慢性中耳炎中耳腔植入硅胶片后的真实反应尚有差距。由于实验动物良好的恢复能力,正常的咽鼓管功能,而且中耳腔内无慢性炎症,可能使本项目研究结果要比实际情况更加乐观,且无法验证硅胶植入是否影响中耳腔细菌生物膜的形成和转归。另外本研究未进行硅胶材料是否会造成全身或局部细胞免疫反应以及细胞毒性反应的相关试验,虽然其原料和加工工艺安全性已在其他假体材料中经过临床验证,但用于新的器官仍然需要重新验证,今后将结合临床数据进一步改进产品性能完善实验。但本实验亦提供了该产品对于鼓膜和中耳黏膜恢复,对听力的影响和对中耳黏膜炎症反应验证的指标,结合本材料加工成的乳房假体、鼻梁假体在人体的应用,为其通过临床试验验证有效性提供了依据。
4 结论
本研究所用硅胶鼓室支撑片置于损伤的中耳黏膜未产生明显的异物反应,未影响鼓膜愈合及造成中耳感染,未产生内耳毒性及加重中耳黏膜炎性反应。

