康柏西普对病理性近视脉络膜新生血管的疗效及视力预后相关性研究
陈丛 闫明 宋艳萍
脉络膜新生血管(CNV)是病理性近视(pathological myopia)最常见的并发症之一,可导致严重的中心视力损害,预后极差[1]。目前,抗血管内皮生长因子(VEGF)被推荐为治疗病理性近视CNV的一线方案[2]。研究表明,抗VEGF药物能有效阻止CNV生长、减轻CNV渗漏、提高患眼视力[3]。康柏西普是一种新型的重组融合蛋白类抗VEGF药物,已被中国食品药品监督管理局批准用于治疗病理性近视CNV。该药物对所有同种型VEGF和胎盘生长因子(PIGF)具有高亲和力[4],并且比其他抗VEGF药物对VEGF-A的亲和力更强[5-6]。目前康柏西普治疗病理性近视CNV的有效性和安全性研究随访时间大多不超过12个月,且有效性观察指标主要集中在最佳矫正视力(BCVA)和黄斑中心凹视网膜厚度(CMT)变化上,而对于CNV大小和活动性以及影响患者视力预后相关因素的研究尚少。因此,我们对一组经玻璃体内注射康柏西普治疗病理性近视CNV的患者进行超过24个月的随访,评估CNV变化特点以及初步探讨影响末次随访视力及总注射针数的相关因素,现将结果报道如下。
1 资料与方法
1.1 一般资料我们回顾性研究了2015年12月至2018年6月在中国人民解放军中部战区总医院眼科确诊的病理性近视CNV患者47例49眼,诊断标准依据RADIANCE研究[7],患眼均只接受玻璃体内注射康柏西普治疗。其中男12例13眼,女35例36眼。年龄(56.67±13.90)岁,屈光度(-13.64±3.92)D,眼轴长度(29.03±1.36)mm。患眼中弥漫性脉络膜萎缩期(Ⅱ期)[8]34眼(69.4%),片状萎缩期(Ⅲ期)15眼(30.6%);中心凹下型CNV 40眼(81.6%),近中心凹型CNV 7眼(14.3%),旁中心凹型CNV 2眼(4.1%)。纳入标准:(1)屈光度>-6.00 D;眼轴长度≥26.5 mm;(2)有继发于PM的活动性CNV病变;(3)年龄>18岁;(4)对数视力表测得其BCVA≥0.025;(5)随访时间>24个月。排除标准:(1)CNV继发于PM以外的原因;(2)合并病理性近视以外的脉络膜视网膜病变(包括中心性浆液性脉络膜视网膜病变、糖尿病视网膜病变、视网膜静脉阻塞、血管炎或葡萄膜炎);(3)既往曾接受光动力治疗(PDT)、玻璃体内注射抗VEGF药物治疗。该研究得到了中国人民解放军中部战区总医院机构伦理审查委员会的批准,并遵循了《赫尔辛基宣言》原则。所有患者均被告知玻璃体内注射的风险,并在治疗前签署书面知情同意书。
1.2 研究方法所有患者均采用1+PRN的治疗方案。患眼玻璃体内注射均在无菌手术室内按内眼手术常规操作进行。使用30号针头将康柏西普0.05 mL(含康柏西普0.5 mg)通过睫状体平坦部注入玻璃体内。再治疗标准:与基线BCVA相比BCVA下降;OCT显示CMT增加≥50 μm;有新的或持续性视网膜囊样改变、视网膜下积液或色素上皮脱离;有新的CNV形成或黄斑部出血;荧光素眼底血管造影(FFA)检查提示有新的持续性的荧光素渗漏。
1.3 随访与检查所有患者治疗后每月随访一次,随访时间大于24个月,平均随访时间26.62个月。BCVA、眼压(IOP)、裂隙灯生物显微镜、扩张眼底检查和光学相干断层扫描(OCT)(Topcon 3D-OCT-2000;Topcon,Tokyo,Japan)、眼底彩色照相在基线和随访后每月检查一次,FFA(HRA-2;海德堡工程公司,德森海姆,德国)在基线和随访后每3个月检查1次。将国际通用视力表测量的BCVA转换成logMAR视力进行记录,CMT由OCT测量。使用图像分析软件(视网膜血管造影术测量程序;海德堡工程公司),在早期像和晚期像的血管造影照片上测量CNV面积和CNV渗漏面积。
1.4 统计学分析使用统计学软件SPSS 19.0进行统计分析。计量资料进行正态性检验后以均数±标准差表示。治疗前后BCVA、CMT、CNV面积、CNV渗漏面积比较采用配对样本t检验;治疗后24个月logMAR BCVA及总注射针数分别与各基线资料(屈光度、眼轴长度、病理性近视分期、CNV位置、logMAR BCVA、CMT、CNV面积、CNV渗漏面积)进行相关分析,其中病理性近视分期、CNV位置为非正态分布数据选择Spearman相关分析,其他资料为正态分布数据选择Pearson相关分析。检验水准:α=0.05。
2 结果
随访期间,所有患者均未出现持续性高眼压、眼内炎、视网膜脱离及心脑血管疾病等与药物或注射相关的眼部并发症和全身不良反应。
2.1 患眼BCVA及CMT检查结果治疗前及治疗后1个月、3个月、6个月、12个月、24个月logMAR BCVA分别为0.92±0.41、0.61±0.33、0.56±0.31、0.52±0.29、0.56±0.30、0.57±0.28。与治疗前相比,治疗后logMAR BCVA均有提高,差异均有统计学意义(t=7.11、7.51、7.88、7.42、7.40,均为P<0.05)。见图1。
治疗前及治疗后1个月、3个月、6个月、12个月、24个月CMT分别为(292.41±60.42)μm、(251.67±48.96)μm、(248.63±64.70)μm、(251.24±69.63)μm、(254.27±78.72)μm、(246.08±77.41)μm。与治疗前相比,治疗后CMT均有下降,差异均有统计学意义(t=6.20、4.58、3.53、3.12、3.81,均为P<0.05)。见图2。
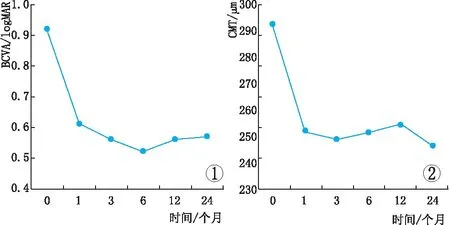
图1 随访24个月患眼logMAR BCVA变化。图2 随访24个月患眼CMT变化
2.2 患眼CNV面积及渗漏面积检查结果治疗前及治疗后3个月、6个月、12个月、24个月CNV面积分别为(0.55±0.63)mm2、(0.45±0.64)mm2、(0.45±0.65)mm2、(0.46±0.64)mm2、(0.45±0.62)mm2。与治疗前相比,治疗后CNV面积均有下降,差异均有统计学意义(t=4.97、6.12、3.66、4.32,均为P<0.05)。见图3。
治疗前及治疗后3个月、6个月、12个月、24个月CNV渗漏面积分别为(1.08±1.05)mm2、(0.38±1.01)mm2、(0.25±0.96)mm2、(0.23±0.95)mm2、(0.19±0.90)mm2。与治疗前相比,治疗后CNV渗漏面积均有下降,差异均有统计学意义(t=6.55、7.83、7.44、7.56,均为P<0.05)。见图4。
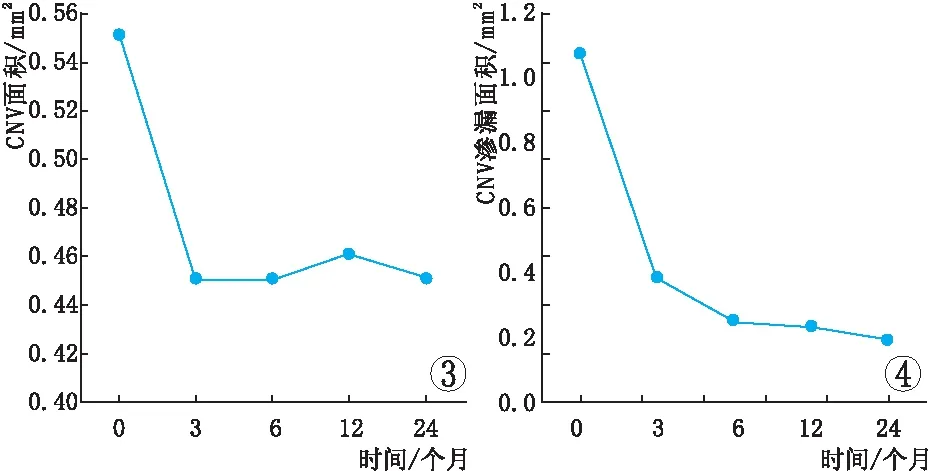
图3 随访24个月患眼CNV面积变化。图4 随访24个月患眼CNV渗漏面积变化
2.3 患眼屈光度、眼轴长度检查结果及注射次数24个月随访后,屈光度由基线(-13.64±3.92)D升高到(-14.78±3.71)D,差异有统计学意义(t=19.26,P=0.000);眼轴长度由基线(29.03±1.36)mm升高到(29.38±1.36)mm,差异有统计学意义(t=-17.58,P=0.000)。在24个月随访期内,患眼第1年注射次数为(3.51±1.54)次,第2年注射次数为(0.57±1.02)次,总注射针数为(4.08±1.75)次。1例典型病理性近视CNV患者治疗结果见图5。
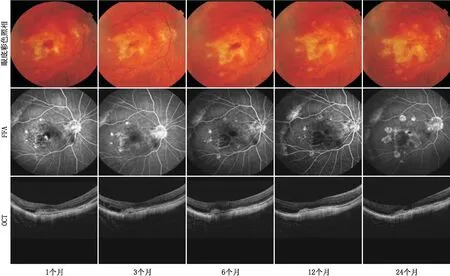
图5 70岁女性患者右眼病理性近视继发黄斑区CNV治疗的典型眼底彩色照相、FFA、OCT结果 玻璃体内注射康柏西普治疗并随访24个月,经初始2针治疗后出血吸收,CNV有所消退,6个月时再次出血,继续注射4针后出血吸收,CNV消退,黄斑区病情24个月维持稳定,1个月、3个月、6个月、12个月、24个月的BCVA分别为0.08、0.25、0.12、0.20、0.15
2.4 相关性分析患眼治疗后24个月logMAR BCVA与基线屈光度、眼轴长度、病理性近视分期、CNV位置、CMT、CNV面积均无明显相关(均为P>0.05),但与基线logMAR BCVA、CNV渗漏面积呈正相关(r=0.595、0.319,P=0.000、0.026)。总注射针数与基线屈光度、眼轴长度、病理性近视分期、CNV位置、logMAR BCVA均无明显相关(均为P>0.05),但与基线CMT、CNV面积、CNV渗漏面积均呈正相关(r=0.297、0.440、0.433,P=0.038、0.002、0.002)。见表1。
表1 治疗后24个月logMAR BCVA及总注射针数与基线资料的相关性
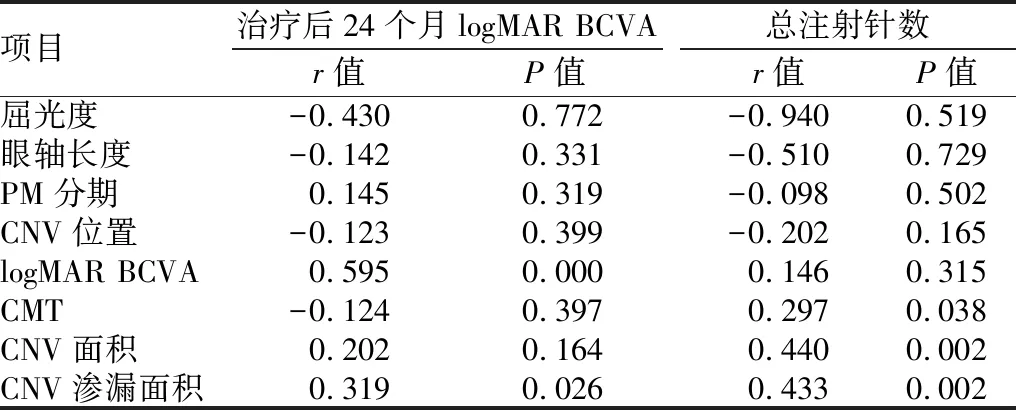
项目治疗后24个月logMAR BCVAr值P值总注射针数r值P值屈光度-0.4300.772-0.9400.519眼轴长度-0.1420.331-0.5100.729PM分期0.1450.319-0.0980.502CNV位置-0.1230.399-0.2020.165logMAR BCVA0.5950.0000.1460.315CMT-0.1240.3970.2970.038CNV面积0.2020.1640.4400.002CNV渗漏面积0.3190.0260.4330.002
3 讨论
病理性近视继发CNV严重影响患者视力和生活质量,尤其是对于年轻患者。一项长期随访研究显示,在没有干预的情况下,病理性近视CNV会导致严重的视力损害[9]。近年来,通过对玻璃体内注射抗VEGF药物治疗病理性近视CNV的几项前瞻性和回顾性研究证明了抗VEGF治疗对视力的改善和长期维持作用,并且可降低CMT的减少和减轻CNV的渗漏[10]。由于抗VEGF药物对病理性近视CNV的安全性和有效性较好,它已经成为病理性近视CNV的一线治疗方案。
康柏西普是一种新型的重组融合蛋白,对所有VEGF-A和VEGF-B同种型以及PlGF具有高亲和力。且与阿柏西普相比,VEGFR-2的第四结合域是康柏西普特有的,由于VEFGR-2的额外结构域,康柏西普降低了对细胞外基质的黏附并增加了受体组合的速率。康柏西普治疗年龄相关性黄斑变性(AMD)的I期[11]和II期(AURORA)[12]研究数据均支持其用于AMD的抗VEGF治疗。有研究显示[12],从基线到术后3个月,0.5 mg和2.0 mg两组药物组的BCVA分别增加到8.97个字母和10.43个字母,在12个月,视力分别提高10.49个字母和13.61个字母。这些获益归因于药物的抑制新生血管作用,同时也为康柏西普治疗病理性近视CNV奠定了研究基础。
目前国内外关于康柏西普治疗病理性近视CNV的研究报道尚少。本研究纳入的患者均为新发病例,既往未受过其他相关治疗,也排除了由其他原因所导致的CNV,能更准确判断康柏西普治疗病理性近视CNV的有效性和安全性。本研究随访时间为24个月,目前已报道的关于康柏西普治疗病理性近视CNV的临床研究随访时间均未超过12个月,延长随访时间能更好地观察康柏西普治疗病理性近视CNV的远期疗效。Yan等[13]回顾性地分析了42眼病理性近视CNV患者,这些患者采用玻璃体内注射康柏西普3+PRN治疗方案并随访12个月后,71.4% 的患眼获得了至少3行的BCVA改善效果,且与基线相比,前3个月有明显的视力改善,并且视力持续改善或稳定至12个月。本研究随访期前12个月,79.6%的患眼获得了至少2行的BCVA改善效果,57.1%的患眼获得了至少3行的BCVA改善效果;随访到24个月,79.6%的患眼获得了至少2行的BCVA改善效果,51.0%的患眼获得了至少3行的BCVA改善效果。Yan等[13]的研究初始治疗方案与随访时间和我们的研究不同,但视力提高都主要发生在前3个月,且均未观察到由康柏西普药物本身所带来的并发症。不过本研究随访前12个月视力总获益低于Yan等[13]的研究结果。
同样作为融合蛋白的阿柏西普被欧洲药品管理局批准为治疗病理性近视CNV的抗VEGF药物。MYRROR研究是一项国际性III期多中心随机双盲对照研究,比较了1+PRN治疗方案玻璃体内注射阿柏西普组和安慰剂对照组治疗病理性近视CNV的效果,阿柏西普治疗组视力获益主要在前6个月,平均12.1个字母数[14]。与MYRROR研究相比,本研究也采用了1+PRN的治疗方案,但视力获益时期主要集中在前3个月。在MYRROR研究中还报道了3.3%眼部和4.4%非眼部不良事件的发生率[14],而本研究中所有患者均未发生眼部或者全身系统的不良反应。
CMT、CNV面积及CNV渗漏面积都是评价病理性近视CNV的重要指标。在本研究中,所有患者在末次随访时,CMT均较基线明显下降,且下降的主要时间与视力获益时间类似,主要发生在前3个月。同样,CNV面积及渗漏面积的下降也在前3个月比较显著,这似乎提示治疗前3个月的视力获益与解剖结构的改善存在着某种关联。在本研究随访的前12个月,73.5%患眼CNV面积下降,其中27.8%患眼CNV完全消退;93.9%患眼CNV渗漏面积下降,其中89.1%患眼CNV渗漏完全消退。在末次随访时,85.7%患眼CNV面积下降,其中28.6%患眼CNV完全消退;93.9%患眼CNV渗漏面积下降,其中95.7%患眼CNV渗漏完全消退。因此我们认为,康柏西普治疗病理性近视CNV不仅能带来视力获益,还能恢复视网膜形态、消退并封闭CNV从而带来解剖结构的获益。
相关分析结果显示,患眼治疗后24个月的logMAR BCVA与基线logMAR BCVA、CNV渗漏面积呈正相关;总注射针数与基线CMT、CNV面积、CNV渗漏面积呈正相关。Iacono等[15]的一项随访12个月以雷珠单抗或者贝伐单抗治疗病理性近视CNV患者来确定影响预后相关因素的前瞻性研究结果显示,基线BCVA、症状持续时间、眼底自发荧光模式与末次随访、视力变化具有相关性,45.8%患者仅接受1~2次玻璃体内注药,比接受3次或以上注药患者的视力预后更好,这部分患者基线年龄较小、CMT较小、CNV面积较小、出血较少。但该研究并未将CNV渗漏面积作为评价指标之一。Battaglia等[16]研究发现,较小的病理性近视CNV渗漏,需要的玻璃体内注药次数更少,且这部分患者基线CMT更小,提示CNV渗漏能更好地帮助识别CNV的活动性。这与本研究结果一致。
综上所述,康柏西普治疗病理性近视CNV安全有效,末次随访BCVA与基线BCVA、CNV渗漏面积具有正相关性,总注射针数与基线CMT、CNV面积、CNV渗漏面积具有正相关性。本研究不足之处为回顾性研究,无对照组,且样本数偏少,未来需要进一步扩大样本量,进行前瞻性多中心随机对照研究。

