负载铁生物炭的制备、表征及其对Cr(Ⅵ)的吸附性能
康 宁,毛 磊,张 宇,梁文懂,马 毅
(1.武汉科技大学化学与化工学院,湖北 武汉,430081;2.武汉科技大学煤转化与新型炭材料湖北省重点实验室,湖北 武汉,430081;3.山西潞安矿业(集团)有限责任公司,山西 长治, 046299)
生物炭可由农业废弃物、动物粪便等低廉生物质在缺氧条件下热解获得,因其具有较高的比表面积、丰富的孔隙结构和官能团而被用作有机污染物和重金属的吸附剂[1]。与商品活性炭相比,生物炭的价格低廉、制备工艺简单、环境效应好,但是,制备工艺简单也造成所制生物炭的表面性质差异较大,表面基团种类有限且分布不均匀[2],导致其吸附污染物的能力受限[3]。为了提高生物炭的吸附性能,研究者常常利用表面改性方法以改善其孔结构及表面官能团的种类和数量[4],如李仕友等[5]采用KMnO4对生物炭进行改性处理,改性后的生物炭含氧官能团明显增多,化学吸附能力进一步增强,对U(Ⅵ)的去除效果较未改性时提高了67.9%。Park等[6]通过蒸汽活化增加了生物炭中可交换阳离子的数量,显著提升了生物炭对Cu(Ⅱ)的吸附性能。不过,经改性后的生物炭虽然吸附能力明显增强,但因生物炭本身颗粒细小,将其应用于废水处理后难以从液相中分离。为此,研究者尝试在生物炭中引入磁性颗粒制备磁性生物炭材料,借助外加磁场的作用来实现固液分离,如Son等[7]在藻类生物炭中掺杂氧化铁颗粒制备了磁性生物炭,李杰等[8]以松树枝为原料制备生物炭,并采用水热法将所制生物炭与Fe3O4和壳聚糖复合,从而制备出复合吸附剂,这些研究通过嵌入磁性金属氧化物实现了固液两相的磁性分离,表明生物炭负载的磁性金属物质能有效促进固液分离,但该类磁性金属对生物炭吸附性能的影响及作用机理仍需要深入分析,基于此,本文以小麦秸秆为原料高温热解制备生物炭,分别利用FeSO4/FeCl3和FeCl3对其进行表面改性,制备出易于固液分离的重金属吸附剂,并采用比表面积分析仪、傅里叶变换红外光谱仪(FTIR)、振动样品磁强计(VSM)、X射线衍射仪(XRD)和扫描电子显微镜(SEM)等对所制生物炭样品进行表征,比较负载Fe前后生物炭样品的物理和化学性质,结合吸附动力学及等温吸附过程研究了负载Fe对生物炭吸附Cr(Ⅵ)性能的影响。
1 材料与方法
1.1 原料与试剂
小麦秸秆,取自湖北省罗田县;FeCl3·6H2O、FeSO4·7H2O、K2Cr2O7、NaOH、HCl,皆为分析纯;自制超纯水。
1.2 样品的制备
生物炭及其分别经FeCl3、FeSO4/FeCl3表面改性的样品制备过程如下:将小麦秸秆洗涤干燥后研磨成粒径为0.2~0.45 mm的颗粒备用,取部分颗粒置于500 ℃的管式炉中,在350 mL·min-1的N2气氛下经炭化制得生物炭样品,标记为BC;再取部分小麦秸秆颗粒浸泡在80 mL浓度为2 mol·L-1的FeCl3溶液中形成小麦秸秆颗粒悬浮液,该悬浮液经磁力搅拌混合0.5 h后继续在70 ℃条件下进行水浴处理0.5 h,以加速其水解及Fe3+的沉淀,之后从悬浮液中分离出小麦秸秆颗粒,将该颗粒置于500 ℃的管式炉中在350 mL·min-1的N2气氛下热解,所得产物即为由FeCl3表面改性的生物炭样品,标记为MBC-1;取30 g 所制BC样品加入300 mL超纯水中,形成生物炭悬浮液,再将3 g FeCl3·6H2O及1.67 g FeSO4·7H2O溶于90 mL超纯水中形成混合液(Fe3+、Fe2+摩尔比为2∶1)并滴入生物炭悬浮液中,借助NaOH溶液将掺入混合液后的生物炭悬浮液pH值调至10.5,该悬浮液在N2气氛中25 ℃条件下经剧烈搅拌1 h后继续煮沸1 h,之后再于室温下老化12 h,最后,将所得混合物过滤并用超纯水冲洗,在105 ℃条件下干燥12 h,所得黑色颗粒即为由FeSO4/FeCl3表面改性的生物炭样品,标记为MBC-2。
1.3 表征方法
使用V-Sorb 2800P型比表面积及孔径分析仪测定样品77 K条件下的氮气吸/脱附曲线,并通过BET法计算出样品的比表面积(SBET)、孔容与孔径的大小;使用德国Bruker Vertex70型傅里叶变换红外光谱仪(FTIR)对样品表面官能团进行分析,测试采用KBr压片法,分辨率为4 cm-1,记录样品在500~4000 cm-1区域的红外光谱图;使用美国LakeShore 7404型振动样品磁强计(VSM)测定样品的磁化强度,测试磁场范围为±100 emu·g-1,测试温度为室温;使用荷兰帕纳科Empyrean锐影型X射线衍射仪(XRD)分析样品的物相组成,扫描速度为2°/min,激发源为Cu-Kα靶,电流为40 mA,电压为40 kV。使用捷克TESCAN VEGA 3 SBH-EasyProbe 型扫描电子显微镜(SEM)观察样品的微观形貌特征,加速电压为20 kV;使用雷磁PHS-3C型酸度计测定溶液pH值;使用美普达UV-1200型紫外可见分光光度计测定溶液中的Cr(Ⅵ)浓度,以波长为540 nm的吸光度进行定量。
1.4 吸附实验
称取干燥后的K2Cr2O7,经超纯水溶解后移入容量瓶中定容,配制成多组一定浓度的Cr(Ⅵ)溶液备用。分别将所制BC、MBC-1、MBC-2样品按4 g·L-1的投加量投入Cr(Ⅵ)溶液,在不同的Cr(Ⅵ)溶液初始pH值、振荡速率及实验温度的条件下,测定溶液经水浴恒温振荡箱持续振荡48 h时的Cr(Ⅵ)浓度并计算出相应的Cr(Ⅵ)去除率,其中溶液pH值借助浓度为0.1 mol·L-1的HCl和NaOH溶液进行调节,范围介于2~12,振荡速率为0~180 r·min-1,实验温度为30~50 ℃,Cr(Ⅵ)去除率η计算公式为
(1)
式中C、C0分别为溶液中Cr(Ⅵ)的实际浓度和初始浓度。
2 结果与分析
2.1 样品的表征分析
2.1.1 比表面积和孔隙结构
改性前后生物炭样品的比表面积和孔结构参数如表1所示。由表1可见,与BC样品相比,MBC-1和MBC-2样品的比表面积、总孔体积及微孔体积均有明显增大,尤其MBC-2样品相应的增幅分别达到234%、125%、233%。这可能是因为在改性过程中,FeCl3/FeSO4、FeCl3的掺入促进了碳链的断裂,从而产生大量新的微孔,微孔的增多使得平均孔径减小。同时,FeCl3/FeSO4和FeCl3在生物炭表面生成氧化铁颗粒,颗粒的增多使生物炭比表面积增大。不过改性后生物炭样品的微孔数量虽有增加,但其在样品总孔体积中所占比例依然很小,样品中的孔隙仍以中孔为主,这有利于金属离子在孔隙中的扩散。

表1 样品的BET比表面积及孔结构参数
2.1.2 FTIR分析
样品的FTIR谱图如图1所示。分析图1可知,MBC-1和MBC-2在618 cm-1处出现的新吸收峰对应Fe—O的伸缩振动[9],这表明生物炭经改性处理后,含铁基团被成功引入其表面;1113 cm-1处出现的吸收峰可能与C—C振动相关[10];1400~1628 cm-1处的振动峰与生物炭中羧基和羰基的伸缩振动有关;2921 cm-1处的吸收峰对应脂肪族C—H的伸缩振动;3415 cm-1处的吸收峰主要是因—OH的伸缩振动而造成的。
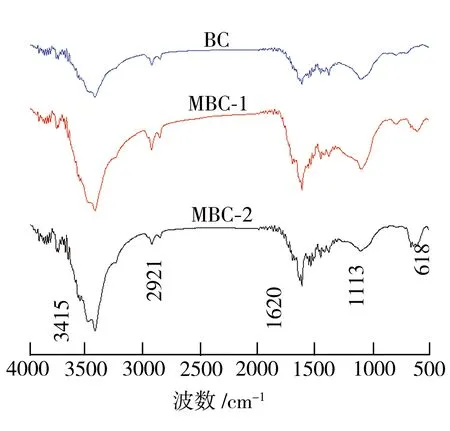
图1 样品的FTIR谱图
2.1.3 磁化曲线
图2所示为样品的磁化曲线。由图2可见,BC的磁化曲线几乎平直,其饱和磁化强度基本为0,而MBC-1和MBC-2的饱和磁化强度分别为15.41、35.53 emu·g-1,故二者作为吸附剂时,在外加磁场作用下易于从水溶液中分离出来,这对于生物炭的回收利用具有十分重要的意义。
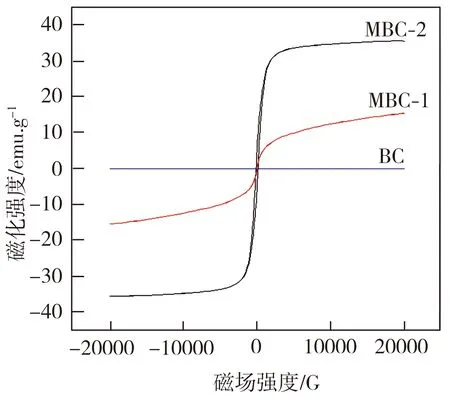
图2 样品的磁化曲线
2.1.4 XRD分析

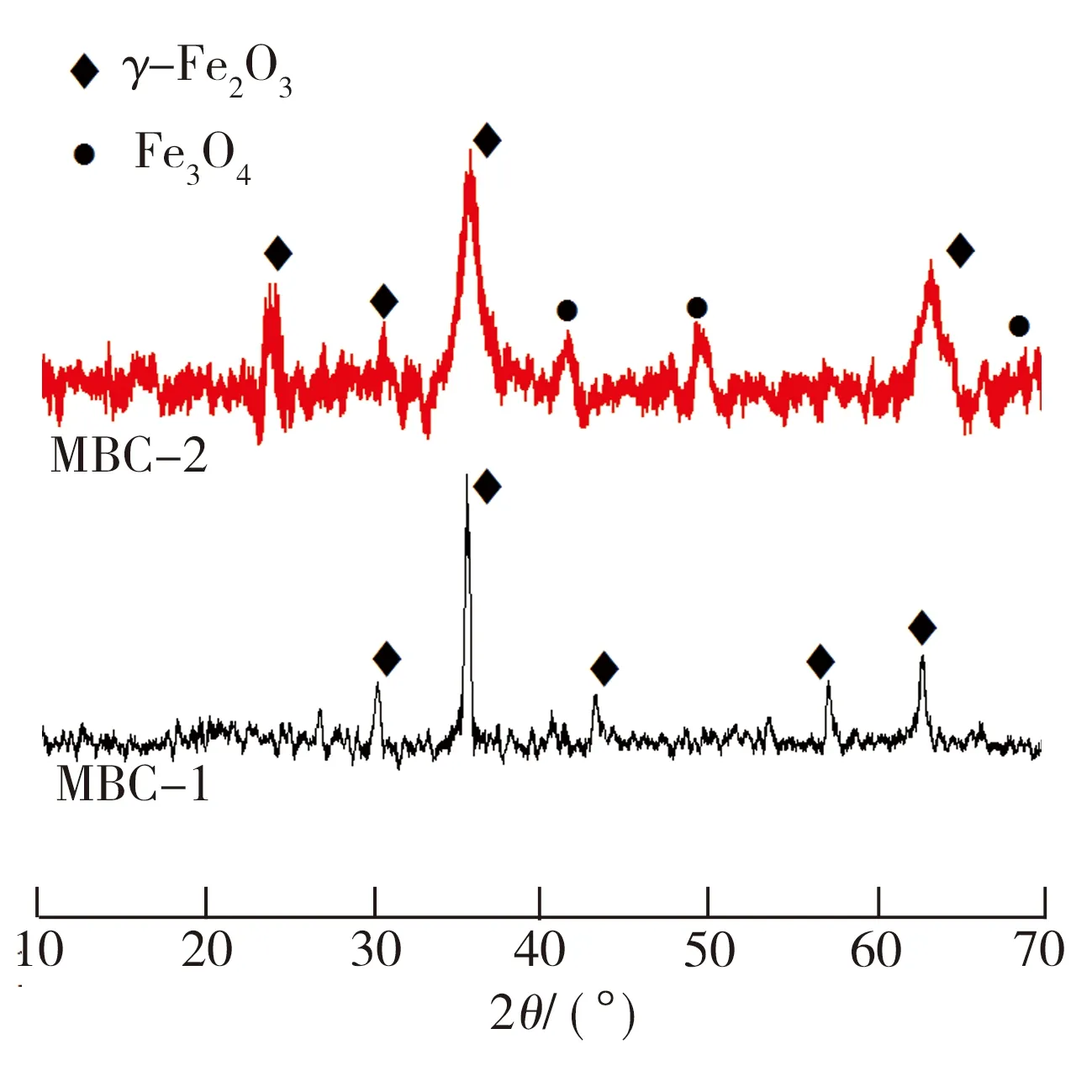
图3 样品的XRD谱图
2.1.5 SEM分析
样品的SEM照片如图4所示。由图4(a)和图4(b)可以看出,BC为多孔管状结构,孔隙结构发达,表面光滑且分布了1 μm左右的小孔;从图4(c)和图4(d)中可见,负载铁后的MBC-1样品保留了完整的管状结构,表面粗糙且均匀密集分布了粒径为0.2 μm左右的细小颗粒,根据XRD表征结果推测其可能为γ-Fe2O3[11];由图4(e)和图4(f)可见,负载铁后的MBC-2样品表面发生了塌陷,并有粒径较大的颗粒物(约为2.5 μm)不均匀分散于其上,小孔数量明显增加,可见负载铁对生物炭的表面形貌有显著影响,并且铁氧化物颗粒分散于炭基质上,提高了比表面积和孔容积,对重金属离子具有较强亲和能力[12]。
2.2 制备条件对生物炭Cr(Ⅵ)吸附的影响
2.2.1 Cr(Ⅵ)溶液初始pH值的影响
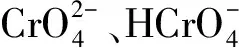

(a)BC,低倍
(b)BC,高倍

(c)MBC-1,低倍
(d)MBC-1,高倍

(e)MBC-2,低倍
(f)MBC-2,高倍
图4 样品的SEM照片
Fig.4 SEM images of samples
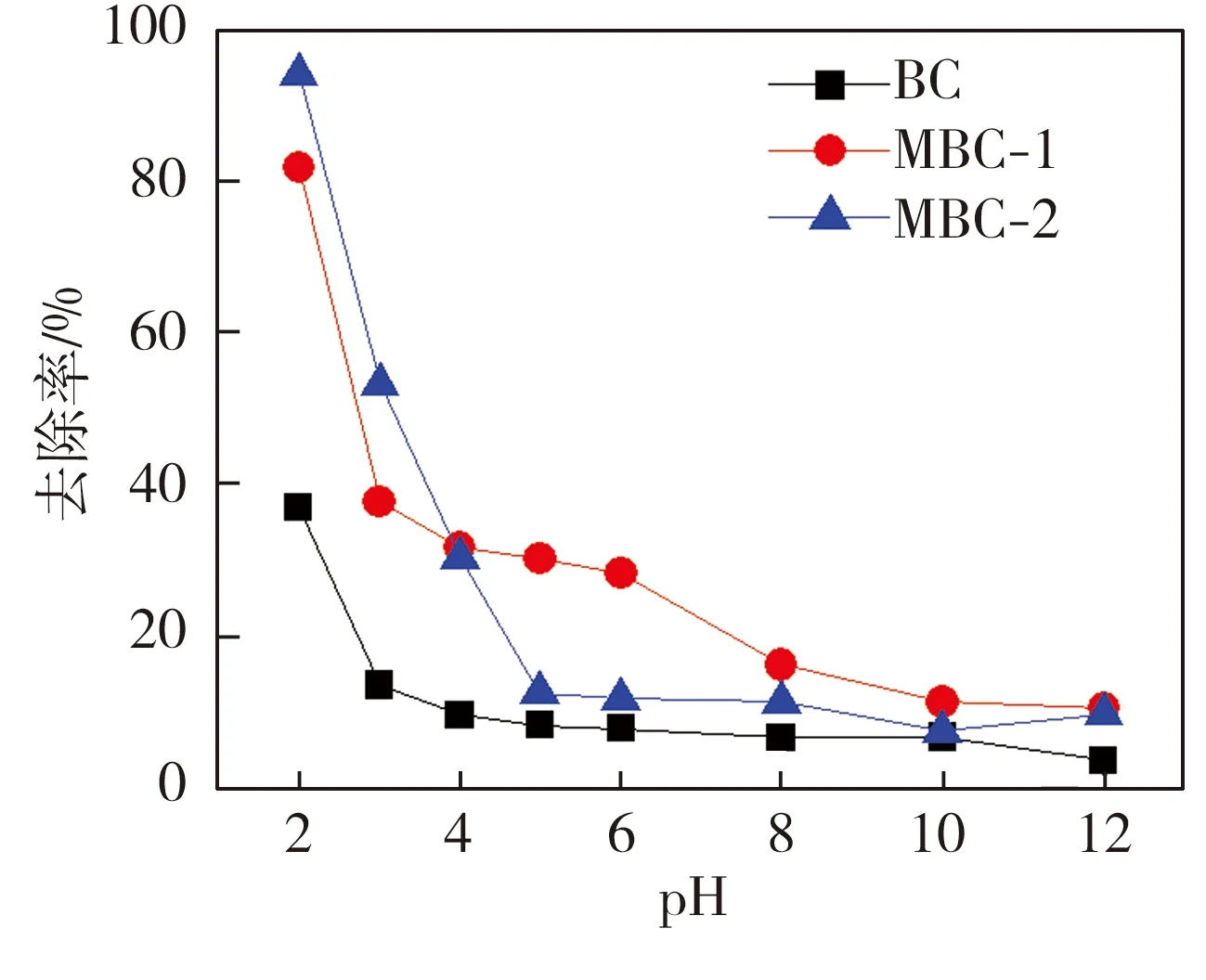
图5 初始pH值对生物炭吸附Cr(Ⅵ)的影响
Fig.5 Effect of initial pH value on adsorption of Cr(Ⅵ) by biochar
2.2.2 振荡速率的影响
当Cr(Ⅵ)溶液初始浓度为100 mg·L-1、初始pH值为2、实验温度为30 ℃时,振荡速率对生物炭Cr(Ⅵ)去除率的影响如图6所示。从图6中可以看出,随着振荡速率不断增加,3种生物炭对Cr(Ⅵ)的吸附能力均随之不断增强,当振荡速率达到150 r·min-1后,相应的Cr(Ⅵ)去除率基本达到稳定值。这表明当振荡速率小于150 r·min-1时,生物炭吸附Cr(Ⅵ)的过程受到液相膜扩散的影响,增大振荡速率可以加快膜扩散从而提高吸附剂吸附效率[17]。
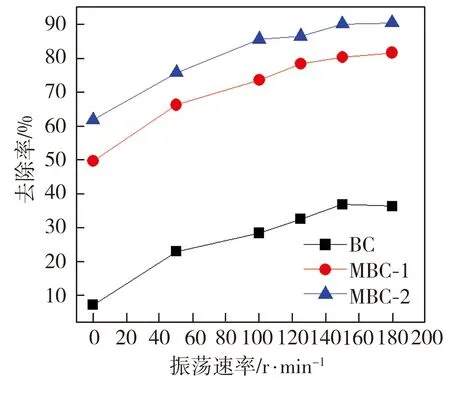
图6 振荡速率对生物炭吸附Cr(Ⅵ)的影响
Fig.6 Effect of oscillation rate on adsorption of Cr(Ⅵ) by biochar
2.2.3 实验温度的影响
当Cr(Ⅵ)溶液初始浓度为100 mg·L-1、初始pH值为2、振荡速率为150 r·min-1时,在不同实验温度条件下,3种生物炭样品对Cr(Ⅵ)的平衡吸附量如表2所示。从表2中可以看出,3种生物炭对Cr(Ⅵ)的平衡吸附量均随实验温度的升高而增大,表现出典型的化学吸附特征。这是因为温度升高加速了溶液中离子的运动,有利于Cr(Ⅵ)克服生物炭表面阻力向孔道内扩散,同时,较高温度下吸附过程需克服的活化能也较低,使得吸附反应更易进行。此外注意到,当实验温度由30 ℃升至50 ℃时,MBC-2对Cr(Ⅵ)平衡吸附量由23.48 mg·g-1增至24.98 mg·g-1,相应增幅不大,表明MBC-2对Cr(Ⅵ)吸附量受实验温度影响较小,从考虑能耗角度出发,实际中宜采用30 ℃的操作温度。
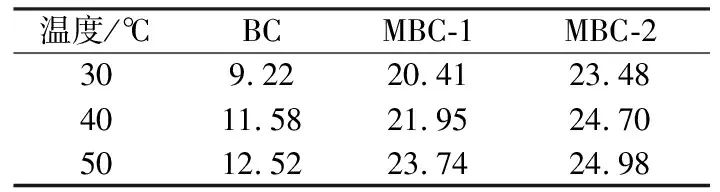
表2 平衡吸附量(单位:mg·g-1)
2.3 吸附动力学
当Cr(Ⅵ)溶液初始浓度为100 mg·L-1、初始pH值为2、振荡速率为150 r·min-1、实验温度为30 ℃时,所制生物炭样品对溶液中Cr(Ⅵ)的吸附量随吸附时间变化的规律如图7所示。由图7可见,随着吸附时间的延长,3种样品对Cr(Ⅵ)的吸附量均呈现出先快速增加而后趋于稳定的变化规律,这与文献[2]所报道的氧化锌改性生物炭吸附Cr(Ⅵ)时的变化趋势相似。究其原因,可能是因为吸附反应刚开始时,生物炭上的吸附位点较多,生物炭表面和溶液中Cr(Ⅵ)的浓度差较大导致传质动力也较大,随着吸附的进行,吸附位点不断减少,生物炭表面和溶液中Cr(Ⅵ)的浓度差逐渐减小,加之Cr(Ⅵ)与生物炭表面间静电斥力增大,最终造成吸附速率不断降低。比较3种生物炭样品在吸附过程中的表现,MBC-2在前360 min内的吸附速率很大,并于720 min左右达到吸附平衡,而BC和MBC-1则先经历了前120 min短暂的快速吸附过程,之后吸附量增速缓慢,直至1440 min时接近吸附平衡,结合表1可知,MBC-2的平均孔径大于BC和MBC-1的相应值,SEM分析也观察到MBC-2表面负载铁化合物颗粒较MBC-1更粗大,因而MBC-2表面传递和孔内扩散的阻力较BC和MBC-1更小,所以其达到吸附平衡耗时较短。该实验结果通过拟一级动力学和拟二级动力学进行拟合,拟一级动力学模型表达式为
qt=qe[1-exp(-k1t)]
(2)
拟二级动力学模型表达式为
(3)
式(2)~式(3)中,qe为平衡吸附量,mg·g-1;qt为t时刻的吸附量,mg·g-1;k1为拟一级动力学速率常数,min-1;k2为拟二级动力学速率常数,g·mg-1·min-1。拟合曲线见图8,相关拟合参数见表3。结合图8和表3拟合结果可知,3种生物炭样品对应的拟二级动力学相关系数R2均比拟一级动力学相应值R1更接近于1,平衡吸附量的拟二级动力学拟合值与其实验值十分接近,且MBC-2的拟二级动力学速率常数k2大于MBC-1的相应值,可以认为MBC-2的吸附速率较MBC-1更大,这与吸附动力学实验结果吻合,上述吸附动力学分析表明,BC、MBC-1和MBC-2对Cr(Ⅵ)的吸附符合拟二级动力9学模型,吸附过程存在Cr(Ⅵ)与吸附剂官能基团间的氧化还原反应以及以络合作用为主的化学吸附效应[18]。

图7 吸附动力学曲线

(a)拟一级动力学

(b)拟二级动力学
为确定吸附过程中的吸附机制,采用Weber-Mornis模型拟合实验结果,其方程表达式为
qt=kidt0.5+C
(4)
式中,kid为颗粒内扩散速率系数,mg·(g·min0.5)-1;C是与边界层厚度有关的常数,mg·g-1。拟合曲线及相关参数分别见图9及表4,表4中Rn为相关系数。综合图9及表4拟合结果可知,分别以3种生物炭样品作为吸附剂时,相应的拟合曲线均可分为2个阶段,第1阶段直线斜率较大,吸附速率较快,为表面扩散阶段;第2阶段为吸附剂的颗粒内扩散阶段,此时吸附剂表面吸附基本完成,开始进入吸附剂内表面吸附,此时C值高于第1阶段相应值,反映出边界层阻力增大,吸附速率逐渐减小。此外,阶段1、2中qt与t0.5线性关系良好,但拟合曲线都不经过原点,表明颗粒内扩散不是唯一的速控因素,吸附速率同时还受颗粒外扩散的影响。

图9 Weber-Morris模型拟合曲线
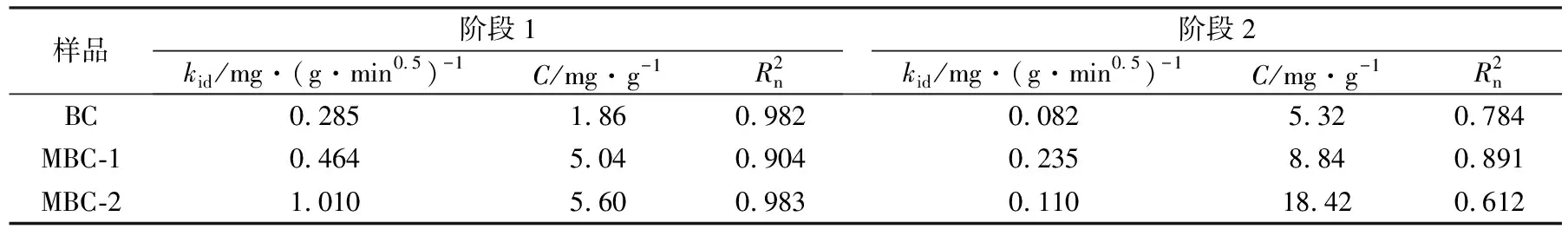
表4 Weber-Morris模型拟合参数
2.4 等温吸附
当Cr(Ⅵ)溶液初始pH值为2、振荡速率为150 r·min-1、实验温度为30 ℃时,3种生物炭样品对Cr(Ⅵ)的等温吸附曲线如图10所示。由图10可见,3种样品对Cr(Ⅵ)的平衡吸附量均随着Cr(Ⅵ)溶液平衡浓度的增加呈现出先增加而后趋于稳定的变化趋势,且改性后的生物炭样品对Cr(Ⅵ)的平衡吸附量较改性前显著提高,这是因Fe的负载增大了生物炭的比表面积和孔体积,使得生物炭表面有效吸附位点增多所致。
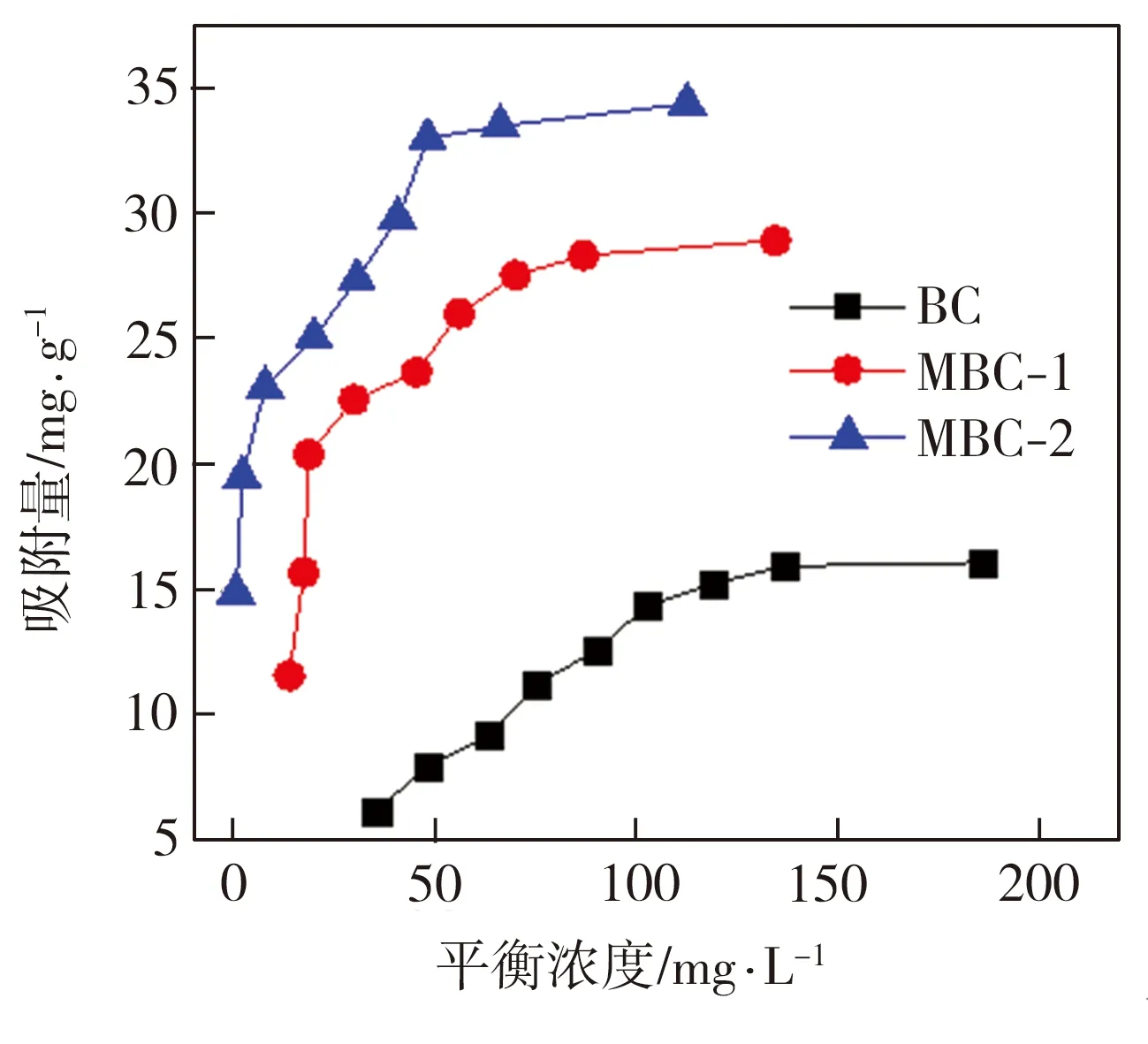
图10 等温吸附曲线
分别采用Langmuir[19]和Freundlich[20]模型对图10所示等温吸附曲线进行线性拟合,相关参数如表5所示,表中qmax为理论最大吸附量,kL为Langmuir方程常数,RT为相关系数,kF和n为Freundlich方程常数。由表5可见,基于Langmuir模型,MBC-2样品对应的kL值远大于BC和MBC-1样品相应值,表明在3种样品中,MBC-2对Cr(Ⅵ)的吸附结合力最强。MBC-1对Cr(Ⅵ)的吸附结合力较BC也有大幅提高,表明通过负载铁在生物炭表面引入了含铁基团,同时还使原始生物炭的比表面积和孔体积增大,均有利于提高生物炭吸附Cr(Ⅵ)的能力。此外,根据Lang-muir方程,计算出BC的分离因子RL值介于0.3175~0.6596之间,MBC-1的RL值介于0.0644~0.2229之间,MBC-2的RL值介于0.0172~0.0678之间,这表明Cr(Ⅵ)易被吸附到这3种生物炭表面,其中MBC-1和MBC-2的RL值更趋近于0,表明MBC-1和MBC-2吸附Cr(Ⅵ)的过程具有不可逆化学吸附特征[21]。另外,3种样品的RL值均随着溶液初始浓度的增加而降低,表明溶液高浓度条件更有利于Cr(Ⅵ)的吸附。基于Freundlich模型,3种生物炭的n值都大于1,也表明三者均易于吸附Cr(Ⅵ)。MBC-1和MBC-2的kF值均大于BC的相应值,同样表明含铁基团的引入有利于提高生物炭对Cr(Ⅵ)的吸附能力。比较Langmuir模型和Freundlich模型拟合条件下的相关系数RT值可知,Langmuir模型较Freundlich模型能更好地描述生物炭对Cr(Ⅵ)的吸附过程。按Langmuir模型拟合结果,本研究中负载铁后的MBC-1和MBC-2样品对溶液中Cr(Ⅵ)的理论最大吸附量分别达到33.36、35.25 mg·g-1,明显高于张英[22]所制小麦秸秆生物炭(17.92 mg·g-1)和市政污泥炭(16.95 mg·g-1)以及Wang等[23]所制FeCl3改性柚皮(21.55 mg·g-1)的相应值,再则,因MBC-1和MBC-2具有磁性,在分离回收方面更显优势,所以实际应用价值更高。

表5 等温吸附模型拟合参数
3 结论
(1)负载铁后小麦秸秆生物炭的比表面积和孔体积增大,孔隙以中孔为主,有利于金属离子在吸附剂孔隙中的扩散。FeCl3改性生物炭(MBC-1)和FeSO4/FeCl3改性生物炭(MBC-2)具有Fe—O基团,且改性后生物炭表面成功负载了磁性颗粒,其中MBC-1上负载了γ-Fe2O3,MBC-2中同时存在γ-Fe2O3和Fe3O4,这使生物炭能够在外加磁场的作用下从水溶液中分离。
(2)在Cr(Ⅵ)溶液初始pH值为2、初始浓度为100 mg·L-1、实验温度为30 ℃、振荡器振荡速率为150 r·min-1、生物炭投加量为4 g·L-1、吸附时间为48 h的条件下,所制MBC-2对Cr(Ⅵ)的去除率高达93.9%。
(3)生物炭对Cr(Ⅵ)的吸附符合拟二级动力学模型,MBC-1和MBC-2吸附Cr(Ⅵ)的过程具有明显化学吸附不可逆特征。改性后生物炭的吸附容量、Langmuir吸附常数kL和Freundlich吸附常数kF均远大于原始生物炭,表明负载铁有利于提高生物炭的吸附性能。

