甲状腺细胞病理学Bethesda报告系统的更新及研究进展
周一帆 王建华 徐书杭
1南京中医药大学附属中西医结合医院(江苏省中医药研究院)普外科 210028; 2南京中医药大学附属中西医结合医院(江苏省中医药研究院)内分泌科 210028
细针穿刺细胞学(FNAC)检查被认为是甲状腺结节评估术前中最准确、最具性价比的诊断手段。许多研究已经表明,在超声评估的基础上,对符合指征的甲状腺结节行FNAC,可有效提高诊断率,减少良性病变的不必要手术。甲状腺细胞病理学Bethesda报告系统(TBSRTC)是目前最广为接受的甲状腺细胞学报告系统,它建立并提供了统一的甲状腺细胞学诊断术语和评判标准,有利于促进细胞病理学家和临床医生之间的沟通,也使世界各地临床研究机构之间的研究交流更为简便可靠。自2007年第1版提出至今,TBSRTC已被美国甲状腺学会(ATA)的成人与儿童甲状腺结节管理指南多次推荐[1-2]。随着临床广泛应用和研究逐步深入,该报告系统也逐步得到完善和更新。2017年,第二版TBSRTC得以问世[3]。临床医师熟悉该报告系统更新的要点,掌握它的临床应用,对于进一步推动甲状腺结节规范化管理具有重要的临床意义。
1 新版TBSRTC更新要点
新版TBSRTC延用了旧版TBSRTC的分类类型,即:Ⅰ类(UD/UNS),标本无法诊断或不满意;Ⅱ类(B),良性病变;Ⅲ类(AUS/FLUS),意义不明的细胞非典型病变或滤泡性病变;Ⅳ类(FN/SFN),滤泡性肿瘤或可疑滤泡性肿瘤,其中嗜酸细胞型(即Hürthle细胞型)需特殊标明;Ⅴ类(SM),可疑恶性肿瘤;Ⅵ类(M),恶性肿瘤。每个类型都提供对应的恶性风险范围及推荐的临床处置措施。与此同时,纳入了近几年颇受关注的“具有乳头状核特征的非浸润性甲状腺滤泡性肿瘤(NIFTP)”亚型[4]。NIFTP是“非浸润性包裹性滤泡型甲状腺乳头状癌(EFVPTC)”的重命名,该肿瘤以前被归类为癌,但现在认为它只是具有低恶性潜能的肿瘤。NIFTP主要归类于细胞学不确定类别(Ⅲ、Ⅳ、Ⅴ类)中[5-6]。新版TBSRTC重新定义Ⅳ类和Ⅵ类界定标准的同时,也将NIFTP纳入并根据是否将其视为恶性肿瘤而分别计算了恶性风险率。最后,结合2015年ATA关于成人甲状腺结节与分化型甲状腺癌管理指南提出的,运用分子标志物鉴别诊断甲状腺结节的推荐[1],新版TBSRTC将分子标志物检测作为Ⅲ、Ⅳ类结节可选择的临床处理方式之一。
1.1 Ⅰ类结节 旧版TBSRTC中,满意的细针穿刺细胞(FNA)标本至少需要6组甲状腺滤泡细胞,每组至少应含有10个细胞,而且这些滤泡细胞团块应该保存完好、适于观察[7]。而新版TBSRTC中,只要满足以下任一特殊情况,就能直接判定为标本满意:(1)胶质结节,为充满胶体、极度扩张的滤泡,完全由胶质组成。(2)有炎性反应的结节(通常出现在自身免疫、传染性或慢性炎性甲状腺疾病的情况),在大量胶质和炎性反应细胞的存在下,少数滤泡细胞足以将结节诊断为良性。(3)纯囊性结节,根据临床特征及超声影像即可判断其是否为满意标本。一项纳入近年8项研究共25 445例甲状腺结节的荟萃分析显示,Ⅰ类结节的恶性率介于1.8%~23.6%[2],显著高于早期推荐的1%~4%。但考虑到术后样本多来自于临床特征或超声怀疑恶性的重复穿刺结节,存在选择性偏倚,新版TBSRTC将Ⅰ类恶性风险率修订为5%~10%。
1.2 Ⅱ类结节 新版TBSRTC对Ⅱ类结节的处理未做改变,只是将其恶性风险率从<1%~3%调整为0~3%。
1.3 Ⅲ类结节 自TBSRTC产生以来,此类结节一直是临床研究的关注点。因为仅有少数Ⅲ类结节因结合超声、分子检测等风险评估后接受了手术治疗,此类结节的恶性风险易被高估[8-11]。反言之,如将其他未接受手术治疗的结节假定为良性,就可能低估了Ⅲ类结节的恶性风险。因此,评估其真实的恶性风险极具挑战性。既往已有不少研究发现,术后诊断为NIFTP的结节术前多为Ⅲ类结节。故而,在新版TBSRTC中,根据是否将NIFTP归为恶性,将Ⅲ类结节的恶性风险分别调整为6%~18%(NIFTP≠癌)、10%~30%(NIFTP=癌),高于旧版TBSRTC推荐的恶性风险率(5%~15%)。
意义不明的细胞非典型病变(AUS)或滤泡性病变(FLUS)是同义词,但意义不尽相同,后者仅用于意义并不明确的滤泡性病变,而非滤泡旁细胞、淋巴和甲状旁腺等非滤泡细胞起源的病变,推荐仅选择使用其中一个作为细胞学诊断结果。在细胞学上,因Ⅲ类结节的组成较为复杂,不同类别的恶性风险率由高到低跨度较大,新版TBSRTC建议可对Ⅲ类结节进行再分类,包括核非典型、结构非典型、细胞和结构非典型、嗜酸性细胞、无特别说明的非典型。但是否再分类,总体上并不影响对此类结节的临床管理决策。对Ⅲ类结节的处置,新版TBSRTC在重复穿刺的基础上增加了分子标记物检测和诊断性甲状腺腺叶切除。应注意尽量减少AUS/FLUS这一类细胞学诊断,考虑到自TBSRTC应用以来将其诊断率控制在7%以下难度较大,新版系统推荐控制在10%以下更为适宜。
1.4 Ⅳ类结节 旧版将FN/SFN定义为由滤泡细胞组成,细胞排列方式变化大,细胞结构改变明显,特征性表现为细胞明显拥挤和(或)细胞微滤泡形成。如出现乳头状癌核的特点,则不属于此类。考虑到NIFTP,新版TBSRTC将无真乳头和核内包涵体的轻度核异型性[包括核增大、核轮廓不规则和(或)透明染色质]纳入该分类中,并将恶性风险率由20%~30%调整为10%~40%(NIFTP≠癌)和25%~40%(NIFTP=癌)。研究显示,Ⅳ类结节诊断性腺叶切除术后的组织学中,大部分是增生性结节或滤泡性腺瘤,小部分是甲状腺滤泡状癌,还有一些与包裹性滤泡型甲状腺乳头状癌对应[12]。新版对诊断术语的修订及NIFTP的引入,有可能减少Ⅳ类结节中甲状腺乳头状癌(PTC)的检出率,继而降低了其恶性风险[5-6,8]。因细胞学检查无法评估结节包膜或血管侵犯,既往推荐对Ⅳ类结节行诊断性切除,新版系统接纳ATA指南的推荐[1],也可对Ⅳ类结节行分子标志物检测,如Afirma基因分类器[13]。
1.5 Ⅴ类结节 Ⅴ类结节包括最常见的PTC、甲状腺髓样癌、低分化甲状腺癌或甲状腺未分化癌。因未完全满足诊断这些肿瘤的细胞学标准但已高度怀疑,故归入Ⅴ类。新版TBSRTC将其恶性风险率由60%~75%调整为45%~60%(NIFTP≠癌)和50%~75%(NIFTP=癌)。但考虑到此类结节恶性风险较高,一些阳性预测值较高的分子标志物检测可能具有一定价值。新版系统仍推荐腺叶切除或全切,尤其是对存在突变(BRAFV600E、TERT启动子、p53等)、超声检查可疑或体积较大(>4 cm)患者。
1.6 Ⅵ类结节 为保证Ⅵ类结节的高阳性预测值,新版TBSRTC中此类仅包含具有PTC多个典型核特征的病例[包括核增大,核膜不规则,常见核沟,透明染色质和(或)核内包涵体]。NIFTP虽然具有乳头状细胞核特征,但较少有发育良好的核异型,且几乎从未具有核内含物。得益于界定标准的改变,Ⅵ类结节的恶性风险率受NIFTP影响较小(NIFTP≠癌 94%~96%,NIFTP=癌97%~99%),与既往类似(97%~99%)。尽管手术仍是Ⅵ类结节的处置方式,但结合ATA指南对低危乳头状癌可行腺叶切除的推荐[1],新版TBSRTC对Ⅵ类结节的处理方式扩展为近全切除或腺叶切除(表1)。
2 TBSRTC在国内的应用与相关研究
TBSRTC已在世界范围和国内得到了应用和实践。由于在术前无法诊断NIFTP,故已发表的相关研究几乎均是参照旧版TBSRTC进行分类和处理。在国内的临床研究中,TBSRTC的敏感性、特异性、阳性预测值、阴性预测值分别为82.61%、74.42%、63.33%、88.89%[9]。然而,相当比例的FNAC结果为细胞学结果不确定(TBSRTC Ⅲ、Ⅳ、Ⅴ类),此类甲状腺结节仍是临床应对的巨大挑战。将不同的术前诊断方式联合,可能有助于提高诊断性能。血清学检查是术前诊断甲状腺疾病的常用方式,尤其是甲状腺功能检测、降钙素、癌胚抗原、甲状旁腺激素等有助于辅助判断结节性质。除此外,超声、粗针活检和分子检测可能是相对较为有效的联合诊断方式。
临床中广为应用的甲状腺超声是最为常用的联合诊断方法,包括超声造影、弹性超声和甲状腺成像报告和数据系统(TI-RADS)。2014年,严佳梅等[10]联合TBSRTC与超声造影观察了184例甲状腺结节,结果显示最大直径≤1 cm的结节,联合超声能够提高甲状腺结节诊断的敏感性和准确性。早有研究表明,TI-RADS评分能够改进不确定类型结节的风险评估[14]。笔者研究表明,美国放射学会的TI-RADS对细胞学不确定结节具有较好的诊断价值,TI-RADS联合TBSRTC能够达到最佳诊断效率[15]。与国际上研究类似,来自国内多个中心的研究均发现,TI-RADS联合TBSRTC诊断时普遍存在特异性降低的问题[15-19]。
粗针活检可能是明确细胞学结果不明确结节的方法。Trimboli和Giovanella[20]纳入了5项研究进行荟萃分析,结果发现,对于细胞学结果不确定的甲状腺结节,粗针活检恶性的正确诊断率为83%,良性的正确诊断率为84%。这表明粗针活检可正确诊断大多数细胞学结果不确定的甲状腺结节。国内Li等[21]对578例甲状腺结节粗针活检结果与术后病理报告对比,结果证实,粗针活检诊断甲状腺结节性质的敏感性和特异性分别高达95.93%和97.30%。因此,对于细胞学结果不确定的甲状腺结节,必要时可考虑行粗针活检。
分子检测是目前最受关注的新技术,目前国内主要检测BRAFV600E突变为主。包括本研究组在内的多个研究中心的研究表明,BRAFV600E突变检测比TI-RADS、TBSRTC诊断的敏感性和特异性均更高,联合后显著提高诊断效能[16,21]。因此,对于细胞学不确定的结节,适当的分子检测联合诊断可有助于明确结节性质。
3 小结
TBSRTC作为解读甲状腺细胞病理学特征的方法,已经成为甲状腺结节穿刺诊断不可或缺的报告系统。经过10余年的临床实践和研究,新版TBSRTC考虑了NIFTP出现后引发的相应变化,更新
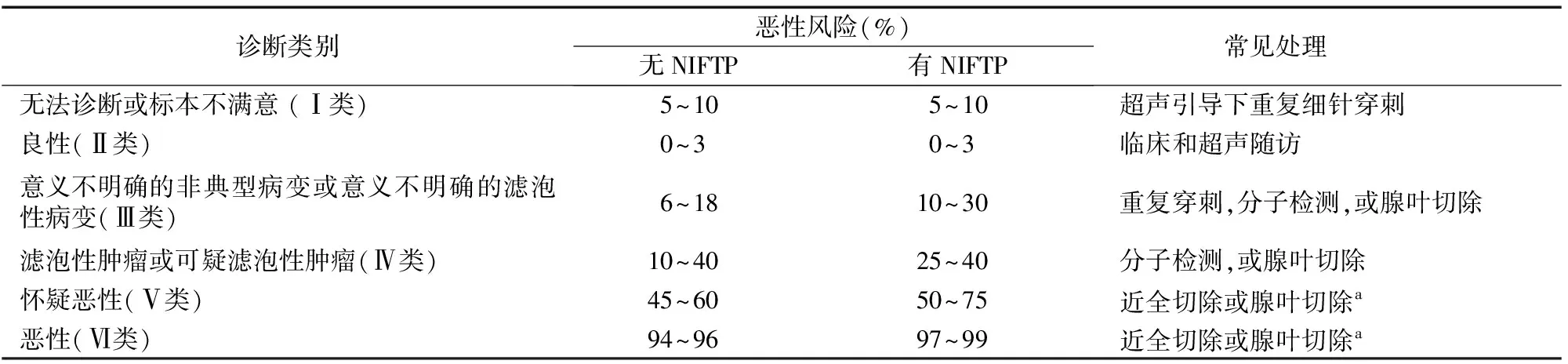
表1 甲状腺细胞病理学Bethesda报告系统:相应的恶性风险及常见临床处理
注:a“怀疑恶性”或者“恶性”若提示为转移癌而非甲状腺原发癌,则应根据情况相应处理,不一定需手术;NIFTP:具有乳头状核特征的非浸润性甲状腺滤泡性肿瘤
了分子检测推荐,不管是在恶性风险率的设置上还是处理方式的选择上都更加丰富、周全。因此,应进一步推动新版TBSRTC的应用和普及,以利于提高基层医院的临床诊疗水平,为患者制定个性化的诊疗方案。

