剥脱综合征白内障者单个核细胞中Notch2基因及其靶蛋白表达研究
丁 琳 王慧琴 凯迪丽亚·阿力甫 买尔哈巴·米吉提 吴卫东
剥脱综合征(exfoliation syndrome)是一种全身性的细胞外基质疾病,与年龄相关。在眼部主要表现为无定形蛋白质碎屑沉积于晶状体前囊、基膜的其他眼组织上,沉积物呈灰白色或蓝白色[1~3]。可继发青光眼,加速白内障的进展,并能增加术中和术后并发症。目前剥脱综合征的发病机制尚不明确,研究表明剥脱综合征是一种多基因遗传并受多因素调控的疾病,地区高发剥脱综合征型白内障患者的病情加速进展及预后值得关注[4~6]。因此本研究在课题组前期工作的基础上就信号通路中重要的受体基因Notch2及其靶蛋白表达进行检测,试探讨Notch2基因及其靶蛋白Notch2与剥脱综合征白内障发病的相关性。
对象与方法
1.研究对象:选取2016~2018年在新疆维吾尔自治区人民医院眼科就诊或住院的剥脱综合征白内障患者18例,其中,男性9例,女性9例;患者年龄45~79(68.17±10.42)岁。选择同一时期来笔者医院体检的无相关病史的健康人群作为正常对照组,正常对照组18例,男女性别比为1∶1;年龄46~80岁(69.11±8.59)岁。采集研究对象外周血5~10ml。
2.纳入、排除标准:所有患者参照Ritch R剥脱综合征的诊断标准;本研究获得医院医学伦理学委员会批准,所有患者或监护人均已签署知情同意书。两组人群均排除眼科手术史、恶性肿瘤、自身免疫性疾病、高血压、糖尿病、强烈红外线接触史。女性患者排除妊娠、哺乳及月经期。
3.外周血单个核细胞(peripheral blood mononuclear cell,PBMC)分离:将采集的静脉血5ml注入盛有等量缓冲液的EP管中,充分混匀。将淋巴细胞分层液3ml加入EP管中,随后注入稀释抗凝血液沿管壁加至分层液上,保持两者界面清晰。室温2000r/min离心20min,管内可分为4层。轻轻吸出乳白色的单个核细胞层,加入另一支已含有4ml PBS的离心管中混匀。室温下,1500r/min离心10min。弃上清,重复洗涤1次。
4.Notch2基因表达量的检测:(1)提取总RNA:按MiRNeasy Mini kit提取试剂盒(德国凯杰公司)说明书进行,收集外周血单个核细胞,然后按步骤添加试剂提取样本总RNA。用超微量核酸蛋白测定仪(美国Thermo公司)测定提取物浓度及纯度,A260/A280比值为1.8~2.2,用于后续实验。(2)反转录合成cDNA:使用miScript Ⅱ RT kit(德国凯杰公司),按反转录试剂盒说明书操作,上样于Bio-Rad C1000 Touch PCR 仪(美国伯乐公司)。反应体系20μl:5×HIFlex Buffer 4μl,10×Nucleics Mix 2μl,RT Enzyme Mix 2μl,Total RNA(浓度约20mg/L)+RNase-Free H2O2共12μl。反应条件:37℃ 60min,95℃ 5min。(3)实时荧光定量PCR反应:应用QuantiFast SYBR®Green PCR kit 试剂盒(德国凯杰公司),引物购自德国凯杰成品序列,其引物序列为专利产品。反应体系20μl:2×QuantiFast SYBR Green PCR Master Mix 10μl,10×miScript Primer Assay 2μl,10×miScript Universal Primer 2μl,RNase-Free H2O25μl,模板cDNA 1μl。反应在荧光定量PCR仪(Rotor Gene-Q德国)上进行,反应条件:95℃ 15min,1个循环;94℃ 15s,55℃ 30s,70℃ 30s,40个循环。每个样本做3个复孔,在相同反应条件下同时检测Notch2和GAPDH的扩增情况,程序运行结束后利用Rotor-Gene Q Series Software软件进行数据分析。
5.免疫印迹法检测Notch2蛋白表达量:将RIPA裂解液加入所收集的单个核细胞团中,提取蛋白,BCA法测定蛋白提取物浓度。12%分离胶进行SDS-PAGE电泳;蛋白样本分离转印至PVDF膜上,5%蛋白质干粉TBST封闭1h;TBST洗膜10min 3次,Notch2一抗(美国Abcam公司)1∶1000室温孵育1h;TBST洗膜10min 3次,二抗1∶1000室温孵育1h;TBST洗膜10min 3次,曝光获得灰度。

结 果
1.实时荧光定量PCR曲线分析:以GAPDH扩增作为参照,样本Notch2基因荧光定量扩增特异性好,扩增效率良好(图1)。Notch2基因在正常人群和剥脱综合征白内障患者中的表达水平分别为0.035±0.033、0.157±0.137,剥脱组中Notch2的表达高于正常组人群,差异有统计学意义(t=3.662,P=0.002)。
2.免疫印迹检测Notch2蛋白表达:剥脱综合征白内障患者Notch2蛋白的相对表达量为0.785±0.092,正常人群Notch2表达量为0.304±0.091,剥脱组Notch2蛋白表达量显著高于正常组,差异有统计学意义(t=15.795,P=0.000,图2)。
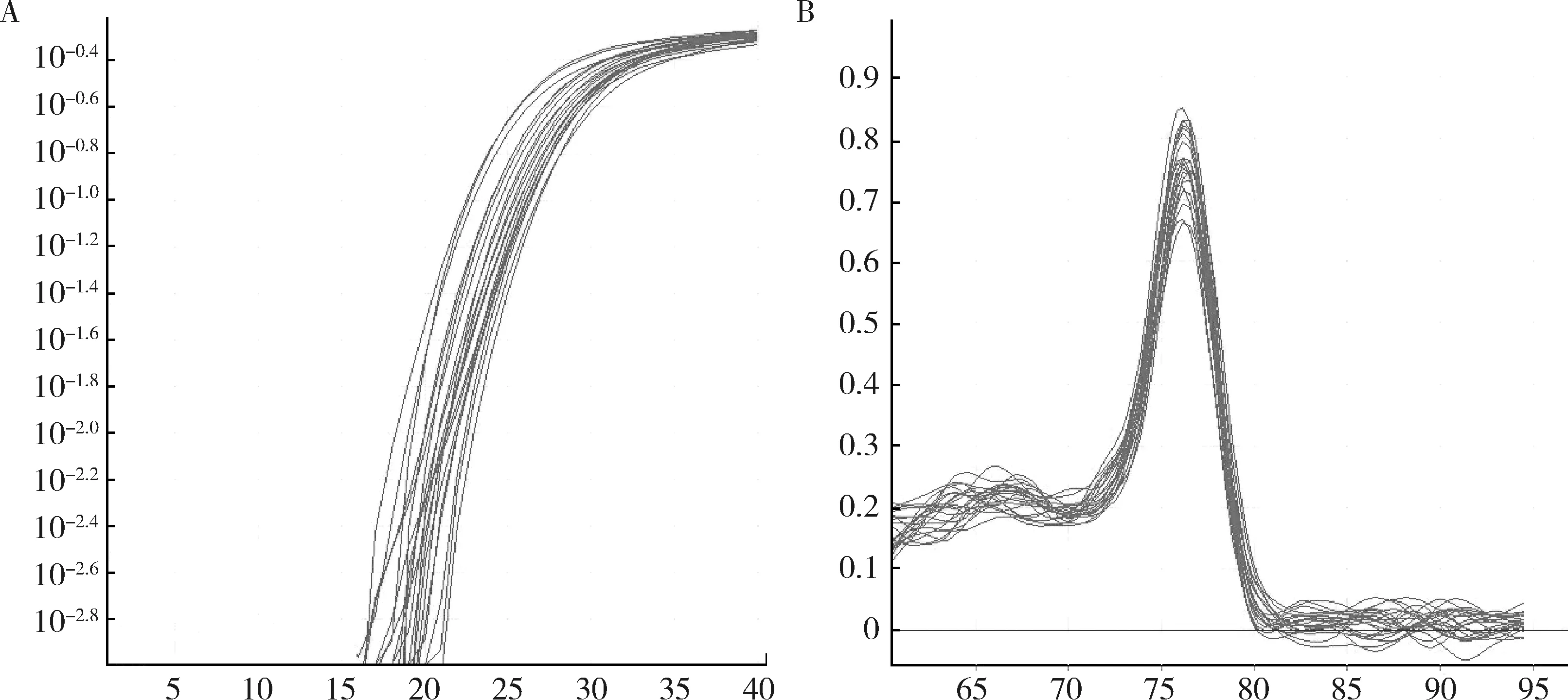
图1 实时荧光定量PCR检测Notch2基因的扩增曲线图和溶解曲线图A.Notch2扩增曲线图;B.Notch2溶解曲线图

图2 Notch2蛋白Western blot法表达水平比较图与正常人群比较,*P<0.01
讨 论
Notch基因最早发现于果蝇体内,由于其基因突变可以引起果蝇出现残翅的现象因而命名。随着研究的深入发现,Notch基因广泛表达于无脊椎动物及哺乳动物体内[7~9]。Notch基因属于跨膜受体蛋白家族,其受体蛋白分为胞外区、跨膜区和胞内区,结合配体并激活受体的部位是胞外区。Notch信号的转导可直接接受临近细胞的信号,不需通过第二信使和蛋白激酶的参与来完成。信号由此转导至细胞核,激活相关转录因子的表达[7~10]。Notch信号通路在进化上具有高度保守性,参与多个系统的发生、发育、功能等生物学活动[9~11]。研究表明Notch信号通路在胚胎发育、血管形成、血细胞形成以及肿瘤发生等的生理、病理过程中发挥重要作用[7~11]。Notch2是Notch信号通路的重要受体蛋白,其与配体结合后可酶切暴露的金属酶切位点,释放出胞内NICD。NICD进入细胞核后与转录抑制因子CSL/CBF1结合活化Hes,从而进行细胞内调控,影响细胞增殖、凋亡等过程[12~18]。剥脱综合征是一种受多基因调控,受多因素作用的系统性疾病,其眼部病变表现为不明纤维物质在眼部组织中沉积,引起房水外流受阻,从而导致眼压增高和视神经受损,并最终发展为青光眼和白内障等疾病,严重者可致盲[1~5]。
目前研究认为剥脱综合征是由遗传、环境、年龄等多因素引起的细胞外基质代谢异常性疾病[1]。在前期工作基础上笔者推测信号通路重要受体Notch2参与了眼部疾病的发生,因此本研究以Notch2为切入点通过进行实时荧光定量PCR来检测其在剥脱综合征白内障患者与正常人群外周血单个核细胞中的表达,并对其下游靶蛋白Notch2展开研究,以此探寻剥脱综合征白内障发生、发展可能的影响因素。
综上所述,实时荧光定量PCR检测结果显示,Notch2在剥脱组中的表达显著高于正常组,差异有统计学意义(t=3.662,P<0.01),推测Notch2在剥脱综合征白内障患者外周血单个核细胞中的高表达可能调控了细胞异常代谢过程,从而参与了剥脱综合征的发展过程,进而加速影响白内障恶化进程。免疫印迹实验结果显示,Notch2蛋白在剥脱组中的表达高于正常人群,差异有统计学意义(t=15.795,P<0.01),受Notch2基因调控其靶蛋白也异常表达。参与这一系列过程可能调控了信号通路,导致细胞外基质异常分泌,从而加速病理过程。与正常人群比较,剥脱综合征白内障患者外周血单个核细胞中Notch2基因呈高表达,同时Notch2蛋白表达也明显上调,这说明二者呈正相关。由整体实验结果推测Notch2基因及其靶蛋白的差异表达共同作用参与了剥脱综合征白内障的发展过程。

