磁性茶籽壳活性炭固相萃取-超高效液相色谱/质谱法测定环境水样中三嗪类除草剂
李小蒙, 邵子纯, 王旭坤, 朱雅文, 张雯宇,高仕谦*,3, 张占恩*,3
(1.苏州科技大学环境科学与工程学院,江苏苏州 215009;2.郑州大学化学与分子工程学院,河南郑州 4500013.苏州科技大学江苏省环境科学与工程重点实验室,江苏苏州 215009)
三嗪类除草剂是广泛用于农作物生长初期抑制杂草幼苗植物光合作用的一类高选择性除草剂。其咪唑环中的3个C原子和3个N原子对称排列,使其水溶性和吸收性增强[1]。该均三氮类物质环境持久性较强,容易残留于农作物、土壤和地表水中,并通过食物链进入人和其他生物体内,给生物和环境带来了潜在的危害[2]。常规检测三嗪类除草剂的方法包括毛细管电泳(CE)、气相色谱(GC)和高效液相色谱(HPLC)[3 - 5]。由于其母体结构中所含的N原子在电喷雾电离正离子(ESI+)模式下很容易被电离,因此采用质谱法检测超痕量的三嗪类除草剂残留,可以获得更理想的检出限。
三嗪类除草剂在环境基质中均以痕量形式存在,目前三嗪类除草剂常用的样品预处理方法有液-液萃取(LLE)[6]、固相萃取(SPE)[7]、固相微萃取(SPME)[8]和基质固相萃取(MSPE)[9]等。基于新型磁性吸附材料的磁性固相萃取(MSPE)技术因操作简便、萃取时间短、分离快速等特点被广泛应用[10,11]。生物质活性炭(Biological Activated Carbon,BAC)是将生物废料经过高温炭化后得到的环保型吸附剂[12],其具有较高的吸附容量,机械强度大且可再生,迄今为止各种生物质原料,包括葡萄、柚皮、花生壳、椰壳、茶籽壳等均已成功用于活性炭的制备[13 - 15]。本文以Fe3O4为磁性供体,以茶籽壳生物质炭作为过程载体,制备具有强富集能力的磁性生物质炭材料,并将其用作固相萃取吸附剂选择性富集环境样品中的三嗪类除草剂,同时结合超高效液相色谱/质谱法(UPLC/MS)进行定量分析。
1 实验部分
1.1 主要仪器和试剂
TSQ Quantum Ultra EMR三重四极杆质谱仪(美国,Thermo公司);Ultimate 3000超高效液相色谱仪(美国,戴安公司);SK-1快速混匀器(金坛市科析仪器有限公司);JJ-1精密增力电动搅拌器(金坛市科析仪器有限公司)。
7种三嗪类除草剂标准品:西玛通、西玛津、莠去通、特丁通、草净津、异戊乙净、特丁津(纯度≥98%,北京生物制品研究所),用乙腈配制成0.05 mg·L-1的单标准储备溶液,储存于4 ℃冰箱中,使用前用乙腈稀释成50.0 μg·L-1的混合标准工作溶液。色谱纯甲醇和乙腈购自美国Tedia公司;分析纯FeCl3·6H2O和FeSO4·7H2O购自国药集团试剂公司;氨水、无水乙醇(分析纯,无锡市晶科化工有限公司)。实验用水均为Milli-Q(美国Millipore)超纯水。
茶籽壳采自当地农户。
1.2 磁性生物活性炭的制备
选用茶籽壳作为生物质炭制备原料。将茶籽壳用水多次清洗后,于110 ℃下干燥4 h除去水分及挥发性杂质,粉碎筛分至200目待用。用50%的H3PO4按1∶3的体积比于室温下浸泡14 h。浸渍的材料于N2保护下600 ℃碳化1.5 h,冷却。用沸水洗涤去除灰分,于110 ℃下干燥2 h得茶籽壳生物质炭。将1 g所制备的生物质活性炭加至200 mL水中,Fe3+和Fe2+按照1∶2的摩尔比加入上述溶液中,N2保护下调节溶液的pH=10,温度升至80 ℃反应1.5 h,得到黑色沉淀,用水和乙醇交替洗涤3次至近中性,于60 ℃的真空干燥箱中干燥12 h,即得磁性茶籽壳生物质炭。
1.3 磁性固相萃取过程
准确称取23.0 mg磁性生物质活性炭于100 mL水样中,振荡萃取22 min,在外加磁场作用下收集磁性材料。倾去上清液,用1.4 mL甲醇解吸1 min,收集洗脱液,如此重复解吸2次。最后将2.8 mL解吸液N2挥干,用1 mL 80%的乙腈溶液回溶至1 mL,经0.22 μm有机滤膜过滤后,进行UPLC/MS分析。回收的磁性生物质活性炭经丙酮和水清洗净化后,可回收利用。
1.4 UPLC/MS条件
UPLC条件:Zorbax Eclipse XDB-C18色谱柱(50 mm×3 mm,1.8 μm);柱温:30 ℃;流动相:乙腈(A)∶水(B)=80∶20(V/V),等度洗脱。流速:0.3 mL·min-1;进样量:10 μL。
MS条件:扫描模式ESI+;离子传输管温度:350 ℃;喷雾温度:300 ℃;喷雾电压:3 500 V;鞘气压力:25 MPa;辅助气压力:10 MPa;碰撞气压力:1.5 mTorr。质谱参数如表1所示。

表1 7种三嗪类除草剂的保留时间、母离子、子离子和碰撞能量
2 结果与讨论
2.1 磁性生物质活性炭的表征
通过扫描电镜(SEM)和傅里叶变换红外(FT-IR)光谱研究材料的表面形貌结构,以及经过复合改性后金属颗粒物在生物质活性炭中的分布。由图1(a)可以看出生物质活性炭表面拥有丰富的微孔,这些微孔与内部的微孔相连,使得茶籽壳生物质活性炭具有较高比表面积。图1(b)中大量附着在球形表面的颗粒团簇则是Fe3O4颗粒,这些Fe3O4颗粒团簇分布均匀,说明生物质活性炭多孔结构能够有效提高Fe3O4颗粒团簇的分散性,分散性越好则吸附效果越好。图1(c)中3 419 cm-1处吸收峰主要是分子间氢键缔合的酚-OH伸缩振动,1 615和1 321 cm-1为苯环或芳香族的特征峰,1 121 cm-1处吸收峰来自C-O-C的振动,547 cm-1处较强吸收峰则属于Fe-O。数据表明,Fe3O4已成功负载于生物质活性炭上。图2为材料的比表面积和孔径分布图,材料的比表面积为115.9 cm2/g,孔体积为0.144 cm3/g,孔径为8.4 nm。

图1 生物质活性炭(a)、磁性生物质活性炭(b)的扫描电镜(SEM)照片及磁性生物质活性炭红外(IR)光谱图(c)Fig.1 SEM images of BAC(a),MBAC(b) and IR spectra of MBAC(c)
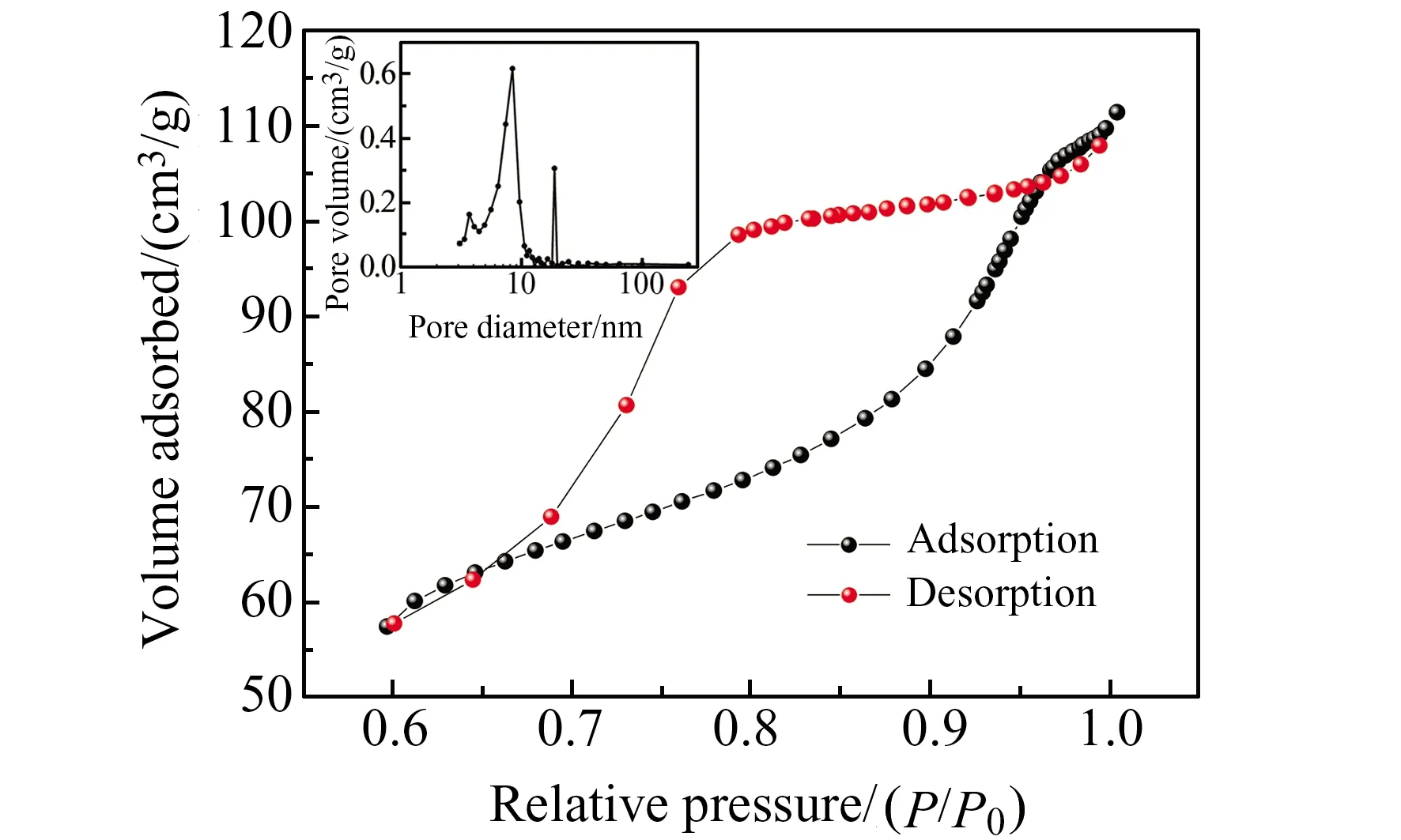
图2 磁性生物质活性炭的比表面积和孔径分布图Fig.2 BET and BJH of MBAC
2.2 磁性固相萃取条件的优化
7种三嗪类除草剂在100 mL环境水样中的加标浓度为1 μg·L-1。在磁性固相萃取中,吸附剂用量、萃取时间、解吸条件以及水样pH等因素影响萃取效率。本实验通过单因素和正交实验对以上影响因素进行优化。
2.2.1 吸附剂的用量准确称取MBAC吸附材料5.0、10.0、15.0、20.0、25.0和30.0 mg作为变量考察吸附剂用量,如图3所示。由图可知,当MBAC用量从5.0 mg增加到25.0 mg时,回收率随之增加,当其用量为25.0 mg时7种三嗪类除草剂的回收率达到最大值;继续增加MBAC用量时有部分物质回收率下降,因此选择25.0 mg MBAC为最佳吸附剂用量。
2.2.2 萃取时间的影响本实验对萃取时间(5~25 min)进行考察。如图4所示,7种除草剂的回收率随着萃取时间的增加而增加,在20 min时达到最大值,萃取时间高于20 min时萃取效率开始降低。选择最佳萃取时间为20 min。
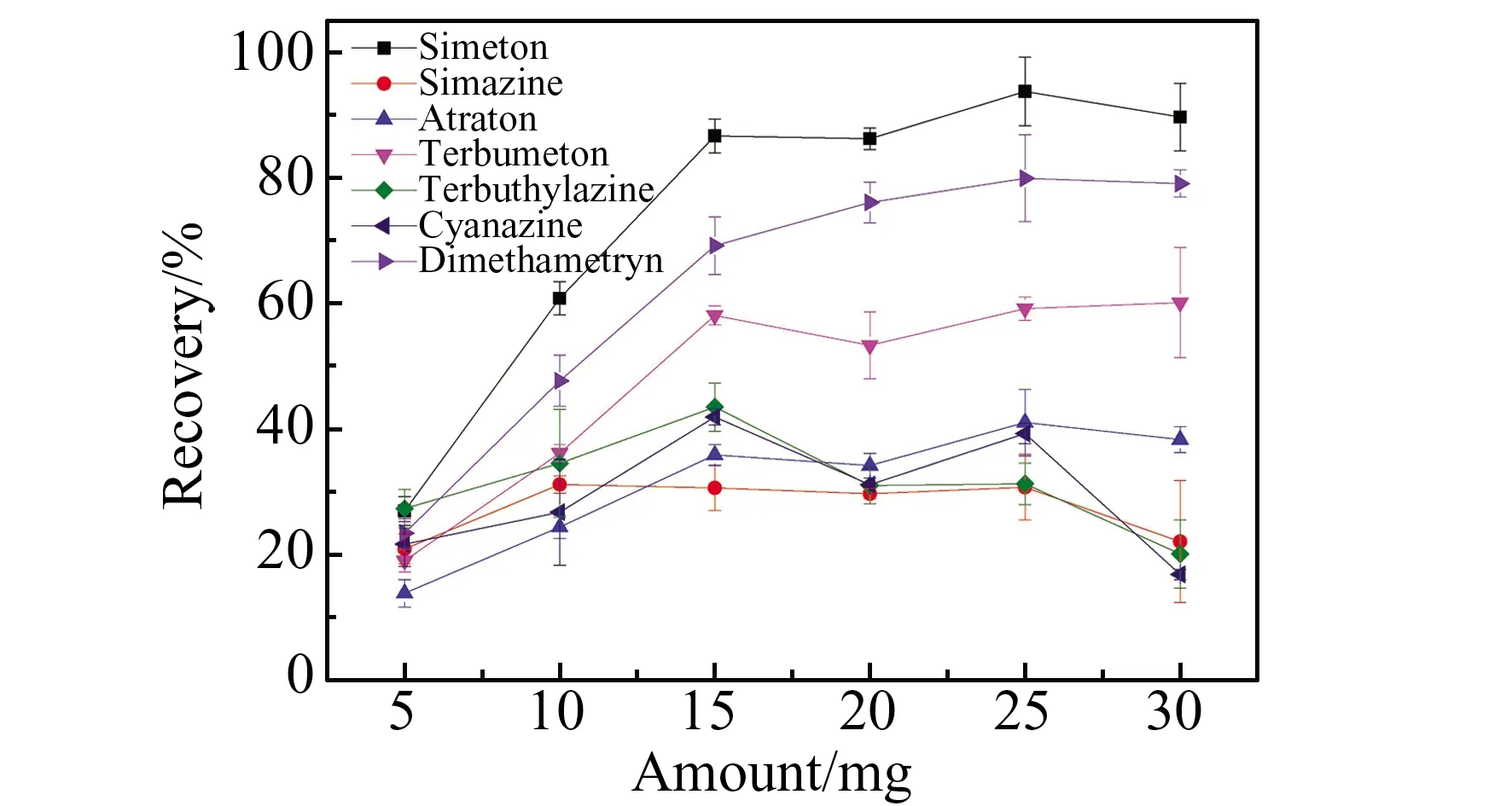
图3 磁性生物质活性炭用量对萃取效率的影响Fig.3 Effect of MBAC amount on extraction efficiency
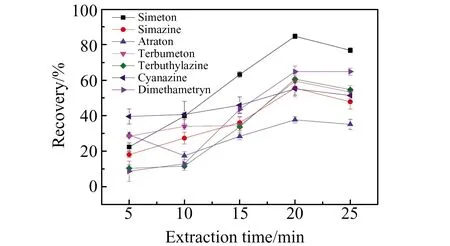
图4 萃取时间对萃取效率的影响Fig.4 Effect of extriaction time on extraction efficiency

图5 解吸溶剂体积对脱附效率的影响Fig.5 Effect of desorption solvent volume on desorption efficiency
2.2.3 解吸条件的影响三嗪类除草剂属于极性有机污染物,水溶性较强,易溶于极性有机溶剂。本实验分别对洗脱剂的类型(甲醇、乙醇、丙酮、乙腈及乙酸乙酯)、用量、解吸次数和时间进行考察。洗脱剂的平均洗脱回收率大小依次为:甲醇>丙酮>乙腈>乙醇>乙酸乙酯,选择甲醇为解吸溶剂。考察解吸溶剂在1~5 mL范围内的洗脱效率,如图5所示。解吸溶剂用量在3 mL时回收率达到最大值,选择解吸溶剂用量3 mL。对解吸次数进行考察(1 mL×3、1.5 mL×2和3 mL×1),发现洗脱2次的回收率高于其他次数,选择1.5 mL洗脱2次。考察解吸时间(2~10 min)的影响,当解吸时间为4 min时,解吸效率即可达到最大值。
2.2.4 水样pH的影响溶液pH通过影响化合物的现有存在形态影响生物炭材料表面与除草剂作用位点。在本实验中通过稀HCl和NaOH溶液调节水样pH,发现pH在5.0~9.0变化时,各物质的萃取效率无明显变化,因此实验中不需要调节水样pH。
2.3 正交试验
2.4 方法的线性范围和检出限
配制系列浓度的7种三嗪类除草剂的混合标准溶液,绘制标准曲线,以标准溶液浓度(x)对色谱峰面积(y)作线性拟合,结果如表2所示。西玛通和特丁津在1.0~500 ng·L-1范围内,西玛津和草净津在5.0~500 ng·L-1范围内,莠去通、特丁通和异戊乙净在0.5~500 ng·L-1范围内,都有着良好的线性关系,相关系数高于0.9980,7种三嗪类除草剂的检出限(S/N=3)在0.1~1.0 ng·L-1范围内。日间和日内精密度(RSD)分别为2.3%~6.1%和4.3%~9.5%。表明本方法的精密度和灵敏度都较为理想。
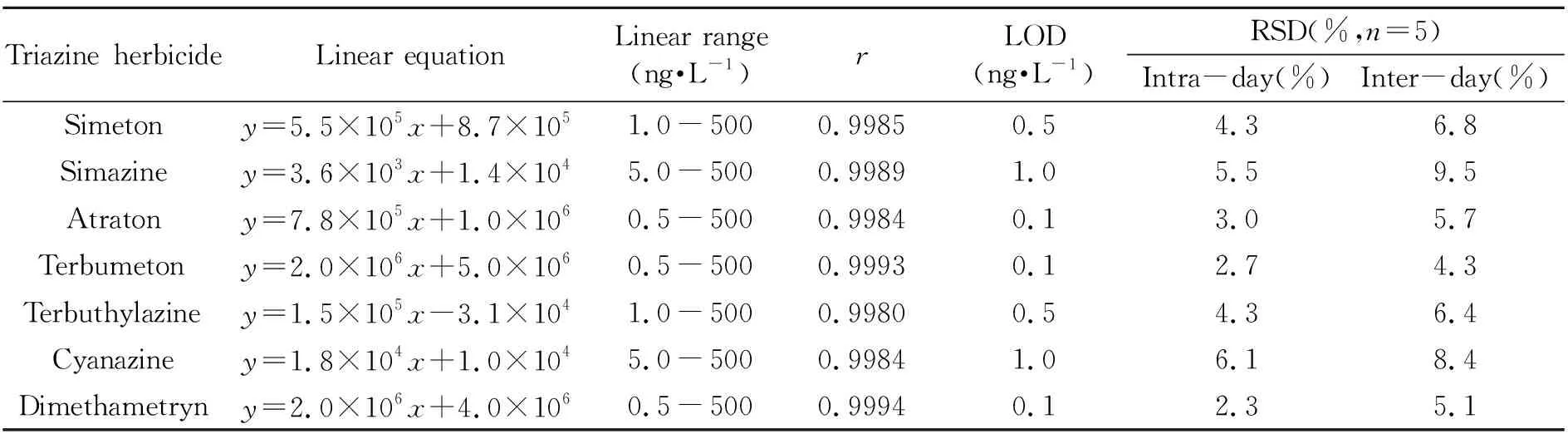
表2 7种三嗪类除草剂的线性方程、相关系数、检出限(LOD)及相对标准偏差(RSD)
2.5 实际水样的测定
实验选取了太湖水样和当地第一污水处理厂的中段水样两个实际水样进行测定。采集回来的水样通过0.45 μm的滤膜过滤后,进行测定(n=5),实际水样中未检测出7种三嗪类除草剂的残留。然后,选择了20.0、100.0 ng·L-1两个浓度水平进行加标(n=5)回收试验,结果见表3。7种三嗪类除草剂的加标回收率在79.9%~103.3%之间,RSD为1.3%~9.6%,说明该方法能满足对实际水样的检测。

表3 7种三嗪类除草剂的回收率和相对标准偏差(n=5)
(续表3)
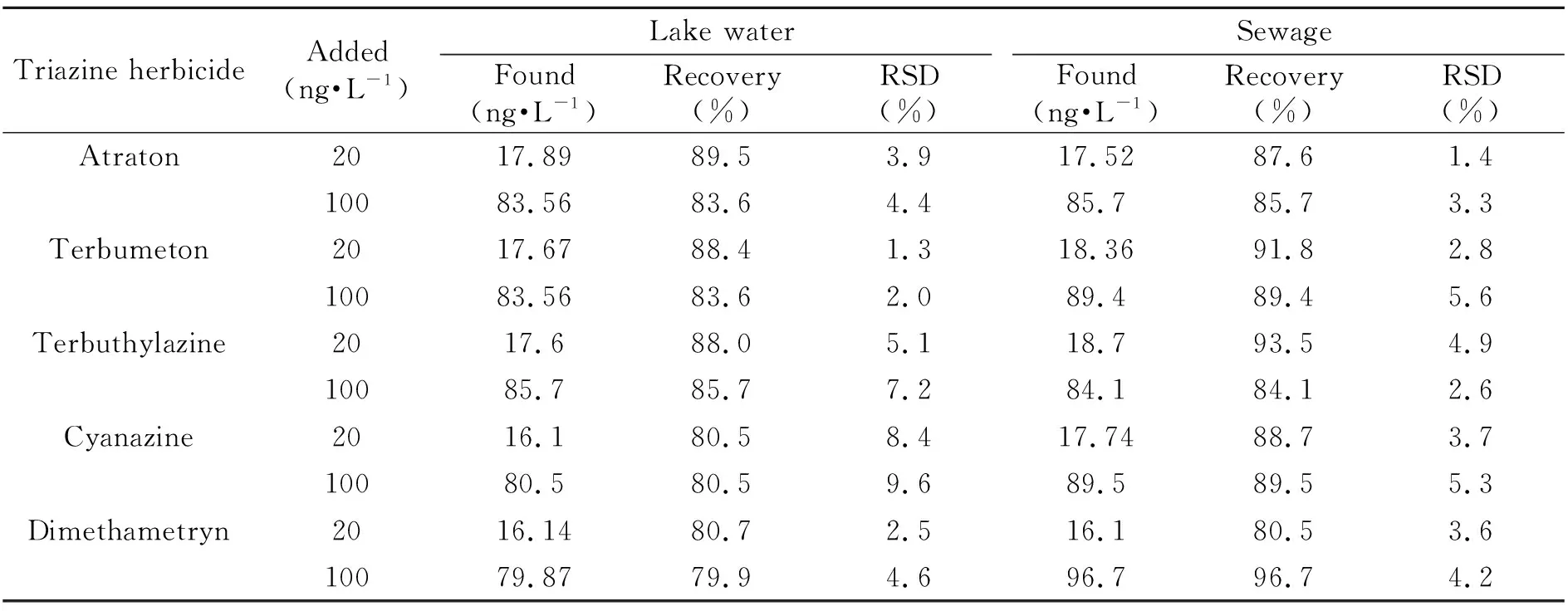
Triazine herbicideAdded(ng·L-1)Lake waterSewageFound(ng·L-1)Recovery(%)RSD(%)Found(ng·L-1)Recovery(%)RSD(%)Atraton2017.8989.53.917.5287.61.410083.5683.64.485.785.73.3Terbumeton2017.6788.41.318.3691.82.810083.5683.62.089.489.45.6Terbuthylazine2017.688.05.118.793.54.910085.785.77.284.184.12.6Cyanazine2016.180.58.417.7488.73.710080.580.59.689.589.55.3Dimethametryn2016.1480.72.516.180.53.610079.8779.94.696.796.74.2
2.6 与其他及同类方法的比较
将本方法与其他(SPE)及同类(MSPE)方法在吸附剂、吸附剂用量、洗脱剂、萃取时间、检出限和回收率等方面进行了比较,结果见表4。本方法在吸附剂用量、萃取时间上优于其他方法,并且检出限低。
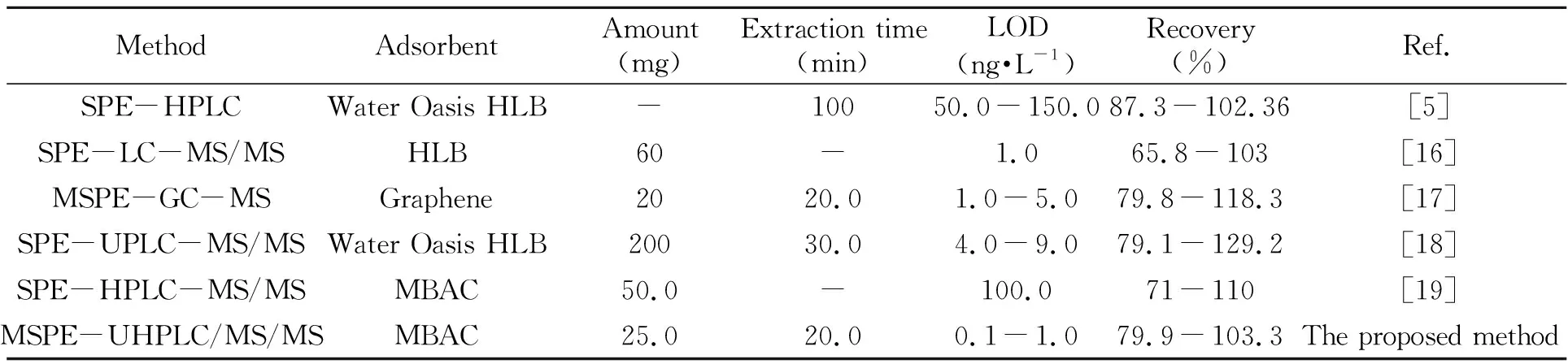
表4 本方法与其他方法对比
3 结论
采用茶籽壳作为吸附剂基体,用一步合成法制备磁性生物质活性炭。将磁性固相萃取法与UPLC-MS结合检测环境水样中7种三嗪类除草剂农药残留。结果显示该方法在0.5~500 ng·L-1范围内可以得到良好的线性关系,实际环境水样中的除草剂回收率在79.9%~103.3%范围内,相对标准偏差低于9.6%。便捷的磁分离和生物质活性炭的强吸附能力使得本方法具有操作简便、快捷和准确,可应用于实际水样中痕量三嗪类除草剂的测定。

