2018年我院药物不良反应报告分析
孙莹

[摘要] 目的 掌握我院藥物不良反应(ADR)发生频次及特点,为临床安全合理用药提供参考。 方法 回顾性分析2018年1~12月于我院住院治疗并上报ADR的181例报告进行汇总,并对年龄、性别、涉及药品种类等多项资料进行归纳整理。 结果 在研究的181份ADR报告中,男性ADR发生率显著低于女性,且随着年龄的增高,ADR发生频次更高。上报例数排名前三的科室为肿瘤外科、呼吸内科和消化内科。最常见的引发ADR的给药方式为静脉给药,占比全部上报ADR的76.24%。在临床各类药品中,抗肿瘤药物及抗感染药物导致ADR出现的概率更高,临床的常见表现包括全身性损害、消化系统和血液系统损害等。按临床关联性标准评价,“肯定”、“很可能”、“可能”和“待评价”分别占比46.96%、38.67%、11.61%和2.76%。按照报告类型分类,已知的一般反应、新的不良反应、严重不良反应分别为147例(81.21%)、19例(10.50%)和15例(8.29%)。 结论 抗肿瘤药物和抗感染药物在临床使用过程中ADR发生频次最高,这可能与药物本身结构及性质有关,临床应加强对此类药物的监控及管理,同时针对该类药物常见不良反应,临床应定期组织医护人员进行该类药物ADR发生的处理培训。
[关键词] 不良反应;合理用药;肿瘤; 感染
[中图分类号] R95 [文献标识码] B [文章编号] 1673-9701(2020)09-0130-04
[Abstract] Objective To know the frequency and characteristics of adverse drug reactions(ADR) in our hospital, and to provide a reference for clinically safe and rational drug use. Methods 181 patients admitted to our hospital from January to December 2018 with ADR reported were retrospectively analyzed, and the age, gender, and types of drugs involved were summarized. Results Among the 181 ADR reports, the incidence of ADR in male was significantly lower than that in female, and the incidence of ADR was higher as age grew. The top three departments with the most reported cases were oncology surgery, respiratory medicine, and gastroenterology. The most common channel inducing ADR was intravenous administration, accounting for 76.24% of all reported ADR. Among various clinical drugs, anti-tumor drugs and anti-infectious drugs caused higher probability of ADR. Common clinical manifestations included systemic damage, digestive system and blood system damage, etc. According to the clinical relevance criteria, the number of “affirmative”, “very likely”, “possible”, and “to be evaluated” accounted for 46.96%, 38.67%, 11.61%, and 2.76%, respectively. According to the type of report, 147 cases (81.21%), 19 cases (10.50%), and 15 cases (8.29%) were known general reactions, new adverse reactions, and severe adverse reactions, respectively. Conclusion Anti-tumor drugs and anti-infective drugs have the highest frequency of ADR during clinical use, which may be related to the structure and properties of the drug itself. The clinical monitoring and management of such drugs should be strengthened. Medical personnel should be regularly organized to conduct training concerning the dealing of ADR caused by such drugs.
[Key words] Adverse reactions; Rational drug use; Tumor; Infection
药物不良反应(adverse drug reactions,ADRs)是指正常剂量的药物用于预防、诊断、治疗疾病或调节生理机能时出现有害的、与用药目的无关的反应[1]。国家食品药品监督管理局联合卫生部于2004年颁布了《药品不良反应报告和监测管理办法》,并于2011年进行修订[2-4],自管理办法新修订以来,我院及时调整药品ADR报告和监测的管理,并组织相关专业技术人员进行培训工作。目前,关于各医疗机构药物不良反应进行总结的文献较多,且多数集中来源于省级三级甲等医院,而市级医院和基层医院来源的数据较少,这可能与基层医院药物不良反应管理强度不足、专职人员较少等因素有关[5]。同时现有回顾性研究发现,不同类型医院ADR特点不尽相同,大型医院、市级医院和基层医院等面临的ADR有较大差异,因此无法完全依据其他医疗机构的ADR数据而推测预估本机构的相关数据指标[6]。鉴于此,本文拟对我院2018年全年院内ADR发生情况进行调查,总结我院ADR发生特点并进行分析总结,拟为改善我院临床合理用药和加强ADR上报和监测工作提供参考。
1 资料与方法
1.1 一般资料
收集整理2018年1~12月期间我院各临床科室上报国家ADR监测系统的ADR报告表,共计181份,其中上报ADR数量前三的科室依次为肿瘤外科、呼吸内科和消化内科。
1.2 方法
采用回顾性分类统计方法,对出现ADR患者的性别、年龄、设计药品种类、给药途径、ADR 累及器官和关联性评价等指标进行统计分析。关联性评价主要采用国家药品不良反应检测中心发布的ADR关联性标准[5],关联性分为肯定、很可能、可能、可能无关、待评价和无法评价6个级别,见表1。
1.3 ADR转归评价原则[4]
ADR转归分为“痊愈”、“好转”和“未出现好转”三类。“痊愈”是指ADR得到有效控制并治愈;“好转”指ADR得到一定控制,但仍存在;“未出现好转”指ADR无改善。
1.4 观察指标
ADR性别与年龄的分布情况,患者给药科室分布情况,给药途径分布情况,引发ADR的药品品种分布情况,累及器官分布及主要临床表现情况,关联性评价情况,不良反应及疗效情况。
2 结果
2.1 患者性别与年龄分布
在上报的全部181例ADR中,男64例(35.36%),女117例(64.64%),按年龄将患者分为四组:≤17周岁组、18~40周岁组、41~59周岁组和≥60周岁组,各年龄区间均有ADR事件上报,其中未成年组上报频次最低,41~59周岁组上报频次最高,见表2。
2.2 ADR發生患者给药科室分布
本研究纳入患者共来自十余个科室,其中上报例数排名前三的科室为肿瘤外科、呼吸内科和消化内科,分别占比25.41%、17.13%和15.47%。见表3。
2.3 ADR发生患者给药途径分布
本次纳入的ADR事件中给药途径包括静脉给药、口服给药、外用给药、皮下注射和肌内注射等常见给药方式,其中静脉给药导致出现ADR例数最高,达138例,占比76.24%,口服给药19例,占比10.50%,外用给药13例,占比7.18%,皮下注射给药和肌内注射给药分别为9例(4.97%)和2例(1.10%),见表4。
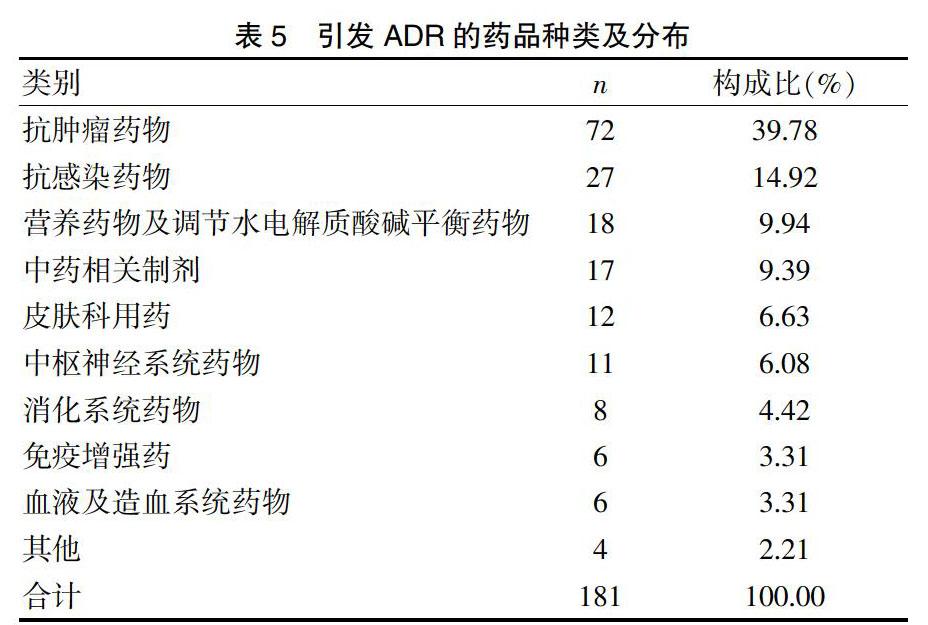
2.4 药品种类及分布
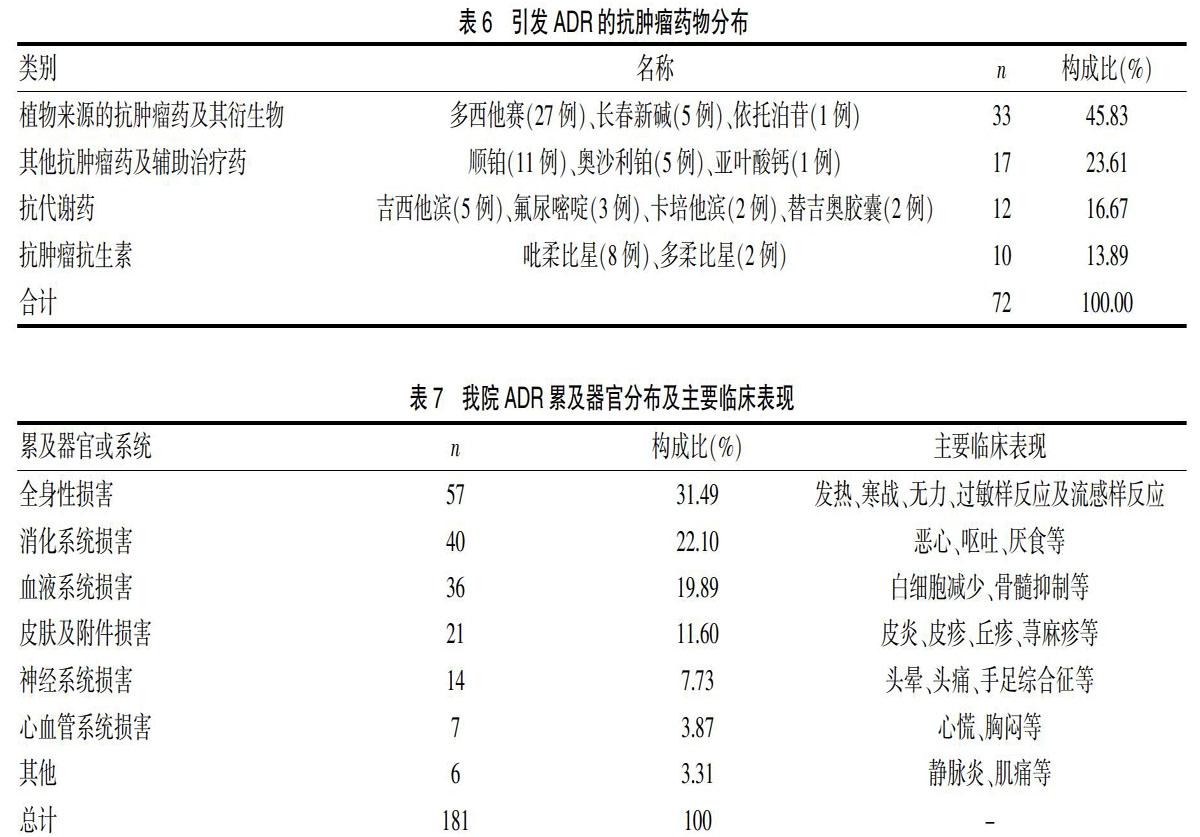
多类药品均有ADR上报,其中最常见的引起ADR的药物为抗肿瘤药物,抗感染药物仅次其后,营养药物及调节水电解质酸碱平衡药物和中药相关制剂分列三、四位,见表5。在引发ADR的抗肿瘤药物中,最常见的为植物来源性药物,其中多西他赛引发不良反应27例,在所有单药中发生率最高,铂类药物也是引发ADR的常见药物之一,见表6。
2.5 ADR累及器官分布及临床表现
在上报的181例ADR中,全身性损害排名第一,共计57例,占比为31.49%,主要表现为发热、寒战等流感样反应及过敏样反应。消化系统损害和血液系统损害分别占比22.10%和19.89%。见表7。
2.6 ADR关联性评价
关联性评价主要采用国家药品不良反应检测中心发布的ADR关联性标准[5],181例ADR报告中,“肯定”的85例(46.96%),“很可能”70例(38.67%),“可能”21例(11.61%),“待评价”5例(2.76%)。
2.7 ADR报告类型及转归
按照报告类型分类,已知的一般反应、新的不良反应、严重不良反应分别为147例(81.21%)、19例(10.50%)和15例(8.29%)。ADR发生后经停药或相应的对症治疗处理,其中116例(64.09%)患者痊愈,63例(34.81%)好转,2例(1.10%)患者未出现好转,未出现因ADR导致的后遗症或者死亡病例。
3 讨论
2018年1~12月期间我院共计上报ADR的181例,其中发生于女性的病例显著高于男性,考虑认为这可能与我院就诊女性患者数量显著高于男性有关。对上报ADR的人群年龄进行分型发现,各年龄段人群均有ADR的上报,其中41~59周岁年龄段上报频次最高,60周岁以上人群上报频次紧随其后,这提示中老年人群是出现药物ADR的高风险人群,考虑这可能与该类人群许多器官储备功能开始下降而导致代偿能力下降,如肾功能下降可导致药物代谢能力的变化,从而导致体内药物处置过程的变化[6-10],亦有研究指出这部分人群用药频次相比年轻人较高,合并用药情况复杂,易导致对医嘱依从性差,是潜在的可能影响ADR发生次数的因素[11]。对引发ADR发生的药物剂型进行分析,可以发现静脉给药是最易导致ADR发生的给药方式,本研究中静脉给药导致ADR占比76.24%,远远高于其他剂型,考虑这可能与静脉药物可以直接进入血液循环,而未经过肝脏代谢系统及消化道系统有关[12]。与此同时,内毒素、微粒、pH值等均为ADR的常见诱因,亦可导致ADR的发生[13-15]。鉴于此,临床医师在医嘱开具时一定要坚持正确的用药原则,将药物本身的理化性质和代谢特点综合纳入考虑,依据疾病情况采用适当的给药途径和药物剂型,同时在静脉给药初期,应密切监控患者情况,根据患者情况调整静注速度,并采取充分措施预防和处理ADR的发生。
针对引发ADR反应的药品种类进行分析,引发我院ADR的药品最常见的为抗肿瘤药物,抗感染药物仅次其后,营养药物及调节水电解质酸碱平衡药物和中药相关制剂分列三、四位,这与以上药物临床使用频次高有关,同时抗肿瘤药物(尤其是化疗药物)在杀伤肿瘤细胞的同时亦可杀伤正常细胞,这可能是该类药物ADR发生率偏高的原因[16-20]。在抗肿瘤药物引发的不良反应中,最常见的临床表现为消化系统及血液系统的损伤,如恶心呕吐、骨髓抑制、白细胞减少等,其中植物来源的化疗药物引发的ADR发生频次最高,如多西他赛引发27例不良反应的发生。从ADR累及器官或系统来分析,全身性损害最为常见,消化系统和血液系统发生频次紧随其后,这提示在今后临床不良反应事件上报过程中要多关注该类ADR,并及时、准确做好处理方案。不可忽视的是,近年来我院中药制剂引发的ADR呈现增长状态,其中2018年度我院中药引发的ADR占全部ADR的9.39%,位居全院药物类型第四位,这与传统认知并不一致,这可能与中药相关制剂质量标准、工艺等原因并不一致有关,同时,中药制剂往往成分复杂,多成分并存亦被视为是引发ADR发生的常见原因之一。提示在今后中药制剂的使用过程中,切不可盲目大意,忽视可能引发的相关不良反应,
在181例报道的ADR中,仅有6例患者明确既往有药物过敏史,而在用药过程中有多例患者出现过敏样症状,这提示无论患者是否具有过敏史,用药前均应询问患者药物过敏史和家族史,如需进行皮肤试验则必须开展相关试验,切不能忽视患者过敏的可能性。同时在临床治疗过程中,还应密切观察患者状况,一旦出现过敏相关情况,要尽快停药并给予相应的处理,同时避免再次使用引发过敏的药物及同类药物,避免引发极端情况。
综合我院就诊人员特点及用药习惯,在保持临床药物合理使用及监测的同时,应针对性制定关于抗肿瘤药物及抗感染药物的ADR监测管理方案,临床医护人员要高度重视这两类药物可导致的常见不良反应,并在用药前综合考虑患者的基础因素(如年龄、病情、配伍禁忌和过敏史等),在综合考虑各方面因素的基础上,制定因地制宜的个体化给药方案,并在用药期间严密监测患者相关指标,同时随时调整给药剂量,最大限度降低ADR发生率。
[参考文献]
[1] 郭钦惠,王南松,周学琴. 运用我院信息系统建立药物不良反应的监测模式在药学监护中的应用[J]. 中国医药导报,2011,8(8):123-124.
[2] 杨延音,董志,夏永鹏.《药品不良反应报告和监测管理办法》下药品生产企业不良反应监测工作模式探讨[J]. 中国中药杂志,2012,37(21):3329-3333.
[3] 杨延音,朱舒兵,董志,等. 重庆市《药品不良反应报告和监测管理办法》的认知调查报告[J].华西药学杂志,2012,27(5):600-603.
[4] 王丹,杜曉曦. 药品不良反应报告和监测管理办法解读及对中药不良反应监测的意义[J]. 中国中药杂志,2012, 37(18):2686-2688.
[5] 杜毅,金樑. 草乌甲素片临床应用的安全性评价[J]. 中国药物经济学,2019,14(7):31-35.
[6] 魏建芳. 我院2015年药物不良反应报告分析[J]. 中国当代医药,2016,23(18):90-92.
[7] 白顺民,李霞丽,范哲. 2016~2017年焦作市第二人民医院中药注射剂不良反应分析[J]. 现代药物与临床,2019,34(6):1921-1926.
[8] 周文雅. 本院232例抗菌药物不良反应报告分析[J]. 中国医学创新,2019,16(4):117-121.
[9] 杜晓慧,许健. 17例奥美拉唑致药品不良反应报告[J]. 中国医院用药评价与分析,2018,18(11):1574-1575.
[10] 孙俊,祁献芳,张磊,等. 注射用益气复脉(冻干)安全性医院集中监测研究[J]. 中国医院药学杂志,2019,39(1):97-100.
[11] 计紫超,林京玉,杨悦. 8503例喹诺酮类药物致ADR/ADE的帕累托图分析[J]. 中国药物评价,2019,36(1):60-64.
[12] 吴军. 抗肿瘤血管生成药物不良反应的发生机制及处理[J]. 医学综述,2016,22(16):3154-3157.
[13] 安胜男,张婉璐,任文静,等. 药师角度对药品不良反应的评价与分析[J]. 中国药物应用与监测,2017,14(6):357-360.
[14] 孙国平,王海飞. 668例药品不良反应报告[J].中国医院用药评价与分析,2018,18(3):409-411,414.
[15] 王金萍,赵旭燕,赵萌,等. 2014~2016年西安市中心医院抗菌药物不良反应分析[J]. 现代药物与临床,2017, 32(9):1791-1795.
[16] 程军,韩一萱,张士洋,等. 369例中药注射剂不良反应/不良事件分析[J]. 药物流行病学杂志,2018,27(2):113-116.
[17] Pastore S,Naviglio S,Canuto A,et al. Serious adverse events associated with anti-tumor necrosis factor alpha agents in pediatric-onset inflammatory bowel disease and juvenile idiopathic arthritis in a real-life setting[J]. Pediatric Drugs,2018,20(2):165-171.
[18] 史筱倩,俸继红. 某三甲肿瘤专科医院2017年411例药物不良反应分析[J]. 昆明医科大学学报,2019,40(2):86-91.
[19] Puig L. Paradoxical reactions:Anti-tumor necrosis factor alpha agents,ustekinumab,secukinumab,ixekizumab,and others[M]//Adverse Reactions to Biologics. Karger Publishers,2018,53:49-63.
[20] 王娜娜,白羽,刘红,等. 787例抗肿瘤药物不良反应特点及预后因素分析[J]. 肿瘤药学,2019,9(1):143-148.
(收稿日期:2019-12-26)

