铁载分离-碘酸钾滴定法测定高钼、高锡物料中的锡含量
刘 娟
(湖南有色金属研究院,长沙410110)
锡在现代工业中主要应用于焊接[1-3]、食品包装和加工、3D打印等领域[4-5]。对锡矿产的过度开采,造成具有开采价值的锡矿资源开始日渐萎缩。从废旧的含锡物料中重新分离提纯是金属锡再生的一种趋势[6-8]。在第三方检测接收到检测锡的样品中,测定高钼、高锡物料中锡含量的样品越来越多。这种物料主要是从锡、钼的氧化物及合金加工行业中得来。锡的含量为5%~50%,而钼的含量为10%~50%左右,甚至更高,其含量波动较大,除了主成分锡、钼之外,还含有少量的铜、铅、铁、钒、镍、锑、银和硅等其他杂质元素。
准确测定高钼、高锡物料中的锡含量,对回收锡的工艺研究具有重要的指导意义。锡的测定方法主要有碘酸钾滴定法[9-10]、YS/T 1120.2-2016和YS/T 372.13-2006中的乙二胺四乙酸(EDTA)滴定法、YS/T 248.2-2007中的分光光度法和电感耦合等离子体原子发射光谱法(ICP-AES)等[11-12]。高钼、高锡物料中的锡含量比较高,须采用化学滴定法测定,而 GB/T 6150.2-2008和 GB/T 1819.2-2004中的化学滴定法中测定锡含量的最经典的方法为碘酸钾滴定法。碘酸钾滴定法测定锡时,样品中高含量的钼对锡的测定产生严重的干扰。目前尚未检索到采用国家标准方法、行业标准方法测定高钼、高锡物料中锡含量的分析方法。本工作按照国家标准方法GB/T 1819.2-2004《锡精矿化学分析方法锡量的测定》中锡精矿的测定方法和文献[13]探究出了一种测定高钼、高锡物料中锡含量的分析方法:即采用焦硫酸钾熔融试样,以硫酸溶液浸取熔块,于氨水溶液中,以铁盐为载体,锡以氢氧化物沉淀,与钼、铜、钒、铬等干扰元素进行分离,过滤,灰化,过氧化钠熔融,在盐酸溶液中用铝片还原,碘酸钾标准溶液滴定。非用国家标准方法中以硫酸铍为载体而采用铁盐为载体是因为硫酸铍有剧毒,是一种高致癌物,人体吸收后可引起皮炎、溃疡、皮肤肉芽肿等,容易对水体和环境造成污染。而铁盐能够起到同样的负载效果,同时对环境和人体均无害。此方法准确可靠,干扰少,重现性好,试剂环保,已用于实际样品的分析检测,对实际分析工作有指导作用。
1 试验部分
1.1 试剂
锡标准溶液:4.000 g·L-1,称取0.800 0 g高纯金属锡,加入80 mL盐酸,使锡自然溶解后转移至200 mL容量瓶中,冷却至室温后用5%(体积分数,下同)盐酸溶液稀释至刻度,摇匀备用。
淀粉溶液:5 g·L-1,称取0.5 g可溶性淀粉于200 mL烧杯中,用少量水调成糊状,将100 mL沸水缓慢倒入,继续煮沸至透明,取下冷却,现用现配。
氯化铁溶液:称取48 g六水合氯化铁(FeCl3·6 H2O)于500 mL烧杯中,加少量盐酸及水溶解后,用水稀释至500.0 mL,其中Fe3+的质量浓度为20 g·L-1。
碘酸钾标准溶液:c(1/6 KIO3)=0.005 mol·L-1,称取0.2 g氢氧化钾,1.1 g碘酸钾及12 g碘化钾于300 mL烧杯中,用水溶解,移至1 L容量瓶中,稀释至刻度,摇匀。
标定:移取锡标准溶液20.00 mL于500 mL锥形瓶中,加入30 mL盐酸、40 mL水、0.5 g还原铁粉,待铁粉反应完后按试验方法进行还原和滴定,随同做空白试验,计算碘酸钾标准溶液对锡的滴定度。
氨水-氯化铵洗涤溶液:将2 g氯化铵溶于100 mL水中,再加入6~8滴氨水,混合均匀。
铝片的纯度大于99.5%,折叠成每片大约1.8 g,用锤子轻打压紧备用;试验所用试剂均为分析纯;试验用水为超纯水。
1.2 试验方法
称取0.15~0.30 g(精确至0.000 1 g)试样于30 mL瓷坩埚中,加入焦硫酸钾8~10 g,将坩埚放入预先升温至500℃的马弗炉中,再逐渐升温至750℃后熔融15 min,取出坩埚,冷却。将坩埚置于250 mL烧杯中,加入5%(体积分数,下同)硫酸溶液80 mL,低温加热浸取熔块。取下,用5%硫酸溶液洗净坩埚。向烧杯中加5 g氯化铵,4 mL氯化铁溶液,搅匀,用氨水中和至Fe3+沉淀完全并过量10 mL,煮沸,静置沉淀分层,用中速定量滤纸过滤,将沉淀全部转移至滤纸上,用氨水-氯化铵洗液溶液洗涤烧杯和沉淀各4次,用滤纸将烧杯擦洗干净,将沉淀连同滤纸放入30 mL铁坩埚内,低温灰化。取出冷却,加入过氧化钠5 g,将铁坩埚放入预先升温至730℃的马弗炉中至坩埚内熔融物呈均匀、透明的桃红色液体,取出稍冷,放入预先盛有50 mL热水的250 mL烧杯中,待剧烈反应后,用5%盐酸溶液洗净坩埚,加入40 mL盐酸,冷却至室温后少量多次的加入还原性铁粉至Fe3+的黄色褪去后,静置0.5 h,中间搅拌数次。用脱脂棉过滤至500 mL锥形瓶中,并用5%盐酸溶液洗涤烧杯和沉淀各3~5次,控制体积150 mL,补加40 mL盐酸。加入1.8 g铝片,不断摇晃至铝片快作用完时,盖上盛有饱和碳酸氢钠的盖氏漏斗,加热煮沸至铝片完全溶解时取下,用流水冷却至室温,取下盖氏漏斗,立即加入5 mL淀粉指示剂,迅速用碘酸钾标准溶液滴定至蓝色为终点,同时进行空白试验。
2 结果与讨论
2.1 坩埚和熔剂的选择
试样中的大部分锡和钼都是以氧化物的形式存在,用盐酸、硝酸、硫酸较难将试样分解,因此需要选择合适的熔剂将试样熔融分解。考虑到后续的分析步骤,银坩埚和镍坩埚与碱性熔剂熔融时会将银、镍带入,对分析方法产生新的干扰,因此两者均不宜使用;铁坩埚和氢氧化钠、过氧化钠一起熔融时会产生大量的氢氧化铁沉淀,过滤比较困难;刚玉坩埚既可以与碱性熔剂或酸性熔剂一起熔融试样,也不会带进新的杂质,可以用来熔融样品,但刚玉坩埚成本太高且容易炸裂;焦硫酸钾在瓷坩埚中也能将样品熔融,且不引入杂质,同时瓷坩埚成本低。综合考虑,试验选择的坩埚为瓷坩埚,熔剂为焦硫酸钾。
2.2 焦硫酸钾用量的选择
试样熔融过程中,焦硫酸钾的用量十分重要,加入不够会造成试样没有熔融完全而使测定结果偏低,而加入太多则造成试剂浪费。试验考察了焦硫酸钾的用量分别为4,6,8,10,12 g时对1#样品中锡测定结果的影响,见图1。

图1 焦硫酸钾的用量对测定结果的影响Fig.1 Effect of the amount of potassium pyrosulfate on the determination results
由图1可知:当焦硫酸钾的用量小于8 g时,试样不能熔融完全,测定结果偏低;当焦硫酸钾的用量大于8 g时,试样熔融完全,考虑到焦硫酸钾的用量过多容易造成试剂浪费。试验选择焦硫酸钾的用量为8~10 g。
2.3 钼对锡测定结果的影响
采用碘酸钾滴定法测定锡时,试样中的钼被还原成低价红棕色化合物,也有可能形成钼蓝,影响终点观察,且消耗碘酸钾标准溶液,严重干扰锡的测定结果。移取锡标准溶液40 mg于500 mL锥形瓶中,分别加入5,10,15,20,25 mg的钼,再加入30 mL盐酸和40 mL水,最后加入0.5 g还原性铁粉,待铁粉反应完后按照试验方法进行还原和滴定。试验考察了钼对锡测定结果的影响,结果见图2。
由图2可知:大量钼的存在确实会影响碘酸钾滴定法对于锡的测定,钼的加入量越大,铝片还原后溶液中钼的红棕色越明显,滴定终点消退越快;当钼的加入量小于5 mg时,钼对锡的测定不产生干扰;当钼的加入量为5~15 mg时,钼对锡的测定产生干扰,但干扰并不明显;当钼的加入量大于15 mg时,钼对锡的测定会产生明显的干扰。
2.4 酒石酸对钼的掩蔽效果

图2 钼对测定结果的影响Fig.2 Effect of molybdenum on the determination results
酒石酸对钼有络合作用,能起到一定的掩蔽作用。移取锡标准溶液40 mg于500 mL锥形瓶中,加入5 g酒石酸,再分别加入5,10,15,20,25 mg的钼,最后加入30 mL盐酸、40 mL水和0.5 g还原性铁粉,待铁粉反应完后按照试验方法进行还原和滴定。试验考察了酒石酸对钼的掩蔽效果,结果见图3。

图3 酒石酸对钼的掩蔽作用Fig.3 Masking of molybdenum by tartaric acid
由图3可知:加入5 g酒石酸后,当钼的加入量小于15 mg时,钼对锡的测定基本不产生干扰;当钼的加入量为20 mg时,钼对锡的测定会产生干扰,但干扰并不明显;当钼的加入量大于25 mg时,钼对锡的测定才会产生明显的干扰。说明酒石酸对钼具有一定的掩蔽作用,加入酒石酸后,样品中钼的含量较低时,不干扰锡的测定,但钼含量较高时仍然对测定存在干扰,需要将杂质分离后才能进行测定。
为了进一步研究酒石酸对钼的掩蔽效果,试验考察了酒石酸的用量对钼掩蔽效果的影响。移取锡标准溶液40 mg钼标准溶液40 mg于500 mL锥形瓶中,分别加入5,10,15,20,25 g的酒石酸,再加入30 mL盐酸、40 mL水和0.5 g还原铁粉,待铁粉反应完后按照试验方法进行还原和滴定,测定结果见图4。

图4 酒石酸的用量对钼掩蔽效果的影响Fig.4 Effect of the amount of tartaric acid on the masking effect of molybdenum
由图4可知:加入酒石酸后,能在一定程度上降低钼对锡的测定产生的干扰,但并不能消除干扰,随着酒石酸用量的增加,钼对锡的测定产生的干扰并没有显著降低或者消除。因此,测定含有较高含量钼的样品时,钼对样品中锡的测定存在较严重的干扰,必须将杂质钼分离后才能测定锡的含量。
2.5 铁的用量对锡、钼分离效果的影响
在含有铵盐的氨性溶液中,以铁盐为载体沉淀锡的过程中,要严格控制补加铁盐的量。补加的铁盐太多,生成的氢氧化铁沉淀量太大,对钼的吸附作用增强会使钼分离不彻底,补加的铁盐太少,不能完全负载样品中的锡,使其进入滤液造成锡的损失。移取锡标准溶液100.0 mg、钼标准溶液100.0 mg,分别加入20,40,60,80,100,200 mg的铁,将过滤后的滤液用盐酸酸化,采用ICP-AES测定滤液中残留的锡含量,同时沉淀连同滤纸用盐酸溶解,经ICP-AES测定其中吸附的钼含量,结果见表1。

表1 铁的用量对锡、钼分离效果的影响Tab.1 Effect of the amount of iron on the separation of tin and molybdenum mg
结果表明:当铁的用量大于20 mg时,氢氧化铁沉淀与锡的氢氧化物基本共沉淀完全,滤液中的残留锡含量均小于0.05%;当铁的用量为60 mg时,滤液中的残留锡含量最小为0.018%,铁与锡共沉淀完全,同时沉淀对钼的吸附作用较小,对锡的测定结果不产生干扰。试验选择铁的用量为60 mg,能够较好地将锡和钼分离。
2.6 混合干扰元素对锡测定的影响
高钼、高锡物料中除了大部分的钼和锡之外,还含有少量的铜、铅、铁、钒、铋、镍、锑、银、硅等其他杂质元素。结果发现:铜、银和钒在氨性溶液中均可在溶液中通过过滤除去,不产生干扰;铅、铁和铝不参与化学反应,对锡的测定均不产生干扰;极少量的砷、锑在铁粉还原除杂时亦可分离而不干扰测定。
2.7 精密度试验
按照试验方法对1#、2#和3#样品进行测定,每个样品平行测定7次,计算测定值的相对标准偏差(RSD),结果见表2。

表2 精密度试验结果(n=7)Tab.2 Results of test for precision(n=7) %
由表2可知:锡的 RSD为0.23%~0.37%,说明方法具有良好的精密度。
2.8 回收试验
为了考察方法的稳定性,按照试验方法对1#样品和3#样品进行加标回收试验,计算锡的回收率,结果见表3。
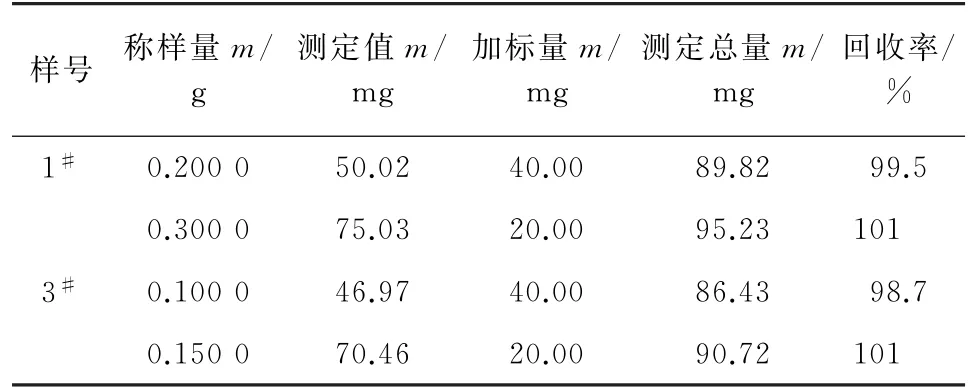
表3 回收试验结果Tab.3 Results of test for recovery
由表3可知:锡的回收率为98.7%~101%,可以满足试样分析要求。
本工作以焦硫酸钾熔融试样,铁盐为载体,锡生成氢氧化物沉淀,与钼、铜、钒、铬等干扰元素分离,消除了钼对碘酸钾滴定法测定锡的干扰。方法准确可靠,可用于实际样品的常规分析,对于第三方仲裁样品的分析,可以采取用ICP-AES补正滤液中的微量锡损失,对检测结果进行修正,可对实际分析工作有较好的指导作用。

