化学PIC教学模式的实践应用
——以“离子键”教学为例
文/汕头市东厦中学
化学探究性教学的“问题—探究—建构(Problem-Inquiry-Construct)”模式(化学PIC教学模式)将化学探究教学过程分为问题、猜想、验证、解释、迁移五个阶段,逐步实践探究学习的要求。本文以《离子键》为例,采用PIC教学模式进行设计,力求展现一节具有探究学习性质的概念型新课。
一、教学环节
情景引入:展示图片,设置问题,游戏环节
通过图片我们可以看到物质是由微粒构成的,那么这些微粒之间是怎样相互结合构成物质的呢?
【游戏环节】你能不能用乒乓球堆积成晶体模型?
在讲台上堆积,游戏失败。
为什么乒乓球堆不出指定的形状?怎样才能堆积成指定的模型呢?
需要用胶水。
胶水在这里相当于一种作用力使乒乓球粘在一起,那微观粒子之间呢?是不是也需要相互作用力才能结合成物质呢?这就是我们这节课要掌握的内容。
【板书】第一课时离子键
任务1:从宏观角度观察氯化钠的形成过程
以氯化钠为研究对象,从宏观和微观两个角度上进行分析。宏观上通过实验来制备氯化钠。
【实验探究】大家先看课本19页实验1-2,钠和氯气的反应。
课本中的实验有没有什么缺点?
氯气有毒,容易泄露,影响我们的健康,同时污染环境。
那能不能在实验中做一些改进呢?
可以加一些尾气吸收。
那可以用什么吸收呢?
氯气可以和强碱反应,用氢氧化钠吸收。
那是不是还得想办法把多余的气体引导出来,得怎么改进?
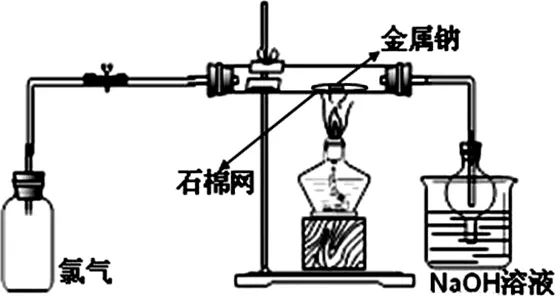
图1
【演示实验】如图1,取一绿豆大小金属钠放在石棉网上加热,待融化成小球后,由学生代表打开止水夹,挤压装有氯气的集气瓶(医用废旧装液瓶),即可观察到产生大量白烟。
你认为发生上述变化现象的原因是什么?
钠和氯气反应生成氯化钠。

任务2:从微观角度分析氯化钠的形成过程
从宏观现象中得出金属钠和非金属单质氯气反应生成白烟——氯化钠。为什么氯气遇到绿豆大小的钠会变成白烟呢,反应的微观本质又是什么?
在化学反应中,分子可以再分,原子不可分。在化学反应中的最小微粒是原子,钠和氯气反应的实质是钠原子和氯原子的反应。
在学案中画出钠原来和氯原子的结构示意图,思考钠原子和氯原子的结构是稳定结构吗?钠原子和氯原子如何变成稳定结构?
【角色扮演】两位同学一位扮演钠原子,一位扮演氯原子,当钠原子遇到氯原子会发生什么对话呢?
氯原子:我需要一个电子就能变成相对稳定的结构,钠原子能给我一个吗?
老师:钠原子,你愿意吗?为什么?
钠原子:我愿意,因为失去一个电子我也能变成相对稳定的结构。
老师:从两位同学的对话中,我们可以很直观的了解到钠原子遇到氯原子非常合拍,一个愿失一个愿得,就都能变成相对稳定的结构。
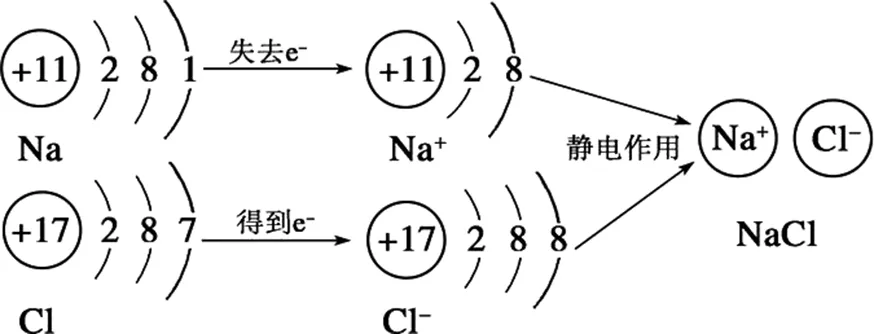
【分析】钠原子失去最外层一个电子变成钠离子,而氯原子得到一个电子变成氯离子,两个离子通过静电作用结合在一起,从而形成与单质钠和氯气性质完全不同的氯化钠,我们把这种带相反电荷离子之间的相互作用称为离子键。
【板书】一、离子键
Mg和O2反应生成MgO,请从微观角度分析MgO的形成过程,并判断能否形成离子键?
镁原子容易失去最外层的两个电子,变成镁离子,而氧原子容易得到两个电子变成氧离子,根据离子键定义,可以形成离子键。
像氯化钠是由钠离子和氯离子所构成的,氧化镁是由镁离子和氧离子所构成的,这两种化合物有一个共同点,都存在着离子键,化学上把这种由离子键所构成的物质叫做离子化合物。
【板书】二、离子化合物
离子化合物的组成元素有什么特点呢?
容易得失电子。
查阅元素周期表,分析哪些元素容易得电子,哪些元素容易失电子?
活泼的金属元素(ΙA、ⅡA)和活泼的非金属(ⅥA、ⅦA)
成键粒子:阴阳离子
成键原因:得失电子
成键本质:静电作用
成键元素:活泼的金属元素(ⅠA、ⅡA)和活泼的非金属(ⅥA、ⅦA)
离子化合物:由离子键构成的化合物
任务3:用电子式表示氯化钠的形成过程
以上我们从原子结构的角度,用原子结构示意图来表示Na原子和Cl原子发生变化生成NaCl的过程,它清晰、直观,但是,书写结构示意图时有些麻烦,而且我们在分析过程中可以发现离子键的形成过程是和最外层电子数有关,那么,有没有一种分析方法能够只用最外层电子数就可以表示离子化合物的形成过程呢?有,电子式,是我们接下来学习的新的概念。
【板书】三、电子式
【分组讨论】请同学们看课本20页的资料卡片,归纳电子式的定义和书写方法。
【练习】请书写出学案表格中原子和离子的电子式。
【总结】(1)阳离子的电子式直接用离子符号表示;
(2)阴离子的电子式不但要画出最外层电子,而且还要用中括号“[]”括起来,并在括号外右上角标出所带电荷。
如何用电子式表示氯化钠的形成过程呢?
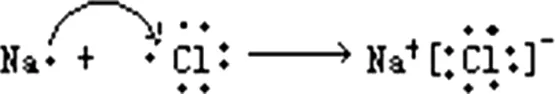
二、教学反思
本节课参加2014年汕头市金平区青年基本功比赛获得一等奖;参加2014年广东省“一师一优课 一课一名师”荣获广东省省级优课;参加2014年国培“自主研修 精彩绽放”优质教学资源评选活动一等奖。这些荣誉都体现了PIC教学模式得到同行教师的认可,有一定的推广价值。
同时,本节课的亮点是对课本实验的改进,课本中钠和氯气的反应是直接将钠放在石棉网上,用酒精灯微热,待钠融成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方。这样很容易造成氯气泄漏,不仅影响师生健康,还会污染环境。通过引导学生跟着老师一起分析该实验的缺点并提出改进方案,激发起学生内心深处的探究意识,燃起学生的探究热情,既增加学生的参与度,又使学生通过自己的思考得出来的改进方案,大大提高学习的兴趣和效果。

