挥发性有机化合物催化氧化技术
张胜硕,武燕娟,张 伟,雍晓静,张安贵
(国家能源集团宁夏煤业有限责任公司煤炭化学工业技术研究院,宁夏 银川 750411)
挥发性有机化合物(VOCs)是指在20 ℃、一个大气压(0.1 MPa)下,饱和蒸汽压超过10.3 Pa,并且参与大气光化学反应的有机化合物,主要是煤化工、石油化工、精细化工以及制药、涂料、印刷、垃圾除臭等行业产生,包括非甲烷烃类、含氧有机物、含氮有机物和含硫有机物等,在室温下很容易挥发,是形成臭氧(O3)和细颗粒污染物(PM2.5)的重要前驱体[1-3]。
《“十三五”挥发性有机物污染防治工作方案》指出,以改善环境质量为核心,以重点地区和重点行业为主要控制对象,以削减活性强VOCs组分为着力点,以全面实施固定污染源排污许可管理为抓手,以强化基础能力建设和加强政策支持为保障,通过采取源头削减、过程控制、末端治理全过程防控措施,全面加强VOCs污染防治,促进环境空气质量持续改善和产业绿色转型发展。在企业发展的同时,加强环保管理,坚决打赢蓝天保卫战。所以,全面有效治理VOCs排放势在必行。
催化氧化技术因其具有起燃温度低、处理效率高、适用范围广以及无二次污染等特点,是去除VOCs工艺中的关键步骤[4]。
本文对挥发性有机化合物催化氧化技术进行综述。
1 反应机理
催化氧化VOCs已经被广泛研究,Hermia J等[5]建立了VOCs可氧化性和分子量之间的相关性,研究表明,分子量越大,VOCs更加不容易被氧化。这个相关性与Tichenor B A等[6]提出的VOCs氧化难易程度相同,即醇<醛<芳烃<酮<乙酸酯<烷烃。
反应过程如式(1)所示,在一定反应温度下,利用催化剂使有机气体被催化氧化,发生无火焰燃烧,主要得到CO2和H2O,同时放出大量的热能[7]。

(1)
研究表明,挥发性有机化合物完全催化氧化的机理通常分为:Mars-van Krevelen(MVK)模型、Langmuir-Hinshelwood(L-H)模型和Eley-Rideal(E-R)模型。
MVK模型[8]认为,催化氧化反应发生在吸附的VOCs和催化剂晶格氧之间,而不是与气相中的氧气发生反应,MVK模型机理如图1所示[9]。
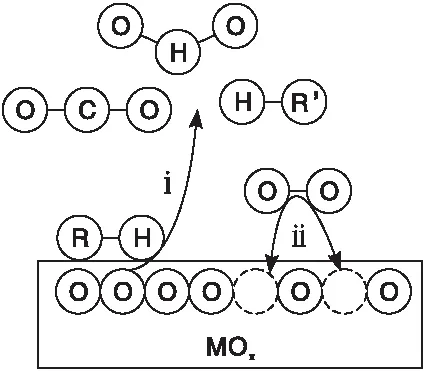
图1 MVK模型机理Figure 1 The mechanism of MVK model
MVK模型假设VOCs氧化分为两步进行。首先,被吸附的VOCs与氧气在催化剂上反应,导致金属氧化物被还原。其次,氧气将被还原的金属氧化物氧化,并继续留在载体内进行下一步连续循环反应[10]。由于催化剂先被还原后被氧化,这种机制可称为氧化还原机制。且在稳定状态下,还原和氧化的速率步骤必须相等。该模型已应用于烃类在催化剂金属氧化物上的氧化反应动力学模拟研究[11]。根据MVK机制,VOCs氧化速率用式(2)表示。
(2)
式中,rvoc为反应速率,mol·m-3·s-1;Pvoc为挥发性有机化合物的分压;Po2为氧分压;Kvoc为挥发性有机化合物氧化速率常数;Ko2为催化剂再氧化速率常数;γ是氧化反应中O2的化学计量系数。
L-H模型机理如图2所示[12]。

图2 L-H模型机理Figure 2 The mechanism of L-H model
L-H模型[13]假定吸附在催化剂上的VOCs和氧气之间发生反应。研究表明,挥发性有机化合物和氧气可能会吸附在相似类型的活动位点上,被称为单一位点L-H模型;或是两个不同类型活动位点上,被称为竞争位点L-H模型。单一位点L-H模型和竞争位点L-H模型的表达式如式(3)和(4)所示。
(3)
(4)
式中,Ko2为吸附氧平衡常数,Kvoc为吸附VOCs平衡常数。该模型优点是其可以表明反应速率,还可以解释VOCs和氧的吸附原因。
E-R模型[14]认为,反应是在被吸附的氧物质和气相中的反应物分子之间发生。其中,吸附的分子和气相中的分子控制反应步骤。基于E-R模型,式(5)代表其动力学。
(5)
综上所述,每种机理的合理性很大程度上取决于催化剂(活性金属和载体)的性质以及挥发性有机化合物的性质。通常状况下,给定类型的VOCs在特定金属氧化物或贵金属催化剂上的反应实验数据至少会与一种动力学模型机制吻合。
2 催化剂
催化氧化是利用催化剂在较低温度和较快反应速率等条件下,将待处理有机气体氧化分解为二氧化碳和水,而且催化剂中负载金属可以促进有机污染物氧化并减少焦炭形成[15]。所以,工艺关键是催化剂的选择。
2.1 贵金属催化剂
污染物浓度和性质对反应温度的选择具有重要作用,但Pt、Pd、Au及Ag是催化氧化过程中常用的催化剂活性相,这些材料通常会在低温下对VOCs具有很高的去除率[16-17]。
Pt基催化剂在(150~350) ℃对于VOCs具有较高的去除率[15-18],Pt是氧化芳香族结构最活跃的元素[15-17]。
Pd基催化剂在(200~300) ℃具有较好的催化活性[19-22],而且对于VOCs气体,Pd基催化剂表现出高的催化活性,比Pt基催化剂更稳定[23]。
Au本身几乎是化学惰性,但可以增加载体氧化的晶格氧迁移速率[24],与Pd和Pt相比,Au基催化剂在(190~400) ℃对VOCs具有更高的去除率[24-27]。但成本高,限制了含Au催化剂的工业应用,特别是含氯的有机化合物对催化性能也有较大影响[15,28-29]。
使用Ag基催化剂处理VOCs有较多研究,Se-Won Baek等[30]采用XRD对负载Ag的HY沸石进行检测,发现随着负载量增加,金属Ag和Ag2O同时增加,并且负载量与催化活性成正比,表明金属Ag可能是甲苯氧化的活性相。使用TEM表明,催化活性增加可能与Ag负载量的增加有关。Ye Q等[31]证实了以上结论,确定了纳米MnO2中Ag的最佳负载质量分数为5%,没有证据表明在高负荷条件下催化活性会降低。Kim S C等[32]也得出类似结果,指出γ-Al2O3的最佳Ag负载质量分数为11%。
研究指出,VOCs氧化的最佳条件为Cu、Mn物质的量比等于1,并且在活性相负载质量分数21.2%(Ag、Cu、Mn物质的量比为13.8∶43.1∶43.1)、温度264 ℃、体积分数0.89%和空速10 000 h-1条件下,对甲苯去除率为最佳[33-34]。数据表明,Ag负载量减少,导致活性中心减少,最终降低了去除效率,但对于更多的负载,活性中心的累积会形成更加低效的整体[35]。
2.2 非贵金属氧化物催化剂
非贵金属氧化物比贵金属便宜,但其催化活性没有贵金属好,混合金属氧化物有可能实现与贵金属相当的催化效率,所以具有有效催化作用能力的非贵金属氧化物催化剂经常被应用于去除VOCs。报道较多的是V、Cr、Mn和Ce,其他如Fe、Co和Mo因其催化性能相对较差,报道较少。
使用浸渍法负载质量分数5%~10%的V可制得用于去除氯化VOCs的V基催化剂。在约470 ℃和100 h负载质量分数5.8%的V基催化剂催化活性>90%[36-37]。这种V基催化剂由于其选择性高,更适合于预处理氯化VOCs。据报道,VOx/TiO2催化剂300 ℃去除约60%的苯(100×10-6,空速37 000 h-1),而且在相同温度下氧化钒在硫酸化TiO2上转化率达95%,超过300 ℃转化率达100%[38]。
Krishnamoorthy S J等[37]研究发现,Cr基催化剂可处理氯化和非氯化VOCs,约280 ℃(600×10-6,空速25 000 h-1)Cr基催化剂可以实现完全去除VOCs中的二氯苯。与V基催化剂相比,起燃温度高,但可以在较低温度下进行催化氧化反应[38]。由于其高毒性和潜在的环境问题,限制了实际应用。
使用锰基/TiO2-Al2O3催化剂在350 ℃(1 300×10-6,空速8 000 h-1)下可去除VOCs中97%氯苯,催化活性表现为(10~20) h增加,随后52 h趋于稳定[38-40]。
报道称有些非贵金属氧化物基催化剂显示出比贵金属催化剂相当或更好的催化能力[41-42]。含有Zr的Mn基催化剂被证明对VOCs有较好的去除率[43-44]。发现负载于活性炭的Co、Mn混合氧化物比Pd或Au对VOCs中甲苯(10 000×10-6)有更好的去除率,250 ℃时去除率>98%。CoMn/AC氧化物催化剂在250 ℃去除乙苯(10 000×10-6,流速55 mL·min-1)转化率超过90%,运行周期超过720 h。350 ℃时,这种混合氧化物去除低活性苯不到10%[41]。该差异有可能为不同污染物性质的不同,或者当发生催化氧化反应时,甲苯和乙苯的电离势能低于苯。
金属Ce因其优异的储氧能力是一种不错的促进剂或载体[45]。被广泛应用于VOCs的去除,Saqer S M等[46]报道了负载CeO2的氧化铝催化剂通常需要更高温才能将污染物去除,且呈现很好的催化活性;同时Cu-Ce和Mn-Ce混合氧化物催化剂在350 ℃能够将甲苯(1 000×10-6)完全去除。
2.3 双功能吸附催化剂
双功能吸附催化剂可以看作是其他类型催化剂既经济又有效率的替代品,分为两步法处理VOCs:(1) 预处理:污染物被吸附;(2) 催化氧化:温度的变化导致污染物解吸、吸附剂再生和有机污染物催化氧化。
制备可控制孔隙大小和比表面积等以增强吸附能力。Brazlauskas M等[47]制备了(100~350) ℃、寿命超过120天可有效氧化醇的双功能夹层型CuO/沸石吸附剂-催化剂。Kolade M A等[48]制备了高比表面积、低压降、低阻力和应用于去除VOCs具备高转化率的负载Pd活性炭吸附催化剂。Roland U等[49]使用Pt-NaY双功能分子筛催化剂可使VOCs中甲苯完全氧化,催化剂再生温度为375 ℃。显然,双功能催化剂可以发挥各自优势,为去除VOCs创造更环保、经济、简单有效的途径。
3 工艺流程
催化氧化法处理挥发性有机废气净化效率超过95%,适用于小风量、中高温度和中高浓度的有机废气,且一次投资成本低,运行费用较低,能量回收效果好,符合清洁生产和绿色能源的相关理念。
催化氧化法工艺流程如图3所示。由图3可见,经合理收集的VOCs首先通过热交换器预热,温度可升高约(50~200) ℃,然后经过加热器进一步将VOCs加热到催化反应温度约(200~300) ℃,最后,VOCs在催化剂作用下,被转化成CO2和H2O,同时释放大量热能[12]。

图3 催化氧化法工艺流程Figure 3 The process for catalytic oxidation
由于热交换器配置简化,CO主要节能和优化空间配置。结果表明,CO热交换效率可达70%,不适合处理大容量、低浓度的VOCs[50-51]。但考虑到初始的低投资和高灵活性,CO适合处理小流量(<5 000 m3·h-1)VOCs。
综上所述,去除VOCs的核心是使反应温度降低,即具有低温和高活性的催化剂。此外,延长催化剂寿命和提高去除效率也可以带来良好的节能效果和降低投资成本。对于低浓度和大体积的VOCs排放,可通过吸附+催化混合法的先进技术实现去除,已成功应用于实践[50-52]。
4 结 语
为了深入实施《“十三五”挥发性有机物污染防治工作方案》,打赢蓝天保卫战,提高挥发性有机化合物治理的科学性、针对性和有效性,研究高VOCs治理效率工艺已迫在眉睫。催化氧化技术因其成本低、工艺简单和处理效率高等优点被广泛应用,而催化剂开发是其核心,目前,复合金属氧化物催化剂是研究热点,因此,结合实际工艺和机理,提高催化剂反应活性和寿命,降低反应温度和成本等是此领域研究重点。
——庆祝中国共产党成立一百周年贵金属纪念币展

