上腔静脉电位指导定位技术在中心静脉置管中的应用价值
中心静脉导管在危重病人中应用日益广泛,这一技术可测定中心静脉压、快速补液并作为高价营养通路,是目前重症医学科静脉通路使用的最佳快速输液途径之一,中心静脉导管可有效降低刺激性药物对血管的毒副作用,具有并发症少、带管保留时间长、成本低等优点,同时可监测中心静脉压[1]。根据不同病人年龄、身形、体重等情况,通过体表卷尺估测法或床旁放射X片影像学确认导管走行及其尖端所在的位置是否位于上腔静脉[2],然而这种方法存在弊端,体表卷尺估测法误差较大,床旁X线判定不便,且部分医院重症医学科或放射科不配备移动式X光机,不同临床技师凭经验判定,主要定位参照物依靠胸椎/后肋、右心耳、气管分叉等,人为误差及参考点变异导致导管头端位置定位不佳,周围静脉血流速不同,实验药物后出现静脉血栓、堵塞、导管移位、心肌穿孔、心包填塞等严重后果[3-5]。若透视后发现导管尖端不在理想位置时,需重新调整导管深度及位置,病人反复透视,每次检查导管头端位置均需承受一定剂量的射线辐射。医护人员在透视射线下实时调整置管,与病人承受同等剂量的射线辐射。因此,需利用现有资源定位准确导管头端,重复记录并精确比对,安全、简便,同时让病人损伤少,无辐射。
目前公认的指南和标准均推荐中心静脉导管前端位置应到达上腔静脉中下1/3处靠近上腔静脉与右心房交界的地方,也是理想位置(CAJ)标记点[6-7],此处心血管解剖特点是细胞组织移行,有较明显的腔内碎裂电位。腔内心电识别在心血管介入科室中,尤其是心律失常射频消融的手术科室是基本要求。锁骨下静脉、颈内外静脉、上腔静脉及右心耳/右心房等组织腔静脉内膜电位具有独立特征,病人窦性心律有P波,进入上腔静脉后近心房处称为A波,其血管内各个腔电位包括上腔静脉电位均能在具有滤波功能心电机上清晰显示,识别并记录上腔静脉电位即可确认导管尖端处于上腔静脉与右心房交界处的CAJ。使用一根双头鳄鱼夹连接心电导线与中心静脉末端导丝,若中心静脉导管末端有输液通道,可在肝素帽上插入注射器针头再夹鳄鱼夹,此法将导管尖端作为心腔内电极片,引导导管尖端位置的静脉血管电位,置管过程中动态观察心电图P-QRS波形特征性变化,判定导丝头端所在位置[8]。重症医学科与电生理射频专业联合开展上腔静脉电位指导定位技术,突破常规12导联心电局限,融合中心静脉置管操作过程,实时读取导管前端电信号,达到精确、实时标记导管尖端位置。置管操作过程联合心电法既环保又经济,同时具有方便、快捷的特点。置管操作可在数分钟内完成,具有零辐射等优点,扩大床旁置管人群适应证。累计通过上腔静脉电位法植入中心静脉置管病人80例,术后1个月内复查肺部CT扫描,查阅影像电子底版,发现前期上腔静脉定位法均使中心静脉导管头端准确到达CAJ,而同片号肺
部CT正位肺窗中,导管头端影像学变化差异较大,多随体表身形、肺部疾病(如占位性病变或积液疾病)偏移。同期使用传统体表尺量及X线下定位置管病人80例,1个月内复查肺部CT,可见导管头端常有未及CAJ或过深入心房上缘,说明上腔静脉电位定位法具有植入精准的优势,本研究植入定位刻度单元可精确在5 mm以内,此法定位精准,操作与定位一体化,操作过程中可及时发现异位,并做出调整,无置管后反复调整复位步骤,不仅减轻病人痛苦,更节省人力、物力,同时有效减少对病人辐射伤害,提高满意度,并具有广泛的适应证。本研究回顾性分析采用两种定位方法的差异,现报道如下。
1 资料与方法
1.1 一般资料 选择2016年3月—2018年9月在大庆龙南医院重症医学科住院行中心静脉置管的心源性休克、重症心力衰竭及因病情需要长期输注各种刺激性药物或需监测中心静脉压病人160例。本研究获得病人及家属同意,并签署中心静脉置管知情同意书。160例病人中,男96例,女64例;年龄33~91(63.7±3.3)岁;经锁骨下或颈内静脉置入中心静脉导管159例,经颈外静脉置入中心静脉导管1例。纳入标准:穿刺血管直径2.6 mm(8F)以上,无凝血障碍。排除标准:植入心脏起搏器病人、凝血功能严重障碍、心房颤动。置管前选取静脉位置均通过超声引导定位,其中选取左右锁骨下静脉置管89例,左右颈内静脉置管70例,右侧颈外静脉置管1例。
1.2 方法
1.2.1 仪器及材料 采用巴德二维彩超型号Site Rite5,福田心电机型号FX8322,ARROW中心静脉导管7.0F、30 cm(型号CS-14703-E),穿刺套件及无菌穿刺包、双头鳄鱼夹导线,探头罩及耦合剂。
1.2.2 置管前准备 操作前为病人连接心电肢体导联LA、RA、LL、RL 4根导联线,设置滤波除去肌电干扰,并标准摆放体表心电图胸前V1导联观察P-QRS波型,同时将V2导联放置于第4肋间隙胸骨左缘即V1导联的胸骨对称位,V3导联放置于穿刺侧手臂同侧锁骨下窝处,并在同侧胸锁乳突肌外缘中点放置V4导联,V5导联放置于穿刺对侧锁骨下窝处,并在对侧胸锁乳突肌外缘中点放置V6导联,应用B超在锁骨下静脉或颈内静脉测量穿刺血管深度及直径,选择血管直径2.6 mm以上及合适穿刺点处穿刺。穿刺位置作常规标识,初步测量预估置管长度。留取并打印2 s胸前导联心电图,以右侧置管为例:走纸约5 cm心电图上可见体表电位(包括Ⅰ导联即右手导联,V1即右心电位,V2即左锁骨下静脉电位,V3即右锁骨下静脉电位,V4即右胸锁乳突肌外缘电位也就是颈外静脉电位,V5即左锁骨下静脉电位,V6即左胸锁乳突肌外缘电位也就是颈外静脉电位)。
1.2.3 置管过程 按流程消毒、超声引导、常规技术穿刺置管,将导管经钢丝送入静脉血管内即停止送入导管,使导管尾端与外露钢丝保持固定长度,并将鳄鱼夹一端连接在导管尾端钢丝上,另一端连接在同侧锁骨下电极V4或V5心电机导联,即在心电机上胸前导联图可见V1~V5导联全部信号,左侧置管以V5为例说明,此时V5导联即显示中心静脉导管头端所接触的外周静脉血管内膜电信号图,并呈现约2/3倍振幅的胸前V1导联P-QRS心电波形,腔内心电图形起始波形及振幅、时长均与Ⅰ导联一致,随着导管尖端深入,腔内心电变形,逐渐演变过度至V3-V1导联波形,依次呈现锁骨下静脉及上腔静脉电位信号(见图1、图2),最终呈现倒置P波及向量向下的高振幅QRS型,到达上腔静脉电位信号所在位置呈现W型P-QRS(见图3),此时导管尖端即到达CAJ。若导管移位至颈内静脉或颈外静脉,在V5导联出现与V4导联P-QRS振幅及起始方向一致的电位信号图形,无倒置P波,呈现短小的P-QRS型,即导管移行至颈部静脉血管内,此时通过超声扫描颈静脉证实。若导管在进入上腔静脉前穿入对侧锁骨下静脉,V5导联出现QRS波形反转,呈现与V3导联时相、振幅几乎一致的电位图。在心电机监控下缓慢推进导管,通过心电上V5导联P-QRS波变化判断导管尖端位置,并具有可重复的操作性。标准操作时推送导管前进,从外周进入上腔静脉前,V5导联P-QRS波振幅中的P波明显逐渐放大、加深,表明导管头端接近进入上腔静脉,P波最低点到达与QRS主波最低点平齐,两者呈尖锐的W型即表明导管尖端已到达上腔静脉与右心房交界处(CAJ),若继续送入右心房后P波呈极深负向(见图4),振幅由低再转高,此时需退回约1 cm或0.5 cm方可回到上腔静脉内。移位/异位导管时电信号变化均通过放大心电波形振幅及走纸速度进行个体化校正,以适应操作者自身的识别方便。
本研究操作时将导管送进出现P波从最低位后逐渐回撤至同导联QRS振幅1/3~1/2(约在最低点回撤0.5 cm),表明已到达理想靶点CAJ,之后撤出导管鞘及导丝,固定导管。术后常规透视或摄片确定导管前端位置并记录但不进行任何调整,术后1个月内病人复查肺部CT扫描,回顾性分析肺部CT影像电子版图片,均证实中心静脉导管头端准确到达CAJ(见图5),而同片号肺部CT的正位肺窗(见图6)及首次置管的胸片或透视报告中,头端深浅差异变化很大,相差1~2个肋间隙,相当于上腔静脉内上下滑动2 cm。病人若心电图P波短小不影响置管,通过预先测量置管长度,导管尖端置管到达预定深度后,仅对比V1及V5导联,识别上腔静脉电位,即可明确导管尖端位置是否标准,上腔静脉电位在小P病人呈现正负双向的细小碎裂电位,波峰尖锐时相短,逆P时相约提前体表心电图QRS波100 ms(在心电图纸上为2小格),将心电机走纸速度由原来的25 mm/s调整为100 mm/s即可识别提早体表心电QRS的上腔静脉电位。若尖端通过CAJ,则V5电位出现与上腔静脉电位反转形态,即反向的负正双向碎裂电位,此时回退导管,避免过深刺激心房,诱发心房颤动。

图1 锁骨下静脉电位信号

图2 上腔静脉电位信号
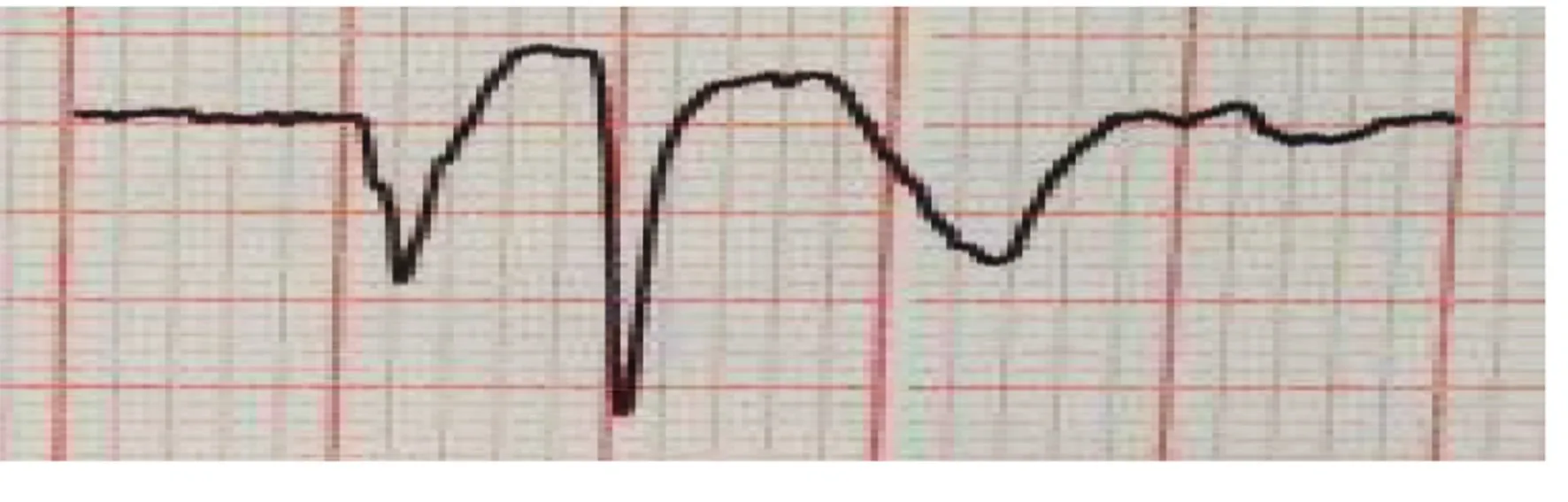
图3 CAJ电位信号

图4 心房上缘电位信号
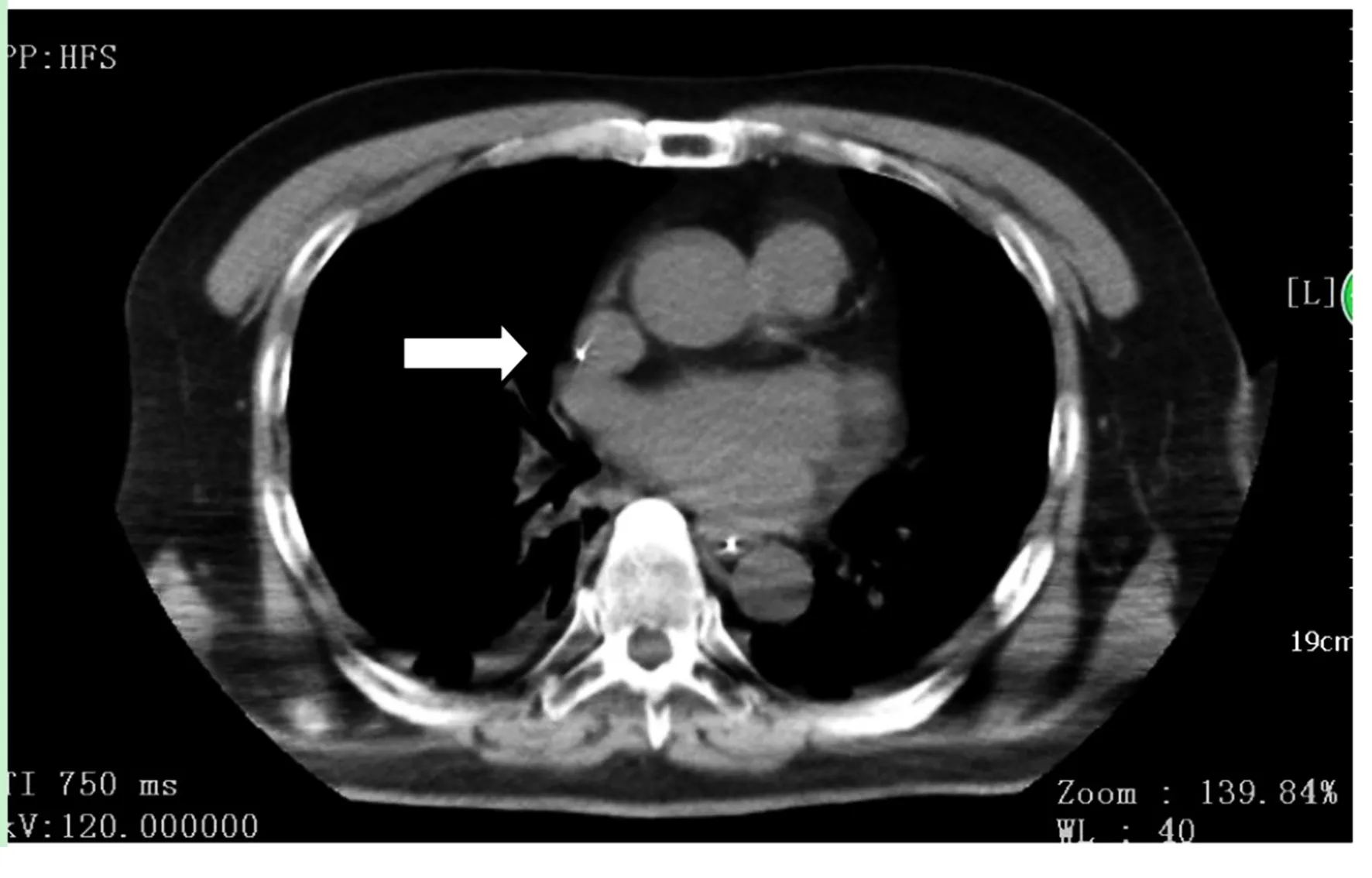
图5 肺CT电子版证实中心静脉导管头端准确到达CAJ

图6 肺部CT的正位肺窗
2 结 果
160例病人中心静脉置管过程顺利,80例病人利用上腔静脉电位定位术中实时操作导管,实时调整推送回撤导管,观察每步节点的理想静脉腔内电位图时继续推入导管,进入上腔静脉后见到CAJ电位均可直接固定置管。术后胸透或拍胸片并记录。同期使用传统体表尺量及X线下定位置管80例,经透视或胸片证实导管尖端在上腔静脉下1/3处。两组均在出院前复查肺部CT,复查后拷贝CT影像电子版,经电脑阅片放大处理,发现上腔静脉电位法置管到位率为100%,所有位置均在上腔静脉根部与心房连接组织移行处CAJ,而根据体表测量法或X片判读,共26例将要植入过深在第4肋骨下,28例在第3肋上缘,相对植入过浅,可见对不同病人身体条件下体表估测置管长度及X片定位心影凹陷处准确率仅30%左右,误差较大。使用常规方法测量及透视等定位法置管80例,1个月内复查肺部CT结果,差异较大,仅22例满足肺部CT薄扫片中可见导管在CAJ,47例在上腔静脉位置过浅,11例进入心房腔上缘,肺部CT检查后均需重
新调整导管头端位置外撤1~2 cm。
3 讨 论
3.1 上腔静脉电位指导定位法在中心静脉置管中的原理 置管过程实时使用钢丝尾端连接电极,摄取全程途径血管壁的电位信号,经心电机滤波筛出并调整走纸速度及波形振幅,探查头端P-QRS波,根据P-QRS波特征变化指引导管尖端定位一种方法[8]。此法将导管尖端本身作为心腔内的电极片,引导导管尖端位置的静脉血管电位,对有肝素帽尾端接头的导管在末端持续接输液联通电信号活动。心内电起源于窦房结,P波为心房除极波,电生理领域称为大A波,实为P波的另一叫法,其形态、振幅取决于电极与心房电向量轴之间的距离位置,头端导管进入上腔静脉后,引出高振幅P波[9]。该项技术的有效性已被国外众多麻醉医师论证和接受[10],并写入麻醉科指南。该方法首先排除心房颤动病人,由于心房颤动病人无P波,电生理射频消融系统学习后,方便并准确识别窦性心律下自身P波电位及P波在上腔静脉的特异电信号A波,实施该操作无难度[11]。
3.2 上腔静脉电位指导定位优点 利用静脉内电信号指导中心静脉导管尖端的定位是本研究目的,定位技术操作步骤简单易学、学习周期短、零辐射,尤其适合孕妇、老人及免疫力低下人群,保护病人白细胞,对行动不便、长期卧床,有床头置管需求及昏迷病人,不局限于放射科床头摄片,避免接受放射线损害。通过心电机清晰记录导管头端的心腔内电生理图像,并打印出来,住院期间任何时间均可重复检查,并将记录的图形按时间顺序排列比对,根据图形差异可知头端导管是否移位、前进和后退,并精准测定中心静脉压。利用上腔静脉电位特征判读导管位置,到达置管和定位一体化,将置管平均时间由原来的30 min缩短至10 min。
3.3 上腔静脉电位定位技术要点 熟悉心电机的使用,掌握基本心电图特征变化[12]。推送导管时速度均匀,导管末端持续连接输液器滴注或注射器推注,末尾用鳄鱼夹夹住将电信号引出至心电机胸前导联。观察监测体表胸前导联心电图。掌握P-QRS波变化,一般送导管至出现P波倒置时即进入上腔静脉下1/3处,控制W型最低点,不必送管过深至P波出现尖锐的正负双向波(表示已进入右心房或右心耳),避免引起病人心慌、心悸、胸闷等不适。针对体形高大的病人,部分中心静脉导管长度不够,故穿刺点选择尤为重要。对特殊病例,若有胸腔手术史或先天性血管变异病人,实时利用静脉内电位引导配合体表参考电极图形指引,可精准到达预定位置,利用该方法成功实施“镜面人”——先天性右位心置管,经颈外静脉置管1例,颈肩胸廓畸形及既往有心胸手术史病人13例,术后CT分辨均在CAJ组织移行处,深浅精确在5 mm内,利用腔静脉内的电信号引导置管,几乎不受穿刺部位及血管长度、扭曲、旋转等影响,导管长度最终的选择取决于终点是否出现上腔静脉电位,穿刺位点可自由选择[13-15]。
综上所述,熟悉上腔静脉电位指引定位技术在中心静脉置管的应用,具有便捷、实时、有效、可靠、安全等优点,可有效精准到达最佳位置,可在临床广泛推广应用。

