雷公藤多苷治疗糖尿病肾脏病临床疗效及安全性的Meta分析
张梦久,柳红芳,郭燕,史扬
(北京中医药大学,北京 100029)
糖尿病肾脏病(diabetes kidney disease,DKD)是糖尿病最主要、最常见的微血管并发症,是引起终末期肾脏疾病,甚至死亡的主要原因之一[1]。根据流行病学统计,预计到2030年,世界范围内的糖尿病患者将达到3.66亿,而DKD患者将超过1亿[2]。目前DKD的病因和发病机制尚不十分明确,主要包括代谢紊乱、肾脏血流动力学改变和遗传易感性等方面,随着炎症反应、氧化应激、足细胞损伤等机制研究的深入[3],DKD的治疗也从基础的控制血压、血糖、血脂、改善肾脏血流动力学转向探索抗炎、免疫抑制、保护足细胞、改善氧化应激等新型治疗手段[4]。
雷公藤为卫矛科、雷公藤属植物雷公藤的根,大毒,性凉,味辛、苦,其药理作用最早记录于《神农本草经》中,属于“从肾论治药物”,具有祛风除湿、解毒消肿、杀虫止痒、通络止痛等功效[5]。雷公藤多苷(tripterysium glycosides,TG)为雷公藤的提取物,研究表明,TG通过抑制炎症细胞因子及相关通路、改善氧化应激、保护足细胞及肾小球内皮功能等多条途径降低蛋白尿、改善肾小球硬化和间质纤维化[6],现广泛应用于肾脏疾病(DKD、肾小球肾炎、肾病综合征等)的治疗[7]。但2012年国家药品安全检测中心报告其不良反应较多,尤以药物性肝损伤显著,还涉及肾脏、血液及生殖系统的损害[8]。董一珠等[9]通过收集雷公藤成分性质的多个靶点,应用“靶点-通路”进行拓扑分析发现,雷公藤的毒性作用可能与药物代谢酶及细胞凋亡有关。本研究主要评估TG治疗DKD的临床疗效和安全性,为循证医学提供最新证据,给临床医师用药提供最新参考。
1 资料与方法
本Meta分析在PROSPERO官网注册,注册号CRD42018115905。
1.1纳入与排除标准
1.1.1纳入标准 ①研究类型:公开发表的国内外随机对照试验(randomized controlled trial,RCT),不受盲法限制,语种限定为中文或英文。②研究对象:糖尿病患者诊断标准符合WHO 1999年诊断标准[10],DKD患者诊断标准符合Mogensen诊断标准[11],DKD分期不限。③干预措施:对照组采用基础治疗,试验组加用TG。基础治疗包括饮食、运动、降糖、降压、调脂、抗凝、利尿等,或使用其他阳性药物包括黄葵胶囊/血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂(angiotonin Ⅱ receptor blocker,ARB)等药物。④结局指标:主要结局指标包括24 h尿蛋白定量、血白蛋白、血肌酐、血尿素氮。次要结局指标包括丙氨酸转氨酶、血白细胞计数。
1.1.2排除标准 ①重复发表、数据不全、无法获取全文的研究;②试验设计不严谨、统计方法不恰当的研究;③合并发热、感染、癌症、严重的心肝肺疾病患者。
1.2检索策略 检索中国知网、万方、维普、Cochrane Libarary、PubMed、Embase、Web of Science数据库,检索时间为建库至2018年12月7日。中文检索词:糖尿病肾病、糖尿病肾脏病、雷公藤。英文检索词:Diabetic Nephropathies,Diabetic Kidney Disease,Diabetic Renal Disease,Leigong Teng,Tripterygium,Thundergod Vine。检索方式为主题检索与自由词检索相结合。
1.3文献筛选与数据提取 两名研究员根据纳入与排除标准,独立筛选文献,按照数据提取表各自提取数据,并交叉核对。任何分歧都将由第三位研究员解决。数据提取表包括以下内容。①文献的基本特征:标题、作者、出版年份、出版国家、作者联系方式;②研究方法:随机方案,分配隐藏,盲法,数据完整性,选择性报告,其他偏倚;③研究对象特征:样本量、性别、年龄;④干预措施:具体用药,剂量,疗程,随访;⑤结局指标:治疗前后数据资料;⑥其他相关数据。如信息不完整,将联系原始作者以获取必要的数据资料。
1.4文献质量评价 采用Cochrane偏倚风险评估工具进行方法学质量评价:①随机序列的产生;②分配方案的隐藏;③盲法的使用,包括对研究者、受试者、结果评价者施盲;④结局数据的完整性,是否有失访及退出;⑤是否选择性报告;⑥是否存在其他偏倚。每条标准按照“是”“否”“不清楚”来划分,对纳入的研究进行“高风险”“低风险”“风险不确定”的判断。
1.5统计学方法 采用RevMan 5.3软件进行统计分析,二分类变量采用相对危险度(risk ratio,RR)为效应量,连续性变量采用均数差(mean difference,MD)为效应量,当对同一干预措施的测量单位/方法相同时,采用加权均数差(weighted mean difference,WMD),否则采用标准化均数差(standardized mean difference,SMD),区间估计采用95%置信区间(confidence interval,CI)。采用χ2检验对纳入的研究进行异质性分析,若I2<50%,P>0.1,表明各研究间无异质性,采用固定效应模型合并效应量,否则采用随机效应模型合并效应量,并根据可能导致异质性的因素进行亚组分析。若各试验间存在统计学异质性,而无临床异质性或差异无统计学意义,则采用随机效应模型合并效应量。若异质性过大或无法寻求异质性来源,则采用描述性分析。采用漏斗图进行发表偏倚的检测。针对研究的特征或类型进行敏感性分析。
2 结 果
2.1文献筛选流程 共检索文献1 396篇,剔除重复文献,再阅读文题、摘要筛选,最后阅读全文复筛,最终纳入文献16篇[12-27],均为中文文献,发表年份为2005—2016年。见图1。
2.2纳入研究的基线特征 纳入的16个RCT均在中国进行,共973例患者,其中试验组523例,对照组450例,有2项RCT未报告患者年龄和性别。纳入的研究中有7项RCT[13,17-18,22,24,26-27]采用TG与常规治疗做对照,有6项RCT[12,14,16,19-20,25]采用TG+ARB与ARB做对照,有1项RCT[23]采用TG与ARB做对照,有2项RCT[15,21]采用TG+黄葵胶囊与黄葵胶囊做对照。有1项RCT[17]的试验组采用低、中、高剂量的亚组。疗程为2~6个月。见表1。
2.3方法学质量评价 纳入的16篇RCT中仅 3篇提及随机分组的方法为随机数字表,其余均以“随机”字样描述,16篇RCT均未提及随机分配方案的隐藏、盲法、是否有选择性报告及其他偏倚。1例 RCT[12]提及个例患者因不良反应而退出试验。见图2。
2.4Meta分析结果
2.4.124 h尿蛋白定量 16项RCT[12-27]报告了24 h尿蛋白定量值(均为治疗终点值),其中1项RCT[17]设计了TG的低、中、高剂量的试验亚组。共973例患者,其中试验组523例,对照组450例。各研究间存在统计学异质性(P<0.000 01,I2=71%),采用随机效应模型合并效应量,结果显示,试验组24 h尿蛋白定量明显低于对照组(SMD=-0.78,95%CI-1.03~-0.54,P<0.000 01),见图3。16项RCT中,有1项RCT[17]TG剂量为20 mg/d,3项RCT[12,15,17]TG剂量为30 mg/d,2项RCT[17,25]TG剂量为40 mg/d,5项RCT[14,22-23,26-27]TG剂量为60 mg/d,1项RCT[20]
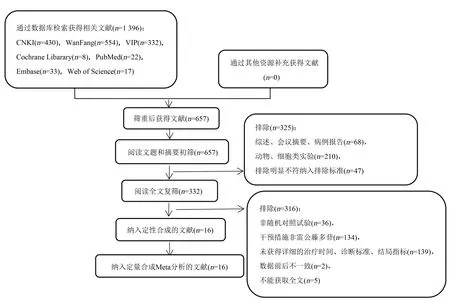
图1 文献筛选流程图
表1 纳入研究的基线信息
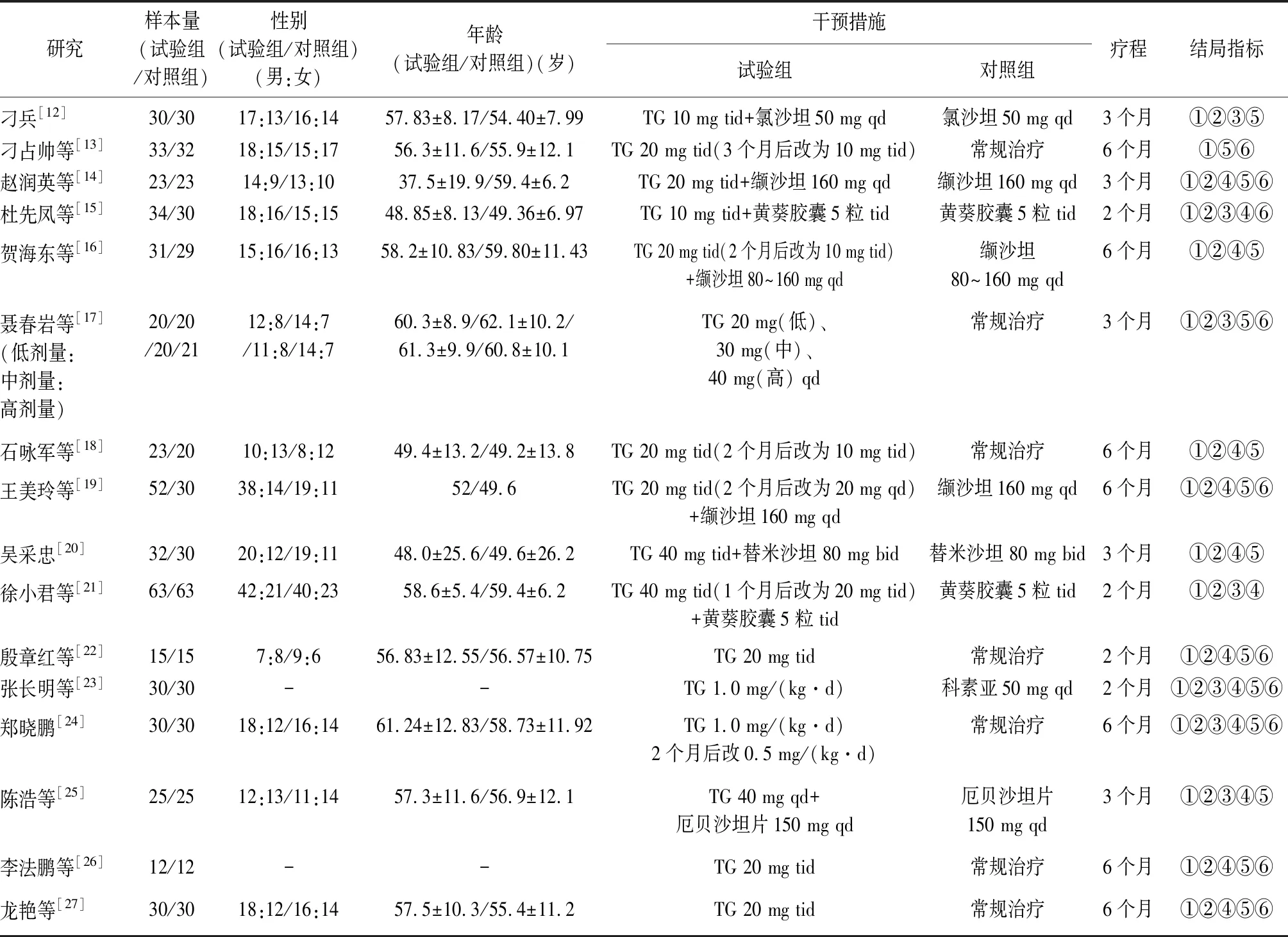
研究样本量(试验组/对照组)性别(试验组/对照组)(男:女)年龄(试验组/对照组)(岁)干预措施试验组对照组疗程结局指标刁兵[12]30/3017:13/16:1457.83±8.17/54.40±7.99TG 10 mg tid+氯沙坦50 mg qd氯沙坦50 mg qd3个月①②③⑤刁占帅等[13]33/3218:15/15:1756.3±11.6/55.9±12.1TG 20 mg tid(3个月后改为10 mg tid)常规治疗6个月①⑤⑥赵润英等[14]23/2314:9/13:1037.5±19.9/59.4±6.2TG 20 mg tid+缬沙坦160 mg qd缬沙坦160 mg qd3个月①②④⑤⑥杜先凤等[15]34/3018:16/15:1548.85±8.13/49.36±6.97TG 10 mg tid+黄葵胶囊5粒 tid黄葵胶囊5粒 tid2个月①②③④⑥贺海东等[16]31/2915:16/16:1358.2±10.83/59.80±11.43TG 20 mg tid(2个月后改为10 mg tid)+缬沙坦80~160 mg qd缬沙坦80~160 mg qd6个月①②④⑤聂春岩等[17](低剂量:中剂量:高剂量)20/20/20/2112:8/14:7/11:8/14:760.3±8.9/62.1±10.2/61.3±9.9/60.8±10.1TG 20 mg(低)、 30 mg(中)、40 mg(高) qd常规治疗3个月①②③⑤⑥石咏军等[18]23/2010:13/8:1249.4±13.2/49.2±13.8TG 20 mg tid(2个月后改为10 mg tid)常规治疗6个月①②④⑤王美玲等[19]52/3038:14/19:1152/49.6TG 20 mg tid(2个月后改为20 mg qd)+缬沙坦160 mg qd缬沙坦160 mg qd6个月①②④⑤⑥吴采忠[20]32/3020:12/19:1148.0±25.6/49.6±26.2TG 40 mg tid+替米沙坦 80 mg bid替米沙坦 80 mg bid3个月①②④⑤徐小君等[21]63/6342:21/40:2358.6±5.4/59.4±6.2TG 40 mg tid(1个月后改为20 mg tid)+黄葵胶囊5粒 tid黄葵胶囊5粒 tid2个月①②③④殷章红等[22]15/157:8/9:656.83±12.55/56.57±10.75TG 20 mg tid常规治疗2个月①②④⑤⑥张长明等[23]30/30--TG 1.0 mg/(kg·d)科素亚50 mg qd2个月①②③④⑤⑥郑晓鹏[24]30/3018:12/16:1461.24±12.83/58.73±11.92TG 1.0 mg/(kg·d)2个月后改0.5 mg/(kg·d)常规治疗6个月①②③④⑤⑥陈浩等[25]25/2512:13/11:1457.3±11.6/56.9±12.1TG 40 mg qd+厄贝沙坦片150 mg qd厄贝沙坦片150 mg qd3个月①②③④⑤李法鹏等[26]12/12--TG 20 mg tid常规治疗6个月①②④⑤⑥龙艳等[27]30/3018:12/16:1457.5±10.3/55.4±11.2TG 20 mg tid常规治疗6个月①②④⑤⑥
TG:雷公藤多苷;qd:每日1次;bid:每日2次;tid:每日3次;-:文献未提及;结局指标:①24 h尿蛋白定量;②血肌酐;③血尿素氮;④血白蛋白;⑤丙氨酸转氨酶;⑥血白细胞计数
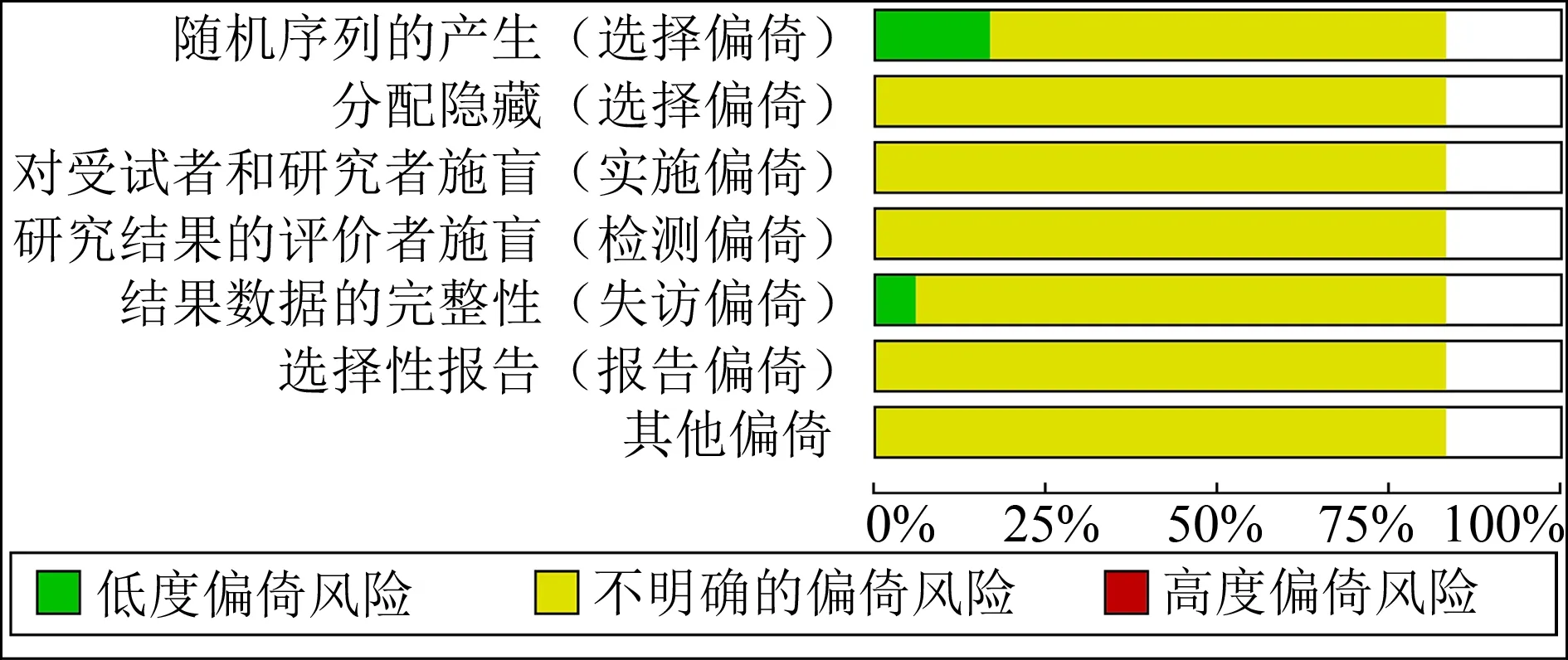
图2 方法学质量评价图
TG剂量为120 mg/d,其余RCT服药期间均有过剂量调整。将未有过剂量调整的RCT按服用剂量不同进行亚组处理,结果显示:TG 30 mg/d组,各研究间无统计学异质性(P=0.37,I2=0%),试验组24 h尿蛋白定量值低于对照组(SMD=-0.38,95%CI-0.69~-0.07,P=0.02);TG 40 mg/d组中,各研究间无统计学异质性(P=0.96,I2=0%),试验组24 h尿蛋白定量值低于对照组(SMD=-0.47,95%CI-0.89~-0.05,P=0.03);TG 60 mg/d组中,各研究间存在统计学异质性(P=0.05,I2=57%),试验组24 h尿蛋白定量值低于对照组(SMD=-1.30,95%CI-1.76~-0.83,P<0.000 01)。见图4。
2.4.2血白蛋白 13项RCT[14-16,18-27]报告了血白蛋白值,试验组400例,对照组367例,各研究间存在统计学异质性(P=0.000 3,I2=67%),采用随机效应模型合并效应量,结果显示,试验组血白蛋白明显高于对照组(SMD=0.61,95%CI0.34~0.87,P<0.000 01),见图5。
2.4.3血肌酐 15项RCT[12,14-27]报告了血肌酐值,试验组490例,对照组460例,各研究间存在统计学异质性(P<0.000 01,I2=89%),采用随机效应模型合并效应量,结果显示,试验组血肌酐值低于对照组(SMD=-0.44,95%CI-0.85~-0.03,P=0.04),见图6。

图3 试验组和对照组24 h尿蛋白定量森林图
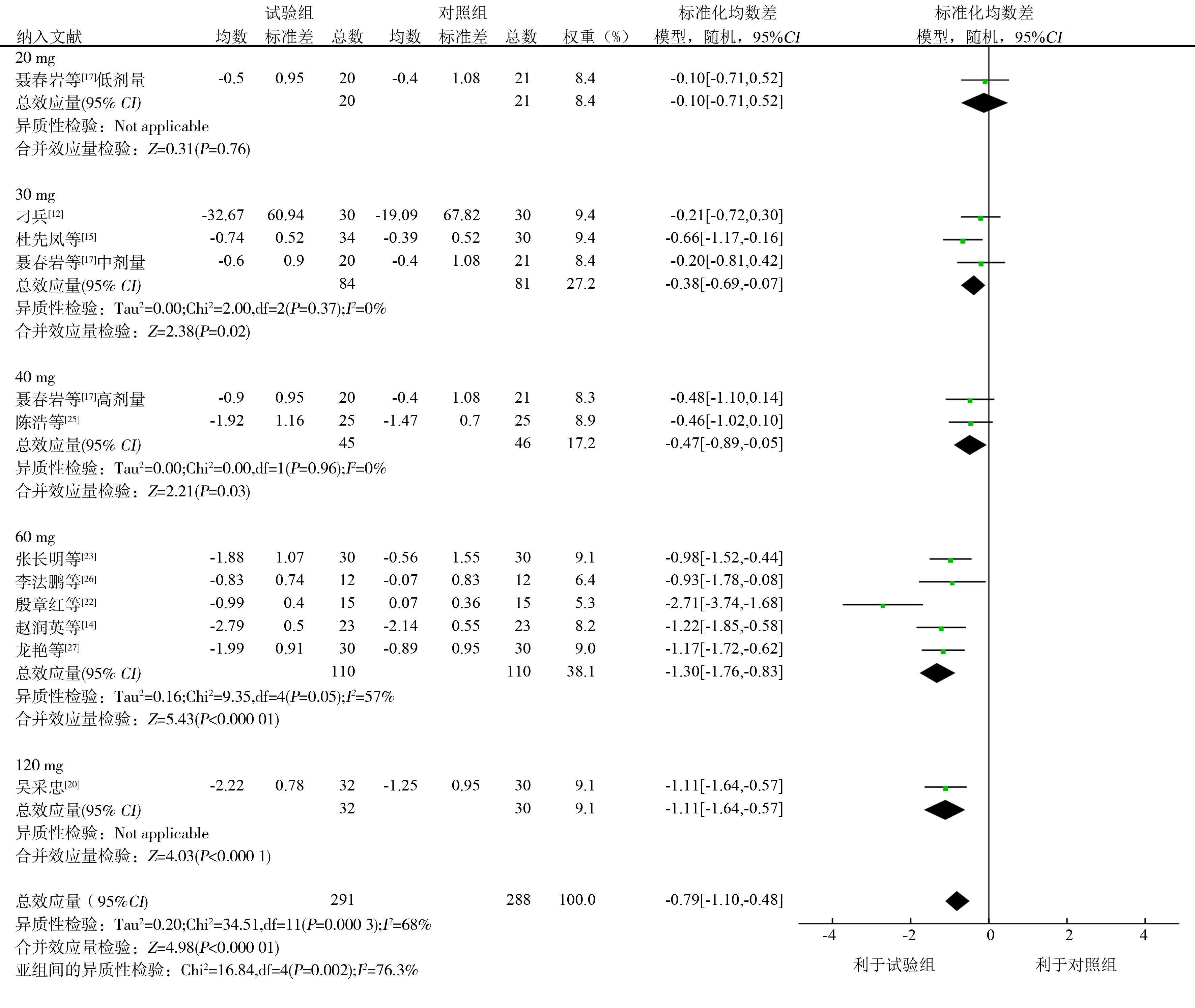
图4 试验组和对照组24 h尿蛋白定量亚组森林图
2.4.4血尿素氮 7项RCT[12,15,17,21,23-25]报告了血尿素氮值,试验组272例,对照组271例,各研究间无统计学异质性(P=0.83,I2=0%),采用固定效应模型合并效应量,结果显示,试验组血尿素氮低于对照组(WMD=-0.30,95%CI-0.59~-0.01,P=0.04),见图7。
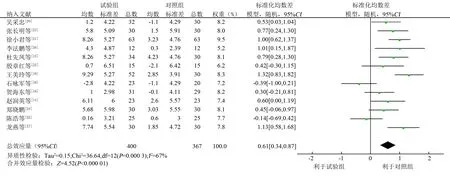
图5 试验组和对照组血白蛋白森林图
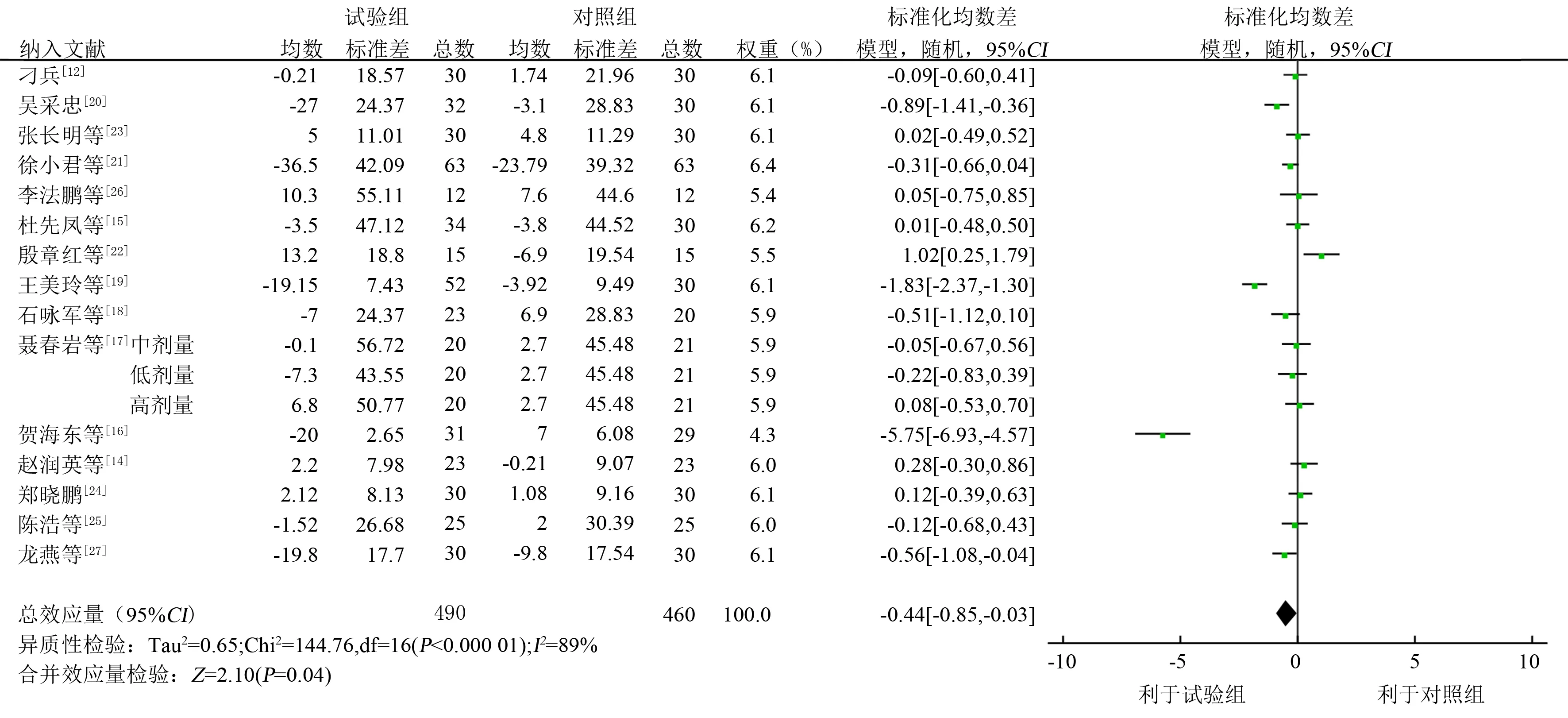
图6 试验组和对照组血肌酐森林图
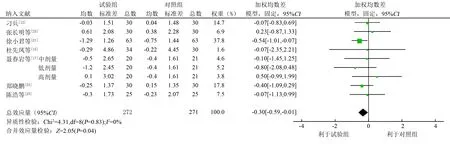
图7 试验组和对照组血尿素氮森林图
2.4.5丙氨酸转氨酶 14项RCT[12-14,16-20,22-27]报告了丙氨酸转氨酶,试验组426例,对照组399例,各研究间存在统计学的异质性(P<0.000 01,I2=81%),采用随机效应模型合并效应量,结果显示,试验组和对照组丙氨酸转氨酶比较差异无统计学意义(SMD=0.26,95%CI-0.06~0.59,P=0.11),见图8。
2.4.6血白细胞计数 10项RCT[13-15,17,19,22-24,26-27]报告了血白细胞计数,试验组319例,对照组295例,各研究间存在统计学的异质性(P<0.000 1,I2=72%),采用随机效应模型合并效应量。结果显示试验组和对照组白细胞计数比较差异无统计学意义(WMD=-0.29,95%CI-0.72~0.14,P=0.18),见图9。
2.5不良反应 13篇RCT中有13篇[12,14-22,24-26]报告了不良反应,其中11篇[12,14-21,25,26]报告了不良反应的类型和例数,2篇[22,24]报告未发生不良反应,3篇[13,23,27]未提及不良反应。共纳入830例患者,其中试验组430例,42例发生不良反应,发生率为9.77%,对照组400例,18例发生不良反应,发生率为4.5%。不良反应主要包括肝功能异常(4.65%)、胃肠道反应(3.02%)、月经紊乱(1.40%)、白细胞减少(1.16%)。各研究间无统计学异质性(P=0.49,I2=0%),采用固定效应模型合并效应量,结果显示,试验组不良反应发生率高于对照组(RR=1.97,95%CI1.22~3.19,P=0.006),见图10。
2.6敏感性分析 本研究纳入的16篇RCT[12-27]方法学质量均较低,均未提及随机分配方案的隐藏、盲法,故未能进行敏感性分析。
2.7发表偏倚检测 以24 h尿蛋白定量为指标绘制漏斗图,共纳入16个RCT[12-27],结果显示各RCT基本分布于漏斗图的顶部,且向中间集中,少数RCT分布偏远,呈偏态分布,提示可能存在发表偏倚,无统计学意义的研究结果可能未被发表。见图11。
3 讨 论
中药雷公藤为雷公藤属植物雷公藤的根,TG则是从雷公藤根提取和精制的混合物,主要包括倍半萜生物碱、雷公藤总内酯、雷公藤内酯醇等多种成分[28],具有抗炎、抗菌、免疫调控等功效,是临床上比较常用的免疫调节药物[29]。TG可以通过多条途径治疗DKD,黄燕如等[30]研究发现,TG可以下调小鼠肾脏组织磷酸化信号通路的关键信号因子磷酸化p38促分丝裂原活化的蛋白酶表达,抑制炎症信号通路,从而改善肾组织的炎症损伤。凌厉等[31]通过检测糖尿病肾病大鼠足细胞Nephrin蛋白的表达,表明TG干预后Nephrin蛋白表达增强,从而改变足细胞的结构保护肾脏。常保超[32]研究发现,TG可以抑制大鼠肾脏组织的Wnt/β联蛋白的信号通路活化,使转化生长因子-β、β联蛋白、Wnt-1、磷酸化糖原合成酶激酶及核因子κB表达明显减少,改善肾小球基膜,减轻肾脏损害,从而延缓DKD的进展。
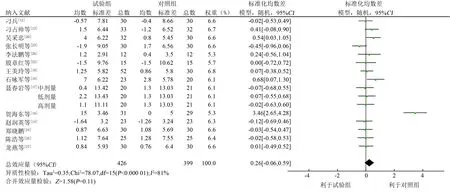
图8 试验组和对照组丙氨酸转氨酶森林图
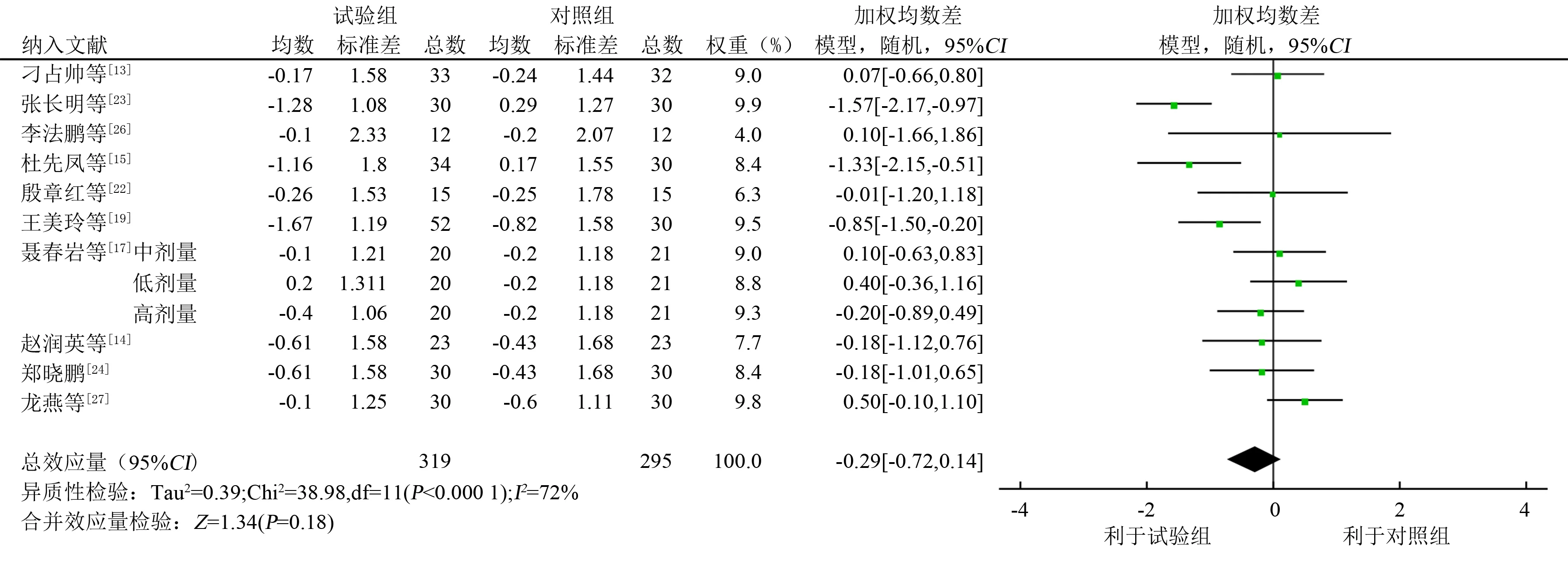
图9 试验组和对照组血白细胞森林图

图10 试验组和对照组不良反应森林图
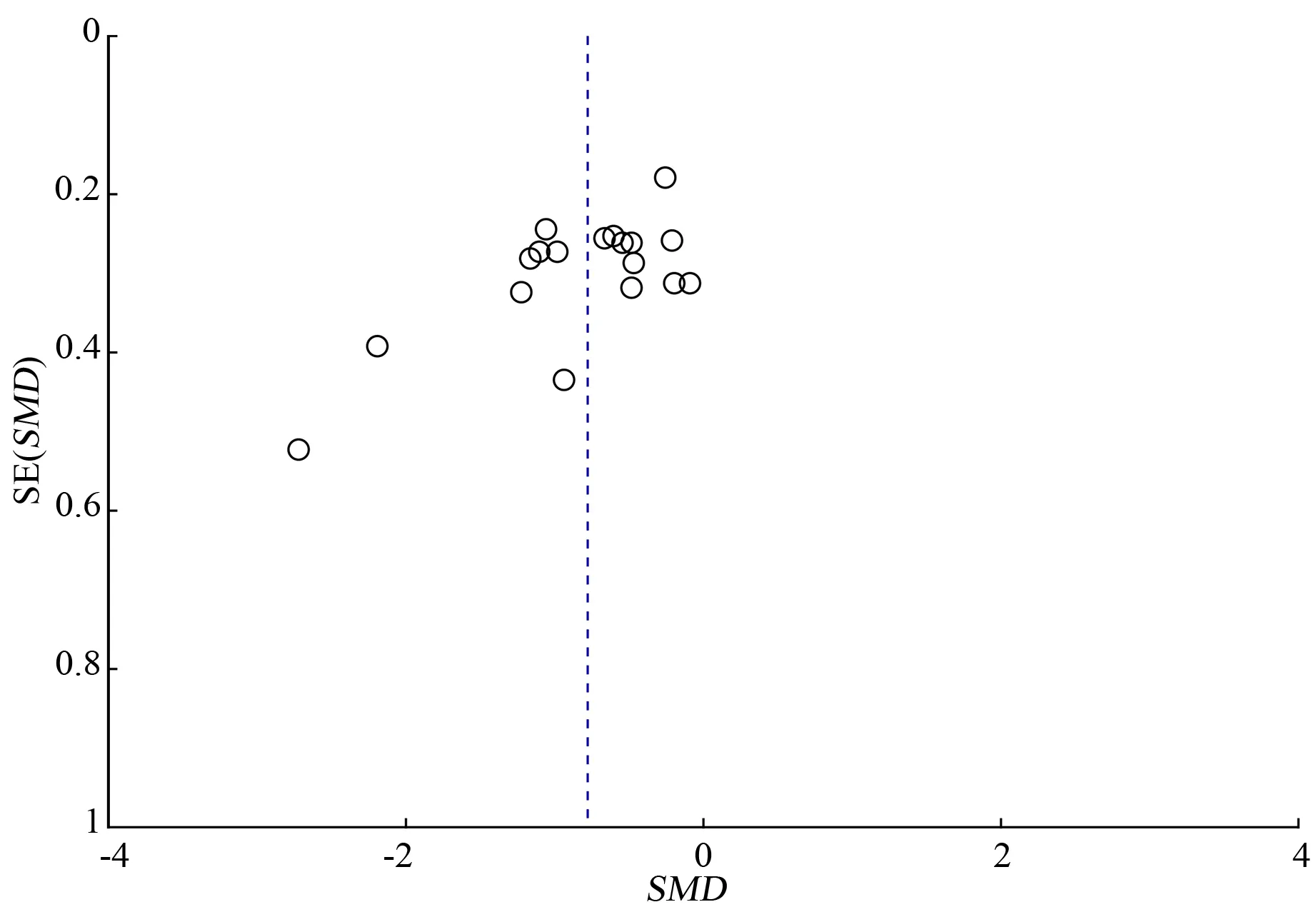
SMD:标准化均数差
本Meta分析共纳入16篇RCT,973例患者。结果显示:相对于常规治疗和单独应用ARB或黄葵胶囊药物,加服TG治疗DKD能显著降低24 h尿蛋白定量,提高血白蛋白水平,根据服用剂量进行亚组分析显示TG口服剂量>30 mg/d时能明显降低24 h尿蛋白定量,且在30~60 mg/d的剂量范围内,随着药物剂量的增大,降低24 h尿蛋白定量的效果越显著,但TG口服剂量为60 mg/d和120 mg/d时,降低24 h尿蛋白定量的效果差别不大。试验组加服TG能够降低DKD病患者血肌酐和血尿素氮,在一定程度上可改善肾功能,延缓肾功能的恶化。试验组与对照组丙氨酸转氨酶、血白细胞计数比较差异无统计学意义(P>0.05),试验组不良反应发生率高于对照组,但不良反应症状均较轻,予停药或对症治疗后均可恢复。
本Meta分析的创新点:①目前TG仍是临床治疗DKD的优势中药提取物,关于其临床疗效与不良反应的大数据统计Meta分析已过于陈旧,不能给临床医师提供最新的参考依据,且有诸多纳入标准限制,为此本研究实施了更新、更全面、更符合临床实际的荟萃分析。②本研究首次创新性的将TG服用剂量作亚组分析,观察不同剂量条件下的24 h尿蛋白定量改善值,虽然存在服用药物时间不齐的临床限制,但本研究纳入的579例患者仍可以粗略的为临床医师提供剂量上的参考。③本研究结果与既往研究存在出入,既往研究认为TG对DKD患者的肾功能无改善作用[33],但本研究结果证实试验组在降低血肌酐、降低血尿素氮方面优于对照组,即TG在一定程度上可延缓肾功能的恶化。
本研究仍存在以下局限性:①方法学质量低下,仅3篇RCT描述了随机序列的产生,对于分配方案的隐藏、盲法,16篇RCT均未提及,并可能存在一定的发表偏倚。②对于临床一线用药且能够降低蛋白尿的血管紧张素转换酶抑制剂/ARB类药物,有些研究的对照组并未提及是否应用。③TG为中药雷公藤的提取物,目前主要是国内应用广泛,国内期刊可见大量报道,而国外则缺乏研究,本研究虽检索了中英文数据库,但最后纳入的973例受试者均为中国人,受到地域、饮食等环境因素影响。以上因素均可能影响本研究结论的真实性和可靠性。
综上所述,联合TG治疗DKD的临床疗效肯定,安全性相当,为临床医师在治疗方案的选择上提供了一定的证据支持。但仍期待更多高质量、大样本、多中心的随机双盲对照试验,为二次评价提供更加准确客观的循证医学结论。

