粉煤灰提铝硅钙渣矿化固定CO2
马卓慧,廖洪强,程芳琴,李 福
(1.山西大学资源与环境工程研究所,国家环境保护煤炭废弃物资源化高效利用技术重点实验室,太原 030006;2.山西大学环境工程系,太原 030006)
0 引 言
硅钙渣是高铝粉煤灰提铝的副产物。其工艺是先加入碱石灰或石灰石溶出粉煤灰中的SiO2,以此达到硅铝的初步分离目的,再通过湿法提取氧化铝。回收碱后剩余的固体残渣,其钙含量(以CaO计)约为50%、硅含量(以SiO2计)约为30%,故称为硅钙渣[1-3]。硅钙渣是米黄色的粉状物,质轻、浆液pH值显强碱性。据报道,采用石灰石烧结法从粉煤灰中提取Al2O3,每提取1 t Al2O3产生的硅钙渣的量为9 t[1];采用碱石灰烧结法从粉煤灰中提取Al2O3,每提取1 t Al2O3产生的硅钙渣的量为2.5 t[1]。目前,硅钙渣的主要利用途径为脱除酸性气体SO2[2-3],制备硅钙肥供农业使用[4],作为水泥原料之一添加在生料中进行焙烧[5-6],制备硅酸钙板[7-8],制备碱激发胶凝材料[9-10]。硅钙渣资源综合利用率并不高,绝大部分的废渣处于无序堆放状态,在不带来经济效益的同时,还污染周边环境。
全世界每年CO2排放量约400亿吨,化石燃料燃烧所导致的CO2污染和“温室效应”已严重威胁环境。中国是CO2排放大国,面临减排的巨大压力,2016年11月《巴黎协议》生效,落实二氧化碳减排行动计划,中国有信心和决心实现减排承诺,承诺到2020年CO2排放比2015年下降18%,2030年比2005年下降60%~65%。CO2减排利用已成为全人类的共识,在众多CO2减排利用技术中,矿化固定CO2因其成本低、固碳规模大和可利用碱性固废等优势,日益受到业内专家学者的关注。
“矿化”一词最早是由Seifritz在1990年首次提出[11],是矿物碳酸化的缩写,原意指的是采用天然矿石或者含钙、镁的碱性工业固废为原料,模仿自然界含钙、镁的天然矿石自发地与空气中的CO2反应生成CaCO3的过程。目前用于矿化固定CO2的碱性固废有钢渣[12-13]、电石渣[14-16]、炉渣[17-18]、粉煤灰[19-20]、脱硫石膏[21-22]等。
硅钙渣中钙元素含量高,并且碱性物质含量大,浆液pH值高,赋予了其可以矿化固定CO2的能力。利用硅钙渣矿化固定CO2的研究在国内还刚刚起步。因此,本论文研究硅钙渣矿化固定CO2的基本特性,以期形成以废渣治理温室气体的“以废治废”新的减排利用模式。
1 实 验
1.1 原 料
硅钙渣取自内蒙古大唐国际再生资源有限公司,先烘干,后粉磨,最终置于封口袋中备用。硅钙渣的粒径分布由激光粒度仪测得,如表1所示。采用钢瓶高纯CO2气体供气,其浓度为99.99%。去离子水由实验室提供。原料硅钙渣的主要化学成分分析如表2所示。

表1 硅钙渣粒径分布Table 1 Particle size distribution of silica calcium slag
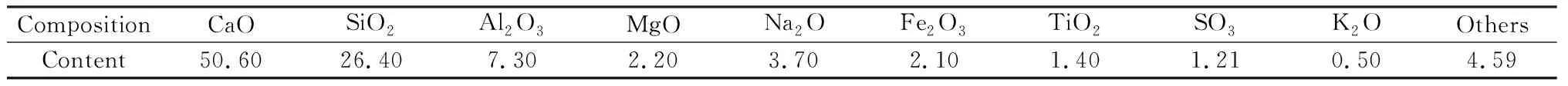
表2 硅钙渣主要成分分析Table 2 Main composition analysis of silica calcium slag /wt%
1.2 实验方法
实验首先将100.00 mL的蒸馏水加入三口烧瓶中,将其放入恒温加热磁力搅拌器中,边搅拌边加热液体到55 ℃。然后称10 mg的硅钙渣,加入三口烧瓶中,以300 r/min的速率搅拌,待pH值稳定5 min后,以1.2 L/min的流量通入CO2,同时在线记录pH值的变化,得到浆液pH值随时间变化的曲线。待pH值接近中性并稳定一段时间后,停止通气,此时反应结束。将反应后浆液抽滤,得到固相产物和滤下液。将固相产物置于105 ℃烘箱中干燥至恒重,将干燥物取出研磨并过200目筛子,取其筛下物装袋密封,测试备用。将滤液置于电炉上加热至近干,再放入105 ℃烘箱中干燥至恒重,将干燥物取出研磨并过200目筛子,取其筛下物装袋密封,测试备用。实验装置如图1所示。
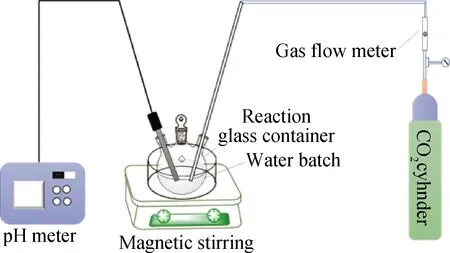
图1 实验装置示意图Fig.1 Schematic diagram of the experimental device
1.3 表征分析方法
(1)用Mastersizer 3000,Malvern(Germany)型激光粒度仪(Laser Particle Size Analyzer,LPSA)测定硅钙渣的粒径分布,固液比为0.10 mg/mL,分散介质为乙醇。
(2)用S8 Tiger,Bruker(Germany)型X射线荧光光谱仪(X-ray Fluorescence,XRF)分析测定原料的化学组成。
(3)用PHS-3E(China)型pH计(pH meter)在线监测水解、矿化过程中浆液的pH值。
(4)用Thermal fisher ICAP 6300(America)型电感耦合等离子体-原子发射光谱仪(Inductively Coupled Plasma Optical Emission Spectroscopy,ICP-OES)测定滤液中各金属元素的溶出量。
(5)用D2-Phaser,Bruker(Germany)型X射线衍射仪(X-ray Diffractometer,XRD)测定水化、碳酸化反应前后原料、产物的矿物组成。测试条件为:狭缝宽度为0.38 mm,衍射角为10°~80°,扫描速率为0.02°·s-1。
(6)用JSM-IT500HR(Japan)型扫描电子显微镜(SEM-EDS)观察原料和矿化产物的形貌和元素组成。
(7)用Pyris 1,PerkinElmer(America)型热重分析仪(Thermal Gravimetric Analysis,TGA)测定原料及产物的热失重特性,测试条件为:N2气氛,升温范围为20~850 ℃,升温速率为10 ℃/min。
2 结果与讨论
2.1 硅钙渣水解、矿化反应过程中浆液pH值变化特性
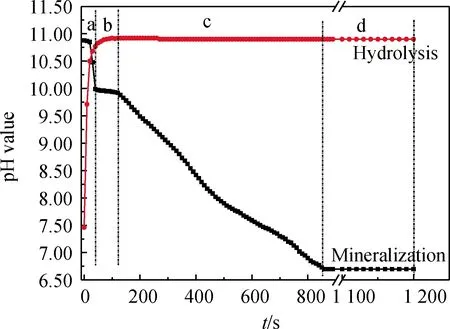
图2 硅钙渣水解、矿化过程中t-pH值曲线Fig.2 t-pH value curves during the hydrolysis andmineralization of silica calcium slag
硅钙渣水解及矿化CO2过程中浆液pH值随时间的变化曲线如图2所示。
硅钙渣的水解反应是矿化反应的先驱步骤。在整个水解、矿化的过程中发生(1)~(10)的化学反应。
CaO(s)+H2O→Ca(OH)2(aq)
(1)
CO2(g)→CO2(aq)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
由图2可知,在水解过程的前90 s内,硅钙渣浆液的pH值从7.47迅速升到10.91,pH值的变化速率为(10.91-7.47)/90=0.038 unit/s。并在随后的反应过程中浆液的pH值几乎保持不变。这是由于发生了反应(1)所致。这说明硅钙渣在水介质中极易发生水解反应,快速释放出[OH]-,使浆液pH值快速升高至10.91,显示出强碱性,和很强的矿化固定CO2的能力。
从矿化过程的t-pH值曲线分析,在矿化过程中,体系中发生的化学反应为(2)~(9)。整个过程分为四个阶段,前40 s内(a段),pH值从10.91迅速下降到9.99,pH值的变化速率为(10.91-9.99)/40=0.023 unit/s。在此阶段内pH值下降速度较快,说明CO2被快速矿化,这可能是由于硅钙渣浆液中事先水解出的大量的Ca2+和OH-可以迅速和CO2发生矿化反应,快速消耗浆液中的OH-,从而导致浆液pH值迅速降低。在40~120 s阶段(b段),pH值保持相对平稳的状态,约为9.95。这说明此阶段CO2矿化反应较为稳定,也就是浆液中硅钙渣水解产生的OH-速度等于浆液吸收CO2所产生的H+速度,使得浆液pH值保持相对稳定。在120~850 s阶段(c段),pH值从9.99下降到6.68,pH值的变化速率为(9.99-6.68)/730=0.005 unit/s。这说明此阶段CO2矿化反应不断缓慢进行,也就是浆液中硅钙渣水解产生OH-速度低于浆液吸收CO2所产生的H+速度,导致浆液pH值不断下降。矿化反应850 s后(d段)的反应时间内,pH值为6.68并保持不变。这说明此阶段的矿化反应基本完成,也就是浆液中硅钙渣水解产生OH-速度远远低于浆液吸收CO2所产生的H+速度,且浆液吸收CO2已经达到饱和状态,硅钙渣水解基本完成,使得浆液pH值保持不变。浆液中因为有CO2的溶入,呈现弱酸性。
2.2 硅钙渣水解、矿化反应后滤液中主要元素溶出特性
硅钙渣水解和矿化反应后滤液中的各主要元素的含量如表3所示。

表3 滤液中主要元素含量Table 3 Contents of main elements in filtrate /(mg/L)
由表3可知,矿化后滤液中Ca、Si元素含量明显增加,这是因为硅钙渣中的Ca2Si2O4在H2CO3存在的条件下发生反应(10),溶液中有Ca、Si元素溶出。Al元素在强碱性体系中可以被消耗掉,故浓度降低。矿化前后Fe元素浓度不变,说明其在整个过程中未发生明显化学反应。Mg元素在H2CO3存在的条件下,可以从磷镁矿中溶出,故浓度增加。
(10)
2.3 XRD分析

图3 硅钙渣原料、矿化产物和滤液蒸干渣的XRD谱Fig.3 XRD patterns of silica calcium slag raw material,mineralized products and filtrate evaporated slag
图3给出了硅钙渣原料、矿化反应后的固相产物、滤液蒸干渣的矿相组成。
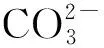
2.4 SEM-EDS分析
为了研究硅钙渣原料、水解反应固相产物、矿化反应后滤液蒸干渣、矿化反应固相产物的形貌及结晶生长情况,对所得固体进行了扫描电镜-能谱测试分析,结果如图4所示。
从图4(a)可知,硅钙渣原料结构致密,未见孔道。表面凹凸不平,这是由于在碱法提铝的过程中,粉煤灰颗粒被碱液侵蚀所致。从图4(b)可知,水解反应后,在硅钙渣表面附着了许多微小的颗粒物。从图4(c)可知,滤液蒸干渣中有棒状的晶体出现,这是反应生成的碳酸钠晶体,此结论和XRD的表征结果一致。从图4(d)可知,硅钙渣矿化反应后生成了方解石型的CaCO3,未见其他晶型的CaCO3生成。且方解石型CaCO3主要附着在硅钙渣表面,沿硅钙渣颗粒表面紧密生长,这种结构势必抑制硅钙渣与CO2进一步深入矿化反应,如何破解这种抑制矿化的碳酸钙原位覆盖生长结构,是提高硅钙渣与CO2矿化反应效率的重要途径。

图4 硅钙渣原料、水解产物、滤液蒸干渣、固相产物SEM照片Fig.4 SEM images of silica calcium slag raw material, hydrolytic products, filtrate evaporated slagand solid phase products
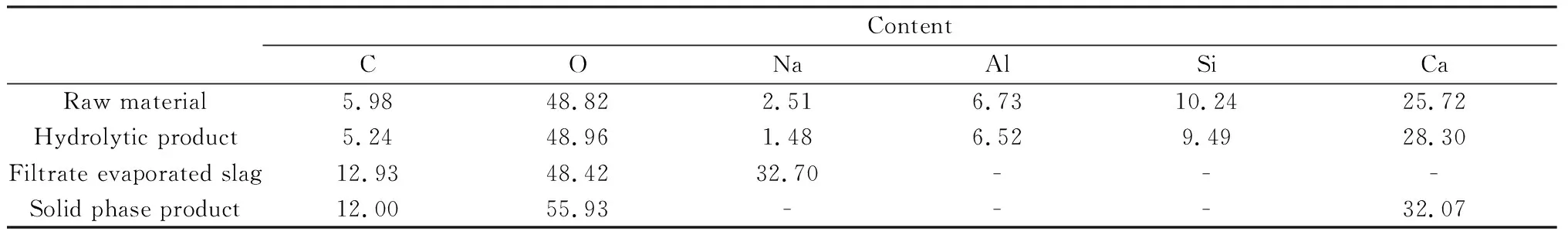
表4 EDS测各元素含量Table 4 Content of main elements in filtrate analyzed by EDS /%
在SEM的同倍数下对硅钙渣原料、水解产物、矿化产物进行EDS面扫描,EDS主要元素百分比含量如表4所示。从表4可知,硅钙渣原料主要含有C、O、Na、Al、Si、Ca元素,其百分含量分别为5.98%、48.82%、2.51%、6.73%、10.24%、25.72%。其中,C、O、Al、Si元素来自于粉煤灰,Na元素来自于提铝过程所加的碱,Ca元素一部分来自于粉煤灰,一部分来自于提铝过程中加入的石灰石。硅钙渣水解反应后元素的种类和含量均未发生明显变化。硅钙渣矿化反应后的固相产物中的主要元素为C、H、O三种,其含量接近CaCO3中三种元素的含量,即矿化反应后的产物为CaCO3。
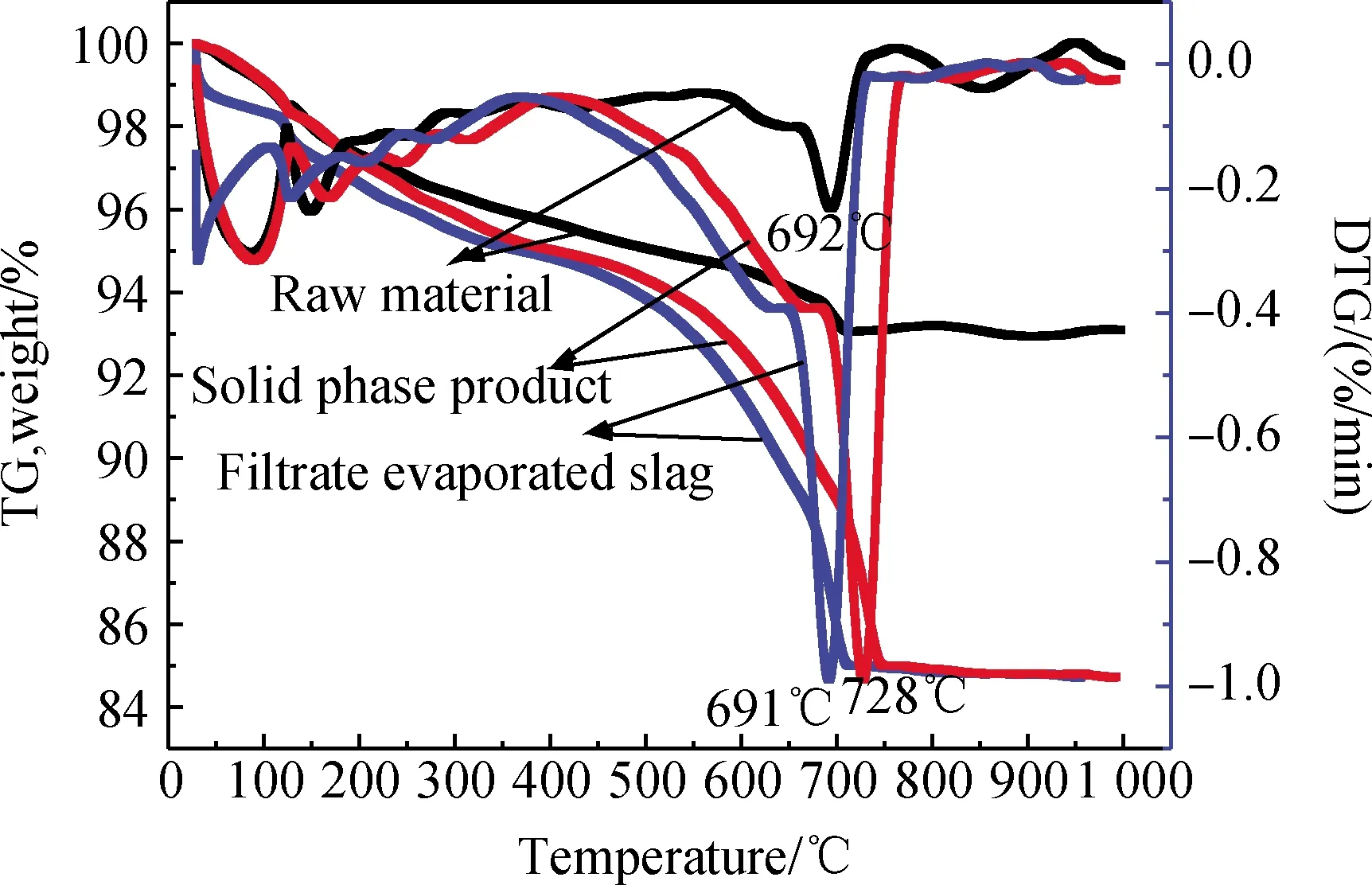
图5 硅钙渣原料及矿化产物TG-DTG曲线Fig.5 TG-DTG curves of raw material and mineralization products
2.5 TG-DTG分析
图5为原料及矿化产物的TG-DTG曲线。由图5分析可知,30~124 ℃、30~108 ℃、30~130 ℃分别是原料、矿化后固相产物、矿化后滤液蒸干渣失去结合水的温度范围。124~188 ℃、108~217 ℃、130~178 ℃分别是原料、矿化后固相产物、矿化后滤液蒸干渣中水化硅酸钙(C-S-H)分解的温度范围。胶体物质,其粒径小于100 nm,故可以穿过滤纸孔道到达滤液当中。硅钙渣原料在温度范围为563~762 ℃,矿化后固相产物在温度范围为402~771 ℃,矿化后滤液蒸干渣在温度范围为383~736 ℃有明显失重。这是由于在此温度范围内,CaCO3发生分解反应放出CO2所致。DTG图上对应三种物质的最大失重峰温分别为692 ℃、728 ℃、691 ℃。其中,矿化后固相产物的最大失重峰温最高,这是因为从SEM图片可以看出,矿化后所生成的CaCO3为方解石型,属于碳酸钙所有晶型中热力学最为稳定的一种,故其分解所需要的温度最高。
由TG图分析可知,硅钙渣原料、矿化后固相产物、矿化后滤液蒸干渣所对应的CO2失重率分别为1.48%、9.95%、9.75%。因在实验条件下矿化后滤液蒸干渣的质量仅为0.2 g左右,故其中所含有的CaCO3的质量可以忽略不计。硅钙渣的固碳率可以根据公式(11)进行计算。
(11)
式中,ζCO2为硅钙渣的矿化效率,%;mrm为原料的质量,g;mCO2为被矿化固定在硅钙渣中的CO2的质量,g;war,CO2为矿化反应后产物对应的CO2的失重率,%;wbr,CO2为硅钙渣原料对应的CO2的失重率,%。
根据公式(11)计算硅钙渣的矿化效率如下:
(12)
即:92.5 kg CO2/t硅钙渣。
3 结 论

(2)矿化反应后的固相产物主要为CaCO3,且晶型全部为方解石型。滤液蒸干渣的主要成分为CaCO3、Na2CO3及硅胶。
(3)在常压、温度为55 ℃的温和条件下,且没有其他化学试剂的加入,硅钙渣的固碳率可以达到9.25%,实现了低成本矿化固定CO2。从SEM照片可以看出,矿化反应所生成的CaCO3已经将硅钙渣表面完全覆盖,这可能是降低硅钙渣固碳率的主要原因之一。

