不同产地何首乌药材质量及差异研究△
李欣,孟磊,魏胜利,2*,祁晓娟,卓冰雨
1.北京中医药大学 中药学院,北京 102488;2.中药材规范化生产教育部工程研究中心,北京 100102
何首乌为蓼科何首乌PolygonummultiflorumThunb.的干燥块根,有解毒截疟、润肠通便、补益肝肾之功效[1]。现代药理研究证明,何首乌主要有补血、抗氧化、抗衰老、抗动脉粥样硬化及神经保护等作用[2-3],其药效成分主要包括二苯乙烯苷类、结合蒽醌类和游离蒽醌类[4-6],同时也是何首乌质量控制的关键指标。但近年来,随着何首乌种植区域的改变[7-8],其质量控制日益困难。已报道不同产地何首乌功效组分含量存在显著性差异[9],甚至基因序列都已发生改变[10]。如何从全国种植区域范围内甄选出特定功效组分的何首乌,是何首乌临床“精准用药”的首要难题。本研究通过典型相关分析方法,研究何首乌主产地的环境因子与品质的相关性,以期得到何首乌质量形成规律,为特种功效组分何首乌选择提供科学依据,其结果对何首乌产地质量评价与临床“精准用药”均有指导意义。
1 材料
1.1 试药
实验材料来源于何首乌传统的道地产区与现在的主要产区,包括广东、贵州、湖北、四川、云南、广西、湖南、山西、安徽、陕西、重庆、河南,共计12个省区,20批样品。具体采样信息见表1。所有样品经50 ℃烘干后作为分析样品,样品标本经北京中医药大学魏胜利教授鉴定为何首乌PolygonummultiflorumThunb.正品。
反式二苯乙烯苷(中国食品药品检定研究院,批号:110844-20512,纯度:99.0%),大黄素、大黄素甲醚、大黄素-8-O-β-D葡萄糖苷(中国食品药品检定研究院,纯度>98%,批号分别为:110750-200110、110758-201415、110758-21415),大黄素甲醚-8-O-β-D葡萄糖苷(上海源叶生物科技有限公司,纯度>98%,批号:Z25F8B30059),甲醇和乙腈(色谱纯,Fisher公司),水为屈臣氏蒸馏水,其余试剂均为分析纯。顺式-二苯乙烯苷参考文献方法[11],通过反式-二苯乙烯苷在紫外365 nm下转化而得。

表1 不同产地何首乌样品信息
1.2 仪器
Agilent 1260高效液相色谱仪,配备G1314F 1260 VWD 检测器、Agilent 色谱工作站;KQ5200D型超声清洗器(江苏省昆山市超声仪器有限公司);ME104型万分之一电子分析天平(美国METTLER TOLEDO公司);BT 25S型十万分之一电子分析天平(德国Sartorius公司);FW100型高速万能粉碎机(天津市泰斯特仪器有限公司)。
2 方法
采用文献报道的HPLC一测多评法通过何首乌中的反式二苯乙烯苷含量对顺式二苯乙烯苷、大黄素-8-O-β-D葡萄糖苷、大黄素甲醚-8-O-β-D葡萄糖苷、大黄素、大黄素甲醚6个单体成分定量(见图1)[12]。
2.1 供试品溶液制备
精密称取何首乌粉末(过四号筛)0.5 g,置于具塞三角瓶中,精密加入甲醇50 mL,称定质量,于室温下超声1 h(200 W,40 kHZ),放冷,称质量,用甲醇补足损失的质量,摇匀,过滤(0.22 μm微孔滤膜)。
2.2 对照品溶液制备
精密称取6种对照品适量,加甲醇配成含顺式二苯乙烯苷0.016 7 mg·mL-1、反式二苯乙烯苷0.167 mg·mL-1、大黄素-8-O-β-D葡萄糖苷0.042 1 mg·mL-1、大黄素甲醚-8-O-β-D葡萄糖苷0.020 3 mg·mL-1、大黄素0.010 3 mg·mL-1、大黄素甲醚0.007 4 mg·mL-1的混合对照品溶液。
2.3 色谱条件
色谱柱:Agilent ZORBAX Extend-C18(120 mm×4.6 mm,5 μm),柱温:30 ℃,样品温度:4 ℃,流速:1.0 mL·min-1,280 nm检测,进样量:10 μL。流动相A(甲醇),B(0.1%磷酸),梯度洗脱(0 min,95%B;10 min,75%B;20 min,55%B;30 min,30%B;35 min,20%B;40 min,10%B;45 min,10%B)。
2.4 方法学考察
2.4.1 线性关系考察 分别进样1、2、5、10、15、20 μL,以进样量为横坐标、峰面积为纵坐标进行线性回归,得回归方程为:Y=1638X+111.43(r=0.999 7),反式二苯乙烯苷在0.240 6~4.812 0 μg与峰面积间的线性关系良好。
2.4.2 相对校正因子 除反式二苯乙烯苷外其他浓度计算方法为:
Ci=fsi×Cs×Ai/As
(1)
式中,C为浓度,f为相对校正因子,A为峰面积,Cs是求出的样品反式二苯乙烯苷浓度,Ci是样品其他成分含量浓度。其中何首乌中顺式二苯乙烯苷、大黄素-8-O-β-D葡萄糖苷、大黄素甲醚-8-O-β-D葡萄糖苷、大黄素、大黄素甲醚5种成分与反式二苯乙烯苷的相对校正因子分别为1.054、2.160、2.072、2.451、2.184。
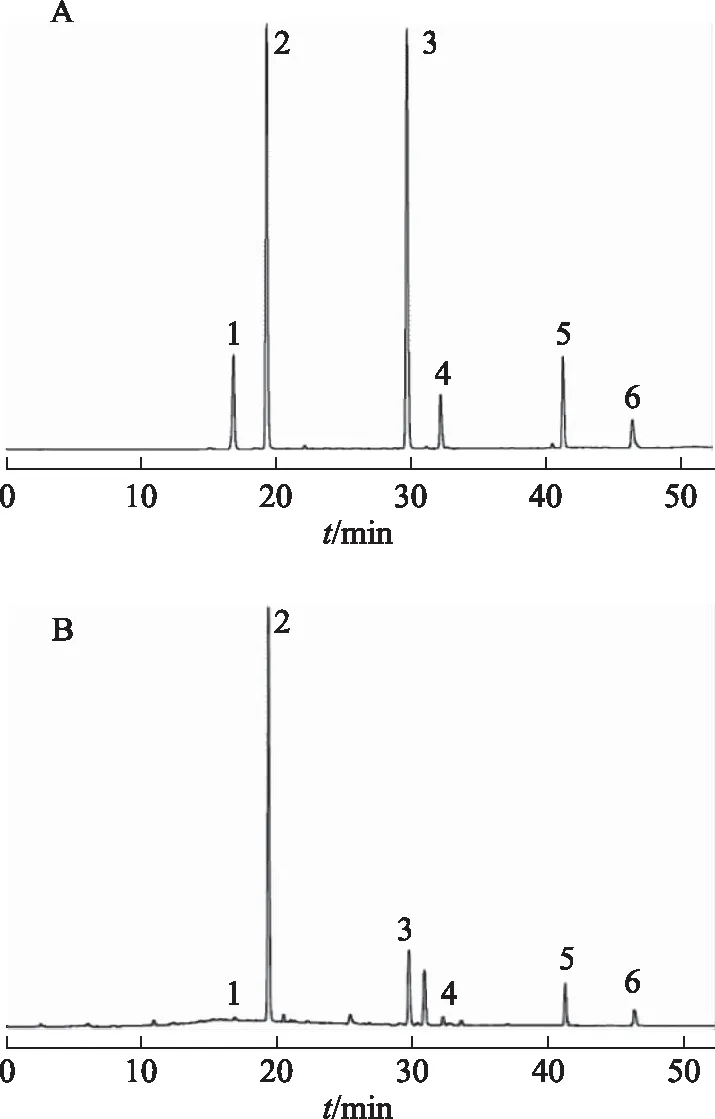
注:A.6种混合对照品;B.何首乌样品溶液;1.顺式二苯乙烯苷;2.反式二苯乙烯苷;3.大黄素-8-O-β-D葡萄糖苷;4.大黄素甲醚-8-O-β-D葡萄糖苷;5.大黄素;6.大黄素甲醚。图1 混合对照品和供试品溶液6种成分的HPLC图
2.4.3 重复性考察 取同一产地的何首乌粉末1.0 g(过四号筛),精密称定,平行6份,采用2.1项下供试品溶液的制备方法,2.3项下的色谱条件进样测定。
2.4.4 精密度考察 精密吸取混合对照品溶液10 μL,连续进样6次,记录峰面积,并计算RSD。
2.4.5 稳定性考察 精密吸取同一供试品溶液10 μL,分别在制备样品后的0、2、4、8、12、16、24 h进样,测定峰面积,计算顺式二苯乙烯苷、反式二苯乙烯苷、大黄素-8-O-β-D葡萄糖苷、大黄素甲醚-8-O-β-D葡萄糖苷、大黄素、大黄素甲醚的RSD。
2.4.6 加样回收率 取同一批己知含量的何首乌粉末(过四号筛)约0.2 g,平行6份,精密称定,分别按样品含量∶对照品量(1∶1)的比例大致加入一定量的顺式二苯乙烯苷、反式二苯乙烯苷、大黄素-8-O-β-D葡萄糖苷、大黄素甲醚-8-O-β-D葡萄糖苷、大黄素、大黄素甲醚的混合对照品溶液。按照2.1项下的方法制备供试品溶液。精密吸取上述供试品溶液10 μL,测定并计算各成分的加样回收率及RSD(见表2)。
2.5 数据来源及处理方法
3 结果与分析
3.1 不同产地何首乌活性成分含量差异分析
不同产地何首乌6种活性成分含量差异有统计学意义(P<0.01),二苯乙烯苷类总量、结合蒽醌类总量、游离蒽醌类总量的最高值和最低值分别相差4.8、30.0和21.7倍,差异有统计学意义(P<0.01)(见表3)。其中,大黄素、大黄素甲醚、大黄素葡萄糖苷最高均产自四川冕宁,分别为1.607 2%、0.499 7%、1.338 3%,顺式二苯乙烯苷含量最高产自重庆钱塘(0.147 5%),反式二苯乙烯苷最高均产自湖北武当山(7.607 4%),大黄素甲醚葡萄糖苷含量最高产自广东德庆(0.168 2%);大黄素含量以广西西林(0.085 6%)最低,其他5种成分:顺式二苯乙烯苷、反式二苯乙烯苷、大黄素甲醚、大黄素甲醚葡萄糖苷、大黄素葡萄糖苷含量最低均产自广东阳春,分别为0.014 2%、1.559 8%、0.065 3%、0.021 4%、0.027 8%。
另外,四川冕宁的何首乌游离蒽醌类总量与结合蒽醌类总量均最高,分别为2.106 9%、1.479 5%;湖北武当山的何首乌二苯乙烯苷类总量最高,为7.720 2%;广东阳春的何首乌二苯乙烯苷类总量、结合蒽醌类总量均最低,为1.574 1%和0.049 3%,而游离蒽醌类总量最低产自广西西林(0.083 7%)(见图2)。
此外,何首乌体内含量最高的成分为反式二苯乙烯苷,平均达到了3.704 2%,其次为大黄素、大黄素苷、大黄素甲醚,平均质量分数分别达到了0.456 4%、0.330 4%和0.169 9%。最低的是大黄素甲醚葡萄糖苷,平均只有0.039 7%,与文献[9]结果一致。
3.2 何首乌质量与气候因子相关分析
3.2.1 简单相关分析 对何首乌6种成分含量与7种环境因子做相关性分析,结果见表4。从表4中可以看出,“气候组”年均温与纬度、海拔呈极显著负相关,r分别为-0.631、-0.573,1月最低气温与年均温呈极显著正相关关系,r为0.649,与纬度的r为-0.846,相关性极显著。“质量组”反式二苯乙烯苷与纬度、海拔呈显著正相关,与1月最低气温显著负相关;结合蒽醌类与7月最高气温、年均气温均呈显著或极显著负相关关系,r达-0.855;游离蒽醌与经度、7月最高气温呈极显著或显著负相关。
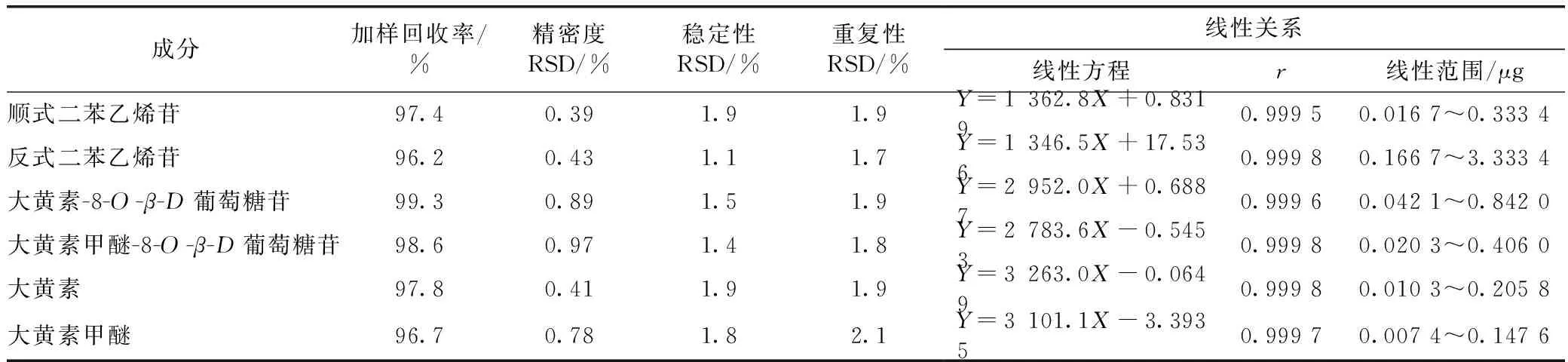
表2 含量测定方法学考察
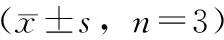
表3 不同产地何首乌6种活性成分含量测定结果 mg·g-1
注:*P<0.05;**P<0.01;—表示未检出。

表4 生态环境因子与药材质量的简单相关分析
注:*P<0.05;**P<0.01。
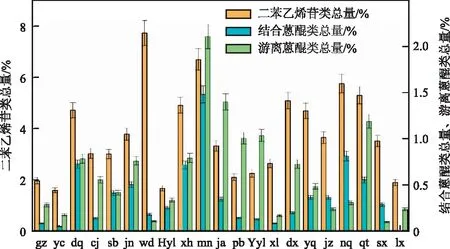
图2 何首乌功效组分比较图
3.2.2 典型相关分析 根据20个产地收集的数据和含量测定的结果,得到X1~6和Y1~6的典型相关系数分别是0.969 0、0.925 2、0.846 1、0.700 7、0.529 3、0.308 5,表明第1、第2对典型变量解释能力较强,显著性检验后发现相关关系显著,故可以用“气候组”来解释药材“质量组”。
本实验采用标准化的典型相关系数建立典型相关模型。由表5可见,何首乌药材质量受气候因素影响可用2对典型相关变量描述。

表5 何首乌气候组与质量组典型相关分析
第1对典型变量模型为 V1=-0.339 6X1-0.083 7X2+0.391 7X3-0.439 0X4+0.974 6X5+0.876 9X6+0.011 3X7,7月最高气温和年均温典型载荷最高,表明气候组变化主要受7月最高气温和年均温控制;W1=0.571 1Y1+0.057 5Y2-0.593 3Y3-0.429 8Y4+0.169 4Y5-0.103 1Y6,大黄素葡萄糖苷和顺式二苯乙烯苷典型载荷最高,表明质量组主要由大黄素葡萄糖苷和顺式二苯乙烯苷控制。因此,第1对典型变量模型显示气候与质量的相关性主要由7月最高气温、年均温与大黄素葡萄糖苷、顺式二苯乙烯苷含量之间的相关关系主导。同样,第2对典型变量模型V2=-1.036 5X1-0.224 7X2-0.185 2X3-0.508 2X4-0.124 2X5+0.745 1X6+0.089 3X7,W2=0.881 4Y1-0.590 4Y2-0.747 0Y3+0.789 9Y4+0.169 6Y5+0.567 0Y6,第2对典型变量模型显示气候与质量的相关性主要受经度与顺式二苯乙烯苷、大黄素葡萄糖苷、大黄素甲醚葡萄糖苷相关关系主导。
由典型相关分析可知,何首乌药材质量主要由大黄素葡萄糖苷、顺式二苯乙烯苷、大黄素甲醚葡萄糖苷含量主导,此3类成分主要受7月最高气温、年均温、经度气候因子控制,与简单相关分析结果基本一致。
4 结论与讨论
现代研究中,何首乌主要的药效成分有2大类:二苯乙烯苷与蒽醌类,其中,蒽醌又可分为游离蒽醌与结合蒽醌,此3类成分也是何首乌及其相关中药制品质量检测的重要指标。
二苯乙烯苷属于多羟基酚类化合物,具有抗衰老[14]、抗肿瘤[15]、防治血栓[16-17]、提高记忆力[18-19]、保肝[20]等药理活性,与何首乌补益肝肾的功效密切相关。《中华人民共和国药典》[1]规定何首乌中二苯乙烯苷含量不得少于1%,本实验中20批不同产地的何首乌二苯乙烯苷含量均达到要求,且四川冕宁含量最高,达6.690 4%。相关性分析结果反映,顺式二苯乙烯苷与经度正相关,反式二苯乙烯苷与纬度、海拔正相关,与1月最低气温负相关,此结果与光照和温度对二苯乙烯苷合成途径中的苯丙氨酸解氨酶基因的表达、调控影响效果一致[21-22]。结合二苯乙烯苷类的药理活性,高海拔、温差大的湖北武当山及其相似环境有利于二苯乙烯苷的积累,所产的何首乌具有补益肝肾的潜在优势。
蒽醌类成分在蓼科广泛分布[23],有较强的药理活性。游离蒽醌类成分可抗菌、抗炎、抗病毒,在解毒截疟等功效上有潜在优势;结合蒽醌类成分有致泻活性,是何首乌润肠通便作用的物质基础。本研究中,各产地何首乌蒽醌类成分含量相差20~30倍,表明产地对何首乌质量蒽醌类成分形成有重要影响。相关性分析结果显示,结合蒽醌类与7月最高气温、年均气温均呈显著或极显著负相关,游离蒽醌与经度、7月最高气温呈极显著或显著负相关。结合蒽醌类成分的药理活性,低温、低湿的四川冕宁及其相似环境有利于蒽醌类成分的积累,所产的何首乌具有截疟解毒、润肠通便的潜在优势。何首乌的肝毒性也是近年来研究的热点之一,而关于何首乌肝毒性物质基础的报道,二苯乙烯苷类和蒽醌类成分均有所提及,但至今无统一的说法,可能与两者在机体内会相互影响有关,推测两类成分可能存在双向调节作用[24]。且有报道何首乌蒽醌类成分达到肝毒性的服用剂量远远超出何首乌的临床使用剂量[25],除此之外,何首乌在高浓度、长时间作用下有细胞毒性,会引发肝毒性等不良反应[26]。因此,何首乌的使用需遵从医嘱。
综上所述,产地是何首乌药材质量形成的主要因素,根据特定功效选择适宜产区的何首乌,是目前临床用药的需求,也是中药质量控制的目标。本研究确定了不同功效型何首乌的主要产地环境影响因子,为何首乌用药选择和质量评价提供一定的参考价值。但阐明何首乌质量形成机制,并将其应用于何首乌生产调控,实现何首乌精准化质量控制,还有很长的路要走。

