非解剖性肝切除与经皮射频消融治疗单发小肝癌的疗效分析
普成华,胡明道,陈鹏
(昆明医科大学第二附属医院肝胆胰外科,云南 昆明 650101)
原发性肝癌是一种在临床上十分常见的严重疾病,在我国发病率很高,是排在我国第4位的常见恶性肿瘤,对人民生命健康构成一种威胁[1]。近年来,随着医疗技术水平的提高,小肝癌可以被早期发现,而小肝癌因其数目多少可分为单发和多发,其数目的多少及大小会影响治疗方式的选择及预后。早发现、早诊断、早治疗,对小肝癌来说可以达到临床治愈的要求。传统的手术切除是治疗小肝癌的主要治疗方式。非解剖性肝切除(non-anatomical hepatectomy,NAP)作为一种传统的手术方式沿用至今,具有其优势。但随着医疗技术的发展,经皮射频消融(radiofrequency ablation,RFA)也成为治疗小肝癌的另一种优选治疗方式。对于单发小肝癌的治疗,国内外对非解剖性肝切除及经皮射频消融一直存在争议,本文将展开非解剖性肝切除及经皮射频消融对治疗单发小肝癌的疗效进行探讨。
资料与方法
一、一般资料
选取我院2014年1月至2016年8月收治的单发小肝癌病人51例,对照组23例行非解剖性肝切除术,研究组28例行经皮射频消融术。对照组男性 13 例,女性 10 例;年龄 (55.18±6.95) 岁(40~ 70岁)。研究组男性 15 例,女性 13 例;年龄( 56.5±5.70)岁(45~67岁)。两组病人术前肝功能主要指标、一般资料比较,差异均无统计学意义(P>0.05),具有可比性。纳入标准:一般情况良好,无明显心、肺、肾等重要脏器器质性病变,肝功能A级,肿瘤分期为Ⅰa期,无肝外转移和门静脉侵犯的直径≤5 cm的单发肿瘤,对照组选择的病例肝癌位置较表浅或位于肝脏边缘,研究组选择的病例肝癌位于肝脏深部或中央。
二、方法
1.对照组非解剖性肝切除术 在全麻状态下开展开腹切除术,选择平卧位体位,常规消毒铺巾之后切口一般采取右肋缘下斜切口或反“L”形切口。逐层进入腹部,入腹后对肿瘤附近脏器情况、肿瘤位置、肿瘤大小等进行观察,探查有无腹水,大网膜周围有无转移性结节,肝脏病变范围、肝硬化程度及其他脏器情况,根据术前CT或MRI影像学精确定位肿瘤位置。 如需肝门阻断, 严格控制肝蒂阻断时间15 min/次,如需多次肝蒂阻断,中间需开放肝蒂血流,约5 min后再次肝蒂阻断,根据肿瘤大小及位置行局部或部分切除,肝断面仔细止血、结扎小胆管,温盐水对腹腔进行全面清洗,放置腹腔引流管,逐层关腹,手术完成,标本送病理科行病理检查。术后给予对症支持治疗。
2.研究组经皮射频消融术 采用超声设备:飞利浦IU22彩色多普勒超声仪,射频设备:北京博莱德光电技术开发有限公司肿瘤射频仪。具体过程:病人仰卧位,开放静脉,持续心电监护,由麻醉医师给予静脉麻醉并监护手术全程。对肝脏进行全面扫查,确定目标病灶。定位后对穿刺点及周围进行常规消毒、铺巾,用2%利多卡因对穿刺点局部麻醉、小尖刀开皮后,在实时超声引导下取多级射频肿瘤消融电极针沿引导线逐层刺入深部病灶内,主针进入目标病灶后通电开始消融,局部温度升高至90 ℃后保持10 min,消融后病灶整体呈高回声。降温至42 ℃以下后收回内套针,退针。消融治疗结束后再次扫查,肝周及腹腔其他间隙未见明显无回声区。结束手术。术毕,局部伤口消毒纱布覆盖,盐袋加压包扎。术中及术后病人无特殊不适。
3.观察指标 记录两组病人的术后住院时间、术后3 d肝功能主要指标,主要包括丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、凝血酶原时间(PT)和活化部分凝血酶原时间(APTT);术后并发症情况(主要有发热、腹腔感染、肺部感染、恶心呕吐、出血、疼痛等);术后1、2、3年的无瘤生存率及总体生存率。
三、统计学方法

结 果
一、两组病人术后3 d血清ALT与AST、凝血功能PT与APTT水平及术后住院时间对比 研究组病人术后3 d的血清ALT与AST、PT和APTT水平及术后住院时间均低于对照组,差异有统计学意义(P<0.05),见表1。
二、两组病人术后并发症发生率对比 研究组病人术后并发症发生率(7.1%)明显低于对照组(34.8%),差异有统计学意义(χ2=4.492,P<0.05),见表2。
三、两组病人术后无瘤生存率及总体生存率对比 两组病人1、2、3年无瘤生存率分别为:对照组为86.96%、69.57%、56.52%;研究组为85.71%、71.43%、60.71%。1、2、3年总体生存率分别为:对照组为100%、91.30%、78.26%;研究组为100%、85.71%、75.00%,两组对比差异无统计学意义 (P>0.05),见表3。
讨 论
肝细胞癌(hepatocellular carcinoma,HCC)通常来自具有背景性肝硬化或慢性肝炎(乙型或丙型肝炎)的肝脏,在所有原发性肝癌中大约有一半发生在中国(每年395 000人)[2]。小肝癌属于早期肝癌,随着医疗水平的提高,其诊断和治疗得到很大的改善。本次研究纳入的病例符合米兰标准,即单发的直径≤ 5 cm 的病灶,并且不伴有血管及远处器官浸润。
手术切除和经皮射频消融一直是小肝癌治疗的争议点,对于单发小肝癌,国内外许多专家也在不断论证哪种方式能使病人获益最大。从本研究的结果来看,与NAP相比,RFA对病人肝功能损伤更小、凝血功能影响更小、术后住院时间更短、术后并发症更少,这一结果与许多专家的研究相符[2-6]。本研究发现1、2、3年的无瘤生存率及总体生存率并无明显差异,这与Chen等[7]的一项随机对照研究相符, 而且,他们通过分析小于3 cm的肿瘤以及3.1~5 cm的肿瘤,两组之间的1至4年总体生存率和无瘤生存率也没有显著差异。 Ruzzenente等[8]的生存分析也证实了对于单个HCC小于5 cm的HCC病人,手术切除和RFA的效果相当,总体生存率和无病生存率差异不明显。马智等[9]认为,肝切除术仍是目前根治小肝癌最有效的方法,可完整切除肿瘤,有较好的远期存活率。且有专家指出,保留肝组织的NAP可减少围手术期并发症和术后肝衰竭的发生,能够较好地保留无瘤的肝脏组织[10-11]。对于单个肿瘤没有破裂、无可视癌栓,如果切缘达到1 cm,NAP是安全有效的,其手术应激的风险也比较低,能更好的维持肝脏储备功能,可有效预防肿瘤的复发[11-14]。但NAP也有其自身的局限。白满灵等[15]专家指出,原发性小肝癌病人癌细胞不断肿大,肝组织坏死会严重影响机体肝功能,且大量研究表明,NAP会导致肝功能不全等并发症的产生。ALT、AST 的水平可以反映肝细胞损伤程度。由于NAP术中对肝门阻断,肝细胞组织缺血缺氧坏死,导致转氨酶释放增多进入血液,从而使ALT、AST 水平在术后升高。而RFA 在这些问题上就与手术切除不同,它对机体创伤小,易于反复多次操作,可以有效避免切除过程中挤压和触摸造成的医源性转移,对单发直径很小的肝癌,可以达到局部根治的标准[16]。肝脏还是凝血因子与抗凝物质合成的重要场所,对机体凝血功能十分重要,HCC等肝脏疾病可对机体的凝血功能产生破坏性作用,诱发凝血功能障碍,导致异常出血或血栓。此外,还有观点认为APTT、PT等凝血相关指标与HCC病人术后肝功能异常关系密切,其可作为评价肝功能恢复的重要指标[17]。Cucchetti等[18]认为对于非常早期的HCC的小结节,RFA比切除术更具成本效益; 对于单个较大的早期肝癌,手术切除仍是最好的策略。而大多数研究发现对于相对较小的单个HCC,选择RFA代替肝切除作为初始治疗时,具有安全性,治疗后有更好的健康相关生活质量[3, 19-20]。

表1 两组病人术后3 d血清ALT与AST、PT与APTT水平及术后住院时间对比

表2 两组病人术后并发症发生情况对比(例)
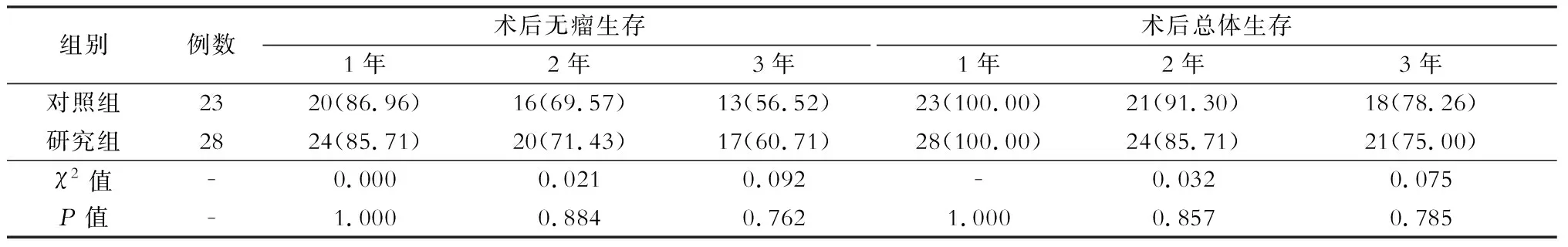
表3 两组病人术后无瘤生存及术后总体生存情况对比[例(%)]
由于本研究样本量太少,结论存在一定的局限性,还需要多中心大样本数据的研究来论证。从本研究结果来说,对于单发小肝癌,RFA可以达到NAP一样的治疗效果,比起NAP,RFA具有更小的创伤性,对病人肝功能损伤及凝血功能影响更小,能有效降低术后并发症的发生,减少病人的住院时间,远期的无瘤生存率及总体生存率无明显差异,为病人提供了一种理想的治疗方式,值得临床推广。

