肝硬化伴食管静脉曲张破裂出血行脾切除加断流治疗与内镜治疗的疗效对比分析
张仕然,陈俊英,胡晓月,陈平
(陆军军医大学大坪医院肝胆外科,重庆 400042)
食管静脉曲张破裂出血(esophageal variceal bleeding,EVB)是肝硬化后期的常见并发症之一。有80%~90%的肝硬化病人有食管静脉曲张的伴随发生,EVB的发生风险为30%~40%[1],还有文献报道高达55.6%[2],而在首次出血的病人中6周致死率高达20%[3]。如何预防及治疗EVB是临床工作关注的焦点问题。目前EVB的主要治疗方式包括内镜下治疗、介入治疗、外科手术[4]。国外的各大指南(欧洲的BavenoⅥ共识、美国肝病研究协会指导、英国指南)均建议采取非选择性β受体阻滞剂(nonselective beta blocker,NSBB)、内镜下套扎(endoscopic variceal ligation,EVL)、经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shut,TIPS)等方案进行治疗。其中最新的BavenoⅥ共识已不再推荐外科手术治疗,而国内指南也仅把外科手术作为病人药物或内镜治疗失败的挽救治疗[3,5-8]。为进一步探讨外科手术在EVB治疗中的价值和意义,我们回顾性地分析了我中心近年来的相关病例,以期为病人在多元化的选择面前提供一定的参考意见,并且希望通过对比分析,找到影响病人再次出血的危险因素。
资料与方法
一、 病例资料
收集2012年1月至2017年11月,因肝硬化后食管静脉曲破裂出血,在我中心肝胆外科行脾切除+门奇静脉断流术者54例,纳入外科手术治疗组;在消化内科行内镜下套扎术和(或)内镜下硬化剂注射术者63例,纳入内镜治疗组。
纳入标准:①因肝硬化而出现食管静脉曲破裂急性出血者;②年龄<65岁;③白细胞计数(1~10)×109/L。
排除标准:①患有恶性肿瘤或其他可能影响病人生存期的疾病者;②急性大出血致死者;③单纯脾切除、单纯门奇静脉断流或其他分流、断流术者;④断流后再行内镜下治疗者;⑤失访者。
二、 治疗方式
手术方式为标准的脾脏切除联合门奇静脉断流术:结扎脾动脉,完成脾切除,离断胃底贲门周围所有曲张静脉,确切离断食管支及高位食管支甚至异位食管支,确保将曲张的交通静脉断流至贲门5 cm以上。
EVL:常用方法为将胃镜镜头调整至与曲张静脉成直角,再行负压吸引,至显示屏上呈完全红色时,注入气体使橡皮圈脱落于曲张静脉的基底,完成套扎。
内镜下硬化剂治疗(endoscopic variseal sclerosisis,EVS):在内镜引导下向破裂及有破裂倾向的曲张静脉注射硬化剂,在透明帽辅助下对各靶点位曲张静脉注射1%聚桂醇注射液10 ml,其后用镜身压迫止血。可根据病情多次反复治疗。套扎后多有再次套扎或硬化注射的序贯治疗方案。
三、 采集指标及统计学方法
采集病人性别、年龄、住院时间、住院费用、肝功、凝血、血常规、脾脏大小(通过CT分别测量脾脏长宽厚)、胃镜检查曲张静脉距门齿距离等资料。采用SPSS(23.0版)软件进行数据处理分析。对满足正态分布且具有方差齐性的计量资料的组间比较采取t检验。对计数资料、百分比、频率行χ2检验。采用Kaplan-Meier法作生存曲线,使用对数秩检验比较组间的再出血率差异。使用COX比例风险模型进行多因素分析。按α=0.05的水准确定P值,P<0.05为差异有统计学意义。
结 果
一、 基线资料
外科手术治疗组共纳入54例,男女比为1.84(35/19),年龄(48.81±10.02) 岁;内镜治疗组共纳入63例,男女比为1.17(34/29),年龄(49.76±9.25)岁。两组病人的肝功能按改良的Child-Pugh评分标准进行分级评估。对计量资料行χ2检验提示:两组间性别构成(χ2=1.414,P=0.234)和和肝脏功能(χ2=2.293,P=0.318)差异无统计学意义。对其他计数资料行t检验,两组间各指标差异均无统计学意义(均P>0.05)。详见表1。
对病因的统计,发现乙型病毒性肝炎后肝硬化为主要病因,占总数的61.5%,酒精性肝硬化、原发性胆汁性肝硬化、丙型病毒性肝炎后肝硬化也是常见病因,同时也有少数为自身免疫性肝病后肝硬化、药物性肝硬化、非酒精性脂肪性肝病引起的肝硬化所致。还有相当一部分病人因检查结果不完善,或者未检查出阳性结果,导致未能明确病因,列入“其他”项,两组病因构成差异无统计学意义(χ2=2.845,P=0.724),详见表2。

表1 病人基线特征

表2 两组病因比较
二、 随访结果
54例外科手术治疗组随访(1 644.35±573.32) d(751~2 764 d),中位随访时间为1 623.50 d;63例内镜治疗组随访(1 934.08±648.40) d(742~3 303 d),中位随访时间为2 033.00 d。
1.再出血率 通过Kaplan-Meier生存分析法,作累积再出血率分析图,见图1。手术治疗组术后总体再出血率为24.1%(13/54),其1、3、5年再出血率分别为9.3%、20.5%、23.1%;内镜治疗组术后总体再出血率为77.8%(49/63),其1、3、5年再出血率分别为39.7%、73.0%、74.8%。手术治疗组的再出血率明显低于内镜治疗组(P<0.001),见表3。

表3 两组病人再出血情况
2.再次出血间隔时间 对于术后再次出血的病人,统计从术后到再次出现出血的间隔时间。手术治疗组为(511.57±491.28) d;内镜治疗组为(483.15±436.18) d。两组再出血间隔时间差异无统计学意义(P=0.835)。
3.多因素分析 将两组再次出血这一事件进行多因素分析,发现治疗方式为影响病人术后再次出血的独立危险因素。接受内镜治疗病人的术后再出血风险是接受外科手术病人的7.2倍(P<0.001)。而病人的性别、年龄、血清白蛋白、总胆红素、凝血酶原时间、白细胞计数、血红蛋白、血小板计数、脾脏大小、既往的呕血史长短、曲张静脉距门齿的距离、肝硬化的病因、腹水的程度等在引起两组再出血这一事件上差异均无统计学意义。见表4。
讨 论
基于统计分析,我们发现手术治疗组的男性比例略高于内镜治疗组。我国乙型肝炎发病率男女比例约为1.90∶1[9],导致EVB男性病人更多。同时以原发性胆汁性肝硬化为主的难以明确诊断的慢性肝炎,病人常就诊于消化内科,这部分与免疫相关的病人中女性较男性发病率更高[10]。基于此造成两组男女比例轻微的差异出现。在术前肝脏功能的统计中,外科手术治疗组有4例为C级,而C级肝功能病人为手术的禁忌。出现这种情况是因为本研究统计的是病人入院后第一次检查、检验的资料,这些可以将肝功能调整好转后再行手术治疗,并且有报道显示脾脏切除有利于改善肝脏的纤维化[11],这也是我们对这部分病人行手术治疗的原因;同时我们发现外科手术治疗组的治疗费用为内镜治疗组的3倍,但由于部分内镜治疗组病人常需分次住院行序贯治疗,或者根据病人随访情况行多次预防性治疗,本研究63例内镜治疗组病人中,仅有43例行单次内镜下治疗,13例接受过2次内镜治疗,7例接受过3次内镜治疗。这导致二者实际费用差距有所缩小。
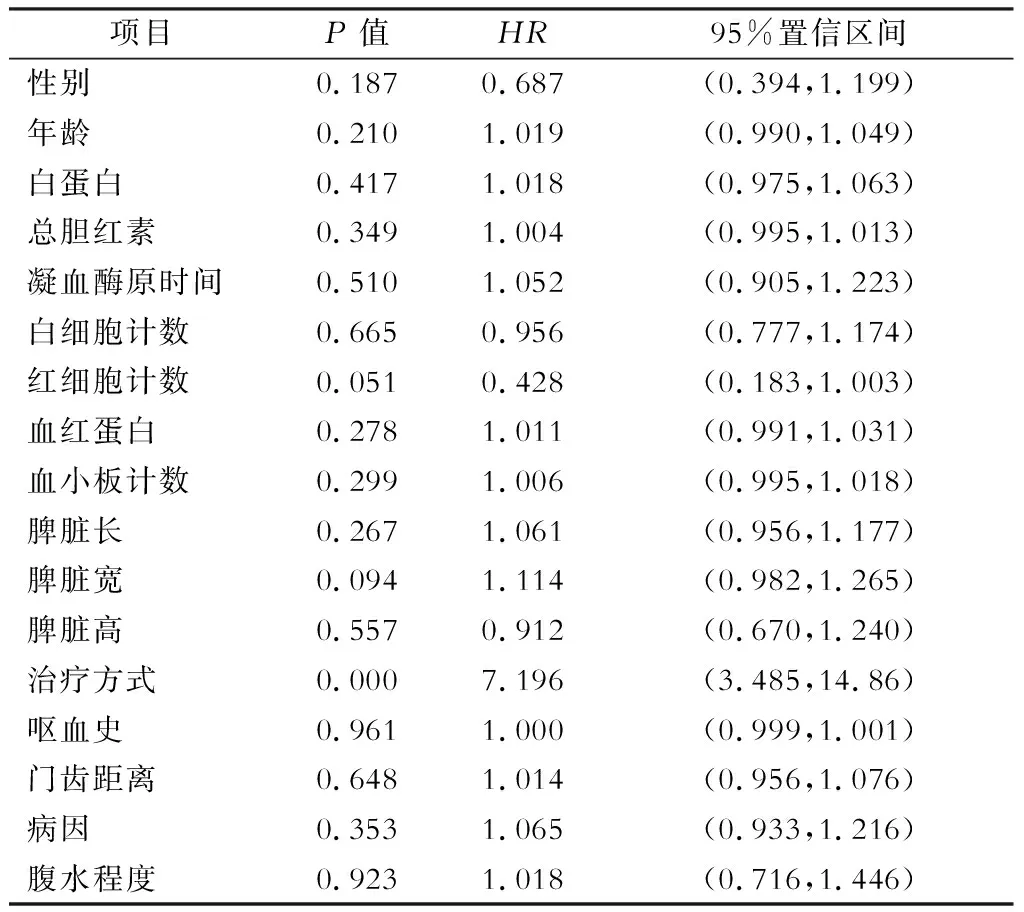
表4 多因素的COX回归分析结果
肝硬化食管静脉曲张破裂出血的病人在首次出血后,若不采取干预措施,1~2年内有60%的再出血率并伴随30%的致死率[12]。而国外报道行内镜联合药物治疗的病人1年再出血率为23%~31.7%[13]。本研究中内镜治疗1年再出血率为39.7%,低于未经干预的再出血率,高于国外内镜治疗后的再出血率。这应该与国外前瞻性随机对照研究纳入病人的一般情况更好有关,但内镜治疗后仍然能明显降低再出血率。本研究中接受手术治疗病人的1年再出血率为9.3%,远低于未经干预的自然再出血率。国内其他研究也显示断流术后随访3~36个月再出血率为11.1%[14]~24%[15],这与我们中心的结论一致。说明行脾切除+门奇静脉断流的确能显著降低病人再出血率。两组间疗效出现明显差异的原因,我们认为主要是脾切断流手术明显改善了病人的血流动力学。肝硬化后门静脉高压的病人,来自脾静脉的血流可占整个门脉血流的60%~80%,而正常人只占20%。有研究显示脾切断流术能够将术前平均约34.33 cmH2O(25.81 mmHg)的自由门静脉压(free portal pressure,FPP)降低到24.52 cmH2O(18.44 mmHg),FPP下降了28.58%[15]。同时国外有队列研究显示在服用NSBB后,肝静脉压力梯度(hepatic venous pressure gradient,HVPG)下降到12 mmHg以下或者较基础水平下降20%以上的病人再出血率仅为10%,而没有血流动力学改变的病人再出血率为64%[12]。鉴于HVPG是FPP的近似值,这说明门静脉压力的降低与否是病人是否再次出血的关键。而EVL、EVS没有从根本上改善门静脉高压,食管内的曲张静脉反复出现。这应该是二者再出血率有明显差异的主要原因。
针对病人再出血的危险因素,有其他研究指出还包括病人血钠、胆碱酯酶、门静脉内径等[16]。由于纳入统计量的差异,本研究没有完全统计上述指标也是本文的不足所在。本研究发现值得注意的是:病人入院时红细胞计数越高,其再出血风险有可能会降低(P=0.051)。原因应该是入院时红细胞计数较高的病人本身门静脉压力相对较低,导致曲张静脉破裂时出血较少,故术后再次出血的风险也降低。但是血红蛋白却未被提示为危险因素(P=0.278),这究竟是模型混杂因素导致了误判,还是因为部分病人长期失血造成的单位红细胞的血红蛋白量降低所致,还需要进一步的研究证实。
在如何处理急性活动性出血病人及预防再次出血上,国内外指南有较大差异。以BavenoⅥ共识为主的欧美标准不再推荐外科手术治疗,而是根据病人具体情况行内镜下止血或TIPS治疗术后再联合药物治疗,而我国肝病指南及外科指南则仍然推荐部分病人可采用外科手术治疗,但也是作为药物或内镜治疗失败的挽救治疗。外科手术治疗是否真的如其在各大指南中的地位一样日渐式微?部分国内外科专家表达了不同的意见,他们仍然认为外科手术在门静脉高压症的治疗中有重要的地位[17]。有文章分析了各大门静脉高压症的指南后发现,BavenoⅥ、美国肝病研究协会指导、我国肝病指南及我国外科指南外科文献占比分别为0、1.4%、6.7%、25%,参与的外科专家占比分别为7.8%、6.3%、1.2%、100%[18]。近年来相关药物、内镜、介入治疗的飞速进步及高质量等级临床证据的发表,为各大指南提供了修订既往治疗方式的依据。由于权威指南均由内科医师主导,同时外科缺乏大样本随机对照研究的证据,外科手术逐渐被各大指南边缘化甚至抛弃,但是指南只是综合了最新的可信知识来为临床实践提供规范的,并不是最终的解决方案。我们的研究结果提示外科手术仍然可以给病人带来明显的治疗获益。
综上所述,在肝硬化伴食管静脉曲张破裂出血的病人中,脾切除联合门奇静脉断流术较内镜下治疗虽然住院费用更高,但在预防病人再次出血上有明显的优势,而曲张的食管静脉距门齿的距离、脾脏的大小、脾功能亢进的程度等与术后再出血与否无统计学相关性。

