基于响应面法的华金6号金银花叶总黄酮有效部位的制备及其体外抗氧化活性研究
姜 珊,张康华,孙 平,代 龙,张 芳,高 鹏
(山东中医药大学 药学院,山东济南 250300)
金银花为忍冬 (Lonicera japonica Thunb.)的干燥花蕾或带初开的花,主要含有木犀草苷等黄酮类成分、绿原酸等酚酸类成分和以马钱苷为代表的环烯醚萜苷类成分(刘婵娟等,2010)。研究表明金银花具有抗病原微生物、抗氧化、抗病毒等药理作用(刘敬盛,2016;潘秋文,2004),尤其是在抑菌、抗氧化领域,其活性甚至比花高(杨海霞等,2013)。因此,金银花叶可应用于饲料抑菌添加剂和食品抗氧化剂等方面。华金6号金银花是山东中医药大学经过10余年培育出的金银花新品种(王玲娜等,2017、2016)。该品种金银花叶资源丰富,成本较低,可作为饲料添加剂,具有很高的开发价值。
近年来,从天然植物中寻找自由基消除剂是现代食品和药品行业的发展趋势。通过化学方法合成的抗氧化剂毒性较大,风险较高,常会引起严重的不良反应。以中草药及其有效成分进行抗氧化研究,已成为近年研究的热点,其中黄酮类成分被认为抗氧化效果较理想。研究表明,金银花叶总黄酮粗提物具有良好的抗氧化活性 (郑必胜等,2013;武雪芬等,1999),但是对于金银花叶总黄酮纯化物的抗氧化活性研究较少。为了得到纯度较高的金银花叶总黄酮有效部位,本试验采用D101型大孔吸附树脂对金银花叶总黄酮进行纯化工艺优选,为今后金银花叶总黄酮类成分抗氧化活性研究奠定基础。
1 试验材料
1.1 金银花叶 金银花叶(2018年6月采集于山东中医药大学药用植物园,样品经鉴定为华金六号金银花)置于室内通风干燥处,自然阴干后粉碎,备用。
1.2 药品与试剂 D101、HPD-100、S-8、NKA-9型大孔吸附树脂 (沧州宝恩吸附材料科技有限公司);芦丁对照品(纯度≥98%,上海源叶生物);DPPH、ABTS(上海麦克林公司);乙醇(天津市四通化工厂);维生素 C(Vc)(购自国药集团);其他试剂均为国产分析纯。
1.3 仪器 高速粉碎机 (上海兆申科技有限公司,XS-02);电子天平(梅特勒-托利多仪器有限公司,AL-204);移液枪(Dragon-Lab);紫外-可见光光度仪(上海仪电分析仪器厂,L3S);超声波清洗器(昆山市超声仪器有限公司,KQ-250);旋转蒸发器(上海申顺生物科技有限公司);恒温振荡仪(金坛市宏华仪器厂,SHA-CA型);电热鼓风干燥箱(林茂科技,101型)。
2 试验方法
2.1 金银花叶总黄酮的提取及含量测定
2.1.1 金银花叶总黄酮的含量测定 根据崔鹏等(2018)方法,采用紫外分光光度法,绘制芦丁对照品(0.1995 mg/mL)标准曲线,以吸光度为纵坐标,芦丁标准品浓度为横坐标得回归方程A=11.95C+0.0059,r=0.9994,线性范围 0~0.2 mg/mL。
供试品含量测定:取供试品溶液1 mL于25 mL容量瓶中加 5%的 NaNO2溶液 1 mL,10%的 Al(NO3)3溶液1 mL,摇匀,静置5 min后加4%的NaOH溶液10 mL,蒸馏水定容至刻度,摇匀后静置15 min,于510 nm处测吸光度,从回归方程中计算总黄酮的浓度。
2.1.2 金银花叶总黄酮的提取 根据李志明(2006)方法,设计 L9(34)正交试验,料液比 1:25、超声时间50 min、乙醇体积分数60%、超声温度30℃时黄酮提取率最高。即金银花叶经干燥粉碎后,精密称取约1 g粉末(过三号筛),于索氏提取器中回流至石油醚无色,将处理后的金银花粉末置于具塞锥形瓶中精密加入25倍量60%乙醇,超声处理 (功率500 W,频率40 kHz)50 min,用60%的乙醇补足减失的重量,放冷至室温,抽滤,抽滤液减压浓缩回收乙醇,浓缩液置100 mL容量瓶中,用蒸馏水定容至刻度,测定含量。
2.2 金银花叶总黄酮的分离纯化
2.2.1 大孔树脂预处理 将 D101、HPD-100、HPD-300、NKA-9型大孔吸附树脂95%醇洗、3%酸洗、3%碱洗后用去离子水洗至中性后,70℃烘干备用。
2.2.2 树脂筛选 根据姚佳等(2018)的方法,分别称取上述预处理好的四种大孔吸附树脂各1 g于100 mL锥形瓶中,分别加入金银花叶总黄酮提取液25 mL(1.53 mg/mL),置于振荡仪中吸附12 h后测定上层液中总黄酮浓度。将上述吸附饱和的树脂加入25 mL 60%乙醇振荡解吸12 h,过滤并检测滤液中黄酮浓度。相关参数计算公式如下:
静态吸附量/(mg/g)=V药液×(C0-C1)/m;
静态解吸量/(mg/g)=V洗脱液×C2/m;
静态解吸率/%=静态解析量/静态吸附量×100;
式中:C0为黄酮初始浓度,mg/mL;C1为黄酮剩余浓度,mg/mL;C2为洗脱液中黄酮浓度,mg/mL;m 为树脂质量,g。
2.2.3 树脂纯化工艺 D101型大孔吸附树脂纯化工艺的优选参考马翠霞等(2018)方法。
2.2.3.1 泄露曲线测定 取30 mL D101型大孔吸附树脂,装柱,取“2.1.2”提取液 (1.53 mg/mL)15 mL上样,上样流速为1 mL/min,收集流出液,每15 mL收集1份,共上样90 mL。按“2.1.1”方法测定总黄酮含量,并以上样液体积为横坐标,吸光度为纵坐标绘制泄露曲线。
2.2.3.2 上样流速的选择 称取4份预处理好的等体积D101大孔吸附树脂,湿法装柱,去离子水平衡后加入“2.1.2”粗提液(1.53 mg/mL),上样液流量分别为 1、2、3、4 mL/min 进行动态吸附,收集并测定流出液中金银花叶总黄酮的浓度,计算吸附率。
2.2.3.3 洗脱溶剂体积的选择 按照 “2.2.3.2”方法装柱5个,上样流速选择最佳值,吸附平衡后,洗脱溶剂流量 2 mL/min,分别以 2、3 、4、 5、 6 BV 60%的乙醇水溶液洗脱,测定流出液中金银花叶总黄酮的浓度,计算解吸率。
2.2.3.4 洗脱溶剂浓度的选择 操作同上,分别以体积分数为20%、40%、50%、60%、80%的乙醇水溶液,以流量2 mL/min进行洗脱,测定流出液中金银花叶总黄酮的浓度,计算解吸率。
2.2.3.5 洗脱流速的选择 操作同上,加入等体积60%的乙醇水溶液洗脱,流量为1、2、3、4 mL/min,测定流出液中金银花叶总黄酮的浓度,计算解吸率。
2.2.3.6 Box-Behnken响应面法优选金银花叶总黄酮纯化工艺 在单因素试验基础上,依据中心组合(Box-Benhnken)试验设计原理,以上样流速(A)、洗脱溶剂体积(B)、洗脱溶剂浓度(C)、洗脱溶剂流速(D)为自变量,总黄酮解吸率(Y)为评价指标进行设计(表1)。在优化条件下,进行3次验证试验。
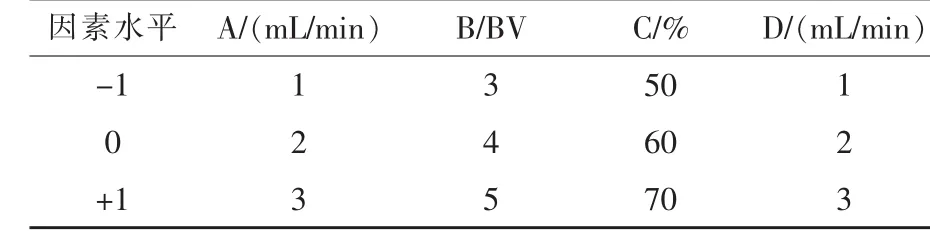
表1 Box-Behnken响应面试验因素与水平表
2.2.3.7 纯度测定 根据张星等(2018)的方法,按最优工艺纯化分离后得到的金银花叶总黄酮进行纯度测定:
纯度=Cd×Vd×100%/m;
式中:Cd为解吸溶液中金银花叶总黄酮的质量浓度,mg/mL;Vd为解吸溶液体积,mL;m 为干膏质量。
2.3 金银花叶总黄酮的体外抗氧化活性试验
2.3.1 DPPH自由基清除能力 参照姚新鼎等(2019)和夏娜等(2014)的测定方法并稍加修改。配制 DPPH乙醇溶液 (52.8μg/mL),取 1 mL DPPH乙醇溶液与1 mL不同浓度的样品溶液或Vc溶液充分混匀,室温下暗处放置30 min,在517 nm波长处测吸光度。计算公式如下:
DPPH 自由基清除率=1-(A1-A2)/A0;
式中:A1为样品组吸光度,A2为样品本底吸光度(以等体积无水乙醇代替DPPH溶液),A0为空白对照组吸光度 (以等体积蒸馏水代替样品溶液)。
2.3.2 ABTS+自由基的清除能力 参照黄琴等(2014)和范艳丽等(2017)的测定方法并稍加修改。配制7 mmol/mL的ABTS+溶液,室温下与等体积的4.9 mmol/mL过硫酸钾溶液混合后暗处放置12 h,制成ABTS+储备液,用pH 7.4的磷酸缓冲液稀释储备液20倍制成ABTS+工作液。取不同浓度的样品溶液和Vc溶液 1 mL,加入 2.0 mL的ABTS+工作液,震摇均匀后常温暗处放置10 min,在734 nm波长处测吸光度。计算公式如下:
ABTS+自由基清除率=1-(A1-A2)/A0;
式中:A1为样品组吸光度,A2为样品本底吸光度(以等体积蒸馏水代替ABTS+溶液),A0为空白对照组吸光度(以等体积蒸馏水代替样品溶液)。
3 结果与分析
3.1 大孔树脂的筛选 由表2可以看出,非极性大孔吸附树脂D101、HPD-100的吸附性能均高于中级性和极性大孔吸附树脂S-8和NKA-9,可达到65%以上。同时,大孔树脂比表面积越大越有利于吸附 (王慧芳等,2018),D101型大孔吸附树脂的比表面积稍大于HPD-100型大孔树脂,兼顾吸附解吸性能,选择D101型大孔吸附树脂进行金银花叶总黄酮的分离纯化,并对其进行工艺条件优化。

表2 大孔吸附树脂静态吸附及解吸分析
3.2 D101型大孔吸附树脂分离纯化工艺优选
3.2.1 泄露曲线测定 由图1可以看出,上样液体积为60~75 mL时吸光度增加0.01,大于75 mL时,金银花叶总黄酮开始大量泄漏,因此最终确定漏点为60 mL,即为2倍柱体积。因此1 mL大孔吸附树脂最大上样量须小于2 mL。
3.2.2 上样流速的选择 由图2可以看出,流速为2~3 mL/min时,黄酮类物质吸附率缓慢上升。流速大于3 mL/min时,黄酮类物质吸附率迅速下降。当上样流速为1 mL/min时,黄酮吸附率为 85%,当上样液流速为2 mL/min时,黄酮吸附率为84%。但是,当流速为1 mL/min时上样较慢,上样时间较长,可能会造成金银花叶总黄酮的死吸附,使解吸率下降。当流速为3 mL/min时,上样较快,容易导致黄酮类物质吸附不完全,造成损失。因此,选择上样流速为2 mL/min。
3.2.3 洗脱溶剂体积的选择 由图 3可以看出,当洗脱剂体积大于4 BV时,解吸率缓慢变化,即4 BV洗脱剂已经足以将金银花叶总黄酮洗脱。洗脱剂用量过大时,造成浪费不经济,并且减压浓缩回收乙醇比较耗时,因此,洗脱溶剂体积选择4 BV。
3.2.4 洗脱溶剂浓度的选择 由图4可以看出,当洗脱溶剂浓度为20%~60%时,解吸率随乙醇浓度的增加而升高,当乙醇浓度继续上升时,解吸率下降。其原因是黄酮类化合物与大孔吸附树脂之间存在范德华力,当两者极性接近时解吸率达到最大(王慧芳等,2018)。D101型大孔吸附树脂为弱极性树脂,金银花叶总黄酮为弱极性分子,因此洗脱乙醇浓度越大,极性越小,越有利于金银花叶总黄酮的洗脱,但是当乙醇的浓度继续增加到80%时,金银花叶总黄酮的解吸率反而降低,这主要是因为,醇溶性杂质随之增多,导致总黄酮的解吸率下降,综上,选择60%的乙醇作为洗脱溶剂。
3.2.5 洗脱流速的选择 由图5可知,当洗脱剂流速为2 mL/min时,解吸率达到最大,当洗脱剂流速继续增大反而使解吸率下降,主要原因是乙醇体积流量流速过大,洗脱液还未来得及洗脱树脂上吸附的黄酮分子就已流了出去,因此选择的洗脱流速为2 mL/min。
3.2.6 Box-Behnken响应面优化D101型大孔吸附树脂分离纯化工艺
3.2.6.1 Box-Behnken响应面分析方案及试验结果 响应面分析方案及试验结果见表3。
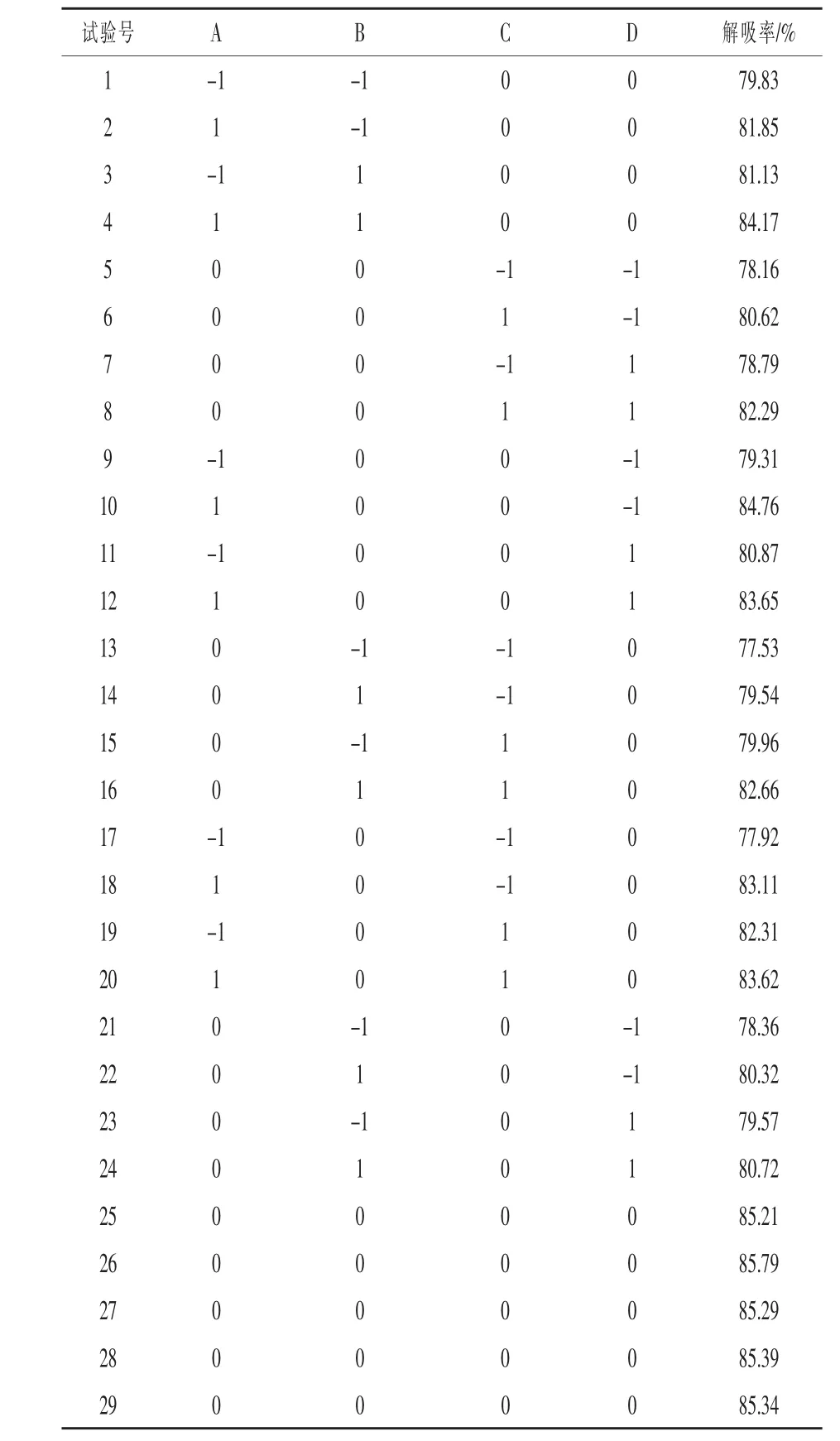
表3 Box-Behnken响应面分析方案及试验结果
3.2.6.2 模型的建立及显著性检验 采用Design-Expert 8.0.5b软件对表3中总黄酮解吸率进行多元回归拟合,得金银花叶总黄酮解吸率与A、B、C、D四因素变量的二次多元回归模型为:
Y=85.40+1.65A+0.95B+1.37C+0.36D+0.26AB-0.97AC-0.67AD+0.17BC-0.20BD+0.26CD-0.76A2-2.87B2-2.77C2-2.65D2,对所得数据模型进行方差分析,结果见表4。
由表4可知,模型P<0.01,是极显著的,说明方程有意义,而失拟项P=0.0684,大于0.05,差异无统计学意义,即模型与试验的差异较小,说明其他因素对试验结果的干扰较小,残差由随机误差引起,能充分反映各因素和响应值之间的关系(姚新鼎等,2019)。另外,总黄酮得率回归方程的相关系数R2a为0.9853,校正系数 R2adj=0.9706,均>0.9,说明此模型能说明试验中97.06%的响应值变化,因此可以用此回归方程对D101型大孔吸附树脂优化金银花叶纯化工艺结果进行分析和预测。从单因素水平来看,各因素对D101型大孔吸附树脂纯化金银花叶总黄酮解吸率影响的主次顺序为:A>C>B>D,即上样流速>洗脱溶剂浓度>洗脱溶剂体积>洗脱溶剂流速。响应面对于单因素A、B、C、D值构成的三维空间及其在二维平面上的等高线图,可以直观地反映各因素之间的相互作用,通过软件处理得到的响应面见图 6。

表4 Box-Behnken响应面方差分析结果
3.2.6.3 D101型大孔吸附树脂最优纯化工艺和验证试验 通过Design-Expert 8.0.5b软件对模型进行预测分析,得到最优纯化工艺:乙醇浓度为60.19%,乙醇体积为4.09倍柱体积,上样流速为2.56 mL/min,洗脱流速为2.16 mL/min,在该条件下金银花叶总黄酮的解吸率为86.1109%。为了实际操作可行性,最终将纯化工艺条件修改为乙醇浓度为60%,乙醇体积为4倍柱体积,上样流速为2.5 mL/min,洗脱流速为2 mL/min。对响应面优化的分离纯化工艺参数进行验证试验,制备3批样品,金银花叶总黄酮的解吸率分别为86.52%、87.09%和85.77%。选用优化后的树脂纯化工艺参数进行试验的3批样品,金银花叶总黄酮的解吸率基本稳定,可用于金银花叶总黄酮的大规模分离纯化。
3.2.6.4 纯度测定 根据纯化工艺参数进行验证试验,制备3批样品的金银花叶总黄酮的纯度见表5。
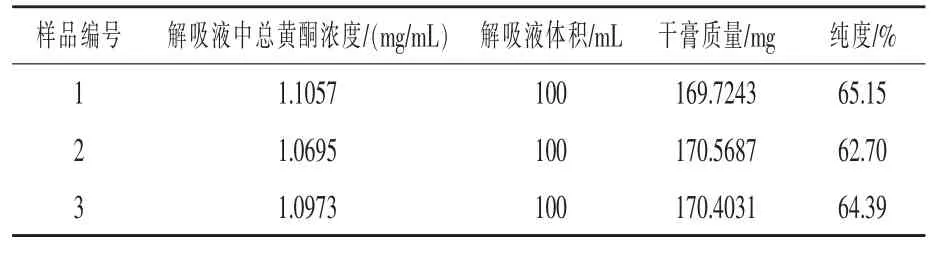
表5 三批金银花叶总黄酮纯度
3.3 抗氧化试验结果
3.3.1 DPPH自由基清除能力试验结果 由图7可知,总黄酮质量浓度为0~28.6μg/mL时,随着总黄酮质量浓度的增加,DPPH自由基清除率随之增加。当总黄酮质量浓度为22.88μg/mL时,对DPPH自由基清除率达到82.40%,阳性对照Vc为77.02%。以上结果表明金银花叶总黄酮对DPPH自由基有良好的清除的能力。金银花叶总黄酮清除DPPH自由基的机理可能是因为黄酮样品中具有供氢体,可以提供质子还原具有氧化性的自由基,终止自由基的连锁反应,起到抑制或清除自由基的作用(罗磊等,2018)。
3.3.2 ABTS+自由基的清除能力试验结果 由图8可知,总黄酮质量浓度为0~35.75μg/mL时,随着总黄酮质量浓度的增加,ABTS+自由基清除率随之增加。当总黄酮质量浓度为21.45μg/mL时,对ABTS+自由基清除率达到92.01%,之后在总黄酮质量浓度为28.60~35.75μg/mL时,ABTS+自由基清除率保持相对稳定。总黄酮质量浓度为35.75μg/mL时,对ABTS+自由基清除率达到91.32%,高于同浓度阳性对照Vc对ABTS+自由基清除率85.97%。以上结果说金银花叶总黄酮具有很高的清除ABTS+自由基的能力。
4 讨论
本试验利用响应面法优化了D101大孔吸附树脂制备华金6号金银花叶总黄酮有效部位的工艺,得到最佳制备方案:粗提液上样流速为2.5 mL/min,洗脱溶剂为60%乙醇,洗脱溶剂体积为4倍柱体积,洗脱流速为2 mL/min;此方法总黄酮提取率与响应面预测值非常接近,纯度可达60%以上,工艺稳定可行,可为华金6号新品种金银花叶总黄酮类成分的大规模生产提供参考。
黄酮类化合物分离纯化的方法有很多种,氧化铝层析法、聚酰胺吸附树脂吸附法、大孔树脂吸附法等,与其他方法相比,大孔吸附树脂具有成本低、分离效率高、操作简单、无毒性、可工业化大批量生产等优点,已广泛应用于黄酮类成分的纯化 (向海燕等,2017;张华潭,2015)。因此,本试验采用D101型大孔吸附树脂对金银花叶进行分离纯化,为金银花叶总黄酮类成分的开发提供基础。
响应面法是一种综合试验设计和数学建模的优化方法,可有效地减少试验次数,缩短试验周期,分析结果直观清晰,且可考察各因素之间的交互作用。本试验通过Box-Behnken响应面法对金银花叶总黄酮纯化工艺进行优选,准确地得到最佳纯化方案,此纯化方案为以后的大规模生产提供参考。
体外抗氧化活性试验表明在一定质量浓度范围内华金6号金银花叶总黄酮有效部位的体外抗氧化能力随质量浓度的增大而增强,并呈剂量依赖性,与罗磊(2018)的研究结果一致。纯化后的金银花叶总黄酮的ABTS+自由基清除能力高于同浓度的Vc清除能力,DPPH自由基的清除能力接近同浓度的Vc清除能力,金银花叶黄酮具有良好的体外抗氧化性。

