表面充氢对TA2在草酸溶液中腐蚀行为的影响
赵文波,赵博深,李广州,师红旗,丁毅
(南京工业大学 材料科学与工程学院,南京 211816)
钛及钛合金以其优异的耐蚀性广泛应用于航空航天、石油化工、生物医药等领域[1-4],在服役过程中,经常面临各种酸性的腐蚀环境[5-6]。目前,关于钛及钛合金在硫酸等无机酸溶液中的腐蚀行为已做过许多研究[7-10],并提出了一些改善钛金属在无机酸溶液中耐蚀性能的方法[11-13],但对钛及钛合金在草酸等有机酸溶液中的腐蚀行为研究较少,也没有可以有效改善钛金属在草酸溶液中耐蚀性能的方法提出。草酸作为一种重要的有机酸,在稀土加工、医药制造、化工等领域有广泛的应用[14-15],这极大地限制了钛及钛合金的应用范围。前期研究工作中发现,钛表面充氢后,可以显著改善其在草酸介质中的耐蚀性,这对于扩大钛材在有机酸中的应用范围具有较为重要的研究价值。
本文采用电化学充氢的方法对 TA2工业纯钛进行表面充氢处理。采用SEM、XRD等对充氢前后TA2试样表面的组成和结构进行分析,采用电化学测试和浸泡实验研究充氢后钛试样在草酸溶液中的耐蚀性。
1 实验
1.1 样品制备及充氢
实验材料采用厚度为2 mm的商业纯钛(TA2)板材,其化学成分(质量分数)为:Fe 0.085%,C 0.030%,N 0.006%,O 0.2%,H 0.001%,Ti余量。电化学测试试样和浸泡实验试样均采用线切割加工。电化学试样为直径1 cm的圆片,预留圆片的一面作为工作面,另一面焊接导线,并用耐高温的环氧树脂将非工作面封装(工作面面积为0.785 cm2)。浸泡实验试样尺寸为 40 mm×22 mm×2 mm(表面积为20 cm2)。用水砂纸将电化学试样的工作面和浸泡试样的各面逐级打磨至2000目,然后依次用去离子水、无水乙醇清洗,冷风吹干后备用。
采用0.5 mol/L H2SO4+ 2 g/L CH4N2S作为充氢介质,以10 mA/cm2的电流密度在常温(25 ℃)下进行电化学充氢。充氢过程中,试样作为阴极,铂片电极作为阳极。为了获得不同氢含量的样品,试样的充氢时间分别为0(不充氢)、2、8、24 h。充氢后的试样依次用去离子水和无水乙醇进行清洗,冷风吹干后进行后续实验。
1.2 表面分析
充氢后,采用FEI QUANTA 200 环境扫描电子显微镜(SEM)观察试样的表面形貌。使用 Axio Observer A1m型蔡司金相显微镜观察试样的纵截面,并测量氢化物层的厚度。采用D Max/RB X射线衍射分析仪,在 20°~90°的范围内,以 10 (°)/min的扫描速率进行XRD分析,以确定充氢试样表面的主要晶相。
1.3 电化学测试
电化学测试采用上海辰华 CHI660E电化学工作站和标准三电极体系:其中工作电极为待测试样,辅助电极为铂电极,参比电极为通过盐桥连接的饱和甘汞电极(SCE)。测试介质为1%的草酸溶液,测试温度为60 ℃,温度通过恒温水浴锅控制。
测试开始前,先将试样在开路状态下保持1 h,使开路电位(OCP)达到稳定状态。电化学阻抗谱(EIS)测试频率范围为100 kHz ~ 10 mHz,交流激励信号幅值为10 mV。EIS数据采用ZSimpwin软件进行拟合。动电位(vs.OCP)极化曲线测量范围为-0.3~3 V,扫描速率为1 mV/s。所有电化学测试重复3次。
1.4 浸泡实验
浸泡实验采用1%草酸作为腐蚀介质,实验温度为60 ℃。浸泡前,先将试样置于真空干燥箱中,在常温下真空干燥8 h,然后称量,并记录。浸泡时,采用三点支撑将试样置于草酸溶液中浸泡24 h。浸泡完成后,先使用毛刷去除试样表面的腐蚀产物,然后依次用去离子水、无水乙醇清洗,并置于真空干燥箱中在常温下真空干燥8 h,称量并记录,计算腐蚀速率。
浸泡实验时,放入尺寸为10 mm×10 mm×2 mm的平行试样。浸泡完成后,将试样取出,并依次用去离子水、无水乙醇清洗,冷风吹干后使用SEM观察试样的腐蚀形貌。
2 结果和讨论
2.1 表面形貌及组成分析
TA2试样以10 mA/cm2的电流密度分别充氢0、2、8、24 h后的表面形貌如图1所示。可以看出,当充氢时间不长于8 h时,试样表面的加工痕迹仍清晰可辨,这说明试样保持了较完整的原始表面形貌。当充氢时间达到24 h时,试样表面部分区域的加工痕迹已难以辨识,甚至出现了剥落的迹象。这是因为长时间的充氢,使原始表面下生成了较多的氢化钛,而α-Ti向氢化钛转变可导致体积膨胀[16-18]。当试样的原始表面无法承受因膨胀而产生的应力时,试样表面就会出现裂纹,再加上充氢过程中,一部分氢原子在试样表面复合,形成氢分子,当这些氢分子以氢气泡的形式从表面逸出时,也会对已经出现裂纹的原始表面产生冲击效应,从而使试样的原始表面出现剥落。
不同充氢时间下,TA2试样纵截面的金相图如图2所示。可以看出,充氢后,试样表面出现了明显的分层现象。XRD分析结果显示(如图3所示),充氢后,试样表面出现了TiH1.5(属于γ氢化物,fcc结构)的特征峰,表明试样表面新形成了以TiH1.5为主要组成相的氢化钛层。这层氢化钛层是电化学充氢过程中透过试样表面的氢原子与钛基体反应生成的。研究表明[16],充氢过程中,钛与氢生成的氢化钛类型与充氢电流密度有关:当充氢电流密度不大于 10 mA/cm2时,生成的氢化钛主要为TiH1.5;当充氢电流密度大于10 mA/cm2时,则会生成TiH1.971(属于δ氢化物,fcc结构)。这与本实验中采用10 mA/cm2的电流密度进行充氢,生成以TiH1.5为主要组成相的氢化钛层的实验结果相符。氢化钛(CAS:7704-98-5)化学性质稳定,不会与空气和水发生作用。随着充氢时间的延长,TiH1.5特征峰的强度不断增强,Ti基体特征峰的强度则逐渐减弱,这也与新物层随充氢时间的延长而增厚的结果相吻合。当充氢时间达到24 h时,试样表面的XRD图谱中几乎只出现了 TiH1.5的特征峰。一方面,这说明当充氢时间达到24 h时,试样表面氢化钛层的厚度已经增加到几乎可以完全遮蔽 Ti基体特征峰的程度了;另一方面,也说明新形成的氢化钛层中几乎不含其他物相。
2.2 电化学测试
不同充氢时间的TA2试样在60 ℃ 1%的草酸溶液中的动电位极化曲线如图4所示。当试样未充氢时(0 h),其自腐蚀电位较负,约-0.7 V(vs.SCE),且存在明显的活化钝化过渡区。这说明未充氢的TA2试样在草酸溶液中会发生活性溶解。和未充氢试样相比,充氢后的 TA2试样没有出现活化钝化过渡区。这说明充氢后的 TA2试样在草酸溶液中处于钝化状态,没有发生活性溶解,具有更强的耐草酸腐蚀性能。这一试验结果证明,在草酸溶液中,充氢后试样表面生成的氢化钛层对钛基体具有保护作用。随着充氢时间的延长,TA2试样的自腐蚀电位不断正移,这说明氢化钛层厚度(见图2)的增加,可以使试样在草酸溶液中的耐蚀性提高。当充氢时间超过8 h时,试样的维钝电流密度出现小幅度的下降。这是因为氢化钛层的存在虽然隔离了Ti基体与草酸介质的直接接触,但当该氢化钛层较薄时,对Ti4+向溶液中扩散的阻碍作用不明显。
不同充氢时间下,TA2试样在草酸溶液中的电化学阻抗谱如图5所示。根据以前的研究结果[19-20],电化学阻抗(EIS)测试结果采用图5a中所示的等效电路进行拟合。虽然未充氢试样与充氢试样的EIS数据所采用的等效电路形式相同,但根据试样的特征和拟合结果综合分析,图5a中的等效电路中除了Rs代表溶液电阻相同外,其余各电化学元件在未充氢试样和充氢试样中的含义则有所区别。对于未充氢的试样,表面只有一层原始的钝化膜,Nyquist图显示出两个时间常数的特征。这说明未充氢的试样表面除了钝化膜的贡献外,还存在Helmholtz双电层。因此,对于未充氢的试样,Ra为表面膜电阻(Rf),Qa为表面膜电容(Qf),Rb为电荷转移电阻(Rct),Qb为双电层电容(Qdl),见图 6a;而充氢后的试样(2、8、24 h),其表面存在原始的钛氧化物外层和新生成的钛氢化物内层,因此Ra为原始表面膜电阻(Rfo),Qa为原始表面膜电容(Qfo),Rb为内层氢化钛层电阻(Rfi),Qb为内层氢化钛层电容(Qfi),见图6b。图5a中,充氢试样的Nyquist图所示的一个表观时间常数似乎与等效电路中两个时间常数的特征不符。这是因为在草酸溶液中,充氢试样外层原始膜的电阻远低于内层氢化钛层电阻,导致电化学行为由内层支配[20]。另外,由于电极表面的不均匀性,会造成表面电容与理想电容存在一定程度的偏差,故在数据拟合时,使用常相位角元件(CPE)代替理想电容[21-23]。拟合结果见表1。
TA2试样的耐蚀性可以用极化电阻(Rp)来评估[24]。对于未充氢的试样,其极化电阻为:
对于充氢后的试样:
式(1)和式(2)基于极化电阻(Rp)的定义得出:
式中:ZF为电路中法拉第阻抗;ω为角频率。未充氢与充氢TA2试样的Rp如图7所示。可以看出,试样的极化电阻(Rp)随着充氢时间的延长而增加,试样的耐蚀性提高,这与动电位极化曲线测试的结果一致。
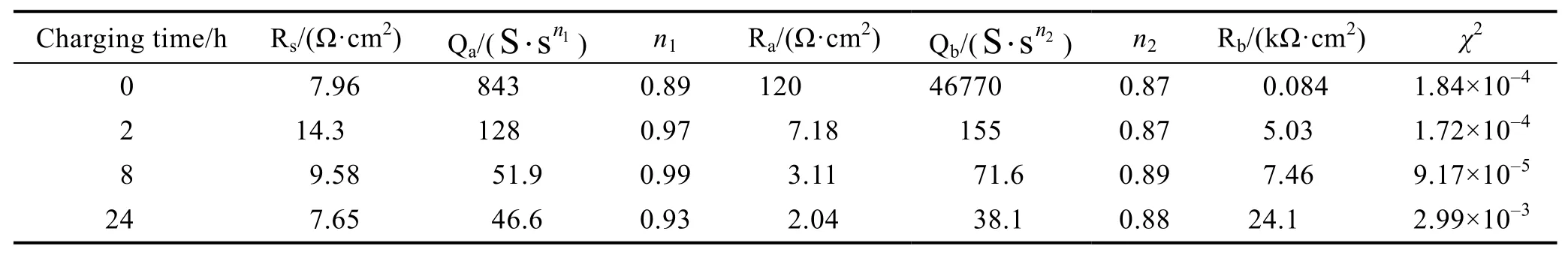
表1 通过拟合EIS数据获得的电化学参数Tab.1 Electrochemical parameters obtained by fitting the EIS data
2.3 浸泡实验
不同充氢时间的 TA2试样在草酸溶液中浸泡前和浸泡后的表面形貌如图8所示。可以看出,随着充氢时间的延长,试样的腐蚀程度不断下降。未充氢试样(图8a、b)发生了严重的腐蚀,试样表面由致密光滑变得疏松多孔。充氢2 h的试样(图8c、d)虽然也发生了腐蚀,试样表面出现了一些腐蚀坑,但其腐蚀程度较未充氢试样要轻得多。和充氢2 h的试样相比,充氢8 h试样(图8e、f)的腐蚀程度进一步下降,试样表面仅出现一些较浅的孔洞。对于充氢24 h的试样(图 8g、h),其表面在腐蚀前后几乎没有出现变化,腐蚀程度轻微。这与电化学测试结果相吻合。
不同充氢时间的 TA2试样在草酸溶液中的腐蚀速率如图9所示。腐蚀速率采用式(4)进行计算:
式中:X为试样腐蚀速率,mm/a;m1、m2分别为试验前后试样的质量,g;k为常数,k=87 600;A为试样表面积,cm2;t为试验时间,h;ρ为试样密度,g/cm3。
由图9可见,随着充氢时间的延长,试样在草酸溶液中的腐蚀速率不断下降。当充氢时间达到 24 h时,腐蚀速率从未充氢时的 4.63 mm/a下降到0.03 mm/a,下降幅度达到了 2个数量级。这说明电化学充氢后,在 TA2试样表面形成的氢化物层,可以抵御草酸溶液对 Ti基体的侵蚀,具有较钛氧化物钝化膜更好的稳定性。随着氢化物层厚度的增加,充氢TA2试样在草酸溶液中的耐蚀性也随之提高。
电化学测试和浸泡试验的结果表明,充氢 TA2试样表面的氢化钛层可以提高其在草酸溶液中的耐蚀性,且氢化钛层的厚度越厚,试样的耐蚀性越好。这说明氢化钛的存在对提高 TA2在草酸溶液中的耐蚀性有益。通过对在草酸溶液中浸泡前后的未充氢试样进行XRD分析发现(见图 10),TA2在草酸溶液中会自发生成氢化钛(TiH1.5),但氢化钛没有对 Ti基体起到应有的保护作用。因为这些氢化钛是在钛腐蚀电池的阴极区形成的,而阳极区是钛的溶解,因此在这种条件下生成的氢化物层不致密,且不完整连续。图8b的微观形貌则能证明这一点,图中众多微小突出物即为阴极区氢化钛,而众多微小孔洞则是阳极溶解区。通过电化学充氢方式生成的氢化物层具有完整且较为致密的结构(图 2),可以更好地隔离 Ti基体与草酸溶液的接触。这说明在草酸溶液中,TA2试样表面的保护层要发挥对 Ti基体的保护作用,除了与其成分有关外,还与其结构相关。完整致密的氢化物层可以对 Ti基体起到很好的保护作用,而疏松多孔的氢化钛不仅不能保护 Ti基体,反而还会促进Ti基体的腐蚀。
3 结论
1)TA2试样在0.5 mol/L H2SO4+ 2 g/L CH4N2S溶液中,以10 mA/cm2的电流密度进行电化学充氢。充氢后,试样表面生成了以TiH1.5为主要组成相的氢化钛层,氢化钛层的厚度随充氢时间的延长而增加。
2)随充氢时间的延长,充氢TA2试样在草酸溶液中的自腐蚀电位逐渐从未充氢时的-0.7 V升高到0 V左右,并由未充氢时的活化状态转变为钝化状态,腐蚀倾向降低;同时极化电阻Rp逐渐从未充氢时的0.2 kΩ·cm2增加到了 24.1 kΩ·cm2,耐腐蚀性能提高。
3)充氢后的TA2试样在草酸溶液中的腐蚀程度随充氢时间的延长而减弱,腐蚀速率随充氢时间的延长而下降。与未充氢试样的腐蚀速率4.63 mm/a相比,充氢24 h试样的腐蚀速率下降到0.03 mm/a,下降幅度达到了2个数量级。
4)在草酸溶液中,电化学充氢后在TA2试样表面生成的氢化钛层对 Ti基体具有保护作用,并且保护效果随氢化钛层的增厚而增强。试样表面氢化钛层对 Ti基体的保护作用除了与成分有关外,还与其结构相关。完整致密的氢化钛层可以对 Ti基体起到很好的保护作用,而疏松多孔的氢化钛不仅不能保护Ti基体,反而还会促进Ti基体的腐蚀。

