黔产红花龙胆药材HPLC指纹图谱及芒果苷含量分析*
刘恩稳,徐仕娟,徐文芬,刘 娇,马敏龙,陈小秀,员 浬
(贵州中医药大学 药学院,贵州 贵阳 550025)
红花龙胆为2015年版《中国药典》一部和2003年版《贵州省中药材、民族药材质量标准》收载品种,是贵州少数民族常用药物,又名青鱼胆草(苗族药名“锐定谋”),来源于龙胆科龙胆属多年生草本植物红花龙胆GentianarhodanthaFranch.的干燥全草,性味苦寒,具有清热燥湿、解毒泻火、止咳的功效,主治湿热黄疸、肺热咳嗽、小便不利[1-2]。现代研究表明,红花龙胆主要含酚酸类、(裂)环烯醚萜类、口山酮类、黄酮类、三萜类等化合物,且主要成分芒果苷,是发掘抑制中枢神经系统、抗炎、止咳、抑菌等药物的主要活性物质,除此之外,其含量甚微的环烯醚萜苷类化合物在提取富集、含量测定和活性方面,近几年来受到国内外学者的广泛关注[3-9]。由于红花龙胆药材多来源于野生,许多地区野生资源蕴藏量急剧锐减,在民间各地区的实际应用中存在混用的现象,因此,加强红花龙胆的质量控制极其重要[10]。红花龙胆作为肺力咳合剂、莲龙胶囊、康妇灵胶囊等制剂的主要原料,需求量不断增加,原料质量是保障相关制剂安全有效和质量可控的前提。在现行《中国药典》红花龙胆质量标准中,虽然已经建立了以芒果苷为含量测定指标的药材质量控制方法。但是,对于中医药理论指导下的中药,产生的疗效不是某一成分作用的结果,检测任何一种活性成分均不能反映中药所体现的整体疗效。因此,从中医药整体作用出发,为较全面地表征红花龙胆质量属性,本文采用高效液相色谱法,以黔产11批红花龙胆药材为研究对象,建立其指纹图谱测定方法,结合多种模式识别方法进行指纹图谱分析评价,并比较其芒果苷的含量差异,以期为红花龙胆药材质量的综合评价及其相关制剂的质量控制提供参考依据。
1 仪器与试药
1.1 仪器
UltiMate-3000型高效液相色谱仪、Thermochromeleon7色谱工作站(美国Thermo Fisher公司),AG135型十万分之一电子天平 (瑞士Mettler-Toledo公司),KQ-500DE超声器(昆山市超声仪器有限公司),DIKMA Diamonsil spusil C18色谱柱(4.6 mm×250 mm,5 μm)等;2004 A版国家药典委员会“中药色谱指纹图谱相似度评价系统”(以下简称指纹图谱软件)。
1.2 材料
芒果苷对照品(购自中国食品药品检定研究院,批号 111607-201704,供含量测定用),甲醇、乙腈为色谱纯(美国Tedia公司),磷酸为优级纯(天津市科密欧化学试剂有限公司),实验用水为重蒸馏水,其他试剂均为分析纯。11批黔产红花龙胆药材经贵州中医药大学孙庆文教授鉴定为龙胆科植物红花龙胆GentianarhodanthaFranch.的干燥全草,洗净后50 ℃烘干粉碎,过三号筛备用,样品采集信息见表1。

表1 11批红花龙胆药材信息
2 指纹图谱方法与结果
2.1 色谱条件
DIKMA Diamonsil spusil C18色谱柱(4.6 mm×250 mm,5 μm);流动相为乙腈(A)-0.05%磷酸水(B),梯度洗脱(0~10 min,93%→89%B;10~33 min,89%→81%B;33~48 min,81%→72%B;48~57 min,72%→69%B;57~61 min,69%→63%B;61~77 min,63%→10%B);流速1.0 mL/min;柱温25 ℃;检测波长242 nm;进样量10 μL。
2.2 溶液的配制
2.2.1 对照品溶液的制备
精密称取芒果苷对照品适量,置10 mL容量瓶中,加60%甲醇制成每1 mL含0.072 mg的溶液,即得。
2.2.2 供试品溶液的制备
取红花龙胆药材粉末1.0 g,精密称定,置100 mL具塞锥形瓶中,精密加入70%甲醇40 mL,密塞并称定质量,超声处理15 min(功率500 W,频率40 kHz),冷却至室温,用70%甲醇补足减失质量,摇匀,过滤,滤液浓缩并转移定容于10 mL容量瓶,摇匀,即得。
2.3 方法学考察
2.3.1 专属性试验
精密吸取70%甲醇溶液、对照品及供试品溶液,微孔滤膜过滤,按“2.1”项下色谱条件进样检测,记录色谱图1。结果表明,该提取溶剂、流动相及色谱条件下,对指纹峰测定无干扰。

图1 供试品(A)、对照品(B)和70%甲醇溶液(C)的HPLC图谱Fig.1 HPLC chromatogram of sample(A),reference substance (B) and 70% methanol solution (C)
2.3.2 完整性试验
精密吸取供试品溶液,按“2.1”项下色谱条件进样检测,按既定条件洗脱结束时的流动相比例继续洗脱至154 min,记录色谱图2。结果显示,按既定洗脱程序运行77 min后未检测到样品色谱峰,表明采集77 min色谱图可基本完整记录红花龙胆药材化学成分信息。

图2 红花龙胆完整性试验的HPLC色谱图Fig.2 HPLC chromatogram of integrity test ofGentiana rhodantha
2.3.3 精密度试验
精密吸取同一供试品溶液,按“2.1”项下色谱条件,连续进样6次,记录色谱图并以芒果苷峰为参比峰,计算各共有峰的相对保留时间及相对峰面积的RSD,前者均<0.41%,后者均<1.4%,表明仪器精密度良好。
2.3.4 重复性试验
按“2.2.2”项下方法制备供试品溶液6份,于“2.1”项下色谱条件进样分析,记录色谱图并以芒果苷峰为参比峰,计算各共有峰的相对保留时间及相对峰面积的RSD,前者均<0.10%,后者均<1.7%,表明该方法重复性良好。
2.3.5 稳定性试验
取同一份供试品溶液,按“2.1”项下色谱条件下分别在第0 h、2 h、4 h、8 h、12 h、24 h、36 h进样测定,并以芒果苷为参比峰,计算各共有峰的相对保留时间及相对峰面积的RSD,前者均<0.59%,后者均<1.9%,表明供试品溶液在36 h内稳定性良好。
2.4 指纹图谱的建立
取11批红花龙胆样品供试品溶液,按上述色谱条件进样测定,记录色谱图。将其原始图谱导入指纹图谱软件进行相似度分析,以S1样品为参照图谱,采用中位数法生成对照图谱,时间窗宽度为0.5,经多点校正、自动匹配后生成红花龙胆的共有模式,得到11批红花龙胆样品的HPLC叠加图谱,结果见图3。
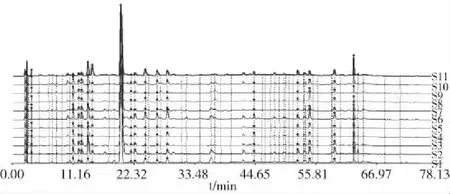
图3 11批红花龙胆药材HPLC叠加图谱Fig.3 HPLC fingerprints of 11 batches of Gentiana rhodantha
2.5 共有峰的标定及指认
根据指纹图谱匹配结果,标定17个共有峰,经过与相同条件测定的芒果苷对照品HPLC图谱比较,供试品图谱中7号共有峰的保留时间及UV光谱图与芒果苷对照品色谱峰一致,且色谱峰的峰形和分离度较好(见图4),故设定7号共有峰为参照峰(S),计算其余16个共有峰的相对保留时间和相对峰面积值。结果详见表2、表3。

图4 芒果苷对照品HPLC图谱(A)及红花龙胆对照指纹图谱(B)Fig.4 HPLC spectrogram of mangiferin reference (A) and HPLC contrast fingerprint of Gentiana rhodantha (B)

表2 11批红花龙胆药材指纹图谱17个共有峰的相对保留时间

表3 11批红花龙胆药材指纹图谱17个共有峰的相对峰面积值Tab.3 Relative peak areas of 17 common fingerprintpeaks in 11 batches of Gentiana rhodantha
2.6 相似度评价结果
11批样品指纹图谱相似度分析结果见表4,其相似度结果为0.589~0.993,其中S1、S2、S6红花龙胆指纹图谱与其他批次指纹图谱相似度较低,均小于0.8,其化学成分存在较大差异,但S1和S2指纹图谱的相似性较高,相似度为0.984。其余批次红花龙胆药材指纹图谱相似度相对较高,表明其化学成分具有一定的相似性。

表4 11批红花龙胆药材的相似度结果
2.7 聚类分析(HCA)结果
聚类分析是建立样本与样本之间相似关系或亲疏关系的一种数据分析手段,目前已广泛应用于中药鉴别、质量评价和品种分类等方面[11-13]。以11批红花龙胆药材指纹图谱中17个共有峰的峰面积为变量,利用SPSS 20.0软件中“系统聚类”,结合“组间距离法”对红花龙胆样品HPLC指纹图谱进行聚类分析,以欧氏距离作为度量标准,结果见图5。结果显示,当欧式距离为15时,11个产地的红花龙胆主要分为3类,黔产有8批不同来源的红花龙胆药材被聚为一类(S1、S3~S5、S7~S10),说明采集的红花龙胆药材不具有明显的地域区分性;而S2和S11批药材与其他批次分开,S6单独成一类。该药材聚类结果与相似度分析结果一致,可用于红花龙胆药材质量的一致性评价。

图5 聚类分析结果Fig.5 Results of hierarchical cluster analysis
2.8 主成分分析(PCA)结果
将11批红花龙胆药材的17个共有峰峰面积数据导入SPSS 20. 0软件,进行PCA分析。对其原始数据Z标准化处理,以主成分的特征值及贡献率为依据,进行相关系数矩阵、主成分特征值及累积贡献率的计算,各变量因子分析结果见表5、表6,碎石图见图6,并根据主成分综合得分进行排名。以特征值(VIP)>1为提取标准,得到前5个主成分的累计方差贡献率为92.725%(>80%),选取前5个主成分进行分析,可反映红花龙胆药材中17个成分量的92.725%的信息量,具有很好的代表性,可用于评价红花龙胆药材的品质。

表5 主成分特征值及方差
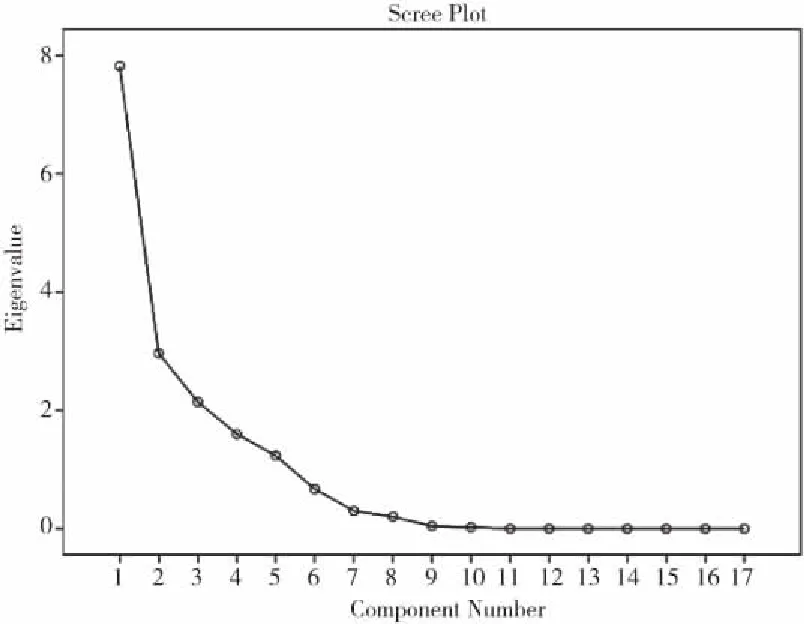
图6 红花龙胆药材的碎石图Fig.6 Scree plot of Gentiana rhodantha

表6 主成分载荷矩阵
主成分载荷矩阵可反映各变量对主成分的贡献大小及方向,据因子载荷矩阵,可推测影响红花龙胆药材质量差异的并不是单一成分,而是多成分作用的结果。由表6可知,17个变量对各主成分的正负相关,共有峰5、9和16对主成分1贡献最大,共有峰2、3和17对主成分2贡献最大,以此类推,可知共有指纹峰5、9~12、14和16号峰等对黔产红花龙胆指纹图谱差异的贡献值较大。对比各共有峰,7号峰对不同产地红花龙胆指纹图谱差异的贡献值较小,且其峰面积较大,适宜作为指纹图谱的参照峰,说明本实验指纹图谱的建立处所选取的参照峰合理。
以上述主成分载荷值建立红花龙胆品质的评价模型,用Z1、Z2、Z3、Z4、Z5代表前5个主成分反映贵州11批不同来源红花龙胆药材样品所表达的信息,得出如下成分的线性组合表达式:
Z1=0.388X1+0.421X2+0.500X3+0.510X4+0.868X5+0.388X6+0.345X7+0.695X8+0.883X9+0.835X10+0.842X11+0.853X12+0.685X13+0.831X14+0.645X15+0.855X16+0.507X17
Z2=0.221X1+0.762X2+0.682X3+0.648X4-0.145X5-0.597X6-0.485X7+0.21X8-0.094X9-0.137X10-0.066X11-0.011X12-0.309X13-0.003X14+0.411X15-0.166X16-0.648X17
Z3=0.782X1-0.022X2+0.218X3+0.384X4+0.407X5-0.041X6+0.361X7-0.260X8+0.091X9-0.494X10-0.414X11-0.355X12-0.165X13-0.214X14-0.195X15+0.353X16+0.429X17
Z4=0.348X1-0.143X2+0.109X3+0.081X4+0.096X5+0.602X6-0.669X7-0.469X8-0.15X9-0.018X10+0.102X11-0.189X12+0.495X13+0.141X14+0.021X15-0.055X16-0.256X17
Z5=-0.105X1-0.379X2+0.427X3-0.230X4-0.052X5+0.151X6+0.130X7+0.248X8-0.379X9-0.001X10-0.297X11-0.290X12-0.110X13+0.331X14+0.509X15+0.205X16+0.005X17
其中,X为17个共有峰量化峰面积的标准化值。将上述所得表达式加合,构建红花龙胆药材质量综合评价指标,得到11批红花龙胆药材的主成分得分、综合得分及排序情况,见表7,其中Z值越大,表明药材的综合质量越高。11批不同产地红花龙胆的综合得分排名为:S6>S10>S8>S11>S2>S3>S9>
S7>S4>S5>S1。结果显示,不同产地之间的红花龙胆药材化学成分含量存在一定的差异,且同一地区药材质量也并不统一。

表7 样本主成分得分及排名
主成分1、2和3的累积贡献率达到76.050%,基本包含了红花龙胆指纹图谱的大部分信息,采用SPSS 20. 0软件,以第1~3主成分得分(Z1~Z3)建立三维坐标体系散点图,见图7。其中11批红花龙胆样品有8批的整体分布较近,说明该8批红花龙胆药材质量差异不大,且样品S6单独聚为一类,其余样品聚为一类,其PCA与HCA分析结果相互得以印证。

图7 11批红花龙胆药材的三维散点图Fig.7 Three-dimensional scatter plot of 11batches of Gentiana rhodantha
2.9 红花龙胆中芒果苷的含量测定
依照2015年版《中国药典》红花龙胆质量标准中的芒果苷含量测定项下方法,色谱柱为Thermo Accucore C18(4.6 mm×150 mm,2.6 μm),测定11批黔产红花龙胆药材中芒果苷的含量,结果见表8。

表8 不同批次红花龙胆药材中芒果苷的含量测定结果(n=3)
由表8可知,贵州不同产地红花龙胆的芒果苷含量具有一定差异,其含量波动范围较大(1.13%~2.85%),其中贵州贵阳乌当区和花溪区、龙里县草原乡、水城县滴水岩村产地红花龙胆药材中芒果苷含量高于2.0%,符合现行《中国药典》规定,其余采自贵州的7批野生样品均不合格且含量差异较大,但贵州有不少药物的主要原料是红花龙胆,因此选择适宜的区域对红花龙胆药材进行规范化种植尤为重要,以保证该药材质量的稳定性,进而确保相关中药制剂的有效性。
3 讨论
指纹图谱色谱条件的优化,由于红花龙胆中主要含酚酸类、(裂)环烯醚萜类、口山酮类等化合物,鉴于此,本实验分别考察了232、238、240、242、243、258、270、300 nm等8个波长,对比不同检测波长下色谱峰容量差异,发现在242 nm条件下色谱峰信息较多,基线平稳,因此选择该波长为检测波长。并考察了不同流动相(甲醇-水溶液,乙腈-水溶液、乙腈-0.02%磷酸水溶液、乙腈-0.05%磷酸水溶液、乙腈-0.1%甲酸水溶液)、色谱柱(DIKMA Diamonsil spusil-C18、Thermo Accucore-C18、Thermo Hyperil GOLD-C18)、柱温(25 ℃、30 ℃)等,比较不同条件下色谱峰容量、峰形、响应值和分离度情况,确定其最优色谱条件,以全面反映红花龙胆指纹图谱中丰富的化学信息。此外,本实验对其提取方法(超声、回流、冷浸)、提取溶剂(水;50%、60%、70%、80%、90%、100%甲醇和乙醇)、提取溶剂比(1∶20、1∶30、1∶40、1∶50)、提取时间(15 min、30 min、45 min、60 min)及提取次数(1次、2次、3次)进行考察,除依据上述指标外,从节约能源及操作简单便捷考虑,最终确定提取溶剂比为1∶40,用70%甲醇溶液超声提取15 min,提取1次为本次实验的提取条件。
本实验采用相似度评价、聚类分析和主成分分析对11批红花龙胆样品指纹图谱进行综合分析,结果基本一致,建立了样品分类模型,S2和S11归为一类,S6单独分为一类,剩余8个批次的样品归为一类。结果表明红花龙胆药材的化学成分组成较为相似,但各批次之间成分的含量存在差异。所建立的红花龙胆指纹图谱分析方法重复性良好,可用于该药材的综合质量评价,指纹图谱结合有效成分的含量测定能够较为直观、准确地反映不同产地红花龙胆化学成分的变化情况,从整体上反映了该药材的质量,为红花龙胆药材综合质量控制和质量评价提供了理论依据。根据本文测定的不同产地红花龙胆中芒果苷含量和指纹图谱的结果,与相关文献报道的结果一致,环境因子可能是影响红花龙胆药材品质形成的主导因子,有待深入研究[14-17]。

