HS-SPME/GC-MS测定石榴酒中香气组分的条件优化
张云飞,李坚斌,2,*,魏群舒,黄嘉雯,方坤
(1.广西大学轻工与食品工程学院,广西南宁530004;2.广西蔗糖产业协同创新中心,广西南宁530004)
石榴是一种营养价值和保健价值都很高的水果,以石榴为原料酿制而成的果酒,保留了石榴特有的果香,是一种容易被人体吸收的保健酒。在发酵过程中,石榴酒挥发性成分发生变化,形成特有的香气。香气是用来鉴定酒类产品优劣的品质之一[1],气相-液相质谱联用已经广泛应用在酒类的香气成分分析检测[2-3]。分析酒类中的香气成分的主要步骤分别是样品制备和挥发性组分的提取、浓缩痕量挥发物、去除杂质并分离目标特定部分。提取浓缩挥发性香味物质的常用方法有液-液萃取[4],静态和动态顶空分析[5]和蒸馏/萃取[6-7]。将顶空固相微萃取(headspace solid-phase microextraction,HS-SPME)与气相质谱联用仪(gas chromatography-mass spectrometry,GC-MS)结合分析酒中的挥发性成分准确且快捷[8]。有许多学者也进行了相关的研究,Athanasios Mallouchos 等[9]采用 HP-SPME/GC-MS 研究了葡萄酒发酵过程中挥发物质的变化情况。Dimitra L.Capone 等[10]采用 HP-SPME/GC-MS 定量检测红葡萄酒与白葡萄酒中的1,8-桉叶素。Liang Chen 等[11]采用HP-SPME/GCMS 方法定性定量分析了葡萄酒中2-甲基-4-丙基-1,3-氧杂奶氧杂萘。但是采用HP-SPME/GCMS 方法分析石榴酒中的挥发性成分未见报道。
本文采用顶空固相微萃取与气质联用对石榴酒香气成分进行分析,研究SPME 不同参数(样品含量、纤维种类、萃取时间、萃取温度)对石榴酒香气组分的影响,选择最优参数以准确的对石榴酒香气成分进行定性定量分析。
1 材料与方法
1.1 材料
石榴酒:河阴软籽石榴农家自酿;NaCl(分析纯):天津市光复科技发展有限公司;正构烷烃(C7-C30)(色谱纯):美国 SUPELCO 公司;2-辛醇(色谱纯):美国Sigma-Aldrich 公司。
50/30 μm DVB/CAR/PDMS、65 μm PDMS/DVB 固相微萃取头及萃取手柄:美国Supelco 公司;GC-7890B/5977A 气相色谱-质谱联用仪:美国Agilent 公司;MR-Hei-Standard 磁力搅拌器:美国Heidolph 公司;TLE204E/02 电子天平:梅特勒-托利多仪器公司。
1.2 方法
SPME 萃取纤维的涂层包括聚二甲基硅氧烷(dimethicone,PDMS)、碳分子筛/聚二甲基硅氧烷(carbon molecular sieve/dimethicone,CAR/PDMS)、聚二甲基硅氧烷/二乙烯基苯(dimethicone/divinylbenzene,PDMS/DVB)、二乙烯基苯/碳分子筛/聚二甲基硅氧烷等(divinylbenzene/carbon molecular sieve/dimethicone,DVB/CAR/PDMS)。根据每种纤维涂层的厚度和涂层物质种类的不同,每种萃取头对挥发性物质的吸附和敏感性不同进行萃取。
1.2.1 萃取头的种类对酒样中化合物种类与含量分析结果的影响
将两组装有5.0 mL 石榴酒样品,0.750 0 g NaCl 的顶空瓶于40.0 ℃,转速为500 r/min 磁力搅拌器上平衡10 min,选取PDMS 萃取头和DVB/CAR/PDMS 萃取头活化后分别置于顶空瓶中萃取40 min。萃取结束后,将纤维缩回迅速注入气相色谱仪进样口,解析3 min 用于GC-MS 分析。
1.2.2 酒样的体积对酒样中化合物种类与含量分析结果的影响
分别将 3.0、4.0、5.0、6.0 、7.0 mL 酒样置于 5 个25 mL 的顶空瓶中,于40.0 ℃,转速为500 r/min 磁力搅拌器上平衡10 min,选取萃取头(1.2.1 优化后的萃取头)活化后于40 ℃萃取40 min。萃取结束后,将纤维缩回迅速注入气相色谱仪进样口,解析3 min 用于GC-MS 分析。
1.2.3 萃取的时间对酒样中化合物种类与含量分析结果的影响
将5 组装有一定量体积(1.2.2 优化后的体积)的石榴酒样品,0.750 0 g NaCl 的顶空瓶于40.0 ℃,转速为500 r/min 磁力搅拌器上平衡10 min,选取萃取头(1.2.1优化后的萃取头)活化后在40 ℃分别萃取20、30、40、50 min 和60 min。萃取结束后,将纤维缩回,迅速注入气相色谱仪进样口,解析3 min 用于GC-MS 分析。
1.2.4 萃取温度对酒样中化合物种类与含量分析结果的影响
将5 组装有一定量体积(1.2.2 优化后的体积)的石榴酒样品,0.750 0 g NaCl 的顶空瓶于40.0 ℃,转速为500 r/min+磁力搅拌器上平衡10 min,选取萃取头(1.2.1 优化后的萃取头) 活化后分别在 30.0、35.0、40.0、45.0 ℃和50.0 ℃条件下萃取一段时间(为1.2.3优化的时间)。萃取结束后,将纤维缩回迅速注入气相色谱仪进样口,解析3 min 用于GC-MS 分析。
1.2.5 GC-MS 测定条件
色谱条件:毛细管色谱柱Agilent DB-Wax(60 mm×0.25 mm×0.25 μm)分离挥发物;程序升温:初始温度40 ℃,保留 3 min,先以 4 ℃/min 的速率升至 120 ℃,再以 6 ℃/min 的速率升至 240 ℃,保持 3 min;进样口温度250 ℃;使用纯度为99.999%的氦气作为载气进行分析,柱流速为1.0 mL/min;采用不分流手动进样,进样量为1 μL。为消除上次进样残留对下次进样的影响,让气质联用仪在设定条件下运行一段时间,每次分析完样品都要进行空样分析以清洗萃取头和除去色谱柱中样品的残留。
质谱条件:进样口温度250 ℃;界面和离子源温度230 ℃;四级杆温度为 150 ℃;EI 电离源,电子能量70 eV,数据在35 amu~500 amu 扫描范围内收集。
1.2.6 图谱中物质的定性与定量
定性分析先通过搜索NIST 14 质谱数据库,再将碎裂模式与先前报道的一些文献进行比较,根据保留指数鉴定挥发性化合物。
保留指数的计算通过正构烷烃C7-C30 采用内插值法得到,计算公式如下:

式中:TR(x),TR(z),TR(z+1)分别代表组分,碳数为 Z,Z+1 正构烷的保留温度[12]。
采用内标法对香气成分进行半定量分析(假定校正因子为1),计算公式为:

式中:Xi为待测化合物的浓度;Ai为待测化合物的峰面积;As为内标2-辛醇的峰面积;Cs为石榴酒中添加的内标物质2-辛醇的浓度(浓度为0.82 mg/mL,添加量 6 μL)。
所有测定样品的GC-MS 总离子流图中2-辛醇的峰面积保持均一,以确保装置和方案稳定并且结果是可再现的。
1.2.7 HS-SPME 对石榴酒的重现性
选择优化的HS-SPME 条件,对石榴酒进行6 次重复性试验测定,内标试剂选择2-辛醇(浓度为0.82 mg/mL,添加量 6 μL)。
1.2.8 数据统计分析方法
所有试验均进行3 次平行测定,使用origin 8.0 进行数据处理。
2 结果与分析
2.1 HS-SPME条件的选择
2.1.1 萃取头的种类对酒样中化合物种类与含量分析结果的影响
GC-MS 离子色谱图见图1。
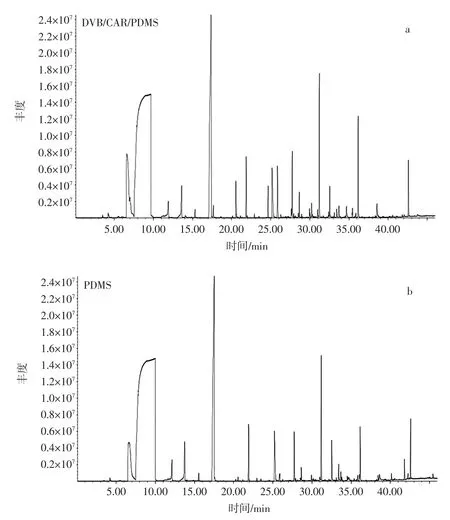
图1 不同萃取头萃取石榴酒中香气组分的GC-MS 图谱Fig.1 GC-MS spectra of aroma components extracted by different extraction fibers in pomegranate
如图1 b 所示,萃取头的纤维涂层使用PDMS 时,经GC-MS 可以检测出峰103 种,总峰面积为39.1×108。采用DVB/CAR/PDMS 纤维萃取头的结果如图1 a所示,共检测出峰140 个,总峰面积为277.4×108。从总峰面积和检测化合物的数量来看,采用DVB/CAR/PDMS 纤维萃取头更具有优势。这种材质的纤维是由3 种固定相(二乙烯基苯/碳分子筛/聚二甲基硅氧烷)组合而成,可以提取大量分子量为40~275 的挥发性和半挥发性化合物,为试验样品提供大多数挥发性化合物。这与刘敬科等[13],陈雨等[14]的研究结果一致。刘敬科等[10]在使用4 种萃取纤维分析小米黄酒中挥发性成分时发现DVB/CAR/PDMS 材质的萃取头对醛、酯等物质的吸收具有优良的效果。陈雨[14]在用不同的纤维萃取朗姆酒中的香气组分时,发现DVB/CAR/PDMS 材质的萃取头能检测出醇、酯、醛酮等不同种类的香气化合物,对朗姆酒中重要的香气组分(酯类)和高沸点物质的吸附能力也明显优于其他单组分材质的萃取头。因此,此种萃取头相较于其他单组分的纤维,不仅具有更广泛的吸收面,同时也具有较好的灵敏性和选择性,更适合酒类挥发性物质的吸附。
2.1.2 酒样的体积对酒样中化合物种类与含量分析结果的影响
萃取化合物峰面积和种类如图2 所示。
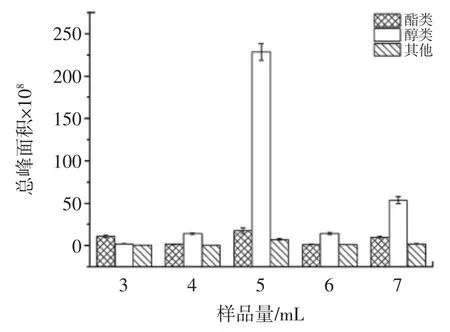
图2 不同的样品量对石榴酒中挥发性化合物的总峰面积和化合物数量的影响Fig.2 Effect of different sample sizes on total peak area and compound number of volatile compounds in pomegranate
当石榴酒样品量分别为 3、4、5 mL 时,SPME 萃取的挥发性化合物的峰面积分别为 13.7×108、16.4×108、253.1×108。随着顶空瓶中石榴酒体积的增多,峰面积逐渐增大。如亨利定律[15]预测的那样,顶空瓶中空气与水的比率对挥发物浓度起着重要作用。当空气与水的比例减小,浓度增加,GC-MS 出峰信号强度将增大。Alexandre Béné 等[16]通过试验数据图表证明了空气/水比例改变,测量的信号高度与宽度(峰面积)也随之改变,表明顶空瓶中的系统遵循亨利定律。然而,当瓶中体积由5 mL 继续增加到7 mL 时,SPME 的萃取纤维在吸附足够的化合物后达到一定的饱和,而顶空瓶中40 ℃的恒温使得解析速度增大,造成萃取纤维吸附的化合物减少,峰面积减少。由图2 看出当样品量低于或者超过5 mL 时,酯类和醇类物质的峰面积大小呈现先增加后减小变化,因此,选择5 mL 作为本试验所选的石榴酒样品量的优化结果。
2.1.3 萃取的时间对酒样中化合物种类与含量分析结果的影响
萃取时间是顶空瓶中液相和气相达到平衡的时间,由石榴酒的分配系数、扩散速率、样品基质、样品体积、萃取涂层厚度等因素决定[17]。所得萃取化合物的峰面积和萃取种类如图3 所示。
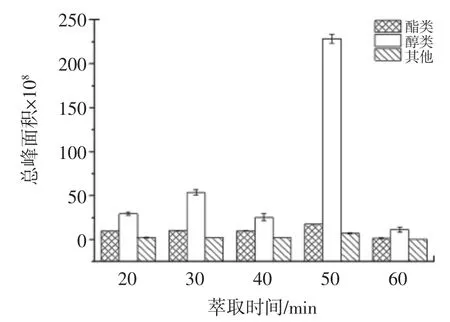
图3 不同的萃取时间对石榴酒中挥发性化合物的总峰面积和化合物数量的影响Fig.3 Effect of different extraction time on total peak area and compound number of volatile compounds in pomegranate
吸附是一个过程,短时间内由于顶空瓶中石榴酒挥发性物质的浓度较高,当萃取时间从20 min 到50 min增加时,导致萃取纤维对挥发性物质的吸附逐渐增多,峰面积增大,尤其是醇类物质的吸附显著增多,萃取时间达到60 min 时总峰面积却显著减少。一般纤维的吸附速度会随着顶空瓶中样品浓度的增大而增大,到达一定的时间后,吸附逐渐达到饱和,达到最大的吸附浓度。随着时间的继续延长,40 ℃的温度使得萃取纤维上吸附的物质的解析速度加快,使得吸附的醇类和酯类等物质减少,总峰面积也减少至13.6×108。这与张妮[18]在使用SPME 不同的萃取时间分析萃取樱桃酒所得到的规律基本一致。在此试验中选取萃取时间为50 min 为萃取时间的优化结果。
2.1.4 萃取温度对酒样中化合物种类与含量分析结果的影响
所得萃取化合物的峰面积和萃取种类如图4所示。
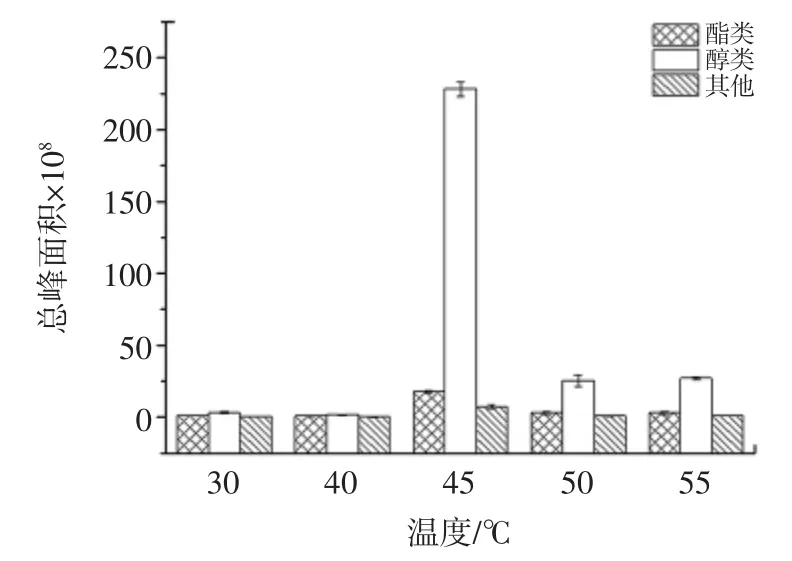
图4 不同的萃取温度对石榴酒中挥发性化合物的总峰面积和化合物数量的影响Fig.4 Effect of different extraction temperatures on total peak area and compound number of volatile compounds in pomegranate
如图4 所示,萃取温度从30.0 ℃到45.0 ℃,总峰面积随着萃取温度的升高先升高,温度的升高可以加速石榴酒中挥发性成分分子的运动,有利于化合物的挥发;当萃取温度从45.0 ℃继续升高至55.0 ℃时,峰面积随着萃取温度的升高而减小,这可能是因为纤维对不同挥发性化合物之间具有选择性,对化合物有不同的亲和力,而且在吸附的同时会发生解析现象,解析过程是一个吸热过程,解析的速率会随着温度的升高加快,当萃取纤维的解析速度大于吸附速度时,会使得萃取纤维吸附的化合物减少,峰面积就会减小;不但如此,温度过高也会使石榴酒中的物质发生变质。Sybille Merkle 等[19]也得出同样的结果,提高样品温度可以缩短提取时间,但过高的温度也会发生不良的化学反应反应。因此,萃取温度选择45.0 ℃更适合石榴酒中挥发性化合物的提取。
根据上述试验对萃取纤维、样品量、萃取时间、萃取温度的优化,选择DVB/CAR/PDMS(二乙烯基本/碳分子筛/聚二甲基硅氧烷)涂层的纤维进行萃取,测定的最适石榴酒样品量为取5.0 mL,萃取时间为50 min,萃取温度为45 ℃时,GC-MS 测定的石榴酒中的小分子物质种类较多。
2.2 HS-SPME的重现性
采用上述优化后的条件对石榴酒进行GC-MS 的6 次重复性测样,验证使用HS-SPME 的前处理方式对石榴酒中的香气化合物的重现性,并进行半定量分析,得出以下GC-MS 的色谱图见图5。
根据GC-MS 和RI 共同定性出57 种挥发性化合物,见表1。
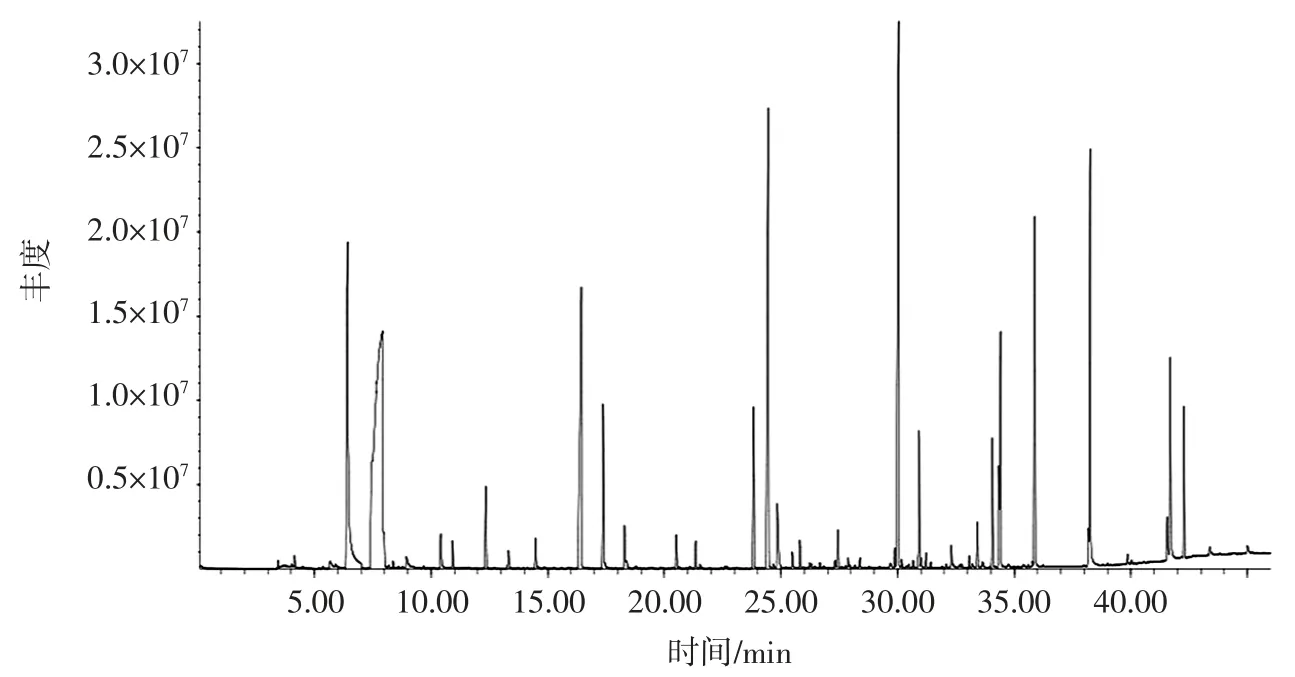
图5 优化后超声波条件的GC-MS 离子色谱图Fig.5 GC-MS ion chromatogram of optimized ultrasonic conditions
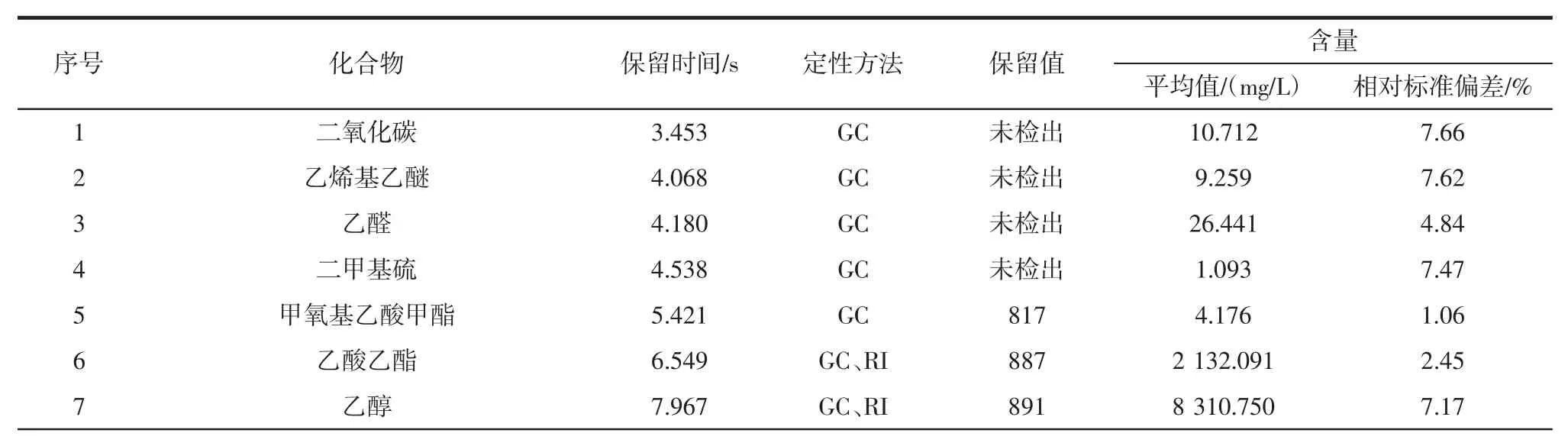
表1 石榴酒原样中香气成分定性结果及定性方法Table 1 Qualitative results and qualitative methods of aroma components in pomegranate wine
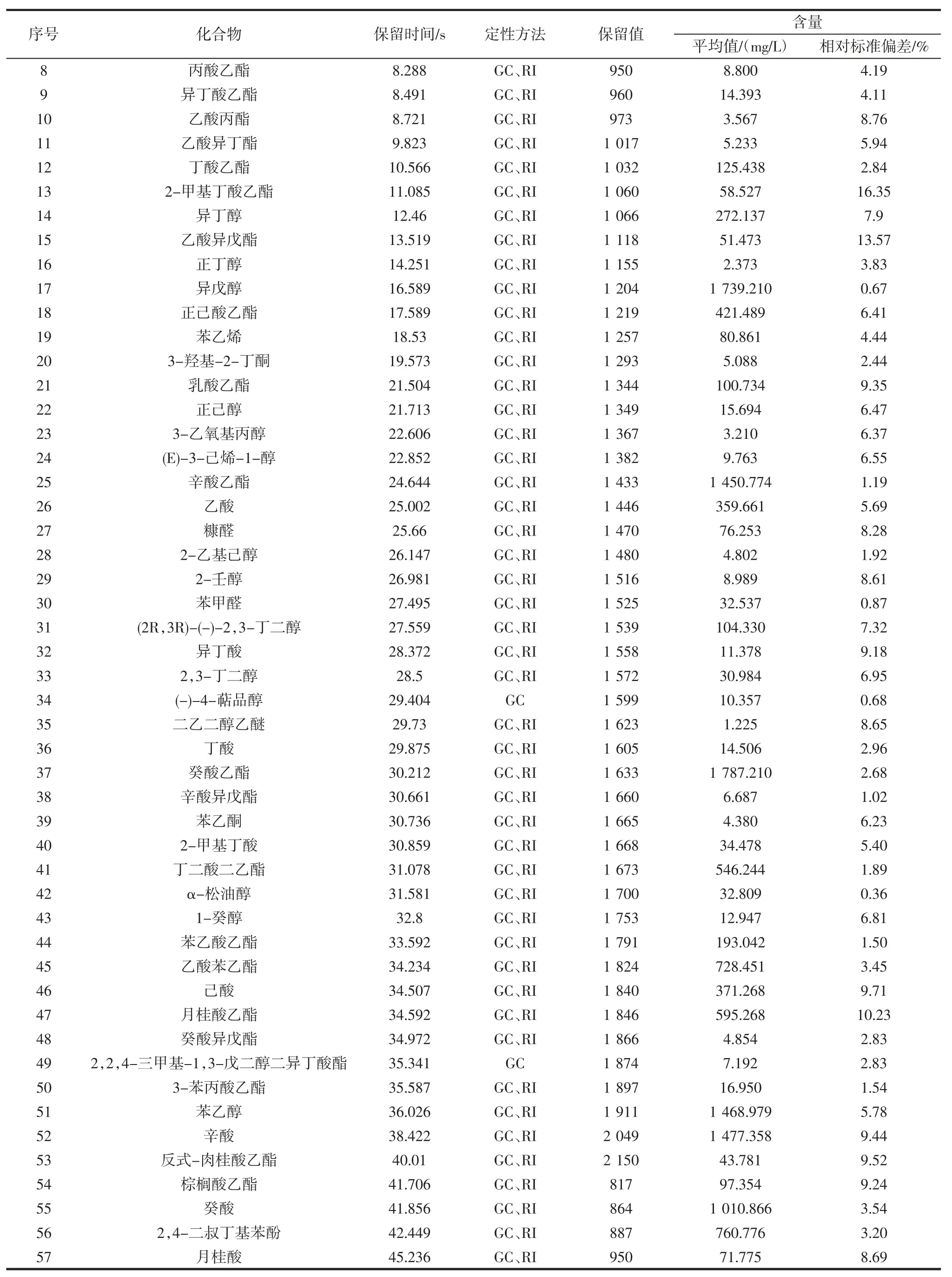
续表1 石榴酒原样中香气成分定性结果及定性方法Continue table 1 Qualitative results and qualitative methods of aroma components in pomegranate wine
由表1 可知,酯类共20 种,主要包括丁酸乙酯、2-甲基丁酸乙酯、乙酸异戊酯、正己酸乙酯、乳酸乙酯、辛酸乙酯、癸酸乙酯、丁二酸二乙酯、月桂酸乙酯、反式-肉桂酸乙酯、棕榈酸乙酯等;醇类14 种,包括乙醇、异丁醇、异戊醇、(2R,3R)-(-)-2,3-丁二醇等;酸类 8种,包括乙酸、己酸、辛酸、癸酸、月桂酸等;芳香族化合物7 种包括苯乙烯、苯甲醛、苯乙酮、苯乙酸乙酯、乙酸苯乙酯、苯乙醇,3-苯丙酸乙酯;醛酮类化合物3 种,包括乙醛、3-羟基-2-丁酮、糠醛;其他包含醚类,硫类,酚类共5 种,包括2,4-二叔丁基苯酚等。可以看出,石榴酒中的香气化合物主要是酯类、醇类、酸类、芳香族化合物和醛酮类物质。
其中,酯类化合物是种类和含量最多的一类香气化合物,是石榴酒中的呈香气味化合物之一。乙酸乙酯(2 132.091 mg/L)、辛酸乙酯(1 450.774 mg/L)、癸酸乙酯(1 787.210 mg/L)含量最高,尤其是辛酸乙酯(果香味)和癸酸乙酯(果香味),是石榴酒中的特征香气化合物,为石榴酒提供特定的石榴香味[20]。根据对每种化合物的相对标准偏差可以看出HS-SPME 的重现性良好。
3 结论
本文通过比较2 种萃取纤维PDMS(聚二甲基硅氧烷)、DVB/CAR/PDMS(二乙烯基苯/碳分子筛/聚二甲基硅氧烷)萃取化合物种类和峰面积,最后选取DVB/CAR/PDMS 作为萃取材质,此萃取纤维是3 种固定相组合而成的材料,对多数的挥发性化合物有较敏感的响应。通过比较不同样品量对石榴酒中香气化合物的分析,选择分析的样品量为5.0 mL,选择萃取时间为50 min,萃取温度为45.0 ℃,在最优条件下,选取DVB/CAR/PDMS 材质萃取纤维,移取 5 mL 石榴酒,在 45.0 ℃萃取50 min,进行GC-MS 分析,定性出57 中化合物,包括酯类、醇类、酸类、芳香族化合物等,且重现性良好。

