对氯甲苯选择性氧化制备对氯苯甲醛
魏世明,胡家明,薛 艺,张 锋
南京大学化学化工学院,江苏 南京 210023
对氯苯甲醛(PCAD)是一种广泛应用于医药、农药行业的有机中间体[1-2],如何高效、便捷地生产PCAD 是化工行业中亟需解决的问题之一。国内生产PCAD 的方法主要是氯化水解法[3-4],该方法对设备要求较高,并且在反应过程中会产生大量的废酸、废水危害环境。对氯甲苯(PCT)选择性氧化可生产PCAD,其原料易得,原子经济性高[5-6],若是能找到合适的氧化剂及催化剂,可以减少三废的产生甚至不产生三废。然而PCT 的氧化反应是一串联反应,采用MC 催化剂(Co/Mn/Br 复合催化剂,Mid-Century)和传统工艺条件,PCT 的氧化产物主要为氯代苯甲酸(PCA),并不会停留在中间产物PCAD 的阶段[7],PCAD 在常温下也会自动氧化为PCA,传统的高温氧化工艺会加速该过程,难以达到较高的选择性和收率,同时会产生少量对氯苯甲酸乙酯(PCE)。HU 等[6]应用乙酸-水体系制备PCAD,选择性72.4%,收率只有14.3%;蔡敏敏等[5]研究了Co/Mn/Br 催化体系下PCT 的空气/氧气氧化,最高收率只有19.6%。因此,寻找合适的氧化剂、催化剂、溶剂以及可以稳定PCAD 不继续氧化的助催化剂至关重要。
H2O2氧化剂虽然在三废控制方面有着得天独厚的优势,但低浓度的H2O2溶液氧化能力不足以进行反应,高浓度的H2O2溶液在工业使用中较为危险,同时储存和运输也存在着风险[8]。空气/氧气氧化因为其廉价易得、安全的优点在化工生产中经常使用,在该反应中,分子氧作为氧化剂也有着不会产生多余的废物的优点。在催化剂的选择上,各种分子筛被制备用以PCT 的选择性氧化[9-11],但在工业上的应用还未成熟;MC 催化剂已经在芳烃氧化方向实现了工业上成熟的应用[7-12]。因此,如果在MC 催化剂的基础上找到合适的溶剂和助催化剂来提高PCAD 的选择性,将会有着重要的实用价值。本工作以此为出发点,寻找合适的溶剂和助催化剂、反应条件以高效制备PCAD,并对产物和原料分离的过程进行设计,以期对实际工业生产PCAD 提供参考。
1 实验部分
在装有冷凝回流装置的250 mL 烧瓶中依次加入醋酸钴、硫酸锰、溴化钾、助催化剂、醋酸和PCT,开启搅拌,升温至反应温度后通入氧气,按一定的时间周期取样,反应瓶中析出大量白色晶体时停止通入氧气,关闭加热,停止反应。反应结束后减压蒸馏(真空度0.09 MPa),在80 ℃下馏出醋酸,100 ℃下馏出未反应的PCT,醋酸和PCT 可循环利用。150 ℃下即可馏出反应产物PCAD(结晶在冷凝管中),无馏分蒸出时停止蒸馏,冷却后用热水溶解剩余反应底物,过滤得到的对氯苯甲酸粗品可通过碱水溶解再调酸的方式精制,溶液蒸干得到催化剂可回收再次使用。
样品用乙醇直接稀释后使用岛津GC-2014C 型气相色谱仪分析。30 m×0.32 m×0.5 μm WondaCap毛细管柱,氢火焰(FID)检测器,载气N2流量为 30 mL/min,H2为 40 mL/min,空气为400 mL/min,汽化室和检测器温度均为300 ℃,进样量为0.1 μL。采用程序升温:初始温度80 °C,保持1 min,以20 °C/min 的速率升至150 °C,保持l min;以20 °C/min 的速率升至280 °C,保持3 min。采用面积归一法进行定量分析。氧化产物用GCMS-QP2020 NX 型气相色谱质谱联用仪定性。图1 为典型的色谱分析结果。
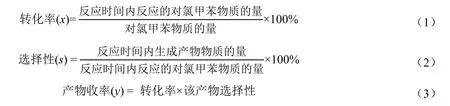
反应的转化率、收率和选择性定义如下:
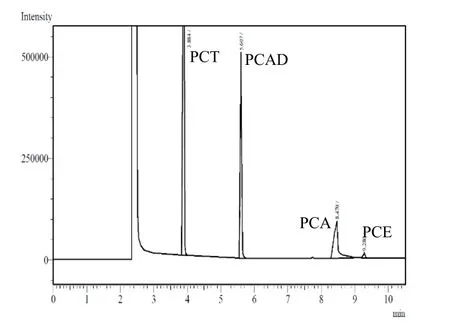
图1 氧化产物气相色谱Fig.1 GC of oxidation products
2 反应条件优化
2.1 溶剂的选择
乙酸是目前钴盐类催化剂选择性氧化甲苯类物质制备醛类最常用的溶剂。对于PCT 的氧化,无溶剂时,由于催化剂不溶于反应底物之中,在较高的温度和较长的反应时间下,对氯甲苯的转化率依然很低(不到1%)。除乙酸(沸点117.9 ℃)以外,其它能够溶解钴盐催化剂的有机溶剂都存在着沸点不合适的问题,如乙腈沸点太低(81.6 ℃)达不到反应所需的温度,二甲亚砜(沸点189 ℃)等高沸点溶剂因为沸点太高不适用于后续的分离,所以选择乙酸作为PCT 氧化反应溶剂。
2.2 溶剂用量的影响
在反应温度为90 ℃,催化剂用量为反应底物质量的3%,钴锰质量比为2:1 的条件下[5],不同溶剂用量时PCT 选择性氧化反应结果如图2。可以看出,反应底物和溶剂的体积比(溶剂比)为1:1 时,PCAD 收率在反应2 h 达到顶峰后即开始下降,说明在转化率不断攀升的同时选择性在迅速下降,反应3 h 后选择性只有58.75%。而溶剂比为1:3 时,反应3 h 后选择性有85.13%,增加溶剂的量可将PCAD 收率达到顶峰的时间推后,但溶剂量过多会导致反应时间增长,能耗增高,不利于工业应用。反应结果在溶剂比为1:1.5 与1:2 时较好,比较这两组实验数据可知,PCAD 收率存在一个平台期,是转化率升高与选择性下降共同造成的结果,平台期过后选择性下降幅度过大导致收率下降。综合来看,溶剂比为1:2 时反应效果最佳,PCAD 收率在反应时长3~4.5 h 内稳定在19%~20%。

图2 不同溶剂比下PCAD 收率随时间的变化Fig.2 PCAD yield vs time under different solvent ratios
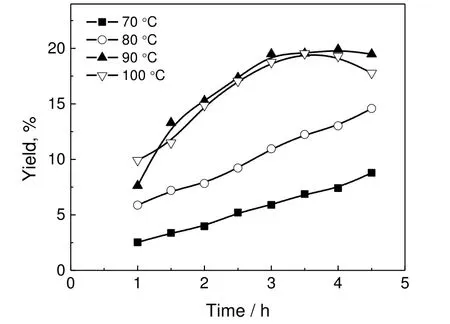
图3 不同温度下PCAD 收率随时间的变化Fig.3 PCAD yield vs time under different temperatures
2.3 温度的影响
在溶剂比为1:2,催化剂用量为3%,钴锰比为2:1 的条件下,温度对PCT 选择性氧化反应的影响如图3。由图3 可知,反应温度较低时,PCT 氧化生成PCAD 的反应较难进行,PCAD 收率随时间增长的变化较小。温度升高后,反应速率加快,转化率明显增长带来收率的提高,而当反应温度达到100 ℃时,PCAD 收率在反应时长3.5 h 达到顶峰后迅速下降,可知高温对PCAD 过度氧化为PCA 的反应有利。综合来看,以反应温度在90 ℃为宜。
2.4 催化剂用量的影响
在溶剂比为1:2,钴锰比为2:1,反应温度为90 ℃,反应时长为4 h 的条件下,考察复合催化剂的用量对PCT 选择性氧化反应的影响结果如图4 所示。催化剂用量较低时,反应难以进行,随着催化剂用量的增加,反应速度加快,转化率不断增长,PCAD 收率开始上升,但是当催化剂用量达到3%时,再增加催化剂的用量,转化率增长较少,且PCAD 的收率变化不明显。由于工业生产中,应尽量避免生成副产物,且催化剂需要回收利用,因此催化剂的用量以原料质量的3%最佳。
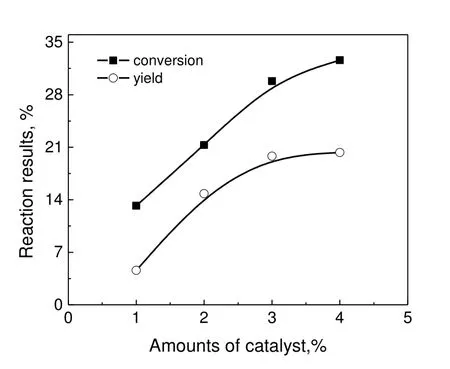
图4 不同催化剂用量所得转化率和收率Fig.4 Yields and conversions obtained with different amounts of catalyst
2.5 助催化剂的影响
为提高PCAD 选择性和收率,对助催化剂的种类进行筛选。在溶剂比为1:2,钴锰比为2:1,反应温度为90 ℃,助催化剂用量为1.25%,反应时长为3 h 的条件下,考察助催化剂对PCT 氧化反应的影响结果列于表1。由表1 可知,助催化剂的加入可以显著提高PCT 的转化率,而PCAD 的选择性并无较大下降,由此得到较高PCAD 收率。三种助催化剂中,FeCl3的效果最好,反应3 h,PCAD 收率可达20.42%。

表1 助催化剂对PCT 选择性氧化的影响Table 1 The effect of co-catalyst on selective oxidation of PCT
2.6 正交实验
为进一步明确反应转化率和PCAD 选择性的影响因素,分別采用醋酸作溶剂,醋酸钴、硫酸锰、溴化钾为催化剂,氯化铁为助催化剂,以溶剂用量、催化剂用量、各催化剂配比(质量比)、助催化剂用量(反应底物的质量分数)、反应温度为参数,设计五因素四水平正交实验。实验结果列于表2。
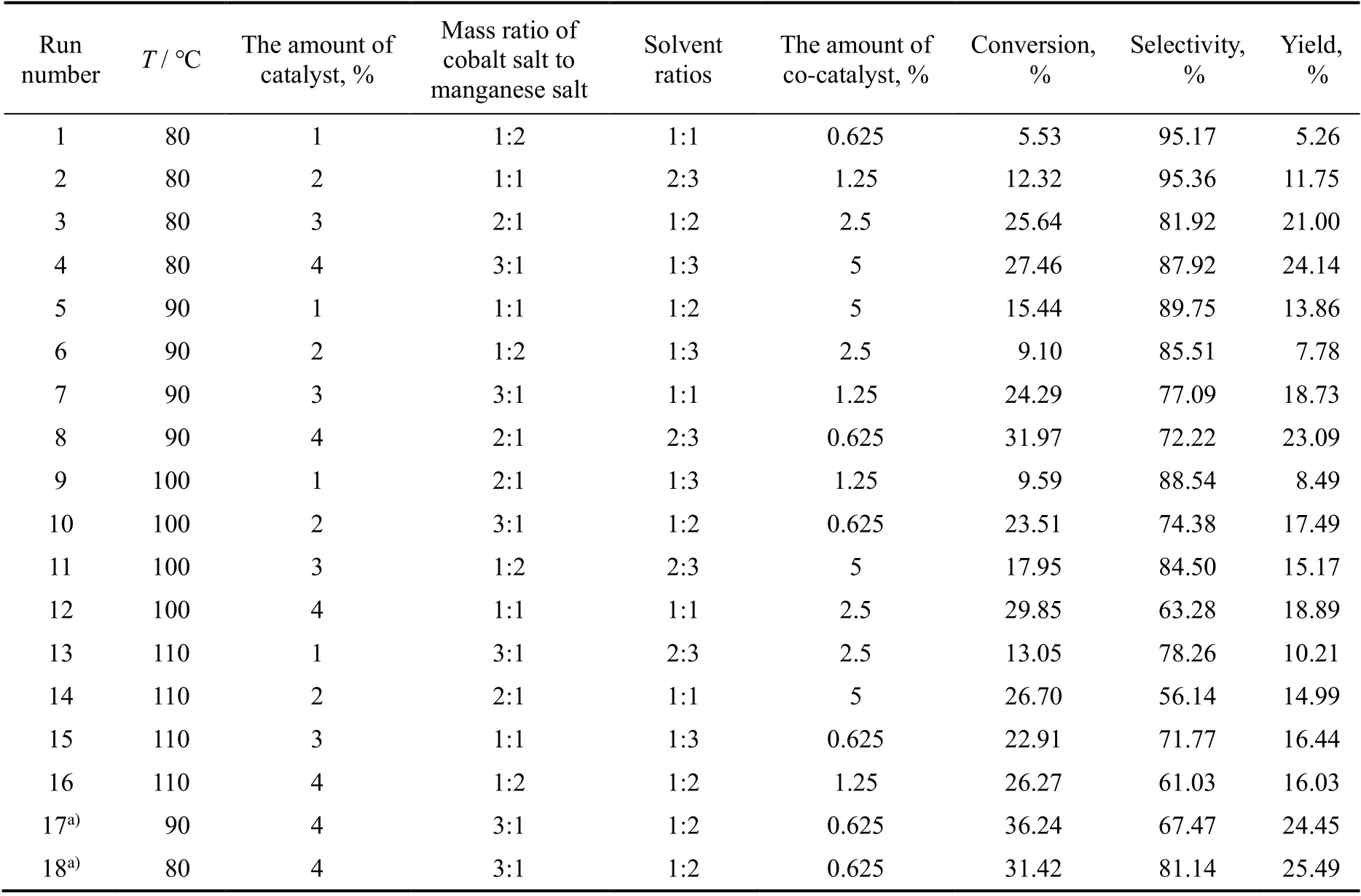
表2 PCT 选择性氧化正交实验结果Table 2 PCT selective oxidation Orthogonal experimental results
分析正交实验结果可知,最适宜该反应的温度为90 ℃,而80 ℃的结果与其相差不大,并且低温对PCAD 的选择性有利;最适宜的催化剂用量为4%,原因是催化剂用量增加可使反应加快进行,在PCAD 的生成速度加快而氧化为PCA 的速率还未爆发时达到PCAD 收率的顶点;最适宜的钴锰比为3:1,可见在该反应中主要催化剂为钴盐,而锰盐在反应过程中起着辅助钴离子价态转变的作用,用量过多则会抑制催化效果;最适宜的溶剂比为1:2,原因在于溶剂对生成的PCAD 有一定的保护作用,减缓链式反应的速度,因此得到PCAD 的高选择性,但过多的溶剂会导致反应变慢,PCT 转化率较低;最适宜的助催化剂用量为0.625%,助催化剂的加入有助于提高PCAD 的选择性和收率。
2.7 反应条件对耐受比的影响
分析反应数据可知,PCAD 的选择性于某一时间点开始迅速下降从而导致PCAD 的收率由上升转为下降,继续进行反应时,收率继续降低,因此最佳反应时间即可用该时间点来指示。为对该时间点进行预测,将体系中PCAD 选择性发生突变时PCT 与PCAD 的浓度之比称为耐受比(tolerance),进行数据分析与重复实验发现该值在相同反应条件下基本为一定值,具有较好的重复性。数据结果列于表3。
由表4 可知,耐受比与PCAD 收率有明显的相关性,第1,2 和3 组实验为单因素实验,耐受比的变化较小,导致PCAD 收率变化不大,而第4 和5 组实验,通过助催化剂的加入以及正交实验筛选优化反应条件,耐受比从4.5 左右降低至3 左右,使PCAD 过度氧化的时间推迟,从而提高PCAD 收率。降低耐受比是提高收率的关键(将PCAD 稳定在较高的水平同时提高PCT 的转化率),这意味着在未来的工作中可以通过加入溶剂或惰性添加剂将PCAD 稳定或者加快PCT 转化到PCAD 的反应速率这两种方式改进该反应。
3 反应动力学
为指导PCT 选择性氧化制备PCAD 的工业应用,方便反应器的设计制造,必须对该反应进行动力学研究,确定反应动力学常数。取样分析发现,除原料PCT、主要产物PCAD、过度氧化产物PCA之外,其它副产物的浓度很低,均在1%以下。因此,PCT 液相氧化反应可看作生成PCAD,然后生成PCA 的连串反应。

假定两步反应均为一级反应,则三种物质的动力学微分方程为:

式中:CA,CB和CC分别为PCT,PCAD 和PCA 的浓度,mol/L;t 为反应时间,h。若PCT 的初始浓度为CA0,积分可得式(8):

在催化剂用量3%,溶剂比为1:2,钴锰比为2:1,不添加助催化剂的条件下,不同温度下的反应结果如图5 所示。因为反应在达到耐受比后PCA 浓度迅速上升,耐受比前后反应动力学常数应是不同的,所以此处只模拟了耐受比之前的反应过程。

图5 不同反应温度下各物质浓度变化Fig.5 The concentration of each substance changes when the reaction temperature
用式(8)对图5 中CA的实验数据进行拟合,由直线的斜率得到k1,不同温度下的结果见图6。
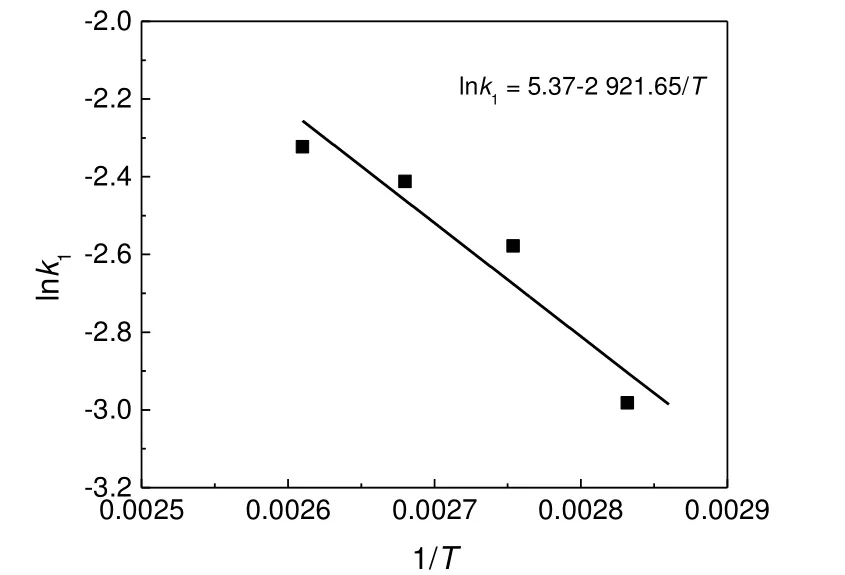
图6 lnk1 与T-1 的关系Fig.6 The relationship between lnk1 and T-1
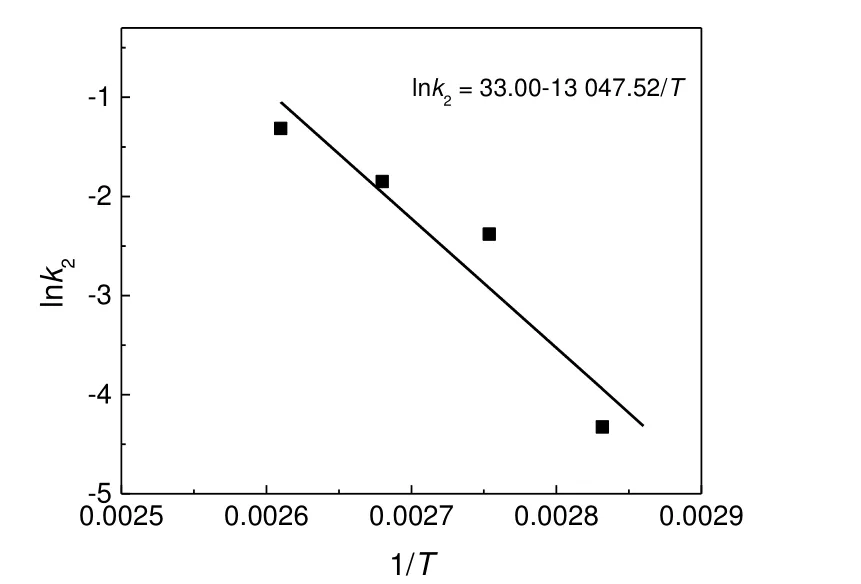
图7 lnk2 与T-1 的关系Fig.7 The relationship between lnk2 and T-1
由式(7)积分可得:

根据Arrhenius 公式:lnk = -Ea/RT+lnk0,对图6 和图7 进行拟合,其斜率为-Ea/R,由此可得反应的活化能Ea1为24.29 kJ/mol,Ea2为108.5 kJ/mol。
将拟合得到的不同温度下的反应速率常数代入动力学方程式(5)~式(8),可计算得到该温度下各组分的浓度,计算得到的浓度也示于图5。从图5 可以看出,拟合数据与实验数据较为符合,实验数据中PCA 的浓度在反应的最后都会明显偏离预期,原因即是反应达到耐受比时反应动力学常数发生变化。另外,从图中也可以看出高温对PCAD 氧化为PCA 的反应有利,且高温会导致反应达到耐受比的时间缩短。
4 结 论
采用醋酸钴、硫酸锰、溴化钾复合催化剂,醋酸为溶剂,考察了溶剂用量、温度、催化剂用量对PCT 氧化反应的影响,然后以温度、催化剂用量、催化剂配比、溶剂用量、助催化剂用量设计五因素四水平正交实验,得出的较佳条件为:反应温度为80 ℃,催化剂用量为PCT 质量的4%,钴盐和锰盐质量比为3:1,PCT 和醋酸之比为1:2,助催化剂用量为PCT 质量的0.625%,在该条件下PCT 转化率可达31.42%,PCAD 的选择性可达81.14%。基于动力学计算可知,PCT 氧化生成PCAD 的反应活化能为24.29 kJ/mol,PCAD 氧化生成PCA 的反应活化能为108.5 kJ/mol。

