液相色谱法测定注射用盐酸博来霉素组分
陆常辉,桂王艳
(1.瀚晖制药有限公司,浙江 杭州 310020;2.浙江海正药业股份有限公司药品研发QC,浙江 杭州 311404)
博来霉素为发酵来源的糖肽类抗肿瘤抗生素类药物,适用于皮肤癌、头颈部癌(上颌窦癌、咽部癌、唇癌等)、肺癌(特别是原发和转移性磷癌)、食道癌等的治疗[1]。博来霉素为多组分药物,因此组分是药品质量控制中重要的项目之一。本文参考相关文献,建立了比各药典标准更优的博来霉素组分检查方法。方法经验证,专属性、线性、精密度和准确度等均符合要求,可保证组分检查结果的准确性。
1 仪器与试药
岛津LC-20AD高效液相色谱仪,软件LabSolutions色谱工作站;安捷伦1269高效液相色谱仪,软件OpenLab色谱工作站;S220型pH计(METTLER TOLEDO公司),XP26型电子分析天平(METTLER TOLEDO公司)。
注射用盐酸博来霉素(浙江海正药业股份有限公司,批号20BH03010、20BH03011、20BH03012);甲醇和乙腈均为色谱纯,己烷磺酸钠为高效液相色谱专用试剂,乙二胺四乙酸二钠和氨水为分析纯,水为纯化水。
2 实验方法
2.1 色谱条件
色谱柱:Agilent SB-C18(4.6mm×150mm,3.5µm);以己烷磺酸钠溶液(取己烷磺酸钠4.7g与乙二胺四醋酸二钠1.86g,加0.08mol/L醋酸溶液使溶解并稀释至1000ml,用氨溶液调节pH值至4.3)为流动相A;甲醇:乙腈(70:30)为流动相B;按表1线性梯度洗脱;柱温为35℃;流速为每分钟1.0ml;检测波长为254nm;进样量10µl。

表1 梯度洗脱程序
2.2 系统适用性
取本品适量,加水制成每1ml约含2500博来霉素单位的溶液,量取10µl注入液相色谱仪,按表1进行梯度洗脱。色谱图中两个主组分峰与各自相邻杂质峰的分离度不小于1.0;理论塔板数按博来霉素A2峰计算,应不低于8000。
2.3 组分测定
取本品,加水制成每1ml约含2500博来霉素单位的溶液,摇匀,精密量取10μl注入液相色谱仪,记录色谱图;按峰面积归一化法计算博来霉素A2,博来霉素B2,博来霉素B4,去甲基博来霉素A2,去甲基博来霉素A2外其他杂质之和。
3 方法学研究
3.1 专属性考察
分别在1.10W/m2强光,0.5N盐酸溶液,0.01N氢氧化钠溶液,5%过氧化氢溶液,以及在40℃、75%RH条件下对样品进行降解。进样测试。
降解幅度最大的热降解条件下样品色谱图见图1,在拟定的色谱条件下,博来霉素的各组分及杂质均能有效分离,方法专属性良好。
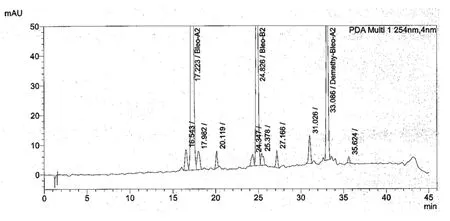
图1 热降解样品溶液典型图谱
3.2 检测限和定量限
此色谱条件下,博来霉素的检测限为0.222 μg/ml,定量限为0.739 μg/ml;去甲基博来霉素A2的检测限为0.242 μg/ml,定量限为0.805 μg/ml;博来霉素B4的检测限为0.227 μg/ml,定量限为0.757 μg/ml。
3.3 线性
配制线性梯度溶液,进样检测,博来霉素A2+博来霉素B2在定量限至2mg/ml范围内呈良好线性,线性方程为y=4.9444x-2.7221(R2=1.0000);去甲基博来霉素A2在0.8 μg/ml~128 μg/ml内呈良好线性,线性方程为y=4.5821x-0.8333(R2=1.0000);博来霉素B4在0.75 μg/ml~30 μg/ml呈良好线性,线性方程为y=3.2560x-0.1221(R2=1.0000)。
3.4 准确度
将已知量的组分加入博来霉素中,再按面积归一化法测定各自的量并计算回收率。结果表明在8.051μg/ml~120.770μg/ml的加样范围内,去甲基博来霉素A2的回收率范围为92.5%~96.1%;在0.750μg/ml~30.019μg/ml的加样范围内,去博来霉素B4的回收率范围为96.4%~103.4%;在8.051μg/ml~120.770μg/ml的加样范围内,去甲基博来霉素A2的回收率范围为92.5%~96.1%;
3.5 精密度
重复性:配制6份加入杂质的供试品溶液,测定组分及杂质。结果显示6份样品溶液中博来霉素A2、博来霉素B2和博来霉素A2+博来霉素B2的RSD小于0.1%,其他总杂质的RSD小于3.2%,重复性符合要求;
中间精密度:在不同HPLC系统、不同批次的色谱柱,不同实验人员及不同日期检测重复性同批次样品。并将结果于与重复性实验对比,博来霉素A2、博来霉素B2及两者的加和的差值在0.1%~0.2%之间。去甲基博来霉素A2、博来霉素B4,及除以上杂质外的其他杂质的和的差值不超过0.06%。证明方法具有良好的中间精密度。
4 组分测定结果
采用以上方法测定海正药业的三批注射用盐酸博来霉素,博来霉素A2与博来霉素B2的和分别为95%、96%、95%;博来霉素B4均小于1%;去甲基博来霉素A2分别为1.0%、0.9%和1.2%;去甲基博来霉素A2外其他杂质之和分别为3.6%、3.4%、3.7%。
5 讨 论
对比本方法与现行版美国药典[2]、英国药典[3]和日本药典[4]收载的博来霉素相关组分方法,本方法能检测出更多的杂质,有利于产品的质量控制。对比结果详见表2。

表2 不同方法组分检测结果对比

