危重症体外循环心脏手术中转体外膜氧合辅助的配合
张艳,孙敏,安乐,程亮,刘金成,金振晓,金艳
危重症心脏病患者拟行心肺转流(cardiopulmonary bypass,CPB)心脏手术患者,由于术前心功能较差,手术后即刻心脏功能难以保证循环状态,从而难以撤离CPB辅助,而CPB辅助时间的延长会进一步增加血细胞损伤,加重炎症反应,导致患者预后更差[1-3]。
体外膜氧合(extracorporeal membrane oxygenation,ECMO)技术能够提供更长时的循环呼吸辅助功能,对于CPB术后难以撤离的患者,中转ECMO辅助可以获得相对长时的呼吸循环辅助,而争取患者自身心肺功能恢复的时间[4-7]。
对于危重症心脏手术患者进行循环辅助,特别是在术中中转ECMO时的快速介入、置管操作、评估、术后转运对手术配合工作都不同于以往的常规手术[8-10],对其配合工作提出了更高的要求。对危重症患者CPB手术前做好充分的术前准备和评估,并结合危重症患者术前情况做好ECMO辅助各项护理预案,有助于缩短术中ECMO介入所需时间,可能降低术后感染等并发症发生率,与患者预后转归有着密切关系。因此,本研究旨在探讨配合预案对危重症CPB心脏手术患者术中中转ECMO辅助的预后影响及配合要点。
1 资料与方法
1.1 患者资料2016 年1月至2018年12月,18例危重症患者接受CPB心脏手术在术中中转ECMO辅助。其中男性12例,女性6例,年龄(58.7±6.2)岁,体重(62.5±7.4)kg。术前诊断包括:退行性瓣膜病4 例,风湿性瓣膜病7例,冠状动脉粥样硬化性心脏病5例,A型主动脉夹层2例。术前有双下肢水肿、胸腔积液、食纳差、不能平卧等严重心功能不全病史者12例,伴肺动脉高压11例,合并Ⅱ型糖尿病3例。术前NYHA Ⅲ级10例,NYHAⅣ级6 例。所有患者术前均行经胸超声及CT 血管成像(CT angiography,CTA)检查或冠状动脉造影明确诊断。术前常规经强心利尿等纠正心功能治疗,术前左室射血分数(left ventricular ejection fraction,LVEF)32%~65%。所有患者均在手术中完成心内操作后自身血压心脏收缩不能维持时行CPB中转ECMO辅助循环。回顾患者诊疗资料,根据术前是否做好中转ECMO的预案,将患者分为预案组(n =8)和非预案组(n =10)。见表1。
1.2 手术操作及方法
1.2.1 预案组针对术前评估较为危重、手术风险高的患者,预计术中可能中转ECMO辅助。术前即按ECMO中转准备,标记双侧股动静脉位置。消毒双侧腹股沟,铺巾预留双侧腹股沟切口位置,手术贴膜覆盖备用。术前耗材准备根据患者身高、体重、股动静脉直径选取股动静脉插管备用,并备好腹股沟切开器械。ECMO设备术前常规检查,装机干备不预充,准备好预充液,准备术中用血,并通知ECMO辅助团队待命。准备患者术后转运用便携呼吸机、氧气瓶及ECMO转运平车。术中常规建立CPB完成相应心内操作,心内操作结束,心脏复跳后常规评估CPB撤机可能,减流量试停机。当循环难以维持时,CPB辅助下切开一侧腹股沟显露股动、静脉,缝置股动、静脉荷包,直视下穿刺,导丝引导下置入股动、静脉插管,同时立即预充ECMO管路。连接ECMO管路后,启动ECMO辅助并停止CPB转流。ECMO辅助下,止血关胸,患者转入重症监护室。
1.2.2 非预案组非预案组患者术前均为常规手术准备。主动脉夹层患者术中直接股动、静脉转流,其余患者均为常规经胸插管转流方式,术前常规准备腹股沟区域消毒。术前不准备ECMO相关耗材及腹股沟切开器械。术中常规正中开胸建立CPB完成心内相应手术操作,心内操作结束,心脏复跳后CPB难以撤离,经评估后中转ECMO。在CPB辅助下进行ECMO中转准备,撤下肢区域铺巾,消毒腹股沟区域,重新铺巾,切开一侧腹股沟显露股动、静脉,缝置股动、静脉荷包,直视下穿刺,导丝引导下置入股动、静脉插管。同时联系ECMO辅助团队迅速就位,检查设备耗材,立即预充,并连接台上管路,启动ECMO辅助后停止CPB转流。余同预案组。
1.2.3 静脉-动脉(veno-arterial,V-A)ECMO中转指征CPB停机后,在使用两种及以上的正性肌力药物平均动脉压小于60 mm Hg;经食管超声心动图(TEE)提示心内畸形矫治后,LVEF<30%;CPB再次转机;在较大量正性肌力药物使用的情况下,仍有顽固性的休克,射血分数降低,心排指数<2 L/(m2·min);或伴有恶性心律失常。以上情况导致难以撤离CPB患者。
1.2.4 ECMO建立本组患者术中均中转为V-A ECMO辅助。V-A ECMO置管方法:行左/右一侧腹股沟下一横指3~5 cm切口,逐层切开皮下组织,股动脉鞘,显露股动静脉2 cm,6-0无损伤缝合线分别在股动静脉缝置5 mm 直径圆形荷包。直视下穿刺并置入0.035超滑泥鳅导丝,导丝引导下置入股动静脉插管,连接ECMO管路开始转流辅助。ECMO辅助系统由Delta 泵(对角线泵Medos)、涂层膜式氧合器(Medtronic)、17 ~19 Fr 涂层股动脉插管(Medtronic)、21~23 Fr 涂层股静脉插管(Medtronic)组成。
1.3 数据采集回顾患者住院资料,记录收集患者术前、术中、术后相关临床数据,术前B超、CTA检查结果、术中及术后ECMO转流相关数据,手术方式、术中B超监测数据、手术时间、ICU停留时间、住院时间等。
1.4 统计方法运用SPSS 18.0及GraphPad Prism8.0软件进行统计分析,计量数据若是正态分布,以均数±标准差(±s)表示,若不是正态分布,以中位数(四分位数间距)[P50(P25,P75)]表示,计数资料以率(%)表示;所有数据经方差齐性检验后采用单因素方差分析、t检验或非参数检验,计数资料采用Fisher's精确检验。以P<0.05判断差异有无显著性
2 结果
2.1 总体临床结果本研究纳入18例患者,顺利脱机12 例(66.7%),患者院内死亡6例,死亡率33.3%,死亡率明显高于常规手术。其中,预案组脱机成功6例,院内死亡2例。非预案组脱机成功6例,院内死亡4例。
2.2 ECMO中转两组预后分析ECMO中转预案组与非预案组比较,术中建立ECMO所需时间较短、总手术时间较短、术中出血量及输血量较少。转入ICU后,呼吸机辅助时间、ICU时间、术后住院时间两组均无显著差异。见表2。
2.3 院内感染情况本组患者术后均行血培养监测。有发热症状、呼吸道症状、血常规白细胞分类计数明显增高者复查血培养、咽拭子、痰培养。院内感染5/18例,发生率27.8%。细菌培养结果显示,血培养阳性5例。其中,预案组1例,为鲍曼不动杆菌。非预案组4例,分别为鲍曼不动杆菌1例,屎肠球菌1例,金黄色葡萄球菌1例,表皮葡萄球菌1例。术后常规预防性应用抗生素3 ~6 d,血培养阳性者,根据药敏结果,选用敏感抗生素。非预案组术后院内感染例数较多,但与预案组比较,术后院内感染发生率两组未见显著统计学差异(P=0.3137)。
表1术中中转ECMO患者术前资料(s)
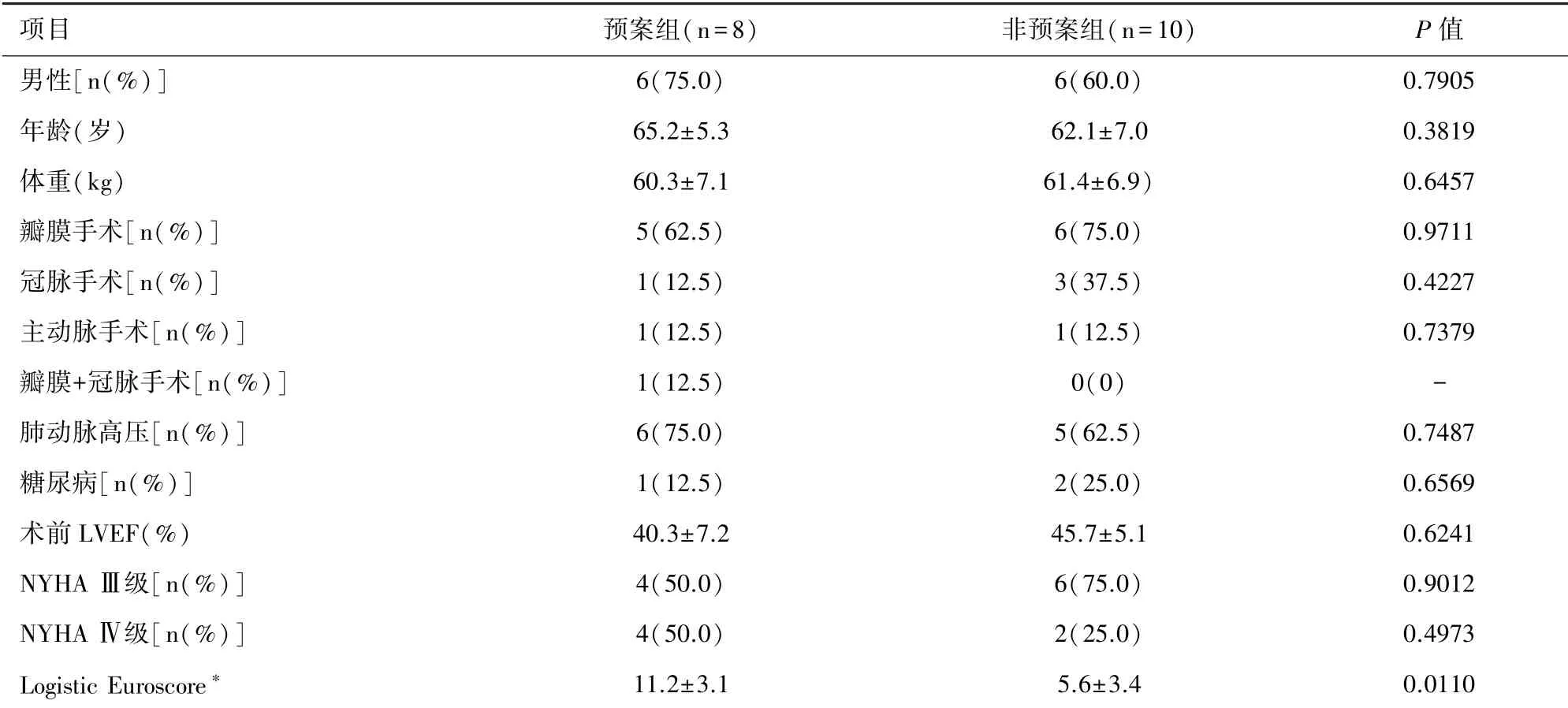
表1术中中转ECMO患者术前资料(s)
注:NYHA:纽约心脏功能分级;Logistic Euroscore:Logistic回归欧洲心脏手术风险评分。
项目 预案组(n =8) 非预案组(n =10)P 值男性[n(%)]6(75.0)6(60.0)0.7905年龄(岁)65.2±5.3 62.1±7.0 0.3819体重(kg)60.3±7.1 61.4±6.9)0.6457瓣膜手术[n(%)]5(62.5)6(75.0)0.9711冠脉手术[n(%)]1(12.5)3(37.5)0.4227主动脉手术[n(%)]1(12.5)1(12.5)0.7379瓣膜+冠脉手术[n(%)]1(12.5)0(0)-肺动脉高压[n(%)]6(75.0)5(62.5)0.7487糖尿病[n(%)]1(12.5)2(25.0)0.6569术前LVEF(%)40.3±7.2 45.7±5.1 0.6241 NYHAⅢ级[n(%)]4(50.0)6(75.0)0.9012 NYHAⅣ级[n(%)]4(50.0)2(25.0)0.4973 Logistic Euroscore∗11.2±3.1 5.6±3.4 0.0110
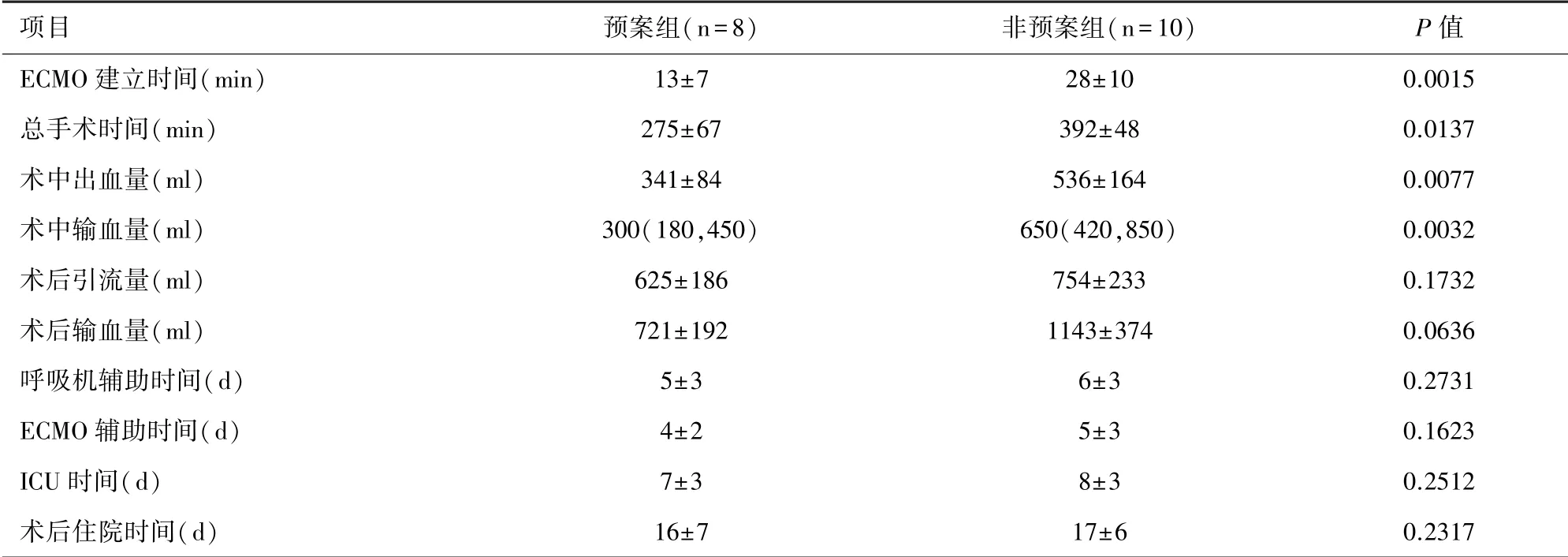
表2中转ECMO患者围术期情况
3 讨论
危重症CPB术后心功能不全即刻难以脱离CPB辅助的患者术中中转V-A ECMO行短时循环呼吸辅助优势明显。ECMO较CPB预充量小,细胞组织损伤小,炎症反应轻,能够避免长时CPB辅助造成的血细胞损伤、炎症反应加重等突出问题,且辅助时间可达到数天至数周[11-13]。同时,相比主动脉内球囊反搏(intra-aortic balloon counterpulsation,IABP),V-A ECMO能够提供更充分的循环支持和呼吸辅助功能。因此,CPB术中中转ECMO辅助在危重症CPB术后应用逐步推广,这对护理工作也提出了更高的要求[14-16]。
术中中转ECMO辅助时的快速介入、置管操作、评估、术后转运对手术的配合工作要求都不同于以往的常规手术[17-18]。充分的术前准备、高效术中配合与患者预后恢复非常相关。本研究结果显示,根据患者病情,合理的术前护理预案能够明显缩短术中ECMO介入所需时间及总手术时间,术中出血量及输血量也显著减少。因此,针对危重症患者术前准备充分的手术配合预案,特别是ECMO中转辅助预案非常重要。相关工作预案可从以下几方面准备。
3.1 术前中转预案对于术前一般情况较差、心功能差、预计CPB时间较长、术后有可能需要ECMO辅助的患者,术前应按术中ECMO中转进行准备。术前准备ECMO相关设备耗材、核对检查。根据患者身高、体重、股动静脉直径选取股动静脉插管备用,并备好腹股沟切开器械。ECMO辅助量比较大的中心,可装机干备不预充,准备好预充液,准备术中用血。术前常规标记双侧股动静脉位置,消毒铺巾预留腹股沟切开股动静脉插管位置。手术开始前联系ECMO团队并告知ECMO团队待命。
3.2 术中配合注意事项心内操作完成后,如停机困难,经评估拟中转ECMO的,应尽快准备器械。配合医生尽快显露股动静脉,准备插管,准备管道台上包。巡回护士立即联系ECMO团队,并协助完成电源气源准备、管路预充、开机调试等。
3.3 撤台转运ECMO辅助患者转运与常规患者转运有很大区别。由于常用ECMO 设备较重,与患者连接的管路较多、长度有限,且需要储备电源、氧气等,在有些中心还需要电梯转运、有空间限制,因此,转运过程前前首先要整理监护、呼吸辅助、引流及ECMO的各条管路,准备适合的转运床,提前准备好储备电、氧气等,特别是对于转运路途较长的患者。确认患者生命体征平稳后,外科医生、麻醉、护理、ECMO团队协作将患者搬动至转运床,检查各项管路安全后开始转运,途中有专人管理各项管路。为了转运方便,监护仪、呼吸机、ECMO设备、氧气瓶、储备电源等尽可能选用便携式仪器设备,并与转运床做好固定。
3.4 交接班到达ICU后,将患者搬动至监护床,并与监护室医护交接患者,尽快转接监护,在确认患者生命体征后协助ICU医护人员整理各项管路,同时连接呼吸机、ECMO设备电源气源。配合医生交接患者病情,并与监护室护理人员详细交接患者护理工作,包括术中情况、患者出入量、携带药物治疗情况、各项管路位置固定方式以及皮肤压疮情况等,并完善护理文书。
本研究为单中心回顾性研究,由于危重症心脏手术术中中转ECMO病例有限,本组仅纳入18例患者,预案组脱机成功率75%,高于非预案组,但两组间未见显著统计学差异。同时,预案组院内感染发生率为12.5%(1/8),低于非预案组40%(4/10)。由于纳入样本量较少,两组间未见显著统计学差异,但预案组中仅1例高龄患者术后呼吸道感染鲍曼不动杆菌,与非预案组院内感染情况明显不同。课题组以后的研究中将纳入更多的病例阐明相关问题。
综上所述,结合危重症患者术前情况,进行充分的术前准备和评估,做好ECMO辅助各项预案,能够缩短术中建立ECMO所需时间及总手术时间,并减少术中出血量及输血量。本研究纳入例数非常有限,且为非随机对照回顾性研究,对于CPB危重症患者术中中转ECMO辅助的护理配合和临床疗效仍需进一步研究。

