深部热疗联合化疗在晚期小细胞肺癌中的疗效观察
苏甲林 赵参军 杨建刚 张辉 郑瑾
肺癌是全世界最常见的癌症,包括非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)[1]。小细胞肺癌是一种侵袭性神经内分泌肿瘤,虽然小细胞肺癌占肺癌的15%,但它是最具侵袭性的亚型,其特点是生长迅速,早期广泛转移,尽管对初始化疗和放疗有短期的疗效,80%未治愈的局限期小细胞肺癌和100%广泛期小细胞肺癌患者的预后仍然很差[2]。小细胞肺癌的治疗选择包括化疗、放疗及少量手术切除,小细胞肺癌患者通常患有转移性疾病,因此,全身化疗是最常见的治疗策略[3]。然而,由于对化疗耐药的快速发展,长期预后仍然很差,导致不良结果。在首次诊断为小细胞肺癌的患者中,大约66%的患者已经为广泛期,5年生存率通常在1%~3%之间[4-5]。虽然大部分小细胞肺癌对化疗的总有效率约为80%,但总生存期的中位数仍在8~12个月,其总疗效仍不满意[6-7]。
肿瘤深部热疗具有化疗增敏性,高温会对癌细胞产生直接的细胞毒性,同时也是全身药物化疗药物的增敏剂[8-9]。深部热疗通过加热身体肿瘤局部使肿瘤组织局部热量聚集,使肿瘤局部温度较高,从而选择性杀灭肿瘤细胞,而周围的正常组织不受影响,并且可以增强细胞膜的通透性,加强抗肿瘤药物的渗透吸收;加温可增加药物的摄取及药物反应速度;深部热疗同时改善肿瘤周边血液循环,血流量增加利于化疗药物进入肿瘤内,引起肿瘤细胞的热破坏来增加某些抗肿瘤药物的细胞毒性效应[10-13]。目前,非小细胞肺癌在综合治疗的作用下取得良好的疗效,然而,对于小细胞肺癌的治疗效果仍未见明显提高,本研究对于晚期小细胞肺癌患者采用热疗和依托泊苷联合顺铂化疗的结合,可显著提高患者的化疗疗效,延长患者无进展生存期,减轻患者化疗的不良反应提高患者生存质量。
资料与方法
一、 一般资料
80例经影像学及病理学确诊为晚期小细胞肺癌患者,均为2017年6月1日至2019年5月31日空军军医大学第二附属医院中西医结合肿瘤专科符合纳入排除标准的住院患者,按住院顺序应用随机数字表法分为2组:治疗组40例,对照组40例,具体资料(见表1)。

表1 两组病人的一般临床资料比较
二、纳入标准
(1)经病理学和(或)细胞学确诊为小细胞肺癌;(2)影像学检查(CT、MR、ECT、PET/CT)有可见肿瘤,经国际抗癌联盟(UICC)推出的第8版肺癌TNM分期诊断为Ⅳ期;(3)KPS评分≥70分,预计存活时间大于6个月;(4)具有1个以上可测量病灶或客观性病灶指标;(5)粒细胞计数≥2.0×109/L,血小板计数≥100×109/L,血红蛋白≥90g/L;(6)胆红素、血肌酐、谷草转氨酶(AST)、谷丙转氨酶(ALT)在正常范围内(若有肝转移,则 ALT 及 AST 应≤1.5 倍正常值上限);(7)签署知情同意书。
三、排除标准
(1)不符合诊断标准;(2)化疗相关禁忌症者;(3)不能坚持治疗或不配合治疗之患者;(4)有颅内转移患者;(5)患者有出血性疾病;(5)体内有金属材料植入者;(6)患有精神障碍疾病,不能配合者。
四、剔除标准
(1)纳入后未按试验方案治疗的病例;(2)出现颅内转移病灶需要全脑放疗者;(3)试验中自行退出或不能坚持治疗者;(4)出现严重不良事件或严重不良反应者;(5)临床试验中出现严重的其它并发疾病者。
研究方法
一、对照组(Chemotherapy,CT)
给予入组患者EP方案全身化疗:依托泊苷注射液(齐鲁制药有限公司)100 mg/m2ivgtt d1-3联合注射用顺铂(齐鲁制药有限公司)75 mg/m2总量分成3 d使用溶于生理盐水 250mL,每21 d一周期。
治疗组(Deep hyperthermia combined with chemotherapy, HCT):化疗方案同对照组,同时于化疗每开始d1-3于化疗结束后给予肿瘤原发灶深部热疗每天1次,患者平躺或俯卧在治疗平台,使用ZD型体外电场热疗机(ZD-2001,Ⅰ类BF型,威海众恒医疗设备有限公司),调节上电极距人体约5cm,频率为 50Hz,输出功率 1650VA,治疗靶区设置在肺内原发病灶处体表投影区域,调节温度持在41~43℃之间(测量患者体外模拟温度在 42℃左右),持续50 min,热疗后嘱患者饮用500温水,避免脱水。
二、观察指标
1 近期疗效 每2个周期复查一次影像学检查,按照 RECIST 1.1 标准进行疗效评价。包括完全缓解(CR)、部分缓解(PR)、进展(PD)以及稳定(SD)。疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。化疗结束后,每月复查一次评估患者的无进展生存期。
2 KPS评分 KPS评分量表:依据病人能否正常活动、病情、生活自理程度,对病人的健康状况进行评分,总分为100分,每10分为一个等级,本研究入组患者符合KPS评分≥70分。
3 不良反应 采用NCI-CTCAE 药物毒副反应评定标准,分为0~Ⅳ度。
三、统计学方法
所有数据采用SPSS16.0软件进行统计分析,计数资料使用χ2检验,计量资料使用t检验,P<0.05 为差异具有统计学意义。
结 果
一、两组患者临床疗效的比较
治疗组患者的缓解率显著高于对照组,差异有统计学意义(P<0. 05)(见表 2)。研究组患者中位PFS为6个月,显著大于对照组的中位PFS为4个月,差异有统计学意义(P<0. 05)(见图1)。
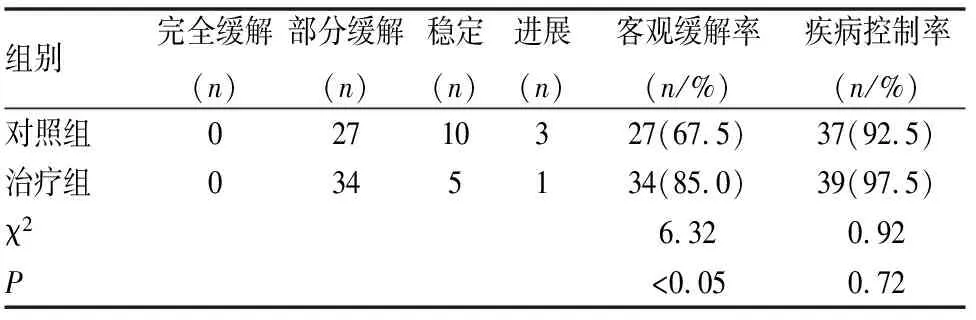
表2 两组细胞肺癌患者的疗效比较
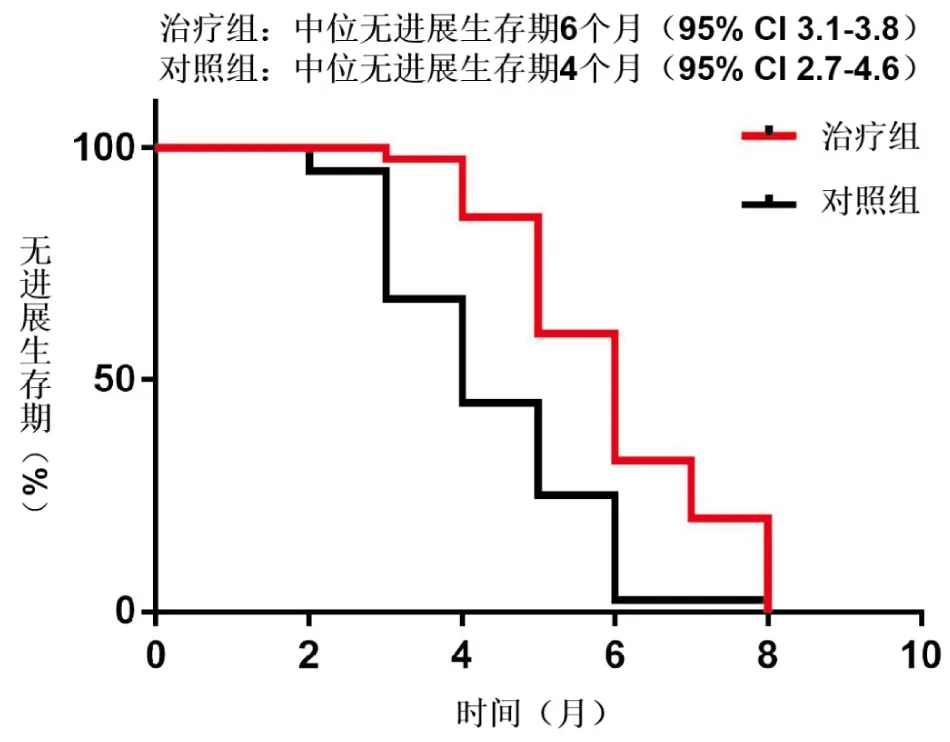
图1 两组小细胞肺癌患者的无进展生存期比较
二、两组治疗前后KPS评分变化
对2组患者在化疗前和化疗结束后均使用KPS评估量表测评,治疗组KPS评分较化疗前显著增加(P<0.05),对照组KPS评分较化疗前比较差异无统计学意义(P>0.05)(见表3)。

表3 两组患者治疗前后KPS评分比较
三、两组小细胞肺癌患者的毒性和不良反应比较
将2组患者于化疗前和化疗结束后,热疗联合化疗组在粒细胞、血小板及恶心、呕吐的副反应均较单纯化疗组降低,但其差异无统计学意义(P>0.05)(见表4)。
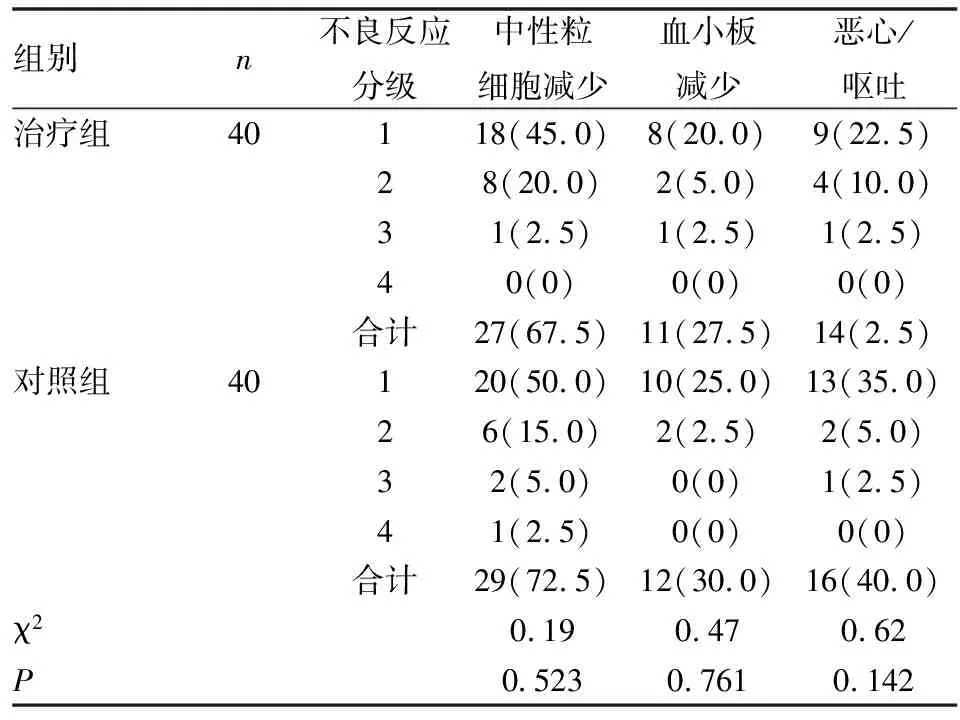
表4 两组小细胞肺癌患者的毒性和不良反应比较[n(%)]
讨 论
小细胞肺癌对化疗非常敏感,大多数患者化疗后肿瘤缩小,广泛期小细胞肺癌的标准治疗是联合化疗,目前依托泊苷联合顺铂是小细胞肺癌的一线治疗方案。研究表明,对于晚期小细胞肺癌依托泊苷联合化疗后患者很快再出现进展,然而,由于小细胞肺癌对化疗的耐药,导致患者总效仍不佳,预后很差[14]。本研究在晚期小细胞肺癌患者化疗的同时给予深部热疗,增强肿瘤细胞膜的通透性,有利于抗肿瘤药物的进入肿瘤细胞,增敏化疗,提高疗效。
肿瘤深部热疗是应用能量加热人体全身或局部,使肿瘤组织局部温度上升到有效治疗温度,并保持一段时间,从而使肿瘤细胞凋亡,又不损伤正常组织的一种辅助治疗方法[15]。热疗是晚期恶性肿瘤的重要治疗策略,已有报道通过与放疗和化疗协同作用来提高某些肿瘤如前列腺癌、卵巢癌、直肠癌、软组织肉瘤的治疗效果[16-17]。虽然确切的分子机制仍然难以捉摸,但一些研究表明,高温会导致细胞的脱氧核糖核酸、蛋白质和膜损伤,并干扰细胞周期 脱氧核糖核酸和蛋白质合成。所有这些都可能直接或通过触发凋亡途径导致细胞死亡[18]。研究发现,高温可以阻碍脱氧核糖核酸的修复,并且可以使癌细胞对脱氧核糖核酸破坏剂敏感,例如吉西他滨、嘧啶类似物、顺铂及环磷酰胺等[19-22]。
研究表明,高温可以提高肿瘤中醌氧还原酶的活性,从而提高β-拉帕醌对癌细胞的体外和体内细胞毒性,此外,热疗可以通过抑制DNA-PK激酶活性来增强无线电敏感性双链断裂修复过程中缺乏非同源末端连接和/或同源重组途径[23]。在一项随机3期多中心研究中,局部热疗的新辅助化疗对局部高风险软组织肉瘤患者的局部无进展生存期明显优于单纯新辅助化疗[24]。多西紫杉醇联合腹腔热灌注化疗能有效改善控制晚期卵巢癌患者腹水率、肿瘤缓解率和CA125下降率的总有效率。本研究对晚期小细胞肺癌患者,在化疗的同时联合深部热疗,可显著提高患者的化疗疗效及减轻患者化疗的不良反应,延长患者生存时间,提高患者生存质量[16,25-26]。
本研究对晚期小细胞肺癌患者给予深部热疗联合依托泊苷和顺铂方案化疗,研究结果显示,治疗组患者中位PFS较对照组患延长2个月,且患者化疗后体能也明显改善;并可以减轻患者化疗的不良反应,提高患者生存质量。综上所述,晚期小细胞肺癌患者采用化疗联合深部热疗的临床疗效优于单独化疗治疗,效果确切,值得临床推广。

