阿帕替尼治疗常规化疗失败晚期卵巢癌对患者血清CCL-18、HE4和卵巢血流的影响
方 军 胡继德
卵巢癌主要为卵巢原发性癌症,其早期缺乏特异性症状,多伴下腹部不适,无明显腹痛,晚期可出现贫血、消瘦、乏力、卵巢血流异常等症状,是危及女性生命安全的主要疾病。紫杉醇联合铂类为晚期卵巢上皮性癌的标准化疗方案,其临床疗效已得到多个研究证实,但仍有少数患者对此化疗不敏感,导致化疗失败[1]。常规化疗失败晚期卵巢癌的治疗是目前临床研究的难点。相关研究报道[2],血管内皮因子(VEGFs)和其受体(VEGFR)可参与肿瘤血管生成及淋巴管生成。阿帕替尼为口服的靶向VEGFR-2酪氨酸激酶抑制剂,通过阻断VEGFR及VEGF结合的信号,阻止内皮细胞增殖,抗血管生成活性明显[3]。本研究旨在研究阿帕替尼对常规化疗失败的晚期卵巢癌的疗效和安全性,并分析其对血清相关物质和卵巢血流的影响。
1 资料与方法
1.1 一般资料
选择2014年1月至2018年1月信阳市中心医院肿瘤内三科收治的100例常规化疗失败的晚期卵巢癌患者。入选标准[4]:①经超声波、细胞学、腹腔镜、肿瘤标志物、病理组织学等检查确诊为Ⅳ期卵巢上皮性癌;②治疗过程中疾病进展或者治疗结束时复发,既往接受系统化疗≥2个周期,前一次抗肿瘤治疗结束距此次用药时间低于4个月。排除标准:①近半年内接受血管内皮生长因子受体抑制剂小分子药物治疗;②给药前4周接受过放化疗、手术、分子靶向治疗;③腹泻、呕吐、恶心等胃肠道疾病;④初诊晚期卵巢癌;⑤严重心血管、肝肾及呼吸疾病;⑥哺乳或者妊娠期;⑦预计生存期低于3个月。患者年龄33~75岁,平均(58.15±8.63)岁;体重46~78 kg,平均(57.95±3.11)kg。本研究均经过本院伦理委员会批准,患者或家属均签署知情同意书。
1.2 方法
所有患者均给予阿帕替尼治疗,起始剂量为每次500 mg,每天1次,期间出现Ⅲ、Ⅳ度不良反应则调整剂量为每次250 mg,每天1次,持续应用至患者无法耐受,无严重不良反应者按原剂量维持至疾病进展。期间均不采用其他抗肿瘤方案,常规监测患者血尿常规、肝肾功能、血压及影像学变化等,治疗4周时评估疗效,记录不良反应。
1.3 观察指标
参照实体瘤疗效评价标准[5]进行,分为完全缓解、部分缓解、稳定、进展,客观缓解=完全缓解+部分缓解,疾病控制=完全缓解+部分缓解+稳定。
于治疗前及治疗4周结束时抽取患者空腹外周静脉血4 ml,采用血液分离机按3 000转/分钟分离10 min,保存于-20 ℃低温箱中待检。选用酶联免疫吸附法检测血清CCL-18、HE4水平。
治疗前及治疗4周结束时采用EMP-3000彩色多普勒超声诊断仪检测卵巢血流,腔内探头频率调整为4.0~9.0 MHz,扇扩角度为120°。嘱患者膀胱排空后取截石位,予以一次性避孕套罩住阴道探头,涂取适量耦合剂后往阴道内缓慢置入阴道探头,调整探头以紧贴于阴道穹窿及宫颈部位,实施多方位及多切面的扫查,常规检查卵巢子宫。选择子宫颈内口水平外侧子宫动脉血流频谱,确保声束和血管夹角在30°以下,取样容积为2 mm。测定搏动指数(PI)、阻力指数(RI)、收缩期峰值流速(PSV),所有患者均予以3次有效测量,取平均值为最终结果。
治疗前及治疗4周结束时采用卵巢癌患者生存质量测定量表[6]评估生活质量,量表总得分由癌症患者核心量表FACT-G(躯体功能、心理功能、社会功能及不良反应)及卵巢癌特异性模块构成,分数越高说明生存质量越好。
参照世界卫生组织抗癌药物不良反应标准[7]评估不良反应,分为0、Ⅰ、Ⅱ、Ⅲ、Ⅳ级。
1.4 统计学分析
2 结果
2.1 晚期卵巢癌患者临床疗效分析
100例晚期卵巢癌患者均无完全缓解,部分缓解39例,稳定36例,进展25例,客观有效率为39.00%(39/100),疾病控制率为75.00%(75/100)。
2.2 治疗前后患者血清CCL-18、HE4水平比较
治疗后,晚期卵巢癌患者血清CCL-18、HE4水平均低于治疗前,差异有统计学意义(P<0.05),见表1。
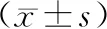
表1 晚期卵巢癌患者治疗前后血清CCL-18、HE4水平比较
注:a为与治疗前比较,P<0.05。
2.3 晚期卵巢癌患者治疗前后卵巢血流比较
治疗后,患者PI、RI高于治疗前,PSV低于治疗前,比较差异有统计学意义(P<0.05),见表2。
表2 晚期卵巢癌患者治疗前后卵巢血流比较
注:a为与治疗前比较,P<0.05。
2.4 晚期卵巢癌患者治疗前后生存质量比较
治疗后,晚期卵巢癌患者共性模块及特异性模块评分均高于治疗前,比较差异有统计学意义(P<0.05),见表3。
表3 晚期卵巢癌患者治疗前后生存质量比较
注:a为与治疗前比较,P<0.05。
2.5 晚期卵巢癌患者治疗后不良反应分析
晚期卵巢癌患者治疗后不良反应以血液毒性、腹泻、皮疹、蛋白尿、高血压及纳差乏力为主,见表4。
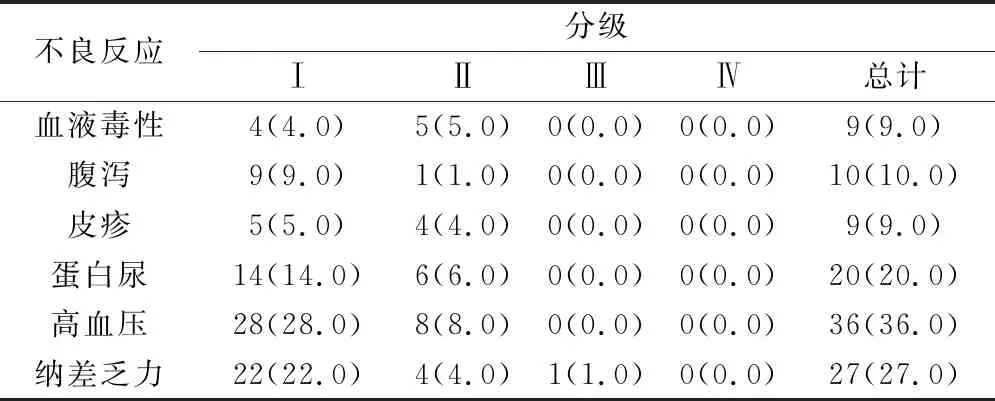
表4 晚期卵巢癌患者治疗后不良反应分析(例,%)
3 讨论
卵巢癌为女性生殖道的常见恶性肿瘤之一,具有发病隐匿、进展快速、易转移、恶性程度高等特点,多数患者就诊时已处于中晚期,预后不甚理想。尽管外科手术及化疗在卵巢癌治疗中已获得明显进步,但部分晚期卵巢癌患者在手术、化疗后容易出现复发、转移,且对化疗药物产生耐药性。
近年来,靶向药物成为常规化疗失败恶性肿瘤的重要治疗手段,可能有利于耐药问题的解决,延缓细胞转移,延长患者生存期。血管生成为恶性肿瘤生长及转移的必要条件,VEGF是刺激血管生成最强的因子,可调节肿瘤血管新生,促进肿瘤生长、浸润和转移,通过阻断此信号传导抑制肿瘤血管新生为恶性肿瘤靶向治疗提供了新途径[8]。贝伐珠单抗作为血管内皮生长因子抑制剂在复发性晚期卵巢癌治疗中的效果肯定,但其价格高昂,且需长期静脉输注,患者依从性差。阿帕替尼是口服靶向药物,可高选择性的阻断VEGFR-2相关信号通路,抑制血管内皮细胞增殖和迁移,起到抗肿瘤作用[9]。既往研究证实[10],阿帕替尼在晚期恶性肿瘤治疗中的效果突出,可明显延长晚期胃癌标准化疗失败患者的生存期。但在常规化疗失败的晚期卵巢癌中的治疗报道较少,本研究结果显示,阿帕替尼治疗后客观有效率为39.00%,疾病控制率为75.00%,说明阿帕替尼的效果确切,但本研究由于观察时间较短,样本量较少,结果可能有一定偏差,因此进一步分析实验室指标改变,明确其疗效。
CCL-18为最新发现的对卵巢癌诊断及预后评估有重要生物学价值的指标,其可起到炎性趋化因子免疫作用,增加肿瘤细胞粘附力,延缓其转移,肿瘤细胞游离状态下又可增加肿瘤细胞侵袭能力,诱导原发灶肿瘤细胞在血管壁及细胞外基质的粘附,增强肿瘤细胞迁移能力,从而促进肿瘤的浸润转移[11]。邸曼等[12]研究表明,已转移的恶性淋巴结中CCL-18阳性表达率明显高于未转移者,进一步多元回归发现其和肿瘤浸润深度有良好关系。HE4为分泌型糖蛋白,为蛋白酶抑制剂家族,主要在生殖道、唾液腺、近端呼吸道上皮中呈高表达,正常卵巢组织中几乎无表达,卵巢恶性肿瘤中高度表达[13]。本研究结果发现,治疗前患者血清CCL-18、HE4水平均较高,治疗后以上指标明显降低,说明阿帕替尼可抑制CCL-18及HE4表达,从而抑制卵巢癌复发及转移,为阿帕替尼治疗晚期卵巢癌提供一定临床依据。
卵巢恶性肿瘤可明显影响卵巢血供,通过测定卵巢血流状态有利于评估疾病情况,但卵巢血流参数变化较大,进一步研究的价值较高[14]。RI能够直观反映子宫内膜灌注及子宫动脉阻力情况,PI能够提示血管壁弹性情况,PSV可反映收缩期峰值状态。本研究显示,治疗前患者PI、RI均较低,PSV较高,说明晚期卵巢癌患者的血流灌注较差,呈高阻状态,治疗后卵巢血流明显改善,考虑其血流速度改善和肿瘤内部血流供应改变有关。晚期卵巢癌可明显影响患者心情、睡眠及活动,随着医学模式的转变及健康新理念的引进,生存质量已成为评估疗效的主要指标之一,为临床方案的选择提供依据。本结果发现,治疗后患者生存质量较治疗前明显提高,说明阿帕替尼可改善患者生存质量。同时本研究显示,治疗期间阿帕替尼不良反应以Ⅰ、Ⅱ级为主,未引起明显不良反应,安全性较高。
综上所述,阿帕替尼治疗常规化疗失败的晚期卵巢癌的近期疗效确切,能够降低血清CCL-18、HE4水平,改善卵巢血流状态,且不良反应可控。

