改良体外测量法联合心电技术在肺癌患者前端开口式耐高压PICC尖端定位中的应用
段盈芳 胡小艳 朱玉欣 赵熙 尹欣欣
肺癌患者在进行周期性化疗过程中需要多次进行增强CT或核磁等检查来判断疾病治疗效果,需静脉注射造影剂,耐高压注射型经外周置入中心静脉导管(power peripherally inserted central catheter,Power PICC)内腔大、流速快、可监测血流动力学和高压注射造影剂[1],真正实现一次置管完成全部静脉治疗,被广泛应用于肺癌患者。Power PICC在使用过程中也存在一些问题,耐高压导管为前端修剪式,对体外测量的准确性要求高,导管裁剪过长会导致末端位置过深,引发心律失常等心脏疾病,或者留置体外的导管过长,增加了固定难度,导管为聚氨脂材质,总体形状为倒椎型,比较硬且尾端重,易发生导管移位或脱出[2]。裁剪过短会导致末端位置过浅,在注射高压造影剂过程中容易出现尖端移位[3],影响导管的功能和保留时间。美国静脉输液协会推荐PICC尖端应位于上腔静脉的下1/3段至上腔静脉与右心房的交界处[4]。临床常用的体表测量方法为横L法,有研究者发现采用横L法易导致导管置入过深[5],开始采用依据身高、预穿刺静脉深度、体重指数等改良的体外测量方法[6],本研究将上腔静脉长度纳入到测量指标中,联合身高、皮下静脉深度将体外测量方法进行了改良。已有研究者报道采用心电定位法引导PICC穿刺,取得了显著效果[7]。P波振幅增高,提示导管头端进入上腔静脉,但P波出现何种形态表明导管头端位于上腔静脉下1/3段到达上腔静脉与右心房的交界处,目前针对不同裁剪式导管结论尚未一致。本研究在置管前采用改良式体外测量法测量导管,通过观察在肺癌患者前端开口式Power PICC置入过程中心电图特异性P波形态变化,证实改良式体外测量联合心电图在前端开口式Power PICC尖端定位的准确性,观察每种P波形态出现的频率,分析此类导管尖端位于理想位置时P波的形态,报告如下。
1 资料与方法
1.1 一般资料 回顾性选取2016年8月至2018年12月在我院肿瘤科治疗,行Power PICC置入的肺癌患者108例,查阅其临床资料和PICC穿刺记录,其中肺腺癌64例,肺鳞癌16例,小细胞肺癌28例;男56例,女52例;中位年龄57岁(42~81岁)。纳入标准:(1)病理诊断为肺癌;(2)患者由于治疗需要置管,知情同意后签署知情同意书;(3)基础体表心电图正常,有正常P波,无心脏疾病;(4)上肢活动功能良好,穿刺处无皮肤破损。排除标准:(1)明确有心脏疾病:房颤、房扑、肺心病;(2)基础体表心电图中P波异常;(3)安装心脏起搏器、植入式除颤仪等。
1.2 材料 本研究使用的材料包括:4Fr的耐高压PICC,一次性PICC穿刺包、十二导联心电图机(型号:MECG-200);便携式超声仪(型号:EDAN-U50);两端带有鳄鱼夹的无菌连接导线。
1.3 操作方法 置管操作由医院取得市级以上PICC置入资质证书的静脉治疗专科护士按医院PICC置管标准化操作流程进行,具体流程:①查看病例:观察患者的基础体表心电图;②选择血管:在患者上臂中段选择穿刺静脉,首选右侧贵要静脉,在超声引导下确定穿刺部位,并标记;③运用改良式体外测量法准确测量和计算导管预置入长度:协助患者取仰卧位,查看患者身高,拟穿刺侧上肢外展90°,测量预穿刺点至右侧胸锁关节的长度,根据身高在此长度基础上进行加减,150~160 cm在此长度的基础上+5 cm;160~170 cm在此长度基础上+6 cm;>170 cm在此长度基础上+7 cm,然后根据CT显示的上腔静脉长度(肺癌患者治疗前为明确病灶会行胸部CT,5~7 cm无需调整;<5 cm 减去1 cm;>7 cm加1 cm)和皮下静脉深度(>1.5 cm加1 cm;0.5~1.5 cm无需调整;<0.5 cm减去1 cm)调整,记录预定长度[6]。④皮肤消毒和铺无菌巾:使用75%乙醇和2%葡萄糖酸氯已定溶液对预穿刺上肢进行消毒,铺无菌治疗巾,建立最大无菌屏障。⑤穿刺静脉:采用超声引导下联合改良塞丁格技术穿刺静脉,穿刺成功后送入导丝和导管到达预定长度时,超声探测,观察导管是否异位至颈内静脉等,若无异位连接心电导联,监测心电图波形,观察P波振幅和形态(若无P波改变,调整至出现P波改变)以及P波起始段是否出现倒置Q波,撤出导丝、给予0.9%氯化钠溶液冲管,连接接头,封管,以无菌敷料固定导管。记录置管过程,每位患者进行胸部X线正位摄片,根据胸片结果观察并记录导管头端位置。
1.4 导管尖端位置的判断标准 美国静脉输液协会推荐PICC尖端应位于上腔静脉的下1/3段至上腔静脉与右心房的交界处[4],一些欧洲的研究和指南认为在右心房上段也可[8]。研究表明,上腔静脉与右心房交界处(cava atrial junction CAJ)在胸片上对应第6~8胸椎水平,第3~4前肋之间,气管隆突下两个胸椎体[9]。本研究以胸片结果为判断依据,由专业医学影像科医师判定导管位置,第6~8后肋作为导管尖端正确位置,第6后肋以上为尖端位置过浅,第8后肋间隙以下为尖端位置过深。
1.5 置管过程中腔内心电图的获得及分析 在置管前先观察患者基础体表心电图是否正常以及P波的振幅和形态,当导管送至预置入长度时,超声判断是否异位至颈内静脉,若无异位,采用心电图肢体导联,将无菌夹连接导线的一端夹于Power PICC金属导丝末端,另一端与心电图机的右上肢电极连接,抽吸20 ml 0.9%氯化钠溶液连接导管进行注射,导管内的导丝以0.9%氯化钠溶液和血液为介质将心电信号导出,得到持续稳定的心电图,观察特异性P波变化(正向高振幅)和P波起始段有无出现倒置的“Q”波。
2 结果
2.1 改良式体外测量法联合心电图定位结果与胸片结果比较 108例患者基础体表心电图均正常,置管过程中均未出现心律失常,出现特异性P波共100例,引出率为93.5%,8例患者没有引出特异性P波,X线片证实1例患者异位于颈内静脉,2例异位于对侧锁骨下静脉,5例尖端在正确位置,灵敏度95.2%,特异度75%。见表1。
2.2 特异性P波形态 出现特异性P波的患者中,P波形态可为单峰或双峰,双峰占39%,5例P波振幅为R波的50%以下,P波振幅为R波的50%~80%有84例,P波振幅大于R波的80%甚至波峰超过R波的有11例(其中1例出现Q波见图4,位置过深到达右心房),每种P波形态下导管头端位置经胸片判断后的正确率。见图1~4,表2。

表1 改良式体外测量法联合心电图判断前端开口式耐高压PICC尖端位置与胸片结果比较 例


图1 单峰P波,P /R振幅比值<50%图2 双峰P波,P /R振幅比值50%~80%图3 双峰P,P /R振幅比值>80%图4 P波起始段出现Q波
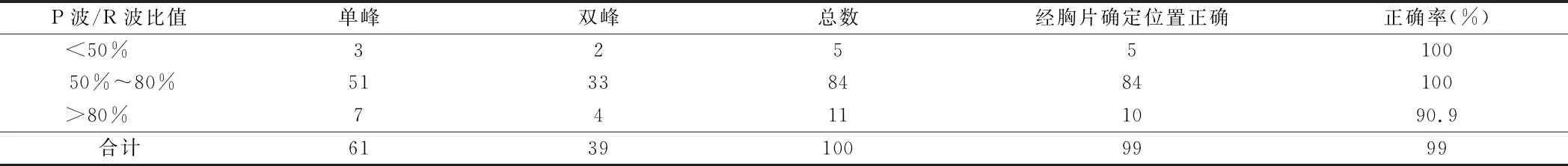
表2 特异性P波形态和尖端位置
3 讨论
3.1 利用改良式体外测量法联合心电定位肺癌患者前端开口式耐高压PICC的准确性 Power PICC采用强化聚氨酯材料,有耐高压、可注射造影剂的优点,已被广泛应用于肿瘤科肺癌患者。传统的体外测量方法为横L法,即患者平卧,置管侧上肢与躯体在同一水平面并且垂直成90°角,用软尺从穿刺点测量至右侧胸锁关节,再向下测量至第三肋间隙的长度,两个测量值之和为PICC预置入长度[10]。有些肥胖患者的胸锁关节、胸骨角等骨性标志不明显,不容易找到准确的第3肋间隙,增加了体表测量的误差。有研究表明此测量方法会导致导管置入过深[5],导管外撤后外露部分过长既增加了感染的风险,又易发生导管脱出。朱玉欣等[6]采用依据身高加数字的PICC体表测量方法,提高了导管理想位置的到位率。封凤等[5]将身高和体重指数纳入到体外测量中,发现从穿刺点至右胸锁关节的长度再加上根据身高及体重指数预加6~10 cm 为预测长度更接近导管理想长度。国内有研究通过胸部薄层CT扫描得出上腔静脉长度为5.2~9.5 cm[11],INS推荐PICC尖端应位于上腔静脉的下1/3段至上腔静脉与右心房的交界处,PICC置入长度与患者上腔静脉长度密切相关,上腔静脉越长,其下1/3的位置越靠下,肺癌患者治疗前为明确病灶会行胸部CT,本研究根据置管前的CT结果判断上腔静脉长度,5~7 cm无需调整;<5 cm减去1 cm;>7 cm加1 cm,综合患者身高、上腔静脉长度、皮下静脉深度调整导管体外测量长度,只有1例出现位置过深(提示导管体外裁剪过长),提高了体外测量的准确性。
近年来心电图被广泛应用于各种类型的PICC头端定位,取得了一定效果。P波为心房除极波,其形态和振幅取决于探测电极与心房综合向量轴间的距离和相对位置,当导管尖端进入上腔静脉时P波振幅逐渐增大,接近右心房的起搏点时,可引出高振幅的正向P波,当导管头端进入右心房入口,可出现特异性P波起始段出现倒置“Q”波;当导管头端进入右心房中部,“Q”波加深,呈双相P波;当导管头端靠近右心室时,可见倒置P波[7]。本研究采用筛检实验的方法,以胸片定位为金标准判断改良式体外测量法联合心电图定位前端开口式耐高压PICC的准确性,灵敏度为95.2%,即利用心电图定位PICC导管头端位置,导管尖端到达上腔静脉下1/3的准确率为95.2%,特异度为75.0%,即利用心电图显示导管尖端未到达上腔静脉下1/3,同时经胸片判断也未到达上腔静脉下1/3的正确率75%,与以往的研究结果[12]相比,灵敏度基本一致,特异度偏低,可能与研究例数少有关,也可能与心电图定位有8例未引出特异性P波有关,而这8例中有3例发生异位,5例经胸片判断在正确位置,提示今后可优化心电图定位的方法,提高特异性P波的引出率,增加心电图定位的准确性。
3.2 心电图指导前端开口式耐高压PICC尖端位置的波形变化分析 国内有研究者运用心电图特异性P波形态变化指导瓣膜式PICC置管的尖端定位,发现在置管过程中出现特异性P波后继续送入导管,P波起始段均出现倒置的Q波,可能是因为三向瓣膜导管为尾端修剪,长度足以获得倒置的“Q”波,提示对于心电波形指导三向瓣膜PICC尖端定位,出现倒置的“Q”波,再缓慢后撤导管直到特异性“Q”波消失 (此时P波为正向高振幅)[7]。本研究只有1例在特异性P波起始段出现倒置的小“Q”波,可能是因为耐高压导管多为前端修剪式,需要在置管前进行测量和裁剪,体外测量准确或裁剪过短的情况下,只出现特异性P波,不出现倒置的“Q”波,如果裁剪过长,有可能会出现倒置的“Q”波,需要外撤导管,导致导管留置体外过长,有脱管的风险。提示心电图波形引导前端开口耐高压导管与尾端修剪三向瓣膜导管有区别,以出现特异性P波(正向高振幅)为依据。本研究结果显示P波形态可表现为单峰和双峰,振幅P/R波比值在50%~80%的居多,与以往的研究结果[13-15]一致。50%下和80%以上的占少部分,其中80%以上有1例尖端位置过深,这1例在置管过程中P波振幅高于R波,且出现倒置“Q”波。由于上腔静脉的下1/3段至上腔静脉与右心房的交界处是一段长度范围,提示对于前端开口耐高压注射型PICC,置管过程中出现特异性P波后,为不增加外漏长度建议继续送入导管,若P波起始段无倒置的“Q”波则将导管送至0刻度,避免增加外漏,防脱管。若出现“Q”波,提示导管置入过深,建议后撤导管。
3.3 改良式体外测量法联合心电图用于前端开口式PICC头端定位的局限性 本研究显示改良式体外测量法联合心电图引导前端开口式耐高压PICC置管可有效监测导管头端是否进入上腔静脉下1/3与右心房的交界处,但结果显示未出现特异性P波的8例患者中有5例患者经胸片判断后在正确位置,原因可能与导丝直径细导致心电信号弱,造成导丝和连接线或连接线和导联之间的失传导有关,或与导管贴近血管壁有关,也可能与操作者推注0.9%氯化钠溶液的力度和速度有关,提示操作者可通过重新调整电极与导丝之间的连接、或让患者变换体位、匀速推注生理盐水等方法来提高特异性P波的引出率,P波的稳定性和影响因素还需要进一步研究。
前端开口耐高压PICC需在置管前进行准确的体外测量,置管过程中通过观察心电图P波改变可有效监测导管尖端是否进入上腔静脉下1/3与右心房的交界处,心电图波形引导前端开口耐高压导管与尾端修剪三向瓣膜导管是有区别的,前端开口耐高压PICC需在置管前裁剪,总体形状为倒椎型,尾端较重,容易脱管,不易体外留置过多,体外测量正确或导管裁剪过短的情况下,一般不出现倒置“Q”波,以特异性P波(正向高振幅单峰或双峰、P波/R波振幅比值在50-80%多见)为提示,建议将导管送至0刻度。裁剪过长的情况下,出现特异性P波后,继续送入导管,P波起始段出现倒置“Q”波,需将导管外撤,增加外漏长度,易脱管而导致非计划性拔管,给病人增加了治疗费用。对于前端开口耐高压PICC,体外测量的准确性对于导管尖端定位同样重要,改良后的导管测量方法根据患者身高、上腔静脉长度、皮下静脉深度进行调整,提高了体外测量的准确性。

