绞股蓝总黄酮提取工艺及抗氧化活性研究
谭曾勇,冉 勤,胡琼丹,赵诗兰,冯汉清,杨 艳
(湖北民族大学化学与环境工程学院,湖北 恩施 445000)
黄酮类化合物广泛存在于自然界,尤其在水果、蔬菜、茶、种子以及植物根部含量丰富。黄酮类化合物具有2-苯基色原酮结构[1-3],虽不属于维生素,但由于其在生物体内反应的重要作用和营养价值,被称为“维生素P”[4-7]。大多数黄酮类化合物具有止咳、祛痰、平喘、抗菌、解肝毒等功效[8-10]。蔓生草本植物绞股蓝富含黄酮类化合物,属药食同源植物,在明朝就被载入《救荒本草》,含人参皂苷等数十种活性成分。国内外大量科研机构和临床试验证明[11-14],绞股蓝具有显著降血脂、净化血液、稳定血压、延年驻颜等功效;同时对提高睡眠质量、防治便秘、消暑解渴、增强免疫、保肝护肝等都有很好疗效;还可缓解因吸烟、饮酒过度等带来的不适[15-17]。文献[18-19]报道,提取工艺对绞股蓝总黄酮的提取量及抗氧化活性影响较大。因此,作者采用单因素实验和正交实验对绞股蓝总黄酮提取工艺进行优化,并通过测定其对羟基自由基和超氧阴离子自由基的清除率来评价其抗氧化活性。
1 实验
1.1 材料、试剂与仪器
某品牌野生龙须绞股蓝,购于恩施市中百仓储。
芦丁标准品(批号008029705),上海甄准生物科技有限公司;无水乙醇、亚硝酸钠、氢氧化钠、硝酸铝、维生素C,国药集团化学试剂有限公司;硫酸亚铁、双氧水,天津光复科技发展有限公司;三羟甲基氨基甲烷,四川西亚化工有限公司;浓盐酸,武汉洪山中南化工试剂有限公司;焦性没食子酸,天津博迪化工有限公司;水杨酸,天津恒兴化学试剂制造有限公司;二次蒸馏水。所用试剂均为分析纯。
UV-2550型紫外分光光度仪,SHIMADZU;D1S型集热式磁力搅拌器,上海予正仪器设备有限公司;FA1004B型电子天平,上海佑科仪表有限公司;800型离心机,上海云楼医用仪器厂;KQ 2200B型超声波清洗器,昆山超声仪器有限公司;DW-2型调温电热器,江苏通州光学仪器有限公司。
1.2 检测波长的确定
以体积分数为60%的乙醇为溶剂,以氢氧化钠、亚硝酸钠、硝酸铝为显色剂,分别绘制芦丁标准溶液及绞股蓝提取液的吸收曲线。结果显示,绞股蓝的最大吸收波长为510 nm,芦丁的最大吸收波长为505 nm。由于芦丁标准溶液在500~510 nm之间吸光度相差不大,因而后续标准曲线的制作及绞股蓝提取液中总黄酮的测定均以505 nm为检测波长。
1.3 标准曲线的绘制
参照文献[7]配制0.200 mg·mL-1的芦丁标准溶液。准确吸取芦丁标准溶液0 mL、0.5 mL、1.0 mL、2.0 mL、3.0 mL、4.0 mL,分别置于10 mL容量瓶中;加入0.3 mL 5%的亚硝酸钠溶液,静置6 min;加入0.3 mL配制好的10%硝酸铝溶液,静置60 min;加入4 mL配制好的4%氢氧化钠溶液,静置15 min;用60%乙醇定容至刻度,静置15 min;测定其在505 nm处吸光度。以芦丁浓度为横坐标、吸光度为纵坐标绘制标准曲线。
1.4 提取工艺的优化
1.4.1 单因素实验
主要考察提取时间、提取温度、乙醇体积分数、固液比、pH值、提取次数等对绞股蓝总黄酮提取量的影响。通过预实验,设计提取时间为30 min、60 min、90 min、120 min、150 min、180 min,提取温度为50 ℃、60 ℃、70 ℃、80 ℃、90 ℃,乙醇体积分数为20%、40%、60%、80%、100%,固液比为1∶10(g∶mL,下同)、1∶20、1∶30、1∶40、1∶50、1∶60,pH值为3、5、7、8、10,提取次数为1、2、3、4。
1.4.2 正交实验
为了更好地进行正交实验方案的设计,分别对比了回流法及索氏提取法提取绞股蓝总黄酮的效果。结果发现,索氏提取法提取的绞股蓝总黄酮提取量更高,因此,正交实验采用索氏提取法提取绞股蓝总黄酮。
在单因素实验的基础上,以乙醇体积分数、固液比、pH值、虹吸次数为考察因素,以绞股蓝总黄酮提取量为指标,采用L9(34) 正交实验优化绞股蓝总黄酮提取工艺。
1.5 抗氧化活性的评价
1.5.1 对羟基自由基的清除效果
水杨酸能捕捉羟基自由基并产生有色物质,该物质在510 nm处有强吸收峰。若在反应体系中加入具有清除羟基自由基的物质时,会使有色物质生成量减少,溶液在510 nm处吸收峰强度会减弱或消失。
在10 mL容量瓶中依次加入9.0 mmol·L-1FeSO4溶液1.0 mL、9.0 mmol·L-1水杨酸-乙醇溶液1.0 mL、8.8 mmol·L-1H2O2溶液1.0 mL;再分别量取1.0 mg·mL-1的绞股蓝总黄酮提取液0.1 mL、0.3 mL、0.6 mL、0.9 mL、1.0 mL、1.2 mL、1.5 mL、1.8 mL于容量瓶中,用蒸馏水稀释至刻度,摇匀,于37 ℃反应30 min;用紫外分光光度仪测定溶液在510 nm处吸光度A样品;样底管不加H2O2溶液,空白管不加绞股蓝总黄酮提取液,同法测定溶液在510 nm处吸光度A样底、A空白,按式(1)计算清除率。取相同浓度VC溶液重复上述实验,以评价绞股蓝总黄酮对羟基自由基的清除效果。

(1)
1.5.2 对超氧阴离子自由基的清除效果
邻苯三酚在碱性条件下发生自氧化反应,生成超氧阴离子自由基以及有色中间产物,该产物在420 nm处有强吸收。若在反应体系中加入具有清除超氧阴离子自由基的物质时,超氧阴离子自由基的生成会受到抑制,溶液在420 nm处吸收峰强度减弱。
在10 mL容量瓶中加入pH值为8.2的0.05 mol·L-1Tris-HCl缓冲溶液4.5 mL,再分别加入1.0 mg·mL-1绞股蓝总黄酮提取液0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL、1.4 mL、1.6 mL、2.0 mL,用蒸馏水稀释到6.0 mL,摇匀,于25 ℃反应20 min;再加入0.4 mL 6.0 mmol·L-1邻苯三酚(含10 mmol·L-1HCl),摇匀,于25 ℃反应4 min;再滴2滴8.0 mol·L-1HCl终止反应;用蒸馏水稀释至刻度,用紫外分光光度仪测定溶液在420 nm处吸光度A样品;样底管用10 mmol·L-1HCl代替邻苯三酚,空白管不加绞股蓝总黄酮提取液,同法测定溶液在420 nm处吸光度A样底、A空白,按式(1)计算清除率。取相同浓度VC溶液重复上述实验,以评价绞股蓝总黄酮对超氧阴离子自由基的清除效果。
2 结果与讨论
2.1 标准曲线与回归方程
以芦丁浓度(c)为横坐标、吸光度(A)为纵坐标绘制标准曲线(图1)。拟合得线性回归方程A=13.05421c+0.00885,R2=0.99963。表明,芦丁浓度在0.010~0.080 mg·mL-1范围内与吸光度呈良好的线性关系。
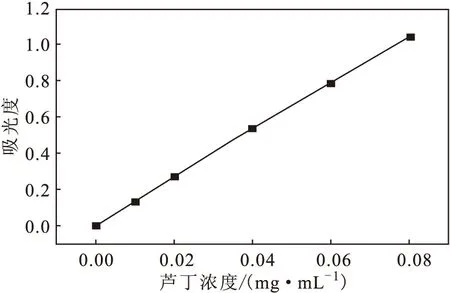
图1 芦丁标准曲线
2.2 最优提取工艺
2.2.1 单因素实验结果
2.2.1.1 提取时间对绞股蓝总黄酮提取量的影响(图2)
由图2可知,随着提取时间的延长,绞股蓝总黄酮提取量不断升高,150 min后趋于稳定。这可能是由于,提取一定时间后,原料中的黄酮类化合物基本被提取,继续延长提取时间,提取量不再升高。因此,最优提取时间为150 min。
2.2.1.2 提取温度对绞股蓝总黄酮提取量的影响(图3)
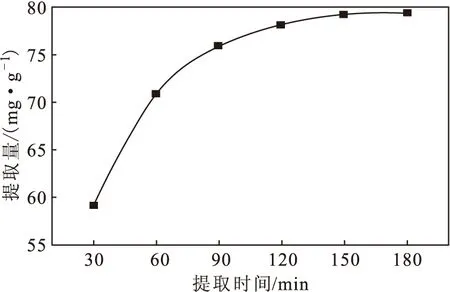
图2 提取时间对绞股蓝总黄酮提取量的影响

图3 提取温度对绞股蓝总黄酮提取量的影响
由图3可知,随着提取温度的升高,绞股蓝总黄酮提取量不断升高,在90 ℃时达到最高。因此,最优提取温度为90 ℃。
2.2.1.3 乙醇体积分数对绞股蓝总黄酮提取量的影响(图4)

图4 乙醇体积分数对绞股蓝总黄酮提取量的影响
由图4可知,随着乙醇体积分数的增加,绞股蓝总黄酮提取量先升高后降低,在乙醇体积分数为60%时达到最高。这可能是因为,乙醇体积分数过大,绞股蓝不能充分溶解,不利于黄酮类物质的提取,导致提取量降低。因此,乙醇体积分数选择60%较为适宜。
2.2.1.4 固液比对绞股蓝总黄酮提取量的影响(图5)
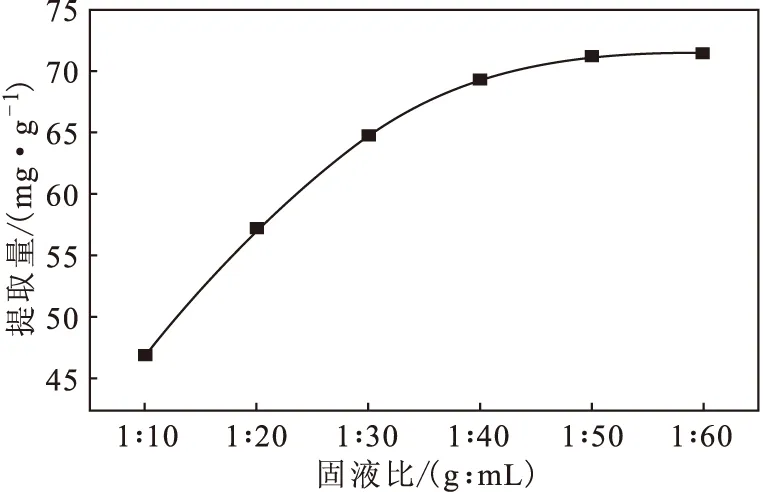
图5 固液比对绞股蓝总黄酮提取量的影响
由图5可知,随着固液比的减小,即溶剂用量的增加,绞股蓝总黄酮提取量不断升高,在料液比达到1∶50后趋于稳定。这主要是由于,增加溶剂用量,有利于绞股蓝中的黄酮类物质向提取液中扩散,从而提高总黄酮提取量;但当溶剂用量增加到一定值时,绞股蓝表面与提取液之间的浓度差不再是影响提取量的主要因素,此时溶剂溶解的蛋白质、碳水化合物等物质也会增多。因此,固液比选择1∶50较为适宜。
2.2.1.5 pH值对绞股蓝总黄酮提取量的影响(图6)

图6 pH值对绞股蓝总黄酮提取量的影响
由图6可见,随着pH值的增大,绞股蓝总黄酮提取量先升高后降低,在pH值约为8时达到最高;过酸条件下,提取量较低;过碱条件下,提取量下降明显。这可能是由于,过酸和过碱环境都有可能破坏黄酮类物质的成分,导致总黄酮提取量降低。因此,pH值选择8较为适宜。
2.2.1.6 提取次数对绞股蓝总黄酮提取量的影响(图7)
由图7可知,提取2次时的绞股蓝总黄酮提取量较提取1次时的提取量呈直线升高;提取3次时,提取量平缓上升;提取4次时,提取量则有下降的趋势。这可能是因为,随着提取次数的增加,提取时间相应延长,造成总黄酮出现分级现象,从而影响总黄酮提取量。因此,最优提取次数为2次。

图7 提取次数对绞股蓝总黄酮提取量的影响
2.2.2 正交实验结果
L9(34)正交实验的因素与水平见表1,结果与分析见表2,方差分析见表3。
表1 正交实验的因素与水平
Tab.1 Factors and levels of orthogonal experiments

水平因素A.乙醇体积分数/%B.固液比/(g∶mL)C.pH值D.虹吸次数/次1 40 1∶30 4 12 2 60 1∶50 8 18 3 80 1∶70 10 24
表2 正交实验结果与分析
Tab.2 Results and analysis of orthogonal experiments

实验号ABCD提取量mg·g-11111156.4742122276.1133133379.0234212368.2065223165.5506231261.1427313257.9998321358.3139332169.542k170.53760.89358.64363.855 k264.96666.65971.28765.085 k361.95169.90267.52468.514 R8.5869.00912.6444.659
表3 方差分析
Tab.3 Variance analysis

因素偏差平方和自由度F比F临界值显著性乙醇体积分数113.82820.7916.940无固液比124.93220.8686.940无pH值252.90321.7576.940无虹吸次数34.97520.2436.940无误差287.884
由表2、3可知,各因素对绞股蓝总黄酮提取量的影响大小依次为:pH值>固液比>乙醇体积分数>虹吸次数,最优工艺组合为A1B3C2D3,即乙醇体积分数40%、固液比1∶70、pH值8、虹吸次数24。
在最优提取条件下,采用索氏提取法提取绞股蓝总黄酮, 2次重复实验的总黄酮提取量分别为83.296 mg·g-1、83.294 mg·g-1,平均值为83.295 mg·g-1。表明,该方法具有非常好的重复性,优化的提取工艺是可行的。
2.3 抗氧化活性
2.3.1 对羟基自由基的清除率(图8)

图8 对羟基自由基的清除率
由图8可知,随着VC浓度的增加,其对羟基自由基的清除率迅速升高,当VC浓度高于0.06 mg·mL-1时,清除率超过95.000%,增幅趋缓;随着绞股蓝总黄酮提取液浓度的增加,其对羟基自由基的清除率逐渐升高,当绞股蓝总黄酮提取液浓度达到0.18 mg·mL-1时,清除率达到56.757%。表明,绞股蓝总黄酮提取液与VC对羟基自由基均具有一定的清除能力,VC对羟基自由基的清除效果更明显。这是因为,VC为人工合成品,纯度高,其抗氧化活性相应较高;而绞股蓝未经处理,提取得到的总黄酮为天然抗氧化剂,安全性高,且有些结构的黄酮类化合物抗氧化能力较差,因此,绞股蓝总黄酮的抗氧化活性较VC差。
2.3.2 对超氧阴离子自由基的清除率(图9)

图9 对超氧阴离子自由基的清除率
由图9可知,随着VC浓度的增加,其对超氧阴离子自由基的清除率迅速升高,当VC浓度高于0.08 mg·mL-1时,清除率超过98.230%,增幅趋缓;随着绞股蓝总黄酮提取液浓度的增加,其对超氧阴离子自由基的清除率逐渐升高,当绞股蓝总黄酮提取液浓度达到0.20 mg·mL-1时,清除率达到65.151%。表明,绞股蓝总黄酮提取液和VC对超氧阴离子自由基均具有一定的清除能力,VC对超氧阴离子自由基的清除效果更明显。
3 结论
在单因素实验的基础上,采用正交实验对绞股蓝总黄酮提取工艺进行优化,并通过测定其对羟基自由基和超氧阴离子自由基的清除率来评价其抗氧化活性。结果表明:各因素对绞股蓝总黄酮提取量的影响大小依次为:pH值>固液比>乙醇体积分数>虹吸次数;最佳提取工艺为:提取时间150 min、提取温度90 ℃、乙醇体积分数40%、固液比1∶70(g∶mL)、pH值8、虹吸次数24,在此条件下,绞股蓝总黄酮提取量达到83.295 mg·g-1;绞股蓝总黄酮提取液和VC对羟基自由基和超氧阴离子自由基均有一定的清除能力,但在相同浓度下,VC的抗氧化活性更高;当绞股蓝总黄酮浓度为0.18 mg·mL-1时,其对羟基自由基的清除率达到56.757%;当绞股蓝总黄酮浓度为0.20 mg·mL-1时,其对超氧阴离子自由基的清除率达到65.151%。

