从铜冶炼废酸中回收磁性铁的试验研究
崔育涛, 黄平锋, 田 静, 张 娜, 高强文
(1.河南省黄金资源综合利用重点实验室, 河南 三门峡 456231;2.河南中原黄金冶炼厂有限责任公司, 河南 三门峡 456231)
铜冶炼企业在生产运行过程中,烟气制酸车间每天都会产生大量的废酸,其主要成分为铜、铁、砷、铼、硫酸以及其他稀有金属,为了保证系统的正常运转,同时回收其中的有价金属,各企业都会对一部分废酸进行开路处理。目前最常用的废酸处理方法为:先回收其中的有价金属金银以及稀有金属铼,再硫化沉淀铜、砷,最后回收铁。当硫化沉淀所用的硫化剂为铁锍时,经沉淀处理后的废酸中主要含有大量的铁元素,其他元素的含量已经很低,回收这部分铁元素后,便可将除铁废液作为废水排放。
因此,本文研究出了一种处理回收废酸中铁元素的方法[1-4]:用碳酸钙降低废酸的酸度,滤液用电石渣调节pH,加入氧化剂制备磁性铁,再通过磁选分离回收铁。整个工艺成本较低,既回收了铁元素也有利于环境的保护。
1 试验原料及试验原理
以某铜冶炼加工企业铁锍除砷后的废酸为试验原料,其主要成分见表1。
从表1可以看出,此硫化后的废酸酸度为8.6%左右,其中金、银、砷含量都已经很低,而铁的含量较高,达到了12.85 g/L,具有较高的回收利用价值。

表1 某铜冶炼企业废酸成分
整个过程中的主要反应见式(1)~(4)。

(1)

(2)

(3)

(4)
此废酸中的铁主要以硫酸亚铁的形式存在,由于废酸的酸度较高,先用CaCO3中和废酸的pH在2.5~4.0之间,以减少沉淀过程的碱消耗;然后加入廉价的电石渣中和至溶液pH为7.5~8.0,目的是使溶液中的Fe2+完全沉淀为青绿色的Fe(OH)2沉淀;待沉淀完全后,缓慢滴加氯酸钠氧化,整个氧化过程中用电石渣维持溶液的pH在7.0~7.5之间,反应一定时间后,过滤、水洗,将得到的固体物质进行磁选分离,最终得到四氧化三铁。其工艺流程如图1所示。

图1 含铁废酸处理工艺流程图
2 试验结果与讨论
试验最终磁选时,影响选矿回收率的直接因素是氧化产物中磁性铁所占的比例,而磁性铁的占比量与氧化过程中溶液的起始pH值、氧化剂的用量、反应温度以及反应时间等影响因素有关。
2.1 氧化过程溶液起始pH值的影响
溶液的pH值对反应有很大的影响,pH值过低或过高都会导致一系列的副反应发生,影响产物中Fe3O4所占的比例,进而影响后续的磁选结果。控制反应温度90 ℃、反应时间2 h,氧化剂的加入量为溶液中Fe2+的2/3。在其他条件不变的情况下,改变溶液的起始pH值,研究氧化过程中溶液的起始pH对选矿回收率的影响,试验结果见表2。

表2 溶液的起始pH值对选矿回收率的影响
从表2可以看出,当溶液的pH低于7.0时,得到的固体物质中有黄色的颗粒状物质,选矿回收率较低。因为溶液中残留的硫酸将部分Fe(OH)2溶解,生成的硫酸亚铁与氧化剂反应生成了黄色的水合氢氧化铁,pH太低也会导致溶液中的Fe2+沉淀不完全。pH过高时,会带入大量的氢氧化钙,最终生成的硫酸钙也就越多,导致氧化产物颜色不纯正,降低产物中Fe3O4的占比,增加磁选的成本。另外氧化过程中会不断耗碱,导致溶液的pH有所下降,因此选择溶液的起始pH在7.5~8.0之间。
2.2 氧化剂加入量的影响
最廉价的氧化剂为空气,但是用空气作为氧化剂时,较难控制氧化的终点,试验最终选择氯酸钠作为氧化剂,其加入量的多少直接影响到氧化阶段Fe3O4的形成,加入量的多少最终体现为溶液中Fe3+/Fe2+的比例。调节溶液起始pH值为7.5~8.0、控制反应温度90 ℃、反应时间2 h,保持其他条件不变,探究氧化剂加入量的影响,试验结果见表3。
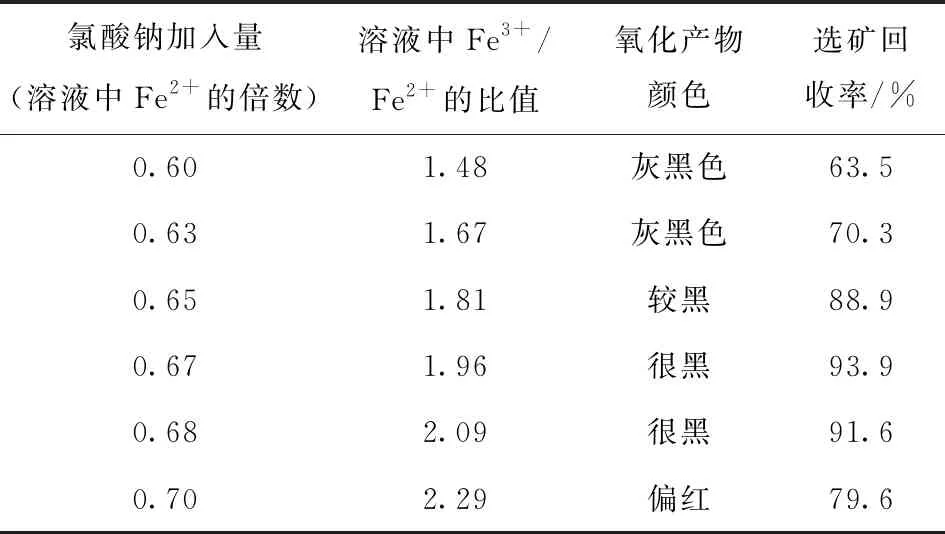
表3 氧化剂加入量的影响
注:氯酸钠加入量以氧化溶液中Fe2+的量计。
从试验结果可以看出,当Fe3+/Fe2+的比值在为1.9~2.1时,溶液颜色纯正,选矿回收率最高。当二者的比值低于1.9时,有一部分青绿色的Fe(OH)2存在,导致选矿回收率低于90%,当二者的比值高于2.1时,选矿回收率低于90%,因为过剩的氧化剂会影响反应(4)的进行,导致产物中存在部分Fe(OH)3。因此氧化阶段加入的氧化剂使得溶液中Fe3+/Fe2+的比值为1.9~2.1时即可。
2.3 反应温度的影响
一般情况下,在化学反应过程中,温度对反应能否进行、反应速率大小以及反应产物种类有很大影响。在合成磁性铁时,不同温度下所得的产物可能不同,所以合成磁性铁须在某一特定的温度进行。调节溶液起始pH值为7.5~8.0、氧化剂的加入量为溶液中Fe2+的0.67倍、反应时间2 h,在其他条件不变的情况下,改变反应温度,研究氧化过程中不同温度对选矿回收率的影响,试验结果见表4。
由表4可以看出,温度越高,得到的固体物质的颜色越黑。当温度低于80 ℃时,固体物质的颜色偏红,选矿回收率很低,这是因为温度较低时,反应(4)很难进行,而反应(3)却可以缓慢进行,生成了氢氧化铁。当温度高于80 ℃时,反应(4)可以进行,每生成一个Fe3+,便会立刻与一个Fe2+结合生成四氧化三铁,因此,氧化过程的反应温度控制在85~95 ℃比较合适。

表4 不同温度对选矿回收率的影响
2.4 氧化阶段反应时间的影响
选择最佳的反应时间尤为重要,过短则影响反应最终的产物,过长则降低工作效率,增加成本。调节溶液起始pH值为7.5~8.0,氧化剂的加入量为溶液中Fe2+的0.67倍,控制反应温度90 ℃,在其他条件不变的情况下,探究氧化阶段最佳的反应时间,结果见表5。

表5 反应时间的影响
从表5试验结果可以看出,当反应65 min后,选矿回收率可以达到80%以上,当反应时间延长至80 min后,选矿回收率达了到90%以上,继续延长反应时间,选矿率的变化不再明显,所以选择氧化阶段的反应时间为90 min为宜。
3 氧化产物分析
在试验得到的最佳条件下,制得的氧化产物显微镜和扫描电镜的照片如图2和图3所示。
由图2和图3可以看出:单偏光下磁铁矿呈不透明粒状颗粒,硫酸钙呈透明针状产出,硫酸钙粒度较粗;扫描电镜下可见磁铁矿同样在硫酸钙晶体表面结晶呈微细集合体产出。磁铁矿集合体粒度一般小于10 μm,硫酸钙长径一般小于25 μm,短径一般小于2 μm。
4 结论

图2 氧化产物显微镜(单偏光)照片

图3 氧化产物扫描电镜(背散射)照片
1) 对于某铜冶炼加工企业铁锍除砷后的废酸采用氧化制备磁性铁的方法进行处理,将其中的铁元素以四氧化三铁产品的形式回收后可直接出售,有一定的经济效益。整个工艺流程简单,成本较低,环境友好。
2) 考察了氧化反应过程中溶液起始pH值、氧化剂加入量、反应温度以及氧化反应时间等因素的影响,得出最优的反应条件:溶液起始pH值7.5~8.0,反应温度85~95 ℃,氧化反应时间90 min,氧化剂的加入量使得溶液中Fe3+/Fe2+的比值为1.9~2.1时最好,最终的选矿回收率可以达到90%以上。

