腐殖质改良植物修复重金属污染土壤的研究进展
胡梦淩,曾和平,董达诚,罗 昱,王 锦
(昆明理工大学环境科学与工程学院,云南 昆明 650000)
随着现代工业的发展,采矿、电镀、冶炼、肥料、杀虫剂、皮革、造纸和电子行业等将大量重金属和石油烃释放到自然生态系统中,严重破坏了生物有机体的正常生理功能[1-2]。2005年4月至2013年12月首次全国土壤污染状况调查结果表明,耕地土壤点位超标率较高,主要重金属污染物为砷(As)、铅(Pb)、镉(Cd)、铜(Cu)、汞(Hg)、镍(Ni);主要有机污染物为多环芳烃(PAHs)和滴滴涕(DDT)[3]。2016年5月28日国务院颁布实施《土壤污染防治行动计划》[4],迫切需要进行土壤重金属污染治理。
农田重金属污染土壤修复技术主要有物理修复、化学修复、生物修复、农业生态和联合修复[5]。重金属污染土壤修复需要注意在修复过程中保护土壤质量、生态系统和人类健康安全[6]。生物修复中的植物修复(phytoremediation)因不破坏土壤结构,不引起二次污染,修复成本低,具有植被恢复功能等优点,被认为是一种极具发展前景的污染土壤修复技术。但生物修复也存在一定局限性,超富集植物(hyperaccumulator)种植在中、高含量重金属土壤中会受毒害作用而导致植株地上部生物量小、生长缓慢等问题[7-8]。而且地区、气候、降雨量和土壤污染程度等因素都会影响植物存活率和富集率,严重限制植物修复的推广应用。开发在改良重金属污染土壤质量的同时又能提高超富集植物对重金属的富集能力的技术具有现实意义。这就需要解决在利用植物修复中、重度污染土壤时,既要确保修复植物的存活率又能提高植物对重金属的富集能力,以便拓宽植物修复的应用范围。因此,寻找可以降低土壤重金属毒性并且能促进植物生长的辅助试剂是提高植物修复重金属污染土壤的关键。
腐殖质(humic substances, HS)作为自然界土壤和水体中广泛存在的稳定的高分子聚合物,是由动植物残体通过一系列物理、化学和微生物分解合成而形成,具有复杂结构并包含羧基、醇羟基等多种活性官能团,对土壤中重金属的形态转化和迁移能力以及生物可利用性具有重要影响[9-11]。HS同时也是土壤肥力的一项重要指标,利用HS改良土壤,可降低土壤重金属毒性,促进植物生长,有助于植物修复的实际应用。但将HS与植物修复联合应用于重金属污染土壤治理的研究尚处于实验阶段。因此,笔者综合前人研究结果,探讨HS应用于植物修复重金属污染土壤的作用机制和可行性,以期为HS在重金属污染土壤植物修复中的应用提供依据。
1 HS与重金属结合的作用及其机制
1.1 HS对重金属单一结合作用
根据在不同pH条件下的溶解性,HS可分为胡敏素(humin, HM)、胡敏酸(humic acid, HA)和富里酸(fulvic acid, FA)[12]。HS主要由C、N、O、H和S组成,包含很多羧基、羟基、羰基和胺基等官能团(图1[13]),其中以羧基和酚羟基最为重要。许多络合物常由这2种功能基组配。HS络合(螯合)金属离子的形式主要分为2种:(1)共价结合,每个附加原子捐赠1个相关电子;(2)协调结合,即每个金属原子从非金属那里接收1对电子[14]。羧基有强酸性和弱酸性的区别,一般认为强酸性羧基形成的络合物最稳定。当pH值为5.0时,有80%的Fe3+和52%的Cu2+为强酸性羧基和酚羟基形成的络合物[15]。HA的羧基和酚羟基主要形成金属-腐植酸配合物[16]。许多研究[17]表明,FA比HA具有更高的金属结合能力,这主要是因为FA拥有较多的活性基团。
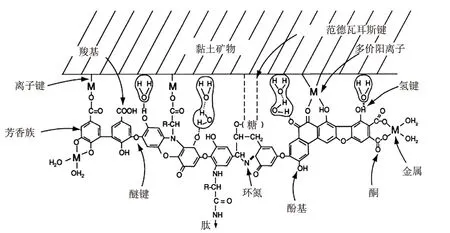
图1 黏土表面腐殖质与金属结合模型[13]
在污染严重的土壤中,分别有98%、82%和96%的有机结合态Cd、Pb和Zn存在于FA中。HA在Zn污染土壤中施用比在Cd污染土壤中施用更能降低重金属元素对植物的毒害。而在Zn和Cd复合污染土壤中施用HA可能会增加Cd的危害,而减少Zn的危害[18]。腐植酸一般指大分子HA,分子质量范围为50~100 kDa之间。而FA分子质量较小,一般为0.500~2 kDa[19]。施用大分子腐殖质(HA和HM)比小分子腐殖质(FA)更能降低重金属植物有效性。HA可与重金属络(螯)合形成不溶于水的大分子络(螯)合物,起到钝化作用。而FA则可与重金属络合形成水溶性络合物,增强重金属活性,提高重金属迁移能力。
HS与重金属结合的官能团主要为羧基和酚羟基,HABIBUL等[20]通过同步荧光、紫外可见吸收光谱结合光谱斜率和二维相关分析探讨了Pb2+与HA相互作用过程,证明羧基和酚羟基是HA与Pb2+结合的主要位点,相关性分析显示羧基结合Pb2+的能力要大于酚羟基(图2[20])。
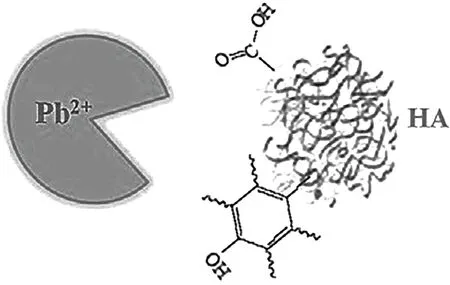
图2 Pb2+与HA官能团结合示意[20]
1.2 HS与其他修复剂协同作用
HA和HM能起到钝化重金属的效果,HA与其他修复剂协同使用可以提高对重金属的钝化效果,减小重金属对植物的毒害。有研究[21]表明,HA、过磷酸钙和粉煤灰3种钝化剂复配处理能促进污染土壤中Pb和Cd由活性高的弱酸提取态向活性低的残渣态转化,从而有效降低Pb和Cd的可迁移性和毒性。也有研究[22]利用生物质炭和腐植酸类物质钝化猪粪堆肥过程中产生的重金属Cu、Pb、Zn和Cd,其中添加以花生壳、玉米秸秆和木屑制成的生物质炭以及嘉博文腐植酸对重金属的钝化能力较好,且嘉博文腐植酸处理对Zn的钝化效果较好。而由于FA分子质量小,酸性基团多,与重金属络合后形成可溶性金属络合物,提高重金属迁移性,可作为淋洗剂。毕冬雪等[11]通过以富里酸钾为主的水溶性腐殖酸钾为淋洗剂活化土壤中Cd,发现腐殖酸钾去除土壤Cd的效率随淋洗剂浓度增加而增加,当ρ(腐殖酸钾)=10 g·L-1时,其对砂质土壤单次淋洗Cd去除率高达38.1%。
1.3 影响HS与金属离子结合作用因素
HS对结合的金属离子最大螯合量与HS酸性功能基含量直接相关,影响HS结合金属阳离子数量的因素包括HS溶液的pH值、离子强度、分子质量和功能基含量[18]。
1.3.1pH对HS结合重金属的影响
pH是决定土壤重金属去除效率的一个重要因素,影响土壤重金属的吸附-解吸行为[23]。李光林等[24]通过吸附-解吸实验发现,在酸性条件(pH<6.5)下,HA溶液pH越高,HA对Cd的吸附速度越快,吸附量越大,解吸越困难;随着pH降低,HA结合Cd的解吸速度越快,解吸总量越大。酸性条件下,与土壤胶体结合的金属离子容易被淋洗剂溶解,导致金属从稳定组分中释放解吸出来。ZHANG等[25]用芝麻秸秆堆肥提取的HS淋洗河道底泥,底泥Cd和Ni去除率随pH值的增加呈明显下降趋势。当pH值为3时,Cd去除率最高。这是由于(1)重金属在土壤颗粒表面的吸附随着pH值的降低而减弱,高pH有利于土壤提供更多的负电荷,从而增加其对金属离子的吸附位点[26-27];(2)在高pH体系中,Cd2+和Pb2+等金属离子易形成稳定的氢氧化物并沉淀,降低了其在土壤中解吸迁移能力[28]。
1.3.2其他因素对HS结合重金属的影响
影响HS与金属离子结合的因素还有离子强度、HS活性官能团含量和HS分子质量[18]。离子强度增加会抑制分子官能团的离解,胶粒间斥力减小而聚集性增加,HS胶粒聚集,位阻效应变大[29]。杨毅等[30]分别采用商用腐植酸和天然腐植酸与Cd2+结合发现,离子强度增加对腐植酸与Cd2+结合有抑制作用。Cd2+与腐植酸官能团结合难度增强,导致腐植酸与Cd2+的表观结合容量逐渐减小。活性基团含量和吸附能力呈正相关,活性官能团数量越多,可以吸附更多金属离子。HS与金属的结合能力随其分子质量的增加而减小,且分子质量小的FA比分子质量大的HM拥有更多的金属键合点位,可以吸附更多金属离子。FA与Hg2+的相互反应可以使Hg在水体和土壤中溶解性剧增,移动性加强,并且能使土壤矿物结合态或沉积物中Hg转化为腐植酸结合Hg[31];相反,HA可作为金属阳离子的集聚点,促进Hg在沉积物和土壤中的富集。
2 HS诱导在植物修复中的应用潜力
2.1 植物修复改良措施
由于很多超富集植物生物量较低,生长周期长,对环境敏感,易受外界气候、土壤影响,致使植物修复效率较低,推广应用受到限制。针对植物修复的影响因素,利用改良技术提高植物修复效率的相关研究已在国内外展开,改良方式主要为化学诱导、接种菌株强化和基因技术[32]。其中化学诱导是植物修复中最活跃、最快捷的技术,越来越受到广泛重视。化学诱导技术主要通过添加螯合剂活化土壤中重金属,使其转化为可溶态,更利于被植物吸收。常用的螯合剂包括乙二胺四乙酸(EDTA)、二乙基三胺五乙酸(DTPA)、乙二醇双(2-氨基乙基醚)四乙酸(EGTA)、柠檬酸和草酸等。JIANG等[33]在自配的Pb污染土壤中种植竹子并添加EDTA,随着EDTA浓度升高,土壤中可还原态和残渣态Pb含量下降,而弱酸提取态Pb含量增加。EDTA能促进土壤中Pb溶解,使竹子吸收并迁移Pb到植株各部位。螯合剂诱导为化学手段,可以很快促进植物对重金属的富集,不过很多螯合剂无法被土壤微生物降解,容易造成二次污染或损伤植物组织。也有研究使用乙二胺二琥珀酸三钠(EDDS)和聚天冬氨酸(PASP)等可生物降解螯合剂作为改良剂。ATTINTI等[34]将香根草种植在野外人造板上,分别在生长3和13个月后施用EDDS,发现使用EDDS不仅能提高Pb在土壤中的溶解度,而且能提高香根草根系对Pb的吸收,促进Pb从植株根系向地上部的转移。在第1次和第2次施用EDDS后,香根草茎中Pb平均浓度分别提高53%和203%,根部分别提高73%和84%。LINGUA等[35]采用盆栽试验对比了将EDTA和EDDS以质量比3∶2混合以及单独添加PASP对银白杨(Populusalba)吸收Cu和Zn的影响,发现EDTA和EDDS混合使用会促进Cu在叶片中积累而抑制Zn,添加PASP能显著促使Cu在植物根部积累和稳定。
虽然EDTA、EDDS和PASP等化学螯合剂可以促使土壤中金属溶出并向植物体内迁移,但其通常不能被土壤微生物降解,会造成土壤的二次污染,且会对植物组织产生一定损伤。而可生物降解螯合剂一般价格较贵,不适合农田大规模应用。所以选择环境友好、价格低廉的诱导剂显得尤为重要。HS来源广泛,可以从农业废弃物和市政污泥中提取。作为化学诱导剂,HS对促进植物修复重金属污染土壤具有明显优势,除对环境无害外,HS还能改善土壤的物理、化学和生物特性[36]。HS可以为植物生长提供养分,促进植物生长,提高生物量,增加超富集植物对重金属的吸收。因此,作为自然界广泛存在的大分子有机弱酸,HS可以作为合成螯合剂的替代品提高植物对土壤重金属的萃取量。
2.2 HS对植物生长的影响
HS是土壤有机质的主要组成部分,其质量约占土壤有机质总质量的85%~90%[37]。HS可以将细小的矿物土壤颗粒粘结成更大的团粒以增加和保持土壤孔隙度[38],同时对植物菌根的形成有重要作用[39]。大部分植物根系会与土壤真菌形成共生关系,土壤有机质可以促进真菌菌丝生长加快,并且有机质含量与菌丝、泡囊和总定殖率呈正相关。丛枝菌根的发育可以促使植物获得更多生长所需的营养物质[40]。所以在土壤中适当添加HS可以改善土壤质量,还可以促进植物生长。与未添加HA相比,当HA用量为2 g·kg-1时,油菜生物量增加35.3%~70.6%[41]。HS不仅可以提高植物生物量,还可以促进植物对营养物质的吸收。袁天佑等[42]利用田间定位试验,研究HA与无机肥料配施对夏玉米产量、氮素吸收及氮肥利用率的影响,发现施用HA可以有效改善夏玉米农艺性状,提高夏玉米产量,促进植株对氮素的累积,提高氮肥利用率。李军等[43]将不同比例HA加入尿素中,发现与仅施普通尿素处理相比,添加HA的处理均可显著提高玉米地上部生物量和籽粒产量,分别提高5.5%~13.8%和6.3%~17.3%,且随HA添加量的增加而提高。
HS可以促进植物根系发育和优化叶片气孔行为,从而使植物在一定温度、光照和CO2浓度条件下维持相对较高的光合同化能力。张佩[44]在铅锌尾矿土壤上种植香根草,添加经腐化后w(HS)=20%的5 kg桔梗和枯草,与未添加HS处理相比,HS处理香根草根系长度由22 cm提高到51 cm。同时,未添加HS的香根草生长受重金属抑制,添加HS后植物株高、分蘖数、叶片大小、根长、地上部干重和根系干重呈现增加趋势。不仅如此,HS调节气孔行为(改善气孔器数量、大小和分布),提高导度和蒸腾速率[45]。HS在促进植物蒸腾和光合作用的同时为植物补充了其生长所需养分,对植株生物量提高和根系发育都有一定促进作用。
2.3 HS对植物吸收重金属的影响
2.3.1HS影响重金属积累部位
HS中FA分子质量较小,活性基团多,其与重金属结合后形成易溶于水的络合物,能提高重金属活性和迁移性。FA不仅可以促进植物对重金属的吸收,还可以促进重金属从植株地下部向地上部迁移。孙磊[46]研究发现当FA浓度增加到一定量时,Cd主要富集在茎、叶和果实中,而As主要富集在玉米棒中,其吸收过程分为2个阶段:(1)FA与重金属高效结合,并跨越细胞壁被植物吸收,重金属在根部积累减少;(2)随着FA浓度增加,玉米中As和Cd含量均呈上升趋势。HS不仅可以促进作物对重金属的吸收,还可以促进超富集植物吸收的重金属由地下部向地上部迁移,这在添加HS后香根草对铅锌尾矿中重金属抗性试验中表现得尤为突出。香根草主要为地下部富集重金属,但添加HS后香根草富集和吸附特点发生明显变化,更多的重金属向香根草地上部分迁移[44]。HS具有亲水性(hydrophilicity)和疏水性(hydrophobicity)[47],疏水性与亲水性的比值(HB/HL)可用于表征HS对根系发育的影响。HS的HB/HL值越大,添加后其促进植物根系发育的效果就越好。PITTARELLO等[48]研究发现在Cd胁迫下,添加HS可以缓解Cd对红树林(亮叶白骨壤)种子的毒害,与未添加HS处理对比,添加含碳量2、4和8 mmol·L-1的HS处理都可显著促进亮叶白骨壤根长和根面积。HS对植物吸收和积累金属的影响包括直接作用和间接作用,HS可络合(螯合)阳离子从而间接改变其在营养液中的浓度,也可直接影响植物膜渗透性或干扰活性离子吸收载体和机制。
2.3.2HS不同施加方式影响重金属吸收
HS能促进植物根系生长、养分吸收,以及植物对环境胁迫的耐受性[49]。不同添加方式会影响植物吸收重金属效果,添加方式主要可分为叶面喷施和土壤添加。在Cd污染土壤中种植莴苣(Lactucasativa),使用0.5 g·L-1的FA进行叶面喷施,结果表明FA能明显减轻Cd对莴苣幼苗的毒害作用,可以缓解Cd胁迫引起的植物生长抑制、光合色素减少、光合机构破坏和活性氧积累等问题。叶面喷施FA可提高莴苣对Cd的去除能力,抑制植株吸收Cd的同时,也抑制了营养元素向地上部转运,从而保护光合器官,保障植物正常生长[50]。而在土壤中直接添加HS,小分子质量的FA可促进土壤中金属溶解并向植物地上部转运。BANDIERA等[51]在富含Cu、Cr、Co、Mn和Zn且有机质含量较低的基质中种植饲料萝卜(RaphanussativusL. var.oleiformisPers.),将0.1和1 g·kg-1HA按基质混合添加、基质表层添加和叶面喷施3种方式添加以研究HA对植物吸收重金属的影响,发现基质添加低浓度(0.1 g·kg-1)HA对萝卜茎叶生长有促进作用并且增加植物对重金属的转移量;而高浓度(1 g·kg-1)HA对植株有毒害作用,但对叶面喷施0.1 g·L-1HA可缓解高浓度添加带来的负面效应。当植物重金属含量较高时,HS会影响植物对氮的吸收以及叶片光合色素完好性,叶面喷施和土壤添加HS对植物吸收重金属会产生不同效应。叶面喷施HS可以抑制重金属向植物地上部转移并保护光合系统;而土壤中添加HS,低浓度条件下可以促进植物对重金属的转运并且缓解重金属对植物的毒害,高浓度条件下则会对植物产生负面效应。因此,在有机质含量较低的贫瘠土壤中直接添加低浓度HS更有利于植物修复应用,提高超富集植物对重金属的富集。
3 HS对土壤修复应用潜力
3.1 HS与重金属生态毒理学效应
3.2 HS应用的环境风险分析
应用HS和植物联合修复重金属污染土壤不仅可以降低重金属对植物的毒害,还可以促进植物生长,且不会造成环境二次污染。在土壤中添加HS溶液时可以采用土柱淋溶实验进行浸出风险评估,评价诱导剂对植物修复造成的次生环境风险。LUO等[54]利用细胞分裂素辅助EDTA进行植物修复并评价修复过程中的生态风险,在14 d的实验中共使用10 990 mL溶液,未种植植物的处理溶液浸出量很大,而种植植物的处理浸出量明显降低。这说明植物可以通过根系吸收和叶片蒸腾等方式阻止土壤溶液向下移动。细胞分裂素与EDTA共用的处理浸出量比单独使用细胞分裂素的处理少,这是因为EDTA可对植物组织产生一定损伤,减少植物对水分的吸收。CHEN等[55]通过土柱淋溶实验也得到相似结果,EDTA能使植物叶片黄化并对幼苗产生毒害,会增加重金属进入地下水的风险。但使用HS作为促进剂则不会出现以上情况,这是因为HS作为土壤有机质重要组成,不仅可以为植物生长提供营养,还能促进植物根系发育和幼苗生长。植物根系发育良好,可以提高根系对土壤溶液持水性,溶液会逐渐被植物吸收,不会下渗污染地下水。所以HS应用于植物修复重金属污染土壤时不会造成次生环境风险。
4 存在的问题与研究展望
HS来源广泛,可以利用畜禽粪便、农业废弃物和厨余垃圾等进行堆肥提取。这不仅可以缓解垃圾处理问题,还可以使废弃物得到充分资源化利用。不同来源的HS可能会对重金属钝化或活化效果产生巨大影响。在利用植物修复重金属污染土壤时,选择FA含量高的HS,可更有效地促进重金属向植物体内迁移。而低水平重金属污染农田则可利用HM和HA钝化,直接降低重金属活性,减少农作物吸收。目前,根据实际需求选择钝化或活化重金属的HS组分以达到土壤修复目的显得尤为重要,将HS与植物修复联合应用还需根据选用的修复植物特性确定相关参数。
在重金属污染土壤中施用HS对改善土壤肥力和缓解重金属对植物毒害的效果较好,具有操作安全、无二次污染、不破坏土壤理化性能等优点。该技术既可用于农田重金属污染土壤修复,也可用于污染场地修复,极具开发潜力。目前就HS组分对重金属吸附-解吸行为和重金属形态变化影响的研究较多,未来还需关注HS组分对土壤理化性质及土壤生物的影响。土壤理化性质在修复前后的变化,不同来源HS对修复效果的影响,以及对土壤动物、微生物等土壤生物学指标的影响,为HS作为重金属污染土壤修复剂的实际应用奠定理论依据。

