氯乙酸甲酯精馏工艺理论塔板数计算及设计
冯 明, 李迎春, 王现洋, 李晓琼, 程伟琴, 王柏楠, 霍二福,4
(1.河南省化工研究所有限责任公司,郑州 450052; 2.平顶山市神马万里化工股份有限公司,河南平顶山 467000;3.兰博尔开封科技有限公司,河南开封 475003; 4.河南省科学院质量检验与分析测试研究中心,郑州 450008)
在化工生产过程中大多数粗产品都是两组分或多组分的混合物,为满足生产和使用要求,需要将这些混合物分离、提纯. 精馏是工业领域应用最广泛的分离技术,具有易于大规模生产应用、技术成熟可靠等优点[1]. 精馏过程是最典型也是最重要的多级分离过程,进行多次部分气化和部分冷凝,使混合液得到几乎完全的分离[2-3],也是在液体混合物的分离过程中最早实现工业化的单元操作.
精馏过程是利用待分离混合液中各组分相对挥发度的差异,经过多次气化和多次冷凝,使液相中的轻组分不断向气相富集,气相中的重组分不断向液相富集,从而达到轻重组分分离的目的[4-5]. 在精馏过程中精馏塔是其核心设备,而理论塔板数的计算在精馏塔的设计中是一项很重要的参考数据,是衡量实际板分离效率的依据和标准. 精馏塔的设计中要先求得理论板层数,用塔板效率予以校正即可求得实际板层数,因此理论塔板数对精馏工艺的分析、计算和设计起到十分重要的作用.
1 氯乙酸甲酯生产工艺简介
氯乙酸甲酯为无色透明液体,有刺激性气味,微溶于水,主要用作溶剂、有机合成原料. 在农药上主要用于合成杀虫剂乐果、氧乐果的中间体硫磷酯、氧硫磷酯及氯乙酰甲胺等;用于医药、黏接剂、表面活性剂的制备. 制药工业用于制取咖啡碱、肾上腺素、氨基醋酸等[6].
氯乙酸甲酯采用氯乙酸与甲醇经酯化反应制备,方法如下:将甲醇与氯乙酸按质量比0.336∶1 混合均匀,在105~110 ℃下进行搅拌酯化反应. 反应过程中不断蒸出氯乙酸甲酯、水和甲醇的三元共沸物,经酯水分离器分离,将分出的甲醇和水重新回流入反应釜内,分出的氯乙酸甲酯粗酯经水洗、中和含量可达到89%以上. 由于该氯乙酸甲酯主要用于农药中间体,其含量达不到要求,要对其进行减压精馏、提纯.
2 精馏塔理论塔板数计算
2.1 计算依据
氯乙酸和甲醇通过酯化反应得到氯乙酸甲酯粗酯,其中氯乙酸甲酯含量89%,水含量11%. 为达到生产和销售要求,需要对其进行减压精馏. 计算依据:减压精馏方式,蒸馏釜投料9000 kg,塔压强13.332 2 kPa,釜残液水<0.5%,塔顶馏出液水>98%.
2.2 计算方法
化学工程中精馏塔的理论塔板数N是精馏塔设计的一个重要数据,板式精馏塔的设计首要的是理论塔板数的计算[7],它与最小回流比Rm、回流比R及最小理论塔板数Nm间具有一个复杂的函数关系.
时景荣、罗传义等[8]的图解法求理论塔板数的基本原理是用平衡线和操作线分别代替平衡方程和操作线方程,用简便的图解法代替繁杂的计算. 虽然图解法的准确性较差,但因其简便,目前在两组分精馏计算中被广泛采用.
彭小平、颜清等[9]的迭代法求理论塔板数是利用物料的气-液相平衡关系和操作线方程联立得到提馏段和精馏段的迭代方程Xn+1=f(Xn),然后利用提馏段的迭代方程由塔釜液相组成开始,逐板算出提馏段各块塔板的液相组成,同时将Xn+1与Xq(由q线方程联立操作线方程所确定)比较,确定进料板位置;进料板位置确定以后,改用精馏段的迭代方程求算精馏段各块塔板的液相组成(注意进料板液相组成必须用精馏段的迭代方程重算),直至Xn+1等于或越过Xd为止,n即为该分离操作所需的理论塔板数.
Gilliland等[10]求理论塔板数是根据五十多种双组分及多组分精馏的实验数据,将最小回流比Rm、回流比R、最小理论塔板数Nm与理论塔板数N进行关联,于1940年发表了以(R-Rm)/(R+1)为横坐标值、(N-Nm)/(N+1)为纵坐标值的非线性关系图形. 当已求得最小回流比Rm,回流比R及最小理论板数Nm时,则先算出(R-Rm)/(R+1)值,利用所画的非线性关系图形,查出对应的纵坐标值(N-Nm)/(N+1),解之即可求出理论塔板数N值.
2.3 计算过程
本文采用图解法来进行理论塔板数的计算.
2.3.1 全塔各组分的计算
水的摩尔质量18 g/mol,氯乙酸甲酯的摩尔分数109 g/mol.
进料中水的摩尔分数XF=(11/18)/(11/18+89/109)=0.43;
馏出液中水的摩尔分数XD=(98/18)/(98/18+2/109)=0.996 7;
釜残液中水的摩尔分数XWE=(0.5/18)/(0.5/18+99.5/109)=0.029 6;
原料液的平均摩尔质量MF=0.43×18+0.57×109=69.87;
原料液流量F=9000/69.87=128.81 kmol/h.
2.3.2 饱和蒸气压与温度的关系方程
1)水的饱和蒸气压与温度的关系方程
安托因方程[11-16]是一个最简单的三参数,用于描述纯组分的饱和蒸汽压P°与温度t的关系,该方程适用于大多数化合物. 其方程式如下:

式中:A、B、C为组分的安托因常数,不同物质对应于不同的A、B、C的值;P°为温度t对应下的纯液体饱和蒸气压,mmHg;t为温度,℃.
经查安托因常数表,水的安托因常数A、B、C分别为7.966 81、1 668.21、228.0,代入安托因方程,求得水的饱和蒸汽压(mmHg)与温度(℃)的关系方程式,如下:

2)氯乙酸甲酯的饱和蒸汽压与温度的关系方程
由于缺少氯乙酸甲酯的基础物化数据,无法用安托因方程求得其饱和蒸汽压与温度的关系方程,因此采用估算法求得. 实用的估算方法[17-22]包括对应状态法和基团贡献法,因已知氯乙酸甲酯的临界参数,故选择对应状态法进行求解. 对应状态法是指所有物质在相同的对应状态下具有相同的对比性质,是关联实际气体及液体物性的一个重要原理.
对应状态法中Clapeyron方程[23-25]提供了纯组分饱和蒸汽压与温度的基本关系方程,已知纯组分的临界参数,即可求出其饱和蒸汽压与温度的关系.基本方程式如下:
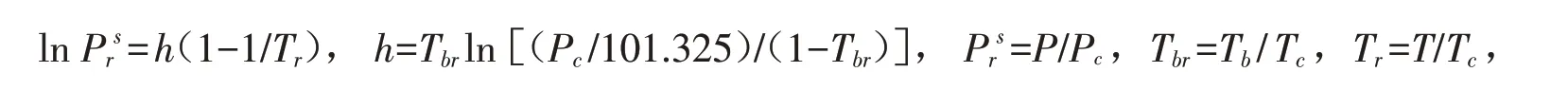
式中:Prs为对比蒸汽压;Pc为临界压强;P为饱和蒸汽压;Tr为对比温度;Tbr为对比沸点;Tb为常压沸点;Tc为临界温度;T为温度.
已知氯乙酸甲酯的常压沸点Tb=402.95 K;氯乙酸甲酯的临界温度Tc=600 K;氯乙酸甲酯的临界压力
Pc=4500 kPa.
将上述已知条件代入Clapeyron方程中,得到氯乙酸甲酯的饱和蒸汽压(kPa)与温度(℃)的关系方程如下:

2.3.3 气液平衡时气液相摩尔分数组成与平衡温度间的关系式
根据两组分理想物系的气液平衡关系,气液平衡是由n个组分的混合物构成一个封闭系统,并有气-液两相共存,一定的温度和压力下,两相达到平衡时,各组分在气液两相中的化学位趋于相等. 得到气液相组成与平衡温度间的关系式如下:

式中:X表示液相中水的摩尔分数;Y表示气相中水的摩尔分数;P表示精馏塔塔顶总压强,P=13.332 2 kPa(即100 mmHg).
2.3.4 绘制水-氯乙酸甲酯的X-Y图
根据方程(1)、(2)、(3)计算的结果列于表1,根据表1计算结果,绘制出X-Y图(图1).
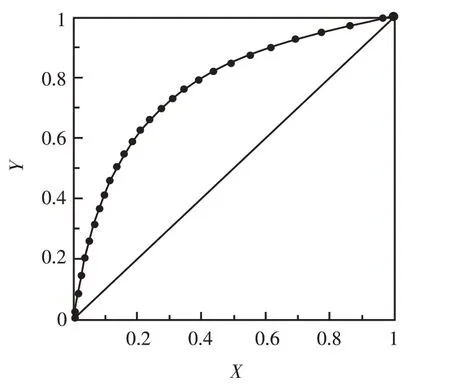
图1 X-Y 图Fig.1 Graph of X-Y
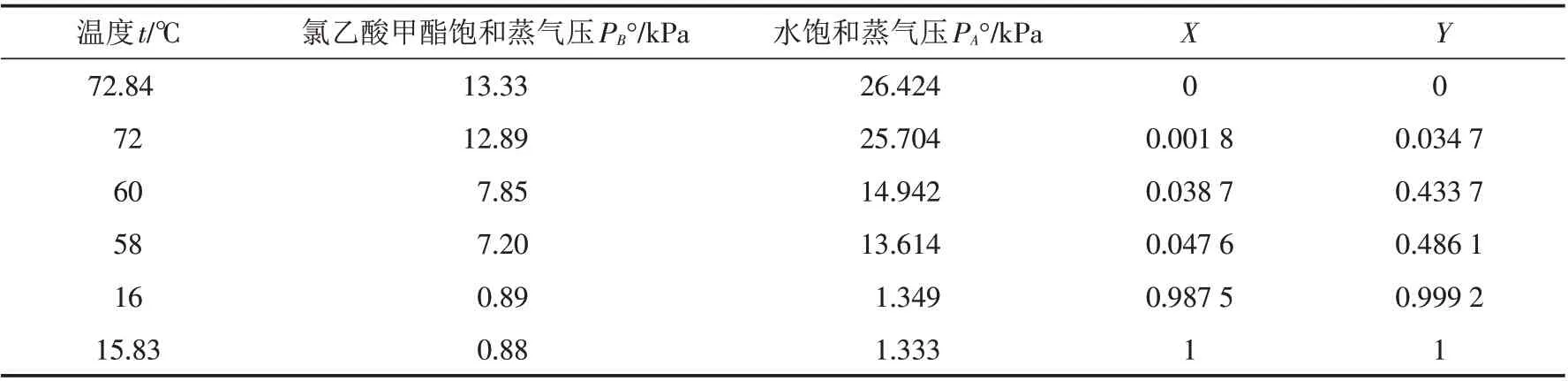
表1 X-Y计算结果Tab.1 The calculation results of X-Y
在图1中查得:最终釜残液中水摩尔分数XWe=0.029 6时,与XWe呈平衡的气相中水的摩尔分数YWe=0.372 1.
2.3.5 回流比的计算
依据回流比的影响及其选择方法[26],最小回流比与馏出液中水的摩尔分数XD、最终釜液中水摩尔分数YWe以及与YWe呈平衡的气相中水的摩尔分数YWe存在以下关系:
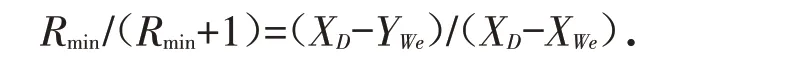
求解得出最小回流比关系式:

将XD、XWe、YWe数值代入,求得最小回流比
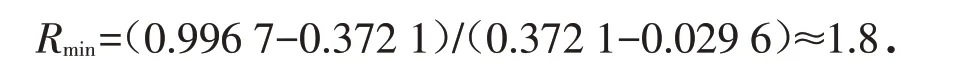
回流比

2.3.6 图解法求理论塔板数
1)计算操作线截距XD/(R+1)=0.331 13,在X-Y 图的Y 轴上定出点b.
2)连接点a(XD,XD)和点b,所得的直线即为此回流比下的操作线.
3)从点a开始在平衡线和操作线间绘梯级,直至梯级铅垂线达到或超过点(XWe,XWe)为止,每一个梯级代表一层理论板.
由图2可知理论塔板数NT为7.
2.3.7 液体黏度-温度关系式的求取
为求取全塔效率,需求得水、氯乙酸甲酯的黏度与温度关系.
1)水的黏度-温度关系式
由化工物性数据[14]查得水的黏度与温度关系如表2所示.

图2 图解法求理论塔板数Fig.2 Graphical method for theoretical plate number

表2 水的黏度与温度关系Tab.2 The viscosity temperature relationship of water
2)氯乙酸甲酯的黏度-温度关系式
由于缺少氯乙酸甲酯的黏度-温度关系式的系数值,因此采用估算方法中的基团贡献法求取氯乙酸甲酯的黏度-温度关系式. 基团贡献法(简称基团法)是将化合物性质与分子的基团构成相联系,其基本假定是纯物质或混合物的性质等于构成此物质或混合物的各种基团对该化合物性质贡献值的总和.
Orrick-Erbar法的黏度-温度的基本计算式如下:

式中:d20是20 ℃下液体密度;M是摩尔质量(g·mol-1);ηL的单位为cp;A,B是基团贡献值(表3).

表3 基团贡献表Tab.3 Table of group contribution
2.3.8 塔顶与塔底温度的计算
采用内插法计算塔顶与塔底温度,内插法是指利用等比关系中的数学直线内插,即用一组已知函数自变量的值和与之对应的函数值来求解另一个未知函数值的计算方法,其基本公式如下:

式中:(a1,a2)、(b1,b2)为已知值,(c1,c2)中已知c1,求c2.
已知塔顶液相组成XD=0.996 7,从表1中查得,当温度为16 ℃时,液相中水的摩尔分数为0.987 5;当温度为15.83 ℃时,液相中水的摩尔分数为1.
将上述数值代入内插公式求得塔顶温度tA:

塔顶温度tA=16.31 ℃.
已知塔底液相组成XWe=0.029 6;从表1中查得,当温度为60 ℃时,液相中水的摩尔分数为0.038 7;当温度为58 ℃时,液相中水的摩尔分数为0.047 6.
将上述数值代入内插公式求得塔底温度tB:

则塔底温度tB=63.06 ℃.
2.3.9 相对挥发度的计算
相对挥发度是指溶液中易挥发组分的挥发度对难挥发组分的挥发度之比,以α表示,它表示气相中两组分的摩尔分数比为与之成平衡的液相中两组分摩尔分数比的α倍,其计算公式为α=PA°/PB°,式中:PA°表示在一温度下溶液中易挥发组分的饱和蒸汽压;PB°表示在此温度下溶液中难挥发组分的饱和蒸汽压.
在温度tA=16.31 ℃下,由公式(1)求得水的饱和蒸汽压PA°=1.376 kPa;由公式(2)求得氯乙酸甲酯的饱和蒸汽压PB°=0.91 kPa.
代入计算公式得:塔顶的相对挥发度αD=15.12. 在温度tA=63.06 ℃下,由公式(1)求得水的饱和蒸汽压PA°=17.191 kPa;由公式(2)求得氯乙酸甲酯的饱和蒸汽压PB°=8.94 kPa.
代入计算公式得:塔底的相对挥发度αW=19.23,平均相对挥发度的计算公式如下:将αD、αW的数值代入上式,求得平均相对挥发度为-α=17.05.

2.3.10 黏度计算
1)塔顶黏度计算:当塔顶温度TA=tA+273.15=289.46 K,由水的黏度与温度关系表查得此温度下的水的黏度ηL1=1.106 mPa·s.
由公式(4)求出此温度下的氯乙酸甲酯黏度ηL2=2.27 mPa·s,塔顶黏度μD=XD×ηL1+(1-XD)×ηL2=0.996 7×1.106+(1-0.996 7)×2.27=1.11 mPa·s.
2)塔底黏度计算:当塔底温度TB=tB+273.15=336.21 K,根据水的黏度与温度关系表查得此温度下的水黏度η′L1=0.445 mPa·s.
根据公式(4)求出此温度下的氯乙酸甲酯黏度η′L2=3.00 mPa·s,塔底黏度μW=XWe×η′L1+(1-XWe)×η′L2=0.029 6×0.445+(1-0.029 6)×3.00=2.91 mPa·s.
3)全塔平均黏度计算:μm=(μD+μW)/2=2.01 mPa·s.
2.3.11 全塔效率计算
全塔效率ET=0.49(αμm)-0.245=0.21.
2.3.12 实际塔板数的计算
实际塔板数NP=NT/ET=33.3≈34(块).
2.3.13 氯乙酸甲酯精馏工艺设计
根据理论计算结果设计了带有“液-液分离器”的氯乙酸甲酯精馏装置(图3),由输液泵将氯乙酸甲酯粗品泵入到精馏釜,开启真空泵,维持系统真空100 mmHg,加热精馏釜升温至60 ℃;开启间歇全回流精馏,当精馏塔的塔顶温度维持在38 ℃时,打开储液罐上方的阀门1,关闭阀门2和3,前馏分经冷凝器全部收集在储液罐中,静置进行液-液两相分离,待前馏分夹带出来的氯乙酸甲酯置于液-液分离装置后,开启液-液分离装置下方的阀门2,将氯乙酸甲酯流至精馏釜中,液-液分离装置中氯乙酸甲酯完全分离、流回精馏釜后,关闭阀门2;当精馏塔的塔顶温度达到65 ℃时,前馏分完全馏出后,关闭储液罐上方阀门1,开启氯乙酸甲酯的成品储液罐进料阀门3,当塔顶温度达到75 ℃时,成品氯乙酸甲酯出料结束;氯乙酸甲酯的收率为80%,氯乙酸甲酯含量99.8%以上,氯乙酸甲酯馏出液中水含量0.1%以下;当精馏塔的塔顶温度达到75 ℃,停止加热,待精馏釜中物料温度降至40 ℃时,放出精馏釜中的残液,完成间歇精馏工艺操作.
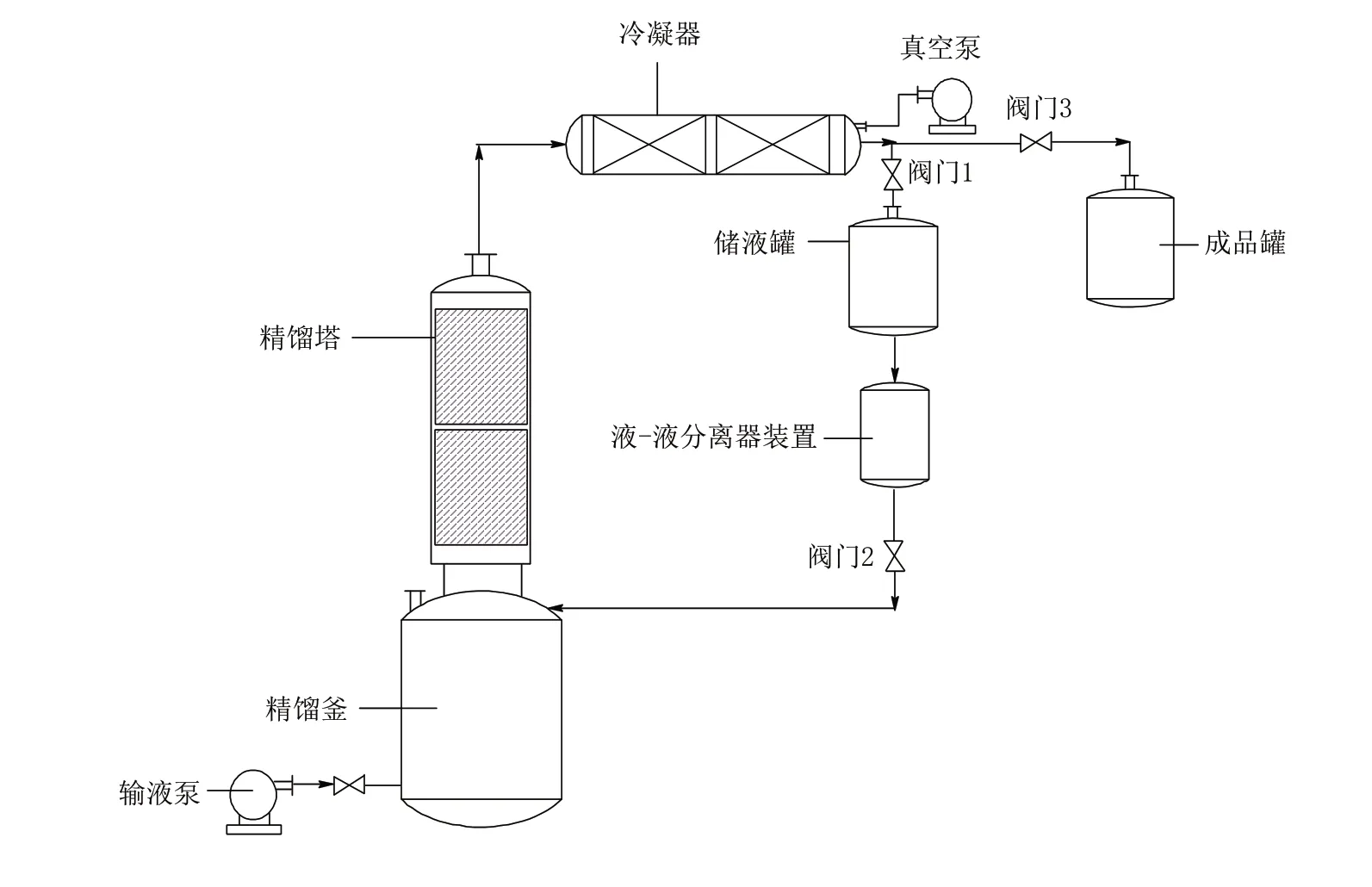
图3 氯乙酸甲酯精馏工艺设计流程图Fig.3 Flow of distillation process design of methyl chloroacetate
3 结论
针对氯乙酸甲酯精馏塔釜液中水和氯乙酸甲酯的二元体系,采用安托因方程、Clapeyron 方程、Orrick-Erbar法和图解法对氯乙酸甲酯精馏塔理论塔板数进行计算,精馏塔的理论塔板数为7块,实际塔板数34块,全塔效率0.21;根据理论计算结果设计了带有“液-液分离器”的氯乙酸甲酯精馏装置. 经工业化实施表明,将前馏分中的水和氯乙酸甲酯进行分层,将下层氯乙酸甲酯回流进塔釜,最大限度地分离出氯乙酸甲酯,使氯乙酸甲酯馏出液中水含量达0.1%以下,氯乙酸甲酯含量99.8%以上,氯乙酸甲酯的总回收率高于80%,减少了氯乙酸甲酯精馏残液的产生量,避免了资源浪费和环境污染,精馏工艺具有处理成本低、投资少、操作稳定、效率高等优点,环境效益、经济效益和社会效益显著.

