拉贝洛尔对妊娠高血压综合征病人CRP、CysC水平及分娩结局的影响
妊娠期高血压综合征(pregnancy induced hypertension syndrome,PIH)是产科常见、多发疾病,主要发生在妊娠20周后,基本病理改变为全身小动脉痉挛,临床表现为血压升高、生理性水肿、蛋白尿等症状[1]。据相关文献统计,目前我国PIH发病率约为9.4%[2],该病可累及多个器官,影响胎盘功能,严重时发生抽搐、昏迷,是孕产妇及新生儿死亡的主要原因之一。对症治疗是PIH的主要治疗措施,既往以硫酸镁解痉为主,辅以降压、适当扩容、使用利尿剂以及镇静等[3]。但其降压速度较慢,在临产危重时刻难以及时控制症状,因而影响分娩结局及预后。拉贝洛尔作为水杨酸氨衍生物,能够选择性竞争性拮抗α、β肾上腺素能受体,扩张外周血管,缓解动脉痉挛[4]。美国食品与药品管理局针对妊娠期控制血压药物的使用提出了参考意见,认为拉贝洛尔可作为选择之一。本研究观察了拉贝洛尔对妊娠高血压综合征病人血清C反应蛋白(CRP)、胱抑素C(CysC)及分娩结局影响,旨在为临床诊治妊娠高血压提供参考,为临床选择合理治疗方案提供理论依据。现报道如下。
1 资料与方法
1.1 临床资料 将2017年1月—2018年5月我院妇产科收治的96例PIH病人作为研究对象,均符合世界卫生组织(WHO)提出的PIH临床诊断标准。入组标准:①孕周>20周,且单胎妊娠;②血压>140/90 mmHg(1 mmHg=0.133 kPa);③伴有蛋白尿、生理性水肿等临床症状;④知晓本研究内容,本人或家属签署知情同意书。排除标准:①既往有慢性高血压病史;②多胎妊娠;③原发性心血管、肾、肝疾病以及糖尿病、免疫变态反应性疾病等相关病变;④合并急慢性感染性疾病;⑤处于产程活跃期;⑥存在拉贝洛尔用药禁忌证。根据所有研究对象入院顺序进行编号,采用随机数字表法分为对照组与拉贝洛尔组。对照组48例,年龄20~33(29.78±4.09)岁;孕周27~37(33.42±4.45)周;初产妇33例,经产妇15例;疾病严重程度:轻度30例,中度15例,重度3例。拉贝洛尔组48例,年龄20~35(29.93±4.13)岁;孕周27~40(33.69±4.51)周;初产妇30例,经产妇18例;疾病严重程度:轻度25例,中度16例,重度7例。两组年龄、孕周、疾病严重程度等临床基线资料比较,差异无统计学意义(P>0.05),具有可比性。本研究已通过我院医学伦理委员会审核批准。
1.2 治疗方法 入院后,病人均取侧卧位,限制食盐摄入量、活动量,补充维生素、营养素,给予降压、解痉、吸氧、抗癫痫、镇静、补液等综合治疗,积极预防并发症发生。对照组予硫酸镁注射液(上海旭东海普药业有限公司,国药准字H31020666,规格10 mL:2.5 g)5 g+5%葡萄糖注射液100 mL,30 min内静脉输注,后续将20~25 g硫酸镁注射液+5%葡萄糖注射液1 000 mL,静脉输注,速度为1.0~2.0 g/h,每日1次。密切监测血镁离子浓度、膝反射等防止镁离子中毒;拉贝洛尔组加用拉贝洛尔注射液(江苏迪赛诺制药有限公司,国药准字H32026121,规格10 mL:50 mg)50 mg+5%葡萄糖注射液250 mL,静脉输注,速度为1~4 mg/min,每日1次。两组用药期间监测生命体征、预防直立性低血压发生等,均持续治疗7 d。
1.3 观察指标 ①血压:采用台式水银血压计测量治疗前后病人08:00~09:00及15:00~16:00血压;②炎症因子:采集治疗前后清晨平静状态下空腹外周静脉血5 mL,3 000 r/min离心15 min,分离血清,待检。采用贝克曼库尔特AU5800系列全自动生化分析仪及配套试剂盒检测血清CRP、肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)水平;③肾功能:采用免疫投射比浊法检测血清CysC水平,乳胶增强免疫比浊法检测尿微量白蛋白(mALB)、24 h尿蛋白,试剂盒均购自南京建成生物科技有限公司,严格按照试剂盒说明书进行操作;④分娩结局:胎儿窘迫/胎盘早剥、胎心异常、终止妊娠、产后出血、新生儿窒息等。

2 结 果
2.1 两组血压比较 治疗前,两组收缩压、舒张压比较,差异无统计学意义(P>0.05);治疗后,两组收缩压、舒张压较治疗前显著降低(P<0.05);拉贝洛尔组收缩压、舒张压较对照组降低明显(P<0.05)。详见表1。

表1 两组治疗前后收缩压、舒张压比较(±s) 单位:mmHg
2.2 两组血清炎症因子水平比较 治疗前,两组血清CRP、TNF-α、IL-6水平比较,差异无统计学意义(P>0.05);与治疗前比较,治疗后两组血清CRP、TNF-α、IL-6水平显著降低(P<0.05);与对照组比较,治疗后拉贝洛尔组血清CRP、TNF-α、IL-6水平显著降低(P<0.05)。详见表2。

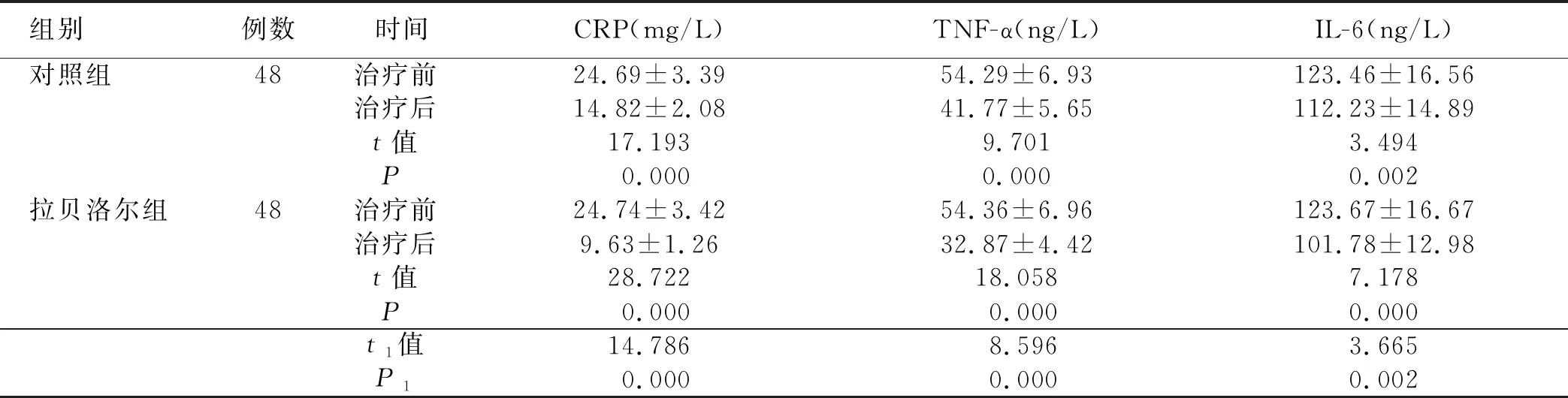
组别例数时间CRP(mg/L)TNF-α(ng/L)IL-6(ng/L)对照组48治疗前24.69±3.3954.29±6.93123.46±16.56治疗后14.82±2.0841.77±5.65112.23±14.89t值17.1939.7013.494P0.0000.0000.002拉贝洛尔组48治疗前24.74±3.4254.36±6.96123.67±16.67治疗后9.63±1.2632.87±4.42101.78±12.98t值28.72218.0587.178P0.0000.0000.000t1值14.7868.5963.665P10.0000.0000.002
注:t1、P1为对照组与拉贝洛尔组治疗后比较的统计值。
2.3 两组肾功能指标比较 治疗前,两组CysC、mALB、24 h尿蛋白比较,差异无统计学意义(P>0.05);与治疗前比较,治疗后两组CysC、mALB、24 h尿蛋白显著降低(P<0.01);与对照组比较,拉贝洛尔组CysC、mALB、24 h尿蛋白显著降低(P<0.01)。详见表3。

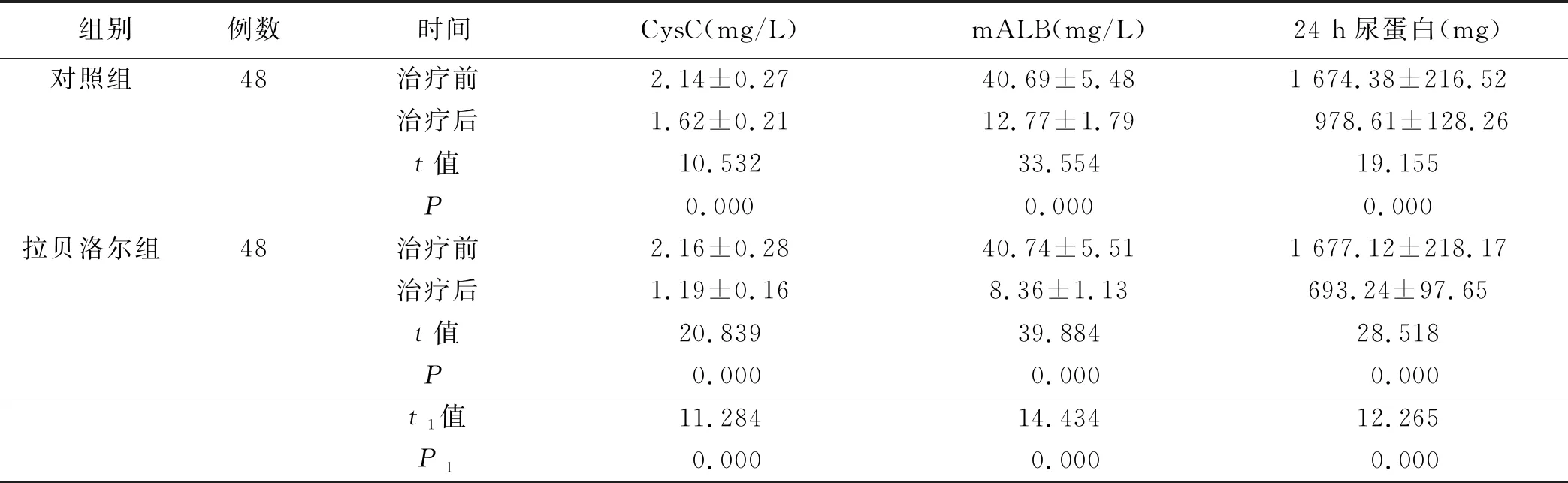
组别例数时间CysC(mg/L)mALB(mg/L)24 h尿蛋白(mg)对照组48治疗前2.14±0.2740.69±5.481 674.38±216.52治疗后1.62±0.2112.77±1.79978.61±128.26t值10.53233.55419.155P0.0000.0000.000拉贝洛尔组48治疗前2.16±0.2840.74±5.511 677.12±218.17治疗后1.19±0.168.36±1.13693.24±97.65t值20.83939.88428.518P0.0000.0000.000t1值11.28414.43412.265P10.0000.0000.000
注:t1、P1为对照组与拉贝洛尔组治疗后比较的统计值。
2.4 两组分娩结局比较 与对照组比较,拉贝洛尔组胎儿窘迫/胎盘早剥、产后出血发生率较低(P<0.05);两组胎心异常、终止妊娠、新生儿窒息发生率比较,差异无统计学意义(P>0.05)。详见表4。
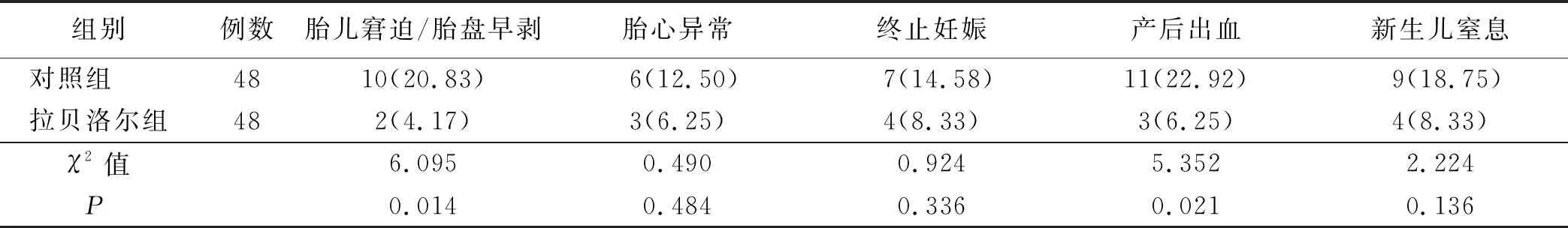
表4 两组分娩结局比较 单位:例(%)
3 讨 论
PIH是妊娠期特有的并发症,严重危害母婴健康。近年来PIH病因研究较多,但确切原因尚不明确,可能与孕期不良心理、生育年龄、体重、产次及高血压家族史等有关[5]。多数学者认为,全身小动脉痉挛为高血压病理特征,血管内皮细胞损伤及激活则是PIH的主要发病机制[6]。病人发病后常会出现水肿、抽搐、昏迷、蛋白尿及肾功能损害,因此不容忽视。临床上治疗PIH主要方法为降压、解痉、吸氧、镇静、补液等,并做好相关并发症预防措施。同时应注意饮食,控制体重,避免过度摄入食盐,钠盐摄入过多可增大血管的外周阻力,使病人血压升高[7]。
有效控制血压是改善妊娠高血压的关键,目前临床治疗PIH主要原则是解痉降压,拉贝洛尔是临床应用最为广泛的药物。拉贝洛尔作为水杨酰胺衍生物,对α、β肾上腺素能受体有选择性阻滞作用。对α受体阻滞作用能够扩张病人外周血管容量,从而降低外周阻力,减轻病人心脏前负荷,其在降低病人血压水平作用较明显[8],不影响脑、肾、子宫、胎盘、胎儿的血流灌注。此外,阻滞α受体还能够促进胎儿肺功能成熟,避免血小板凝聚现象[9]。对β受体阻滞作用较强,使心脏传导时间减慢,能够相应抵消部分血压降低所引起的心动过速,降低心肌耗氧量,增加心输出量,提高肾脏血流灌注[10]。有研究表明,拉贝洛尔为α、δ受体激动剂,能降低儿茶酚胺分泌及交感神经兴奋性,并降低心脏前负荷、扩张血管、减少心脏做功,从而达到降血压目的,且降压持久、快速[11]。Xie等[12]报道给予妊娠期高血压疾病病人拉贝洛尔治疗后,能够有效降低及稳定病人心率,停药后无反跳现象,但不适用于窦性心动过缓、哮喘、严重房室传导阻滞。同时,在降压的同时能够增加肾脏血流量,但不改变肾小球滤过率,有效改善肾脏功能[13]。最近1项Meta分析亦证实,拉贝洛尔不仅能够预防轻中度高血压向重度高血压发展,还能预防单纯高血压向子痫前期发展,有利于减少严重并发症发生[14]。
PIH主要病理特征为全身小动脉痉挛[15],其导致管腔狭窄,周围血管阻力增大,血管内皮细胞通透性增加,致使体液和蛋白质渗漏增加,临床表现为血压升高、蛋白尿、水肿等。由此可见,有效控制血压是治疗PIH的关键。本研究结果显示,两组治疗后收缩压、舒张压较治疗前显著降低(P<0.05),但拉贝洛尔组下降更加明显(P<0.05),表明拉贝洛尔可有效控制PIH病人血压。PIH病人存在内皮细胞损伤,引起机体内免疫反应失调,使某些免疫复合物沉积在肾脏,激活补体系统,导致血管损伤且通透性增加,从而使肾小球、肾小管受损,产生大量蛋白尿[16],而炎症因子在其中起到重要作用。CRP作为炎症反应标志物,由活化巨噬细胞分泌炎症细胞因子促进肝脏合成释放所致,其可结合卵磷脂及核酸,通过经典途径激活补体系统产生大量终末反应蛋白沉积而致使血管内膜损伤[17]。TNF-α通过释放氧自由基直接损伤血管内皮,使全身小动脉痉挛,造成管腔狭窄,周围阻力增大。IL-6则与TNF-α等炎症因子相互促进、相互诱导,损害血管内皮细胞,血管通透性增加,促进血管钙离子浓度升高,引起血管收缩和血压升高,最终出现一系列PIH临床表现。本研究结果显示,与对照组比较,拉贝洛尔组治疗后血清CRP、TNF-α、IL-6水平显著降低(P<0.01),说明拉贝洛尔通过缓解全身小动脉痉挛,扩张血管,减轻血管内皮损伤及免疫失衡,从而使血液CRP浓度降低。
孕妇随着孕周增加,其机体可能会出现某些病理、生理改变,尤其妊娠期高血压疾病、妊娠期糖尿病等并发症,容易对肾脏造成损害,可能危及孕妇与胎儿生命安全,因此,临床对PIH病人肾功能损伤的早期诊断尤为重要。mALB是肾小球滤过膜允许通过的一种较小的蛋白,正常状态下其几乎被近曲小管全部重吸收,只有当肾小球病变时,mALB 滤过量超过肾小管重吸收量才会导致尿中有mALB出现。近年来认为尿mALB是反映肾脏功能病变可靠及灵敏的指标[18]。CysC是一种由机体有核细胞以恒定的速率产生的常见糖基蛋白,正常生理状态下,肾小球能够完全过滤血液中CysC,当其流经肾小球时,可以被近曲小管重吸收并完全代谢,不出现肾小管的分泌与重吸收现象,因此血液中CysC一直是反映肾功能受损程度的内源性标志物质。PIH病人肾小球处于高过滤、高灌注状态,孕妇及胎儿的代谢产物、血容量增加会导致病人出现不同程度肾功能损害,促使血液中CysC 浓度升高[19]。24 h尿蛋白定量检查是评估肾功能的常用指标,对肾小球损伤判断早于血肌酐。本研究结果显示,拉贝洛尔组CysC、mALB、24 h尿蛋白显著低于对照组(P<0.01),提示拉贝洛尔通过降低病人血压,减少肾脏血流量,保护肾功能,与谢桂英等[20]报道一致。
综上所述,拉贝洛尔能够有效控制PIH病人血压,保护肾脏功能,改善临床分娩功能,以上作用与下调机体CRP等炎症因子表达有关。

