早发性卵巢功能不全患者体成分分析
蔡 雯 浦丹华 陶新城 从 静 吴 洁
南京医科大学第一附属医院/江苏省人民医院,江苏省妇幼保健院(210029)
早发性卵巢功能不全(POI)以月经紊乱(如停经或稀发月经)伴有高促性腺激素和低雌激素为特征[1-2]。本研究通过测定POI患者的体成分,评估其营养状况,以期减少POI患者潜在代谢疾病的风险。
1 资料与方法
1.1 研究对象
收集2017年5月—2019年5月在南京医科大学第一附属医院妇科内分泌门诊确诊的90例POI患者为研究对象,初诊年龄13~39岁,就诊原因主要为第二性征发育不良、月经紊乱、闭经、不孕等。同期收集90例月经正常(卵巢功能正常)的女性作为对照组。本研究经医院伦理委员会批准,患者均知情同意并签署同意书。
1.2 研究方法
1.2.1诊断标准①年龄<40岁;②月经稀发或停经≥4个月;③≥2次血清基础卵泡刺激素(FSH)>25U/L(间隔>4周)。
1.2.2体成分测定通过人体成分分析仪(InBody S10,拜斯倍斯医疗器械贸易有限公司)对研究对象进行体成分测定。测试在禁食8h清晨空腹进行。 测定项目包括:①体重、腰臀比、体脂肪、内脏脂肪面积(VFA)、去脂体重(FFM)、蛋白质和肌肉重;②成分评价:体质指数(BMI)和体脂率(PBF)。
1.2.3性激素检测于月经期第2~4天或闭经时随机上午空腹检测外周血,应用化学发光法测定雌激素(E2)水平。根据E2水平分为3组,<74pmol/L组42例,≥74~148pmol/L组35例,>148pmol/L组13例。
1.3 数据分析
2 结果
2.1 一般情况
POI组体重、BMI和腰臀比均高于对照组(P<0.05),见表1。
2.2 体成分分析
2.2.1POI组与对照组比较POI组全身脂肪含量、PBF和VFA高于对照组(P<0.05);POI组与对照组的去脂体重、蛋白质和肌肉等成分无差异。见表2。
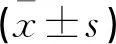
表1 两组对象一般情况比较
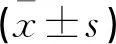
表2 两组体成分指标比较
2.2.2不同E2水平组比较不同E2水平组年龄与身高均无统计学差异。体重、BMI和体脂相关指标(全身脂肪含量、 PBF、VFA),E2<74pmo/l组均低于≥74~148pmol/L组与>148pmol/L组(P<0.05),而E2≥74~148pmol/L组与>148pmol/L组无统计学差异(P>0.05),见表3。
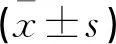
表3 POI患者不同E2水平组一般情况及体成分比较
3 讨论
POI患者随着卵巢功能逐渐衰退,会先后出现月经改变、潮热出汗和骨量下降等雌激素缺乏症状[3]。人体生物电阻抗分析(BIA)技术是利用人体中不同成分的导电性差异测定人体成分的含量,一般采用仰卧位[4-5]。传统BMI是诊断和评估肥胖严重程度最重要的指标,BMI的增加往往会显著增加脂肪量,尤其是绝经后,但对于瘦型体重而言脂肪量增加并不明显[6],BIA技术可以较全面评估人体营养状况。
本文中POI患者的体重、BMI、腰臀比和体脂相关指标(全身脂肪含量、PBF、和VFA)较健康对照组明显增高,这与Franklin等[7]研究基本一致。POI患者体质指数升高可能与雌激素下降所致的脂肪重新分布有关[8],这将影响其远期健康,如肥胖、高血压、高血脂、糖代谢异常和心血管疾病等风险增加。
根据雌激素水平对POI患者体脂进行分析,结果显示雌激素水平相对较高时(E2≥74pmol/L),体脂相关指标较高。推测可能原因:①脂肪组织在雄激素的芳香化过程中起着重要的作用,体脂较高女性的雌激素较高,这与Eldridge等[9]报道的雌激素水平与体脂的关系一致。有研究表明,绝经女性内脏脂肪组织成为雌激素的主要来源,部分弥补了卵巢雌激素分泌的减少,雌激素分泌的减少导致内脏脂肪的膨胀,而内脏脂肪的膨胀反过来又会分泌更多的雌激素,所以绝经女性因雌激素低导致内脏脂肪增加,形成腹型肥胖[10]。而本文POI患者年龄相对较轻,大部分患者并未进入卵巢完全衰竭状态,所以绝经后雌激素和脂肪的关系不完全适用于POI患者;②绝经后/围绝经女性的雌激素水平可能受到除了脂肪组织以外的其他因素的影响[9];③最重要的是,POI患者在卵巢功能逐渐衰退的过程中卵泡刺激素(FSH)逐渐升高,而雌激素水平呈波动性下降,且POI患者就诊时卵巢衰退程度不同,因此雌激素差异较大,其与体脂相关指标的关系存在一定的异质性;④本研究POI样本量相对较少导致数据可能存在偏倚。目前国内外关于POI激素水平和体脂关系报道极少,所以本研究根据雌激素将POI分组,初步探讨卵巢不同衰退状态下脂肪水平。据报道,与体重正常的女性相比,在成年早期或中期体重过轻的女性,早绝经的风险更高[11]。Khorram等[12]报道,低出生体重的后代发生卵巢早衰可能是成年后发生肥胖和高瘦素血症的继发性原因。此外,糖尿病可能增加女性提前绝经风险,其体内雌激素比正常女性耗竭得更快,从而增加心血管和骨骼疾病风险[13]。
本研究结果显示,POI组较正常女性组身高偏低,推测原因可能是部分患者就诊时尚在青春发育期,未达到最终身高,同时由于雌激素不足影响生长发育导致身高偏低。雌激素可通过减少骨吸收和刺激骨形成保护骨组织,而POI由于雌激素低下,导致骨量积累不足。大量研究表明,肥胖增加某些部位骨折的风险,肥胖的绝经后妇女增加踝关节和上肢骨折的风险[14]。
此外,POI组与正常对照组去脂体重、蛋白质和肌肉等成分无明显差异;但雌激素水平较低的POI患者蛋白质和肌肉量明显低于雌激素较高者。也有研究指出,POI患者的肌肉强度和肌肉质量均有下降[15],所以应强调优质蛋白的补充。有研究报道,激素替代治疗(HRT)可能间接影响骨骼肌蛋白的转化,从而中和与年龄相关的肌肉质量和力量的丧失[16]。因此,只要没有禁忌证,POI患者均应给予HRT[17-18]。
综上所述,体成分分析可充分评估临床上POI患者营养状况,尽管未发现POI患者存在明显的营养不良,但存在超重/肥胖和身高不足的问题。临床实践中,对年轻患者需注重生长与骨量的积累,对年龄较大、病史长的患者应关注代谢疾病风险,治疗上除保持积极良好的心态,适量运动,适当补充钙剂及维生素D,最重要的是综合评估激素治疗指征并尽早启动,定期行体成分分析将有助于更好地管理POI的生命周期,降低潜在代谢相关疾病的风险。

