中药外敷配合内服加味海七丸治疗膝骨性关节炎的临床研究
黄桂忠, 王少伟, 蔡煜林
(广东省汕头市中医医院骨科,广东汕头 515031)
膝骨性关节炎(knee osteoarthritis,KOA)是中老年人常见病、多发病,多因膝关节的局部损伤及炎症和慢性劳损引起关节面软骨变性,软骨下骨板反应性骨损,从而导致膝关节出现一系列的症状和体征。据流行病学统计数据[1]显示,女性患者发病率远高于男性患者,其致残率可高达50%以上,严重影响患者生活质量。随着社会的发展和逐步的老龄化,该病的发病率呈逐年上升趋势,因此,如何更好地治疗中老年人KOA具有重大的现实意义。现代医学治疗多以消炎止痛等对症处理为主,后期关节变形严重、疼痛难忍者多以关节置换术、截骨术等手术治疗为主[2],给患者身心健康带来严重影响的同时也加重了家庭的经济负担。目前,中医药在治疗KOA方面发挥着重要的作用。笔者根据本地区患者实际情况,制定简单、价廉的治疗方法,采用自制中药包外敷患膝及口服加味海七丸治疗KOA患者,取得满意的疗效,现将研究成果报道如下。
1 对象与方法
1.1 研究对象及分组 选取2017年1月至2018年6月在广东省汕头市中医医院骨科门诊及住院部就诊的明确诊断为KOA的患者,共120例,其中男37例,女83例。按患者就诊次序,采用随机数字表将患者随机分为治疗组和对照组,每组各60例。
1.2 诊断标准 参照2007年中华医学会骨科分会制定的骨关节炎诊治指南(2007年版)[3]:①近1个月反复发生的关节痛;②X线片(宜站立位或负重位)示关节间隙变窄、软骨下硬化和(或)囊性变、关节炎骨赘形成;③关节液检查无明显改变[清亮、黏稠,白细胞(WBC)<2 000/mL];④X线片改变不明显,但患者年龄≥40岁;⑤有≤30 min的晨僵;⑥活动时有关节摩擦音(感)。综合临床、实验室及X线检查,符合①②或①③⑤⑥或①④⑤⑥者即可诊断为KOA。
1.3 纳入标准 ①符合上述KOA诊断标准且无其他膝部疾病;②下肢力线尚可,膝关节无明显畸形;③无严重内科疾病及其并发症;④同意参加本研究并签署知情同意书的患者。
1.4 排除标准 ①既往有外伤病史的患者;②下肢力线差,膝关节外观明显畸形的患者;③存在严重内科疾病及其并发症的患者;④不按规定方法配合治疗,或自行加用其他有治疗作用的药物或方法的患者;⑤拒绝跟踪随访或随访中断的患者。
1.5 治疗方法
1.5.1 治疗组 给予中药外敷配合加味海七丸内服治疗。(1)中药外敷。中药包为院内制剂,处方如下:丁香、桂枝、红花、路路通各10 g,络石藤30 g,当归、五加皮各20 g,羌活15 g。将处方上不同剂量中药切碎,然后将每剂125 g药材装进大小约20 cm×20 cm的布包内并将封口装订,形成1个立体药包。使用方法:①先将药包放置水中浸泡;②将浸泡过的药包捞起,放置于锅内蒸20~30 min,以药包发热为度;③每日热敷2次,每个药包可重复使用6次;④使用时用毛巾包起,以防烫伤;⑤使用完毕后放通风处,以便下次使用时再浸泡。(2)中药内服。加味海七丸(为院内制剂,制作方法:党参15 g、海马15 g、西洋参10 g、白术15 g、白芍15 g、枸杞子10 g、淫羊藿15 g、骨碎补30 g等共为细末,炼蜜为丸),口服,每日1次,每次6 g,疗程为1个月。
1.5.2 对照组 给予塞来昔布胶囊口服治疗。用法:塞来昔布胶囊(辉瑞制药有限公司进口分包装;批准文号:国药准字J20140072)口服,每日1次,每次0.2 g,疗程为1个月。
1.6 观察指标及疗效评价
1.6.1 临床疗效评价 参照《中药新药临床研究指导原则》[4],观察膝关节疼痛、晨僵、活动度等治疗前后变化,计算相应积分。积分减少率=(治疗前积分-治疗后积分)/治疗前积分×100%。①临床控制:症状消失,关节活动正常,积分减少率≥95%。②显效:症状消失,关节活动不受限,70%≤积分减少率<95%。③有效:症状基本消失,关节活动轻度受限,30%≤积分减少率<70%。④无效:症状与关节活动无明显改善,积分减少率<30%。总有效率=(临床控制例数+显效例数+有效例数)/总例数×100%。
1.6.2 西安大略和麦克马斯特大学骨关节炎指数(WOMAC)[5]评分 观察2组患者治疗前后WOMAC评分的变化情况。WOMAC评分共包括3方面内容:①关节疼痛程度;②关节僵硬程度;③膝关节活动功能情况。分数越高,症状越严重。
1.6.3 Lysholm评分[6]观察2组患者治疗前后Lysholm评分的变化情况。Lysholm评分内容包括:是否跛行,是否需要支撑,有无交锁症状,关节是否不稳定,肿胀程度,以及上楼、下蹲疼痛程度。
1.6.4 炎症指标检测 观察2组患者治疗前后血清白细胞介素1(IL-1)、肿瘤坏死因子α(TNF-α)水平的变化情况[7]。有学者[8]认为,骨关节炎中软骨基质的降解和破坏,与细胞因子的合成和分解代谢的平衡失调相关。
1.7 统计方法 采用SPSS 20.0统计软件进行数据的统计分析。计量资料以均数±标准差()表示,组间比较采用两独立样本t检验,组内治疗前后比较采用配对样本t检验;计数资料以率或构成比表示,组间比较采用χ2检验;等级资料组间比较采用秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 2组患者基线资料比较 2组患者均获随访,时间为0.5~1年。治疗组60例患者中,男19例,女41例;年龄41~72岁,平均(56.21±7.07)岁;病程1~28个月,平均(1.91±3.78)个月。对照组60例患者中,男18例,女42例;年龄40~79岁,平均(58.74±6.96)岁;病程1.2~25.8个月,平均(1.98±3.67)个月。2组患者的性别、年龄、病程、病情等基线资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 2组患者临床疗效比较 表1结果显示:治疗1个月后,治疗组的临床控制率及总有效率分别为56.67%和93.33%,对照组分别为20.00%和73.33%;组间比较,治疗组的总体疗效(秩和检验)、临床控制率及总有效率(χ2检验)均优于对照组,差异均有统计学意义(P<0.05或P<0.01)。

表1 2组患者临床疗效比较Table 1 Comparison of clinical efficacy in the two groups [n/例(p/%)]
2.3 2组患者治疗前后WOMAC量表评分比较 表2结果显示:治疗前,2组患者WOMAC量表各项评分及其总分比较,差异均无统计学意义(P>0.05)。治疗后,2组患者WOMAC量表各项评分及其总分均较治疗前降低(P<0.05),且治疗组的降低作用均明显优于对照组,差异均有统计学意义(P< 0.05)。
2.4 2组患者治疗前后Lysholm量表评分比较 表3结果显示:治疗前,2组患者Lysholm量表各项评分及其总分比较,差异均无统计学意义(P>0.05)。治疗后,2组患者Lysholm量表各项评分及其总分均较治疗前升高(P<0.05),且治疗组的升高作用均明显优于对照组,差异均有统计学意义(P< 0.05)。
表2 2组患者治疗前后WOMAC量表评分比较Table 2 Comparison of WOMAC scores in the two groups before and after treatment (,s/分)
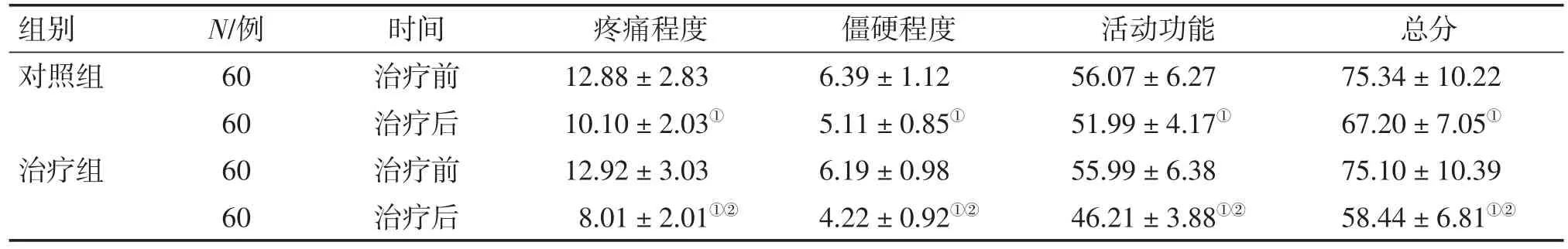
表2 2组患者治疗前后WOMAC量表评分比较Table 2 Comparison of WOMAC scores in the two groups before and after treatment (,s/分)
①P<0.05,与治疗前比较;②P<0.05,与对照组治疗后比较
组别对照组治疗组总分75.34±10.22 67.20±7.05①75.10±10.39 58.44± 6.81①②N/例60 60 60 60时间治疗前治疗后治疗前治疗后疼痛程度12.88±2.83 10.10±2.03①12.92±3.03 8.01± 2.01①②僵硬程度6.39±1.12 5.11±0.85①6.19±0.98 4.22± 0.92①②活动功能56.07±6.27 51.99±4.17①55.99±6.38 46.21± 3.88①②
表3 2组患者治疗前后Lysholm量表评分比较Table 3 Comparison of Lysholm scores in the two groups before and after treatment (,s/分)

表3 2组患者治疗前后Lysholm量表评分比较Table 3 Comparison of Lysholm scores in the two groups before and after treatment (,s/分)
①P<0.05,与治疗前比较;②P<0.05,与对照组治疗后比较
组别对照组治疗组总分46.24±24.29 58.09±25.74 47.48± 23.08①65.88± 21.55①②N/例60 60 60 60时间治疗前治疗后治疗前治疗后跛行2.06±0.89 3.11±0.98①2.13±0.85 3.82± 0.64①②支持3.91±0.61 4.11±0.78①3.93±0.85 4.01± 0.74①②交锁7.42±4.23 9.12±4.69①7.56±4.85 11.01± 4.75①②不稳定10.18±5.63 13.37±6.76①10.56±4.96 15.01± 4.81①②肿胀5.02±3.21 5.88±2.69①5.06±3.11 6.79± 2.74①②上楼5.23±3.12 5.91±2.78①5.45±2.61 6.24± 2.49①②下蹲2.13±0.88 3.12±0.93 2.11±0.86①3.87± 0.65①②疼痛10.29±5.72 13.47±6.13 10.68±4.99①15.13± 4.73①②
2.5 2组患者治疗前后血清IL-1和TNF-α水平比较 表4结果显示:治疗前,2组患者血清IL-1和TNF-α水平比较,差异均无统计学意义(P>0.05)。治疗后,2组患者血清IL-1和TNF-α水平均较治疗前明显降低(P<0.05),且治疗组的降低作用均明显优于对照组,差异均有统计学意义(P< 0.05)。
表4 2组患者治疗前后血清IL-1和TNF-α水平比较Table 4 Comparison of serum IL-1 and TNF-α levels in the two groups before and after treatment[,ρ/(pg·mL-1)]

表4 2组患者治疗前后血清IL-1和TNF-α水平比较Table 4 Comparison of serum IL-1 and TNF-α levels in the two groups before and after treatment[,ρ/(pg·mL-1)]
①P<0.05,与治疗前比较;②P<0.05,与对照组治疗后比较
TNF-α 36.32±8.76 25.01±7.86①36.39±8.97 24.23± 7.94①②组别对照组治疗组N/例60 60 60 60时间治疗前治疗后治疗前治疗后IL-1 16.97±2.86 10.12±2.13 17.04±3.07 10.03±2.04
3 讨论
膝骨性关节炎(KOA)是一种常见的慢性退行性疾病,多发病于中老年患者,以关节疼痛、活动受限、下肢关节畸形为主要症状。本病应属于中医学“骨痹”“膝痹病”的范畴。《黄帝内经》中有“肾主骨”“肝主筋”的记载。《素问》中曰:“骨痹,是人当挛节也”;“病在骨,骨重不可举,骨髓酸痛,寒气至,名曰骨痹”;“风寒湿三气杂至,合而为痹也。其风气盛者为行痹,寒气盛者为痛痹,湿气盛者为著痹”。《景岳全书》亦曰:“痹者闭也,以气血为邪所闭,不得通行而病也”。可见在中医学方面,本病的病因病机与老年患者肝肾亏虚、肢体筋脉失养,外感风寒湿邪,长期慢性劳损、筋骨受累等相关。《济生方·痹》亦云:“皆因体虚,腠理空疏,受风寒湿气而成痹也。”其中,正气虚弱、肝肾亏虚为内在因素,感受风寒湿邪为外在因素,内外因相互作用,从而形成本病本虚标实之证。
白细胞介素1(IL-1)是由单核细胞、内皮细胞、成纤维细胞和其他类型细胞在应答感染时产生的细胞因子。而肿瘤坏死因子α(TNF-α)是一种主要由巨噬细胞和单核细胞产生的促炎细胞因子,参与正常炎症反应和免疫反应。有研究[9]表明,老年骨性关节炎患者炎症因子与疾病活动具有相关性,能在一定程度上通过患者炎症水平反映患者的疾病严重程度。因此,抑制炎症反应对治疗KOA具有重要意义。现代医学治疗KOA多以消炎止痛为首选方法,常用口服非甾体类抗炎药(NSAID)。本研究所使用的塞来昔布胶囊,为选择性环氧化酶-2抑制剂,隶属于解热镇痛抗炎的NSAID类。与传统的NSAID相比,塞来昔布具备较低的消化道不良反应,且镇痛抗炎疗效确切,故本研究选其作为对照药。但也有研究[10]表明,长期使用仍会引起胃肠道黏膜的损伤风险。
随着中医领域对本病研究的不断深入,较多研究[11-12]表明,中医药治疗KOA疗效确切,能明显降低炎性因子,在缓解膝关节局部症状、改善膝关节功能、降低WOMAC评分方面均取得不俗的成果。可见针对本病,采取中药外用加内服治疗具有一定优势,尤其是使用中药外敷,能直接作用于患膝局部,具有明显优势。本院所使用的中药包由丁香、桂枝、红花、路路通、络石藤、当归、五加皮、羌活等中药组成,方中当归、红花活血袪瘀,行气止痛;络石藤、路路通、五加皮、羌活袪风除湿,行痹止痛;桂枝温经通络,散寒止痛;丁香温中暖肾。诸药合用,共奏活血化瘀、袪风除湿、行痹止痛之功效。结合本病本虚标实的特点,给予配合内服由党参、海马、西洋参、白术、白芍、枸杞子、淫羊藿、骨碎补等中药组成的加味海七丸,方中党参、白术补益脾气,淫羊藿、海马补肾壮阳,骨碎补补肾强骨,续伤止痛,白芍柔筋止痛;诸药合用,达到补益脾肾、袪风湿、止痹痛之功效。内服与外用配合,补正与祛邪兼施,从而达到标本同治的效果。
本研究结果表明,中药外敷配合内服加味海七丸治疗KOA,疗效满意,能有效降低WOMAC评分,提高Lysholm评分,降低血中炎症因子水平,改善膝关节功能,提高患者生活质量,具有较高的临床推广价值。但由于本研究的病例数较少,随访时间不长,对内服加味海七丸还缺乏相应的药理和毒理方面的数据支持,其有效性还有待多中心、大样本的随机对照试验的进一步证实。

