利用轻烧镁粉制备纳米氢氧化镁工艺与机理研究
李 男,冉 言,杜高翔,帅 欢,任凤国,王 佼
(1.中国地质大学(北京)材料科学与工程学院,北京 100083;2.非金属矿物与固废资源材料化利用北京重点实验室,北京 100083;3.北京工业职业技术学院基础教育学院,北京,100042)
0 引 言
氢氧化镁是一种新型绿色高效无机非卤型材料,因兼具阻燃、热稳定性好、高效、无毒、抑烟、阻滴、环保及填充安全等优点[1],被用于塑料橡胶等有机材料的无卤阻燃、酸性废水的中和处理和制药等多个领域。近年来研究发现,将轻烧镁粉通过进一步加工处理可以获得纳米氢氧化镁,不但可以降低纳米氢氧化镁的制作成本,还可以利用纳米材料的特殊性能用于环境废水治理中等多领域。如陈志航等[2]以氯化镁、氢氧化钠为原料,采用双注-水热法制备出高分散氢氧化镁纳米片,其粒径为130~150 nm。Wu 等[3]以硝酸镁和氢氧化钠为反应物,采用微波辅助合成法制备出了纤维状氢氧化镁纳米粒子。吴健松等[4]采用微波-水热高压釜制备出氢氧化镁晶须,其晶形好、粒度分布均匀、纯度高。龙旭等[5]采用低温回流法合成出多晶、长径比较高的一维(或准一维)氢氧化镁纳米丝和纳米棒。赵华等[6]利用轻烧镁为镁源,氢氧化钠为沉淀剂制备了高纯片状氢氧化镁,结果表明,制备的氢氧化镁纯度高达98%以上,颗粒分布均匀,形貌规整。朱国才等[7]在专利中研究了从菱镁矿煅烧轻烧粉制备纳米氧化镁的方法。此方法得到的纳米氧化镁的粒度为15~50 nm,纯度达98.7 %。梁勇等[8]研究了利用轻烧氧化镁粉合成片状阻燃剂氢氧化镁。该方法制备的氢氧化镁纯度达到97 %、粒径约1 um,提高了轻烧氧化镁粉的利用价值。赵娜等[9]以苦卤水和烧碱为原料,采用直接沉淀法在表面活性剂的辅助下制备出纳米氢氧化镁粉体。因此,对氢氧化镁的开发和利用并且进一步研究不同晶型的高质量产品尤为重要。[10]
1 实验
1.1 原料与试剂
本实验主要使用的是原料是由西陇科学股份有限公司提供的轻烧镁粉(分析纯),其中氧化镁的含量≥98.5 %,杂质最高含量化学成分为(wt%):盐酸不溶物,0.05;灼烧矢量,4.5;氯化物(Cl),0.02;硫酸盐(SO4) ,0.05;铁(Fe),0.005;钡(Ba),0.003;重金属(以Pb计),0.005。实验过程中用水均为实验室专用蒸馏水;研磨介质均为氧化锆磨珠,其级配为Φ1.5 mm∶Φ1.0 mm∶Φ0.8 mm=5∶3∶2。
1.2 仪器设备
X射线粉末衍射仪,TTRIII,日本理学电机公司(Rigaku);扫描电子显微镜,Quanta600,FEI香港有线公司;激光粒度仪,Bettersize2000(B&E),丹东百特仪器有限公司;马弗炉,KSL-1100X,合肥科晶材料技术有限公司;超细搅拌磨,GSDM-S,北京古生代粉体科技有限公司。
1.3 实验方法
本实验采用机械力化学法和水化法制备纳米氢氧化镁。根据图1所示的技术路线图,用轻烧镁与适量蒸馏水混合后倒入搅拌磨桶,使用玻璃棒搅拌1~2 min,再将研磨锆珠缓缓倒入进行超细研磨和反应,反应总时长为240 min。在反应过程中,每隔30 min取样品测试粒度,再将少部分样品取出放置于烘箱中60~80 ℃烘干保存。利用激光粒度仪测试、X-射线衍射(XRD)、扫描电子显微镜(SEM)等手段分析不同累积研磨时间的样品粒度、物相、形貌,进而分析机械力化学法处理工艺参数(研磨时间、搅拌速度、固液比)对氧化镁水化率、氢氧化镁的产物结构和性能的影响。根据分析,从而找出最佳的工艺条件并分析反应机理。
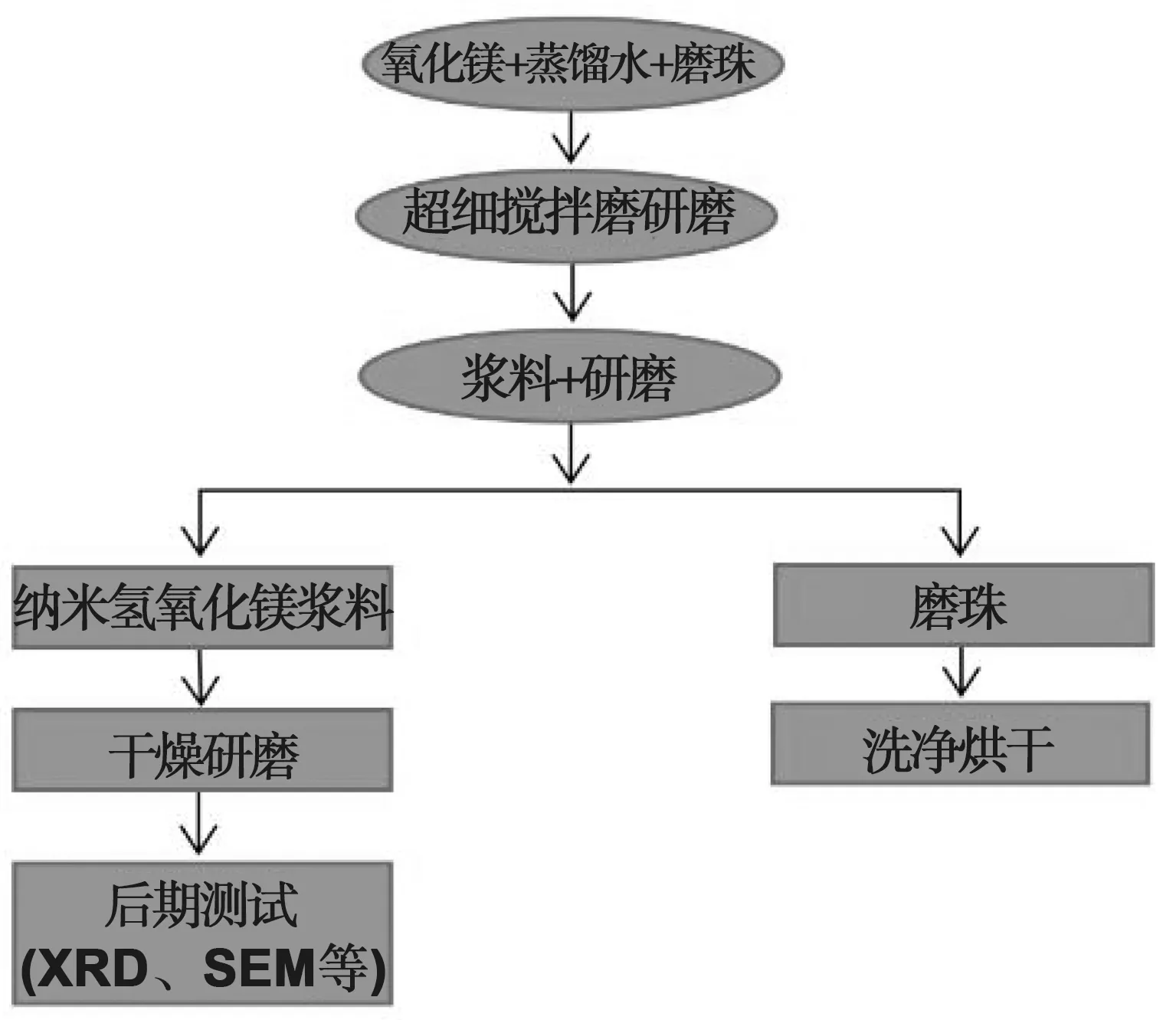
图1 工艺流程图
1.4 颗粒形貌测试方法
扫描电子显微镜(Scanning Electron Microscope,简称SEM)是分析样品表面形貌的仪器,原理是利用二次电子信号成像来观察样品表面形态。
通过SEM对碳酸钙样品的微观结构进行表征,通过测试可以直接分析出粉体的团聚程度、粒径大小。
1.5 粒度分布的分析
粒度可以直观的表征碳酸钙颗粒大小及分布范围。本次试验采用的是丹东百特的仪器BT-2000,测试范围是0.02~2000 μm。具体测试方法是加入六偏磷酸钠为分散剂,进行超声、搅拌,一段时间后在水槽中加入碳酸钙样品进行测试,经过多次测试取其平均值。通过粒度仪可以得到样品的平均粒径、中位粒径、d90以及粒度分布等重要数据。[11]
1.6 物相分析
通过XRD衍射和Search-Match软件可以分析样品的矿物成分,再经过由Scherrer公[12]可以计算出晶粒尺寸。
(1)
式中,D表示晶粒尺寸(nm),K为常数,λ是X射线的波长(nm),B为待测样品的衍射峰宽,b为无宽化的标准样品的宽度,θ则是衍射角。
本次实验的测试条件:Cu靶,40 kV,100 mA扫描速度8°/min,扫描角度5°~90°。
1.7 水化率分析
将干燥研磨好的产物称取1.00 g置于坩埚中,在初始温度20 ℃,升温速率5 ℃/min,最终温度500 ℃,保温30 min的马弗炉进行灼烧,由灼烧前和灼烧后的质量差,可得出氧化镁的水化率。氧化镁的水化率按照公式(1~2)计算。
(2)
其中,MMgO:氧化镁的摩尔质量,MH2O:水的摩尔质量,m1:水化产物干燥完全后产物的质量,m2:水化产物煅烧后的质量。[1]
2 结果与讨论
实验反应过程中有众多影响因素,搅拌磨搅拌速率-研磨时间以及料浆固液比是较为主要的影响因素。
2.1 搅拌磨搅拌速率-研磨时间
为了探究实验反应过程的搅拌磨搅拌速率-研磨时间的最佳条件,所以设计对比实验进行分析研究。在氧化镁:去离子水:研磨介质质量比为1:4:4的条件下,称取200 g的轻烧镁粉进行实验反应,采用机械力化学法湿法研磨轻烧镁制备纳米氢氧化镁,分析不同的搅拌速度(700、900、1100、1 300 r/min)和不同研磨时间(时间间隔为30 min)对样品粒度的影响。
2.1.1 粒度分析
对32份实验样品进行粒度测试,粒度变化图如图2、图3所示。当搅拌速度为1 300 r/min时,不同时间段的样品的粒度d50和d90相对其他搅拌速度时偏小,此结果说明随着搅拌速度增大,研磨过程中的机械力和剪切力增强,即通过研磨球、研磨罐和颗粒的频繁碰撞次数增多,不仅能有效的阻止氢氧化镁的团聚,还能进一步将颗粒表面化学键打断,产生大量不饱和化学键、自由离子和电子等,提高了原子的活性,加快了生成氢氧化镁的反应。观察1 300 r/min搅拌转速下颗粒粒度d90随时间的变化折线中可以看出,随着研磨时间的增长,粒径达到最小值后反而会随着研磨时间的增长而有所增大,这是由于晶粒细小到一定的程度,其表面效应能显著增大,过度球磨造成晶粒团聚加速所致。由图中还可以看出,700、900、1100、1 300 r/min搅拌转速下研磨时间为180、210、240 min时d50和d90基本上达到了最小,在1 300 r/min的搅拌速度和180 min的研磨时间下,d90=2.27 μm是最小值。
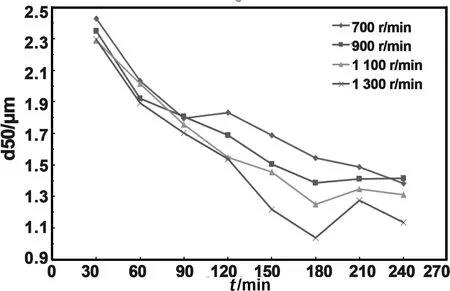
图2 不同搅拌速度下,样品粒度d50(μm)随研磨时间变化图
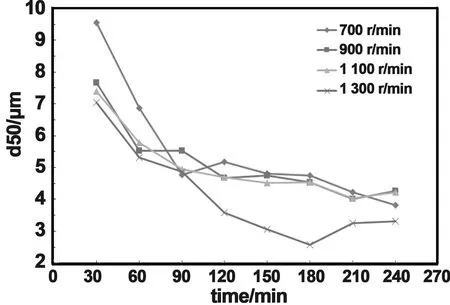
图3 不同搅拌速度下,样品粒度d90(μm)随研磨时间变化图
2.1.2 水化率分析
计算所得样品的氧化镁水化率,并将得到的数据进行了直线拟合,如图4、图5、图6、图7所示。可以得出结论,当搅拌速度为1 300 r/min时,拟合直线的斜率最低,是最为稳定的,在研磨时间为30 min时,样品的氧化镁水化率就已达到了91.083%,大于其他搅拌速度30 min时样品的氧化镁水化率。还可以得出在实验最初的30 min内,实验整体的水化速率是最快的,由于在机械力化学法湿法研磨氧化镁的体系中,转轴不断旋转提供剪切力并加强研磨介质与浆料之间的碰撞,使得氧化镁和水进行充分的水合反应,能较快反应生成氢氧化镁。随着研磨时间的增大,氢氧化镁生成量越来越多,水化过程则会越来越难。在研磨时间为180 min时,此时不同搅拌速率的样品氧化镁水化率都到达了95%左右,说明此时氧化镁与水反应生成了氢氧化镁到达了极限水化程度。
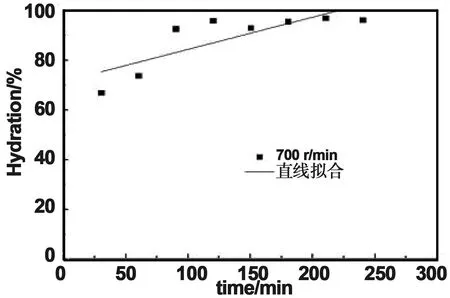
图4 700 r/min水化率直线拟合图
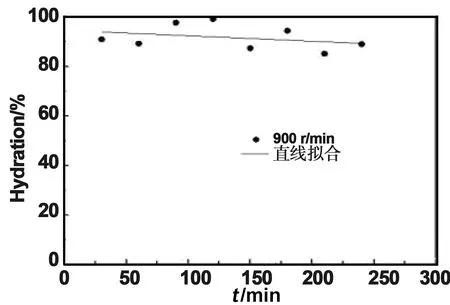
图5 900 r/min水化率直线拟合图
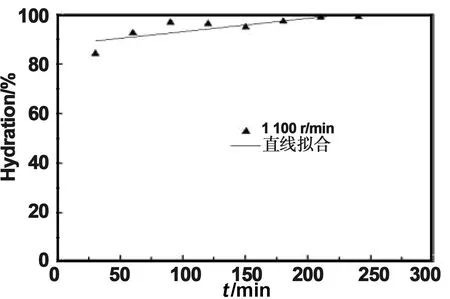
图6 1 100 r/min水化率直线拟合图
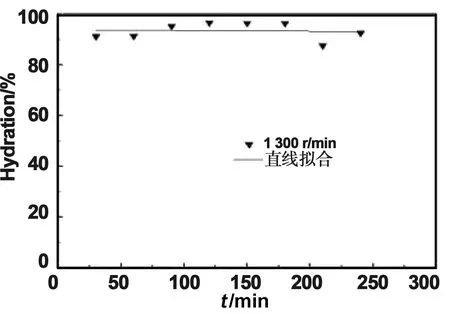
图7 1 300 r/min水化率直线拟合图
2.1.3 X射线衍射(XRD)分析
对搅拌速度为1 300 r/min不同研磨时间得到的样品进行XRD测试,XRD衍射图谱如图8所示。通过XRD图谱分析,30 min时,样品中氢氧化镁衍射峰强较低,图谱中的氧化镁衍射峰出现在2θ=43.09 °,峰强较高,说明此时氧化镁还未反应完全,尽管氧化镁水化速率很高,但生成的氢氧化镁的结晶度不高。随着研磨时间的增长,氧化镁衍射峰逐渐减弱至消失;氢氧化镁衍射峰强均有所增加,其结晶度均有不同程度的增加。[14]在(101) 面,氢氧化镁晶体的表面极性较强,所以氢氧化镁颗粒通常表现为团聚状态,导致其二次粒径较大。随着(101)面显露的越多,生成的氢氧化镁晶体的表面极性和微观内应力就会越强,导致氢氧化镁结构处于不稳定状态,从而会影响晶体的宏观性质,容易使晶粒团聚。[15]针对极性较弱的(001)面而言,样品(f) 的(001)面显露较其他样品少,由此可以得出180 min时氢氧化镁晶体结构更稳定。
180 min时,氧化镁衍射峰2θ=43.09°消失,图谱中样品衍射峰出现在2θ为18.54、33.06、38.16、50.97、58.84、62.21、68.35、72.23、81.38°,与标准衍射图谱ICSD#44-1482的衍射峰完全重合,显示实验制备样品为纯度非常高的水镁石型氢氧化镁。结果表明此时氧化镁转化率高,氢氧化镁完全生成。经Scherrer公式计算出180 min时样品的晶粒尺寸为6.3 nm,通过计算(001)和(110)晶面的衍射强度之比I(001)/I(110)值为2.242得出此时纳米氢氧化镁的晶型属于六方晶型。
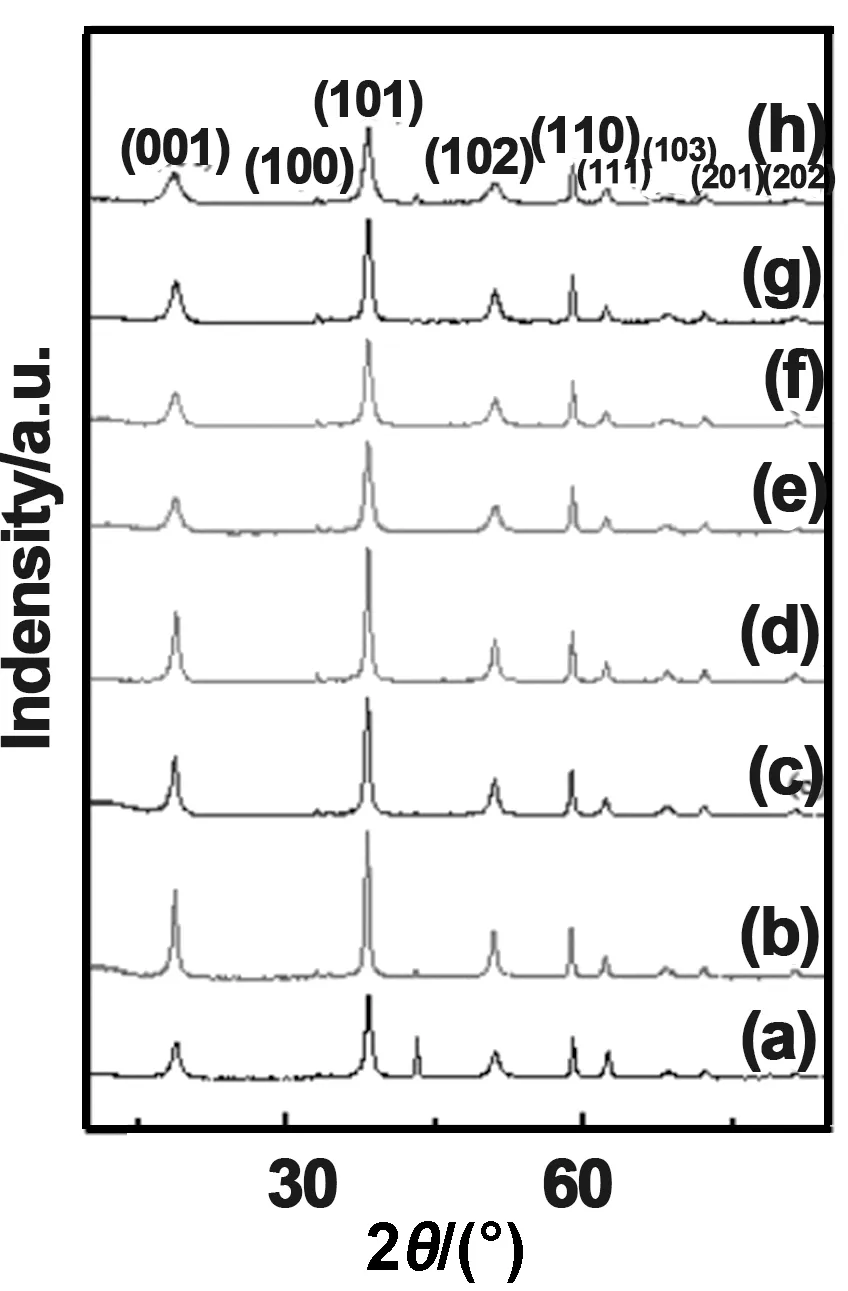
图8 搅拌速度为1 300 r/min、研磨时间为30 min(a)、60 min(b)、90 min(c)、120 min(d)、150 min(e)、180 min(f)、210 min(g)、240 min(h)下的XRD衍射图谱
2.1.4 扫描电子显微镜(SEM)分析
对搅拌速率为1300 r/min,研磨时间为180 min的样品做扫描电镜测试,扫描电镜照片如图9:氢氧化镁颗粒形貌规则,为较完整的六方片状,厚度大约为5~20 nm,大量的六方形纳米氢氧化镁堆积在了一起,团聚较严重,整体分散性较差。

图9 搅拌速度为1 300 r/min,研磨时间为180 min的样品SEM图
2.2 浆料固液比
为了进一步探究实验反应过程的固液比的最佳条件,所以设计对比实验进行分析研究。在氧化镁:研磨介质质量比为1∶4、实验搅拌速率为1 300 r/min、反应时长为180 min的条件下,称取200 g的轻烧镁粉进行实验反应,采用机械力化学法湿法研磨轻烧镁制备纳米氢氧化镁,分析不同的料浆固液比(1∶3、1∶4、1∶5、1∶6、1∶7)对样品粒度的影响。
2.2.1 粒度分析
对5组实验样品进行粒度测试,粒度变化图如图10、图11所示。由图可知随着固液比的降低,粒度减小,在固液比为1∶4时粒度最小,d50=1.04 μm,d90=2.27 μm。这说明超细搅拌磨高速旋转所产生的剪切力和磨珠浆料之间的冲击力就随着料浆浓度升高而增强。
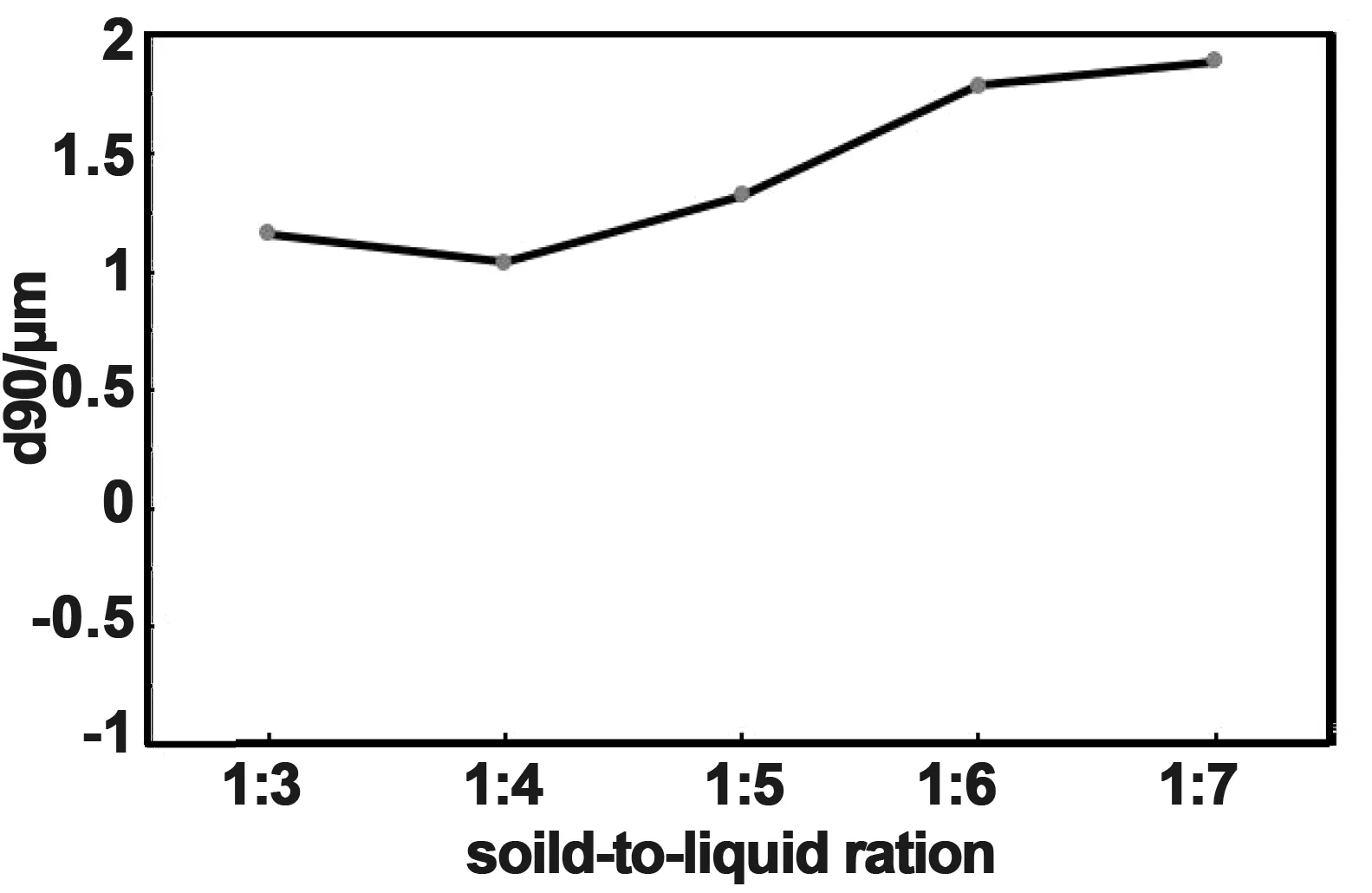
图10 不同固液比-d50变化图
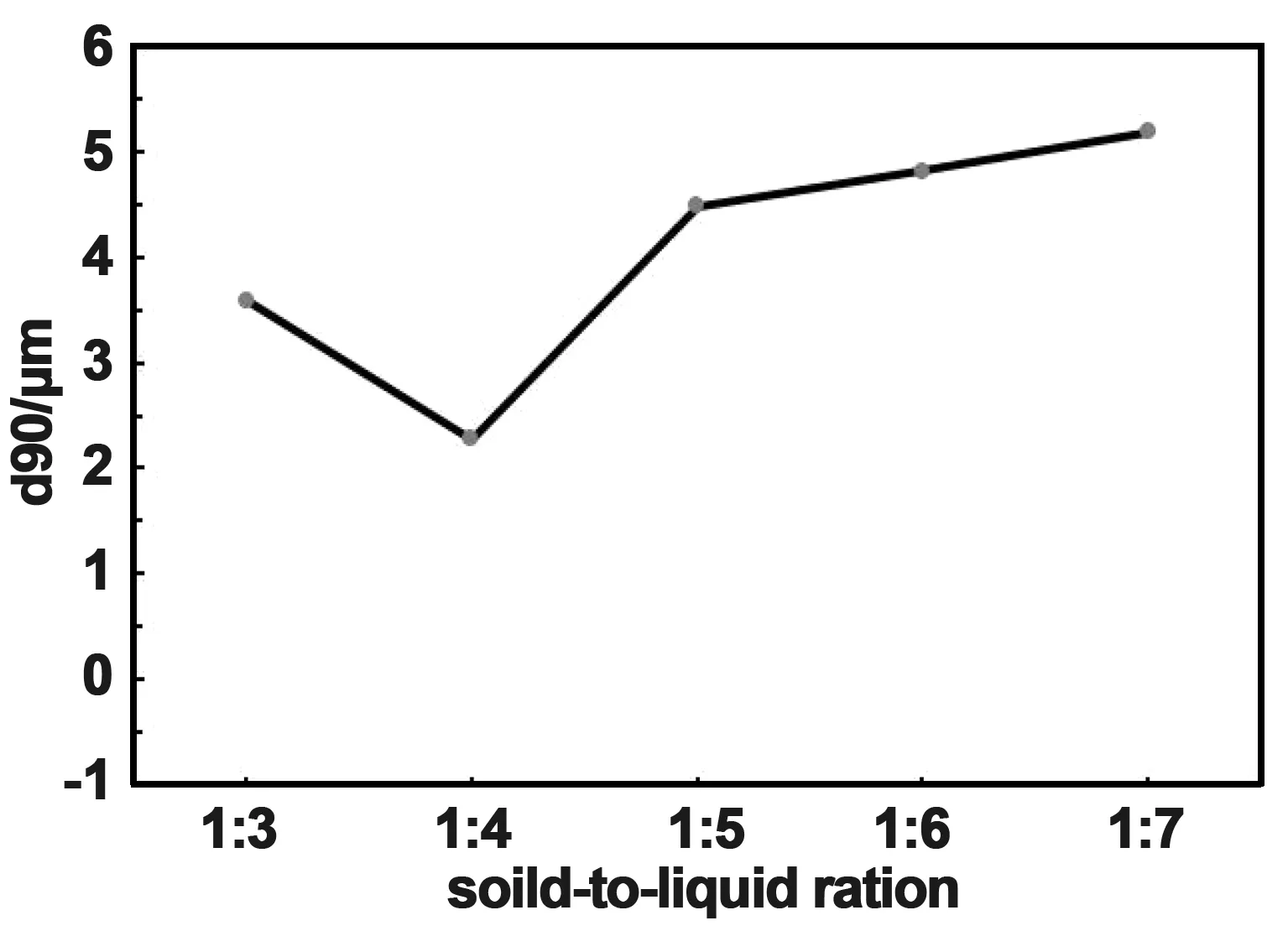
图11 不同固液比-d90变化图
2.2.2 X射线衍射(XRD)分析
固液比为1∶3、1∶4、1∶5、1∶6、1∶7的X射线衍射衍射图谱如图12所示,样品(c)、(d)(e)图谱中的氧化镁衍射峰2θ=43.09 °仍存在,说明在1∶5、1∶6、1∶7的固液比下,研磨180 min时氧化镁还不能完全水化生成氢氧化镁,并且氢氧化镁结晶度不高;样品(a)、(b)图谱上衍射峰与标准衍射图谱ICSD#44-1482对比完全匹配,并且几乎无任何杂质峰,说明氧化镁水合完全,生成了结晶度高的水镁石型氢氧化镁。 经谢乐(Scherrer)公式计算,固液比为1∶3、1∶4的样品的晶粒尺寸为9.9 nm、6.3 nm,结合粒度测试结果可知实验最佳条件浆料固液比1∶4;通过计算固液比为1∶4条件下样品的(001)和(110)晶面的衍射强度之比为2.559得出此时纳米氢氧化镁的晶型属于六方晶型。
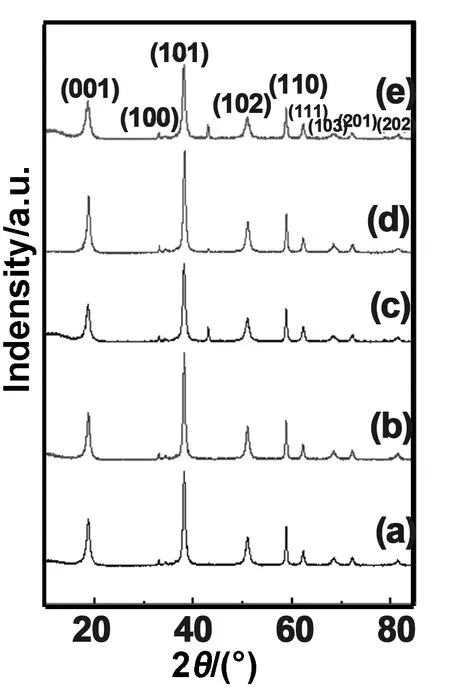
图12 固液比为1∶3(a)、1∶4(b)、1∶5(c)、1∶6(d)、1∶7(e)的样品XRD衍射图
3 结 论
以分析纯轻烧镁粉作为原料,采用机械力化学法和水化法制备得到纳米级氢氧化镁,探究了搅拌速度-研磨时间以及固液比对产物粒度、产物形貌和结构的影响。对实验产品进行相关测试、结果讨论和机理分析,所得结论如下:
(1)机械力化学法制备纳米氢氧化镁的最佳工艺条件:反应浆料固液比为1∶4,超细搅拌磨的搅拌速度为1 300 r/min,反应研磨时间为180 min,可制备出d50粒度为1.04 μm,d90粒度为2.27 μm,平均晶粒尺寸为6.3 nm的六方片状纳米级氢氧化镁。
(2)对最佳反应条件生成的样品进行了XRD测试,氧化镁几乎完全水化生成了结晶度较高的氢氧化镁,其晶型主要为水镁石型。对样品进行了SEM测试并观察了样品的表面形貌为较为完整的六方片状,薄片厚度大约为5~20 nm,大量的六方形纳米氢氧化镁堆积在了一起,团聚现象较为严重。

