二次水热法制备Co3O4@MnO2复合材料及其电化学性能研究
庄 雪,潘 双,王子寒,王 冰,唐立丹
(辽宁工业大学 材料科学与工程学院,辽宁 锦州 121000)
0 引 言
为了解决传统电容器和电池在储存能力,循环寿命和环境污染方面的问题,研究者们花费大量的努力去寻找便宜,环境相容性较好同时又能展现出高比容量的活性物质。经过近100多年对各类电极材料的应用和研究,电极材料主要分为碳电极、金属电极、金属氧化物电极、导电聚合物电极、导电陶瓷(含金属间化合物)电极和复合电极共六大类体系。在金属氧化物电极中,自Lee和Goodenough在1999年首次报道了锰氧化物的赝电容性质后,锰氧化物电池材料的应用和二氧化锰新型电极材料的开发引起了广大研究者的关注[1]。二氧化锰作为氧化物电极材料因其具有较宽的电位窗口和电化学性能良好等诸多优点,在电容器研究领域得到广泛应用[2]。但单一的二氧化锰作为电极材料仍存在很多问题,如比表面积较低造成实际比电容远远小于理论比电容、电阻较高使其功率特性很差、在水溶液中溶解度较大使得二氧化锰电极在水系电解液中难以有很好的循环稳定性等[3],因此纯相二氧化锰电极的比电容在实际测量中往往不高[4]。为了解决单一二氧化锰导电性不佳、稳定性较差等问题,利用二氧化锰掺杂、包覆和复合等方法制备二氧化锰的复合电极材料是目前的一个重要研究方向和趋势[5-6]。
本文利用二次水热法制备了Co3O4@MnO2复合材料,通过XRD、FESEM和电化学检测,进行结构和形貌分析确定最佳复合参数,讨论水热反应温度对Co3O4@MnO2的结构、形态和性能的影响[7]。
1 实验内容与方法
1.1 实验材料的制备
1.1.1 泡沫镍的预处理
将泡沫镍裁成小片,并放入浓盐酸与水溶液体积比为1∶2的溶液中超声清洗10 min,以清洗其表面金属氧化物;然后用酒精继续超声10 min进行清洗;最后用去离子水超声清洗30 min两遍,干燥2 h备用。
1.1.2 Co3O4@ MnO2复合材料的制备
用电子天平按摩尔数2:3来称量氯化钴(CoCl2·6H2O,分析纯)和尿素,同时溶解于50 mL去离子水中,在磁力搅拌器中搅拌直至形成均匀的粉红色溶液,将处理好的泡沫镍垂直置于反应釜中随混合液在160 ℃下反应10 h,待反应完全后取出泡沫镍,用去离子水多次冲洗泡沫镍,然后放入真空干燥箱内在80 ℃下干燥6 h,最后在350 ℃的卧式立炉中煅烧2 h取出,得到Co3O4前驱体。
然后按配比2:3称取定量2.37 g KMnO4,溶于30 mL去离子水中, 并将溶液放入水浴锅中加热到90 ℃,直至试剂全部溶解后,将前驱体浸泡在KMnO4溶液中不断搅拌,并将其转移到高压反应釜中设置不同的水热参数,在温度(100、120、160和200 ℃)下反应10 h,进行二次水热反应。待反应完成后,将泡沫镍用去离子水反复洗涤,放入80 ℃的真空干燥箱内干燥6 h,标记所获样品分别为A、B、C、D。
1.2 材料物理表征
X射线衍射分析是用来进行物相的定性和定量分析,晶体的织构分析等[8]。实验采用D/max-2500/PC X-Ray Diffractometer的型号的X射线衍射仪,最大功率18 kW,测角仪半径为185 mm,扫描方式为θ/2θ单动或联动。具体参数为:Cu靶,Kα射线,扫描速率为8°/min,扫描范围为10~90 °。X射线波长λ=0.15418 nm。采用Sigma-500型场发射扫描电子显微镜观察样品形貌,仪器的加速电压为5 kV。
1.3 材料化学表征
将具有活性材料的泡沫镍样品A、B、C、D(直径为1 cm的圆)充当工作电极,饱和甘汞(SCE)电极作为参比电极,铂片作为辅助电极进行三电极体系测试。电化学测试采用荷兰IviumStat.Xri的电化学工作站,其最大电流为±10 A;最大输出电压±10 V;恒电位仪带宽:大于1 MHz;施加电位范围:-10 V到+10 V;电流范围:1 pA~10 A,共14档;交流阻抗频率范围:10 μHz~8 MHz。通过循环伏安法(CV)、恒电流充放电(GCD)和电化学交流阻抗(EIS)方法测试Co3O4@MnO2复合材料的电化学性能。
2 实验结果与分析
2.1 XRD的分析
图1为不同水热温度(100,120,160和200 ℃)下得到的Co3O4@MnO2的XRD图谱。当水热温度为100 ℃时,样品A在2θ=18.96、31.26、36.86、38.56、55.84、59.36和65.32°的位置出现7个衍射峰,与标准卡Co3O4(JCPDS 42-1467)基本相吻,说明此时样品中主要成分是Co3O4。此时在衍射图谱中,除了Co3O4晶体的衍射峰以外,在2θ=21.45°附近出现了γ-MnO2特征衍射峰,半峰宽B=0.152,衍射峰强度较弱,表明γ-MnO2结晶程度较弱。随着反应温度升高到120 ℃,可以看到生成了Co3O4、α-MnO2和γ-MnO23种晶型的MnO2,在2θ=21.45,32.62,46.64和54.00°出现了γ-MnO2,半峰宽分别为B=0.294,0.181,0.271和0.348。在2θ=25.04,42.85和62.14出现了α-MnO2,这三处的半峰宽B=0.201,0.254,0.038。也就是说在120 ℃温度条件下的γ-MnO2已经几乎完全生成,所占总体比例高于正处于生成阶段α-MnO2。当温度为160 ℃时,在2θ=12.37,24.00,43.19和62.76°出现了α-MnO2的特征衍射峰,其在2θ=25.04,43.19和62.76°附近处的半峰宽B=0.185,0.225,0.027,此时曲线的最大变化就是其他晶面处γ-MnO2特征衍射峰已经消失,得到的结构稳定的α-MnO2,且此条件下的α-MnO2结晶性较其他温度优异。而当温度升高至200 ℃时,发现Co3O4的衍射峰几乎消失,仅在2θ=19.22,31.58,37.10°有较为明显的衍射峰,在附近2θ=12.52,25.22,37.78,42.68和65.60°出现了多处α-MnO2特征衍射峰,但高温下水热反应过快,α-MnO2结构不稳定。综合整组水热反应温度条件分析得到,在水热温度160 ℃反应10 h的条件下,得到的α-MnO2占总体的比率高,半峰宽较小,图像对称性良好,结晶性能最优越[9]。
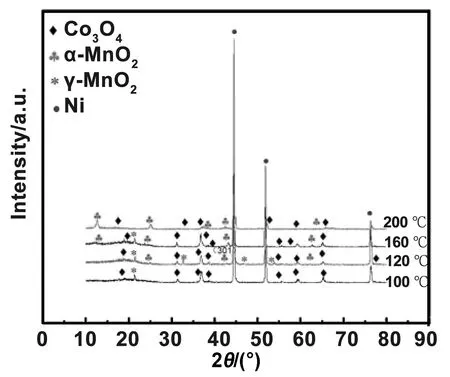
图1 不同水热温度下Co3O4@MnO2的XRD图像
2.2 形貌分析
图2(a)~(d)为Co3O4@MnO2复合材料在不同水热温度(100,120,160和200 ℃)的FESEM图。从图2(a)中可以看到,水热温度较低为100 ℃时,图中有大量未成型的纳米棒结构,排列杂乱无章,且由于较高的表面能,出现明显的团聚现象。说明此时的水热反应温度,对MnO2的生长起阻碍作用。随着反应温度增加到120 ℃,如图2(b)所示,Co3O4表面覆盖MnO2,复合材料形成分布均匀,大小均一的条形纳米棒,棒直径约为100 nm。当水热温度为160 ℃时,纳米棒直径继续增加,α-MnO2产生新的晶面,产生纳米球型结构,这正与XRD结果相对应,出现了明显的α-MnO2衍射峰,有利于提高Co3O4@MnO2复合材料的电化学性能。与图(c)进行比较,较高温度下(200 ℃)的Co3O4@MnO2复合材料表面结构由棒状的MnO2向团絮状MnO2转变,渗透性降低,结构稳定性较差。结合图2综合分析,随着水热温度的升高,可以明显的看到MnO2的生长变化(γ-MnO2-α-MnO2)与形貌转变(棒状-团絮状),160 ℃是一个转变过程中的温度,在这个温度梯度内,Co3O4@MnO2的形貌转变为溶解-重结晶-各向异性生长[10]。即Co3O4@MnO2复合材料在160℃的水热温度下提高了二氧化锰结构稳定性、渗透性的同时又改善了二氧化锰的性能。

图2 Co3O4@MnO2复合材料的FESEM图
2.3 电化学测试
2.3.1 不同水热温度下的Co3O4@MnO2循环伏安曲线
循环伏安法是电化学测试中常用的研究方法之一,峰电位和峰电流是循环伏安曲线主要的测量参数[11]。图3为不同水热温度(100,120,160和200 ℃)下制备的Co3O4@MnO2的循环伏安曲线。由于实际体系中电极的极化内阻的存在,循环伏安曲线相对于零电流坐标轴的理想矩形对称形状有一定的偏差。在图3中可以看到,温度的变化导致材料呈现不同的化学状态。在较低温度(100 ℃)和较高温度(200 ℃)下的曲线均未出现氧化还原峰,但是反应温度为120 ℃时,曲线明显出现2个氧化峰和2个还原峰。说明此时反应物和反应物的产物同时参与电化学反应,且反应物的吸附作用比产物的吸附作用更强[12]。当水热温度下由100 ℃提高到160 ℃,响应电流也几乎提高了一倍,表明材料能尽快的进行离子传递,具有良好的电容特性。观察图中水热温度为160 ℃,反应10 h的CV曲线,存在一对明显的氧化还原峰,各氧化峰和还原峰所对应的电流差值,随扫描速度的增大和增大,具有良好的响应关系。并且从氧化还原峰的位置可以看出此体系为准可逆过程,说明此时材料具有良好的可逆性且反应速率较快,即在电极表面发生了快速的氧化还原反应。CV曲线的面积可以用来估计电极材料的比电容[13],图3中红线的CV曲线围成的面积最大,比电容最大,获得的赝电容性最好,这与XRD检测结果一致,表明水热温度160 ℃,水热时间10 h复合材料Co3O4@MnO2的电容量最佳。
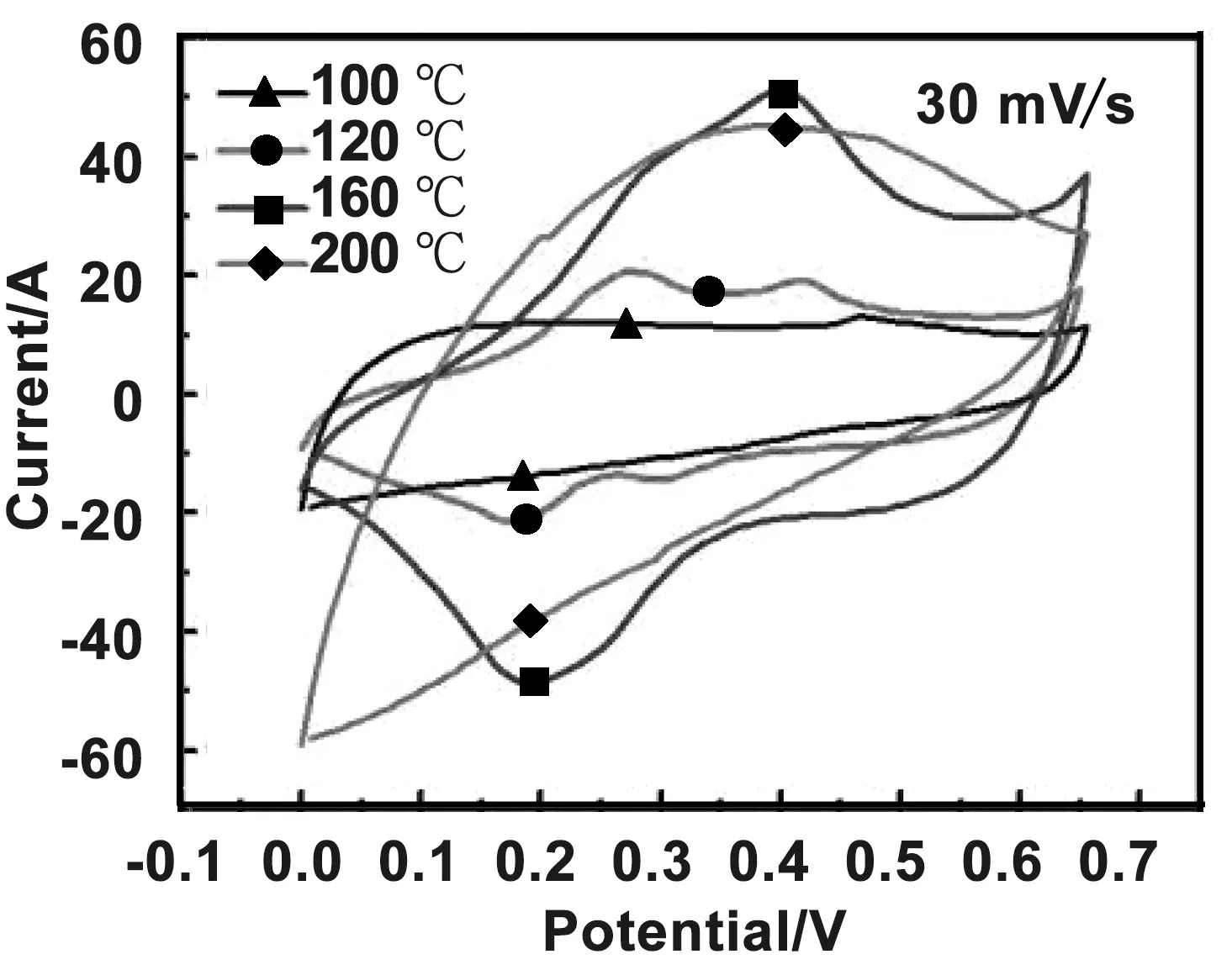
图3 不同水热温度的Co3O4@MnO2循环伏安测试曲线图
2.3.2 恒流充放电测试
恒流充放电法是另一种常用的电容器性能测试方法,在施加恒定电流下,使电极在恒定电流下充放电,同时通过测试装置监测电位随时间的变化,从而研究电极的电化学性能[14]。如图4(a)为样品A、B、C、D的恒流充放电曲线,电流密度是0.3 A/g。根据比电容公式Cm=IΔt/m·ΔV(m为活性物质质量(g);v为扫描电位范围(V);t为放电时间(s);I为放电电流(A)),计算样品材料A、B、C、D的比电容分别522.2、1 464.8、2 747.3、2 149.0 F/g,通过计算样品材料的电容量的可以看出,在水热温度160 ℃,反应10 h的条件下电极比电容最大,材料最稳定,具有良好的放电性,对应了循环伏安曲线的氧化还原峰,且与上述CV曲线的检测结果一致。图4(b)是在最佳水热参数下制备的电极材料在不同电流密度(0.3、0.5、0.8、1和3 A/g)下的恒流充放电曲线。从图中可以看出,不同电流密度下的充放电曲线由于比电容会随着电极电位的变化而变化均存在不同程度的弯曲,并未呈现理想的线性关系,体现典型的赝电容特性[15]。但图中曲线均呈现出良好的对称性,具有理想的电容行为,充放电时间几乎相等,表明Co3O4@MnO2的复合材料在充放电过程中表现出良好的库仑效率。由公式Cm=IΔt/m·ΔV,计算出电流密度为0.3 A/g时,电极材料的比电容为2 747.3 F/g;当电流密度为3 A/g时,电极材料的比电容为1 385.0 F/g。将图4(a)、(b)进行图像对比分析,确定电流密度为0.3 A/g电极材料比电容最大,电化学性能优异。随着电流密度的增加,电极材料的比电容呈现减小的趋势。引发该实验现象的原因可能是大电流放电时,电势降较大和电活性物质法拉第反应不充分[16]。对于单一的MnO2电极,R.B.Rakh等[17]人以碳纤维为基底,水热合成的四氧化三钴电极检测出且其等效串联电阻仅为0.79 Ω和高达911 F/g的电容量,但仍远小于Co3O4@MnO2复合材料的在最佳水热参数下的电容量。结果表明Co3O4@MnO2复合电极材料相比于单一的MnO2电极具有优异的放电性和稳定的电化学性能。
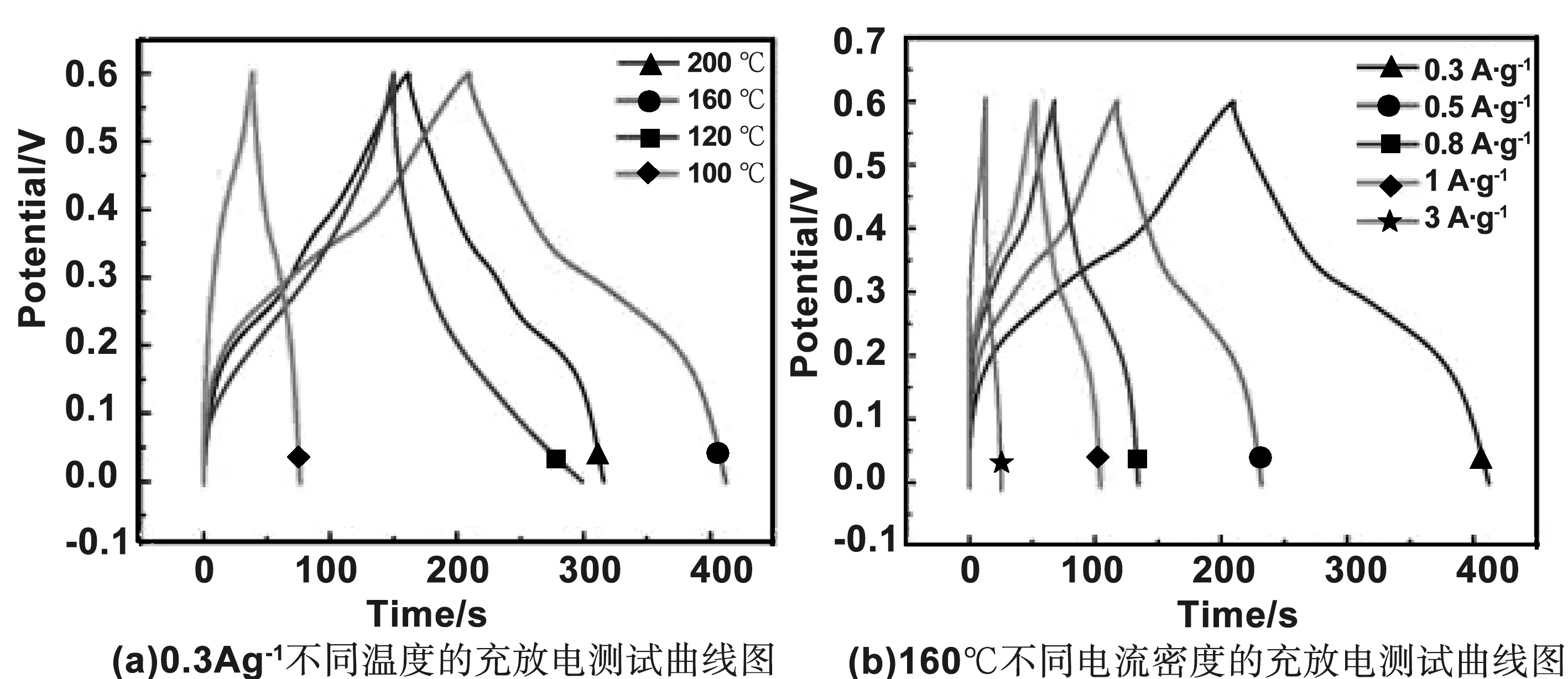
图4 样品A、B、C、D的恒流充放电曲线
2.3.3 不同水热温度的Co3O4@MnO2交流阻抗测试
电化学阻抗谱(EIS)是一种有效的技术方法用以检测修饰电极的界面性能[18]。图5是不同水热温度(100,120,160和200 ℃)下制得的Co3O4@MnO2交流阻抗图,曲线上Z′为阻抗的实部,-Z″为阻抗的虚部。图中可以看出,不同水热温度下的电化学阻抗谱均由直线和圆弧两个部分组成,低频区的斜线部分对应于体系扩散受阻过程;高频区的圆弧代表传荷阻抗,交流阻抗曲线半圆直径的大小的变化对材料的内阻存在一定的影响。高频区半圆弧与实轴的截距表示电极材料内阻,在160 ℃,反应10 h的水热条件下,电极材料内阻Rs=0.65 Ω小于单一电极的电阻0.79 Ω,即相较于单一的MnO2电极阻抗较小,表现出优异的电化学性能,得出结论与恒流充放电曲线中电极比电容的计算结果相同。此时图5中红色曲线(160 ℃反应温度)的内阻最小,斜率远远大于其它3组,说明该条件下所制得Co3O4@MnO2电极的扩散速度较快,材料具有较好的导电性和赝电容行为。通过前文的XRD、FESEM图像和电化学测试研究了样品的电化学性能,分析确定水热温度为160 ℃,时间为10 h时材料的电化学性能最佳。
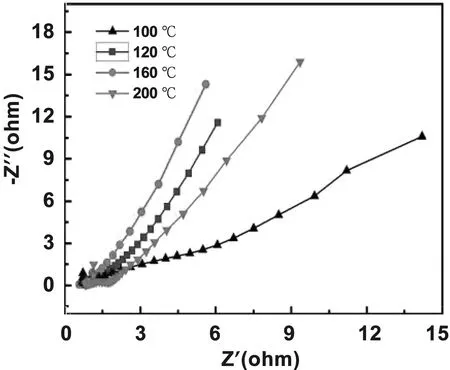
图5 不同水热温度的Co3O4@MnO2交流阻抗图谱
3 结 论
(1)、水热温度的改变影响Co3O4@MnO2的结构。当温度过低(100℃)时,不利于MnO2的生长;但较高温度下(200 ℃)的Co3O4@MnO2复合材料表面结构由棒状的MnO2向团絮状MnO2转变,渗透性降低,结构稳定性较差。综合分析,水热温度为160 ℃时,α-MnO2产生新的晶面,复合材料结构由纳米片状向纳米团状转变, Co3O4@MnO2复合材料的电化学性能显著提高。
(2)、水热温度为160 ℃,时间为10 h,电流密度为0.3 A/g电极材料比电容最大为2 747.3 F/g,电化学性能优异。在最佳水热参数下,随着电流密度的增加,电极材料的比电容呈现减小的趋势。但是相比于911 F/g的电容量的单一MnO2电极仍具有优异的放电性和稳定的电化学性能。

