砷硒胁迫对小麦毒性效应及预测模型研究
李建秋,龚 冰,季 节,周子琛,仇 浩
近年来,土壤和地下水中砷(As)、硒(Se)污染已成为世界性难题。As是一种广泛分布于环境中的类金属元素,其在地壳中的丰度列于第二十位[1]。世界卫生组织(WHO)规定,成人每日As摄入量上限为15 μg·kg-1[2]。随着工农业的迅猛发展,含As矿的开采和冶炼,杀虫剂、除草剂[3]的使用等人为来源产生的As大量进入自然界中,造成土壤和水环境中As含量的严重超标,对生态环境安全乃至人体健康产生潜在危害[4]。《全国土壤污染状况调查公报》显示,我国土壤总超标率为16.1%,其中As点位超标率达到了2.7%,问题尤其突出,仅次于8大重金属中的Cd(7.0%)和Ni(4.8%)[5-6]。与As不同,Se是人体和动物必需的微量元素[7],具有重要的生物学功能,但其是否是高等植物的必需元素还没有被证实。WHO规定,Se每日摄入量上限为400μg[2]。自然界中过量的Se会对土壤、大气和水造成严重污染,给人体健康带来很大的危害[8]。近年来,环境中Se污染现象越来越普遍[9-12],因而受到广泛关注。As和Se具有相似的化学性质,因此多以混合物形式存在于土壤、植物以及水环境系统中,很多环境效应无法用单一金属的作用机理来解释[13]。有研究表明Se可以减轻植物生长过程中的重金属胁迫,增强植物的抗氧化能力[14]。例如营养液中添加Se能显著降低As对水稻幼苗的毒害效应,二者之间存在拮抗作用[15]。与此相反,一些研究者报道了As和Se通过抑制彼此的代谢物从而强化毒害效应,二者之间存在协同作用[16-17]。As、Se之间矛盾的相互作用引起了人们的广泛关注,因此,有必要深入开展As、Se复合毒理效应研究,并构建能准确评价含氧阴离子型金属毒性和生态风险的有效预测模型。
在分析和预测复合污染物毒性作用时,有两个常用的加和参考模型(Reference model):浓度加和(Concentration Addition,CA)和独立作用(Independent Action,IA)模型[18]。CA模型假设混合物组分具有相同的作用机理或作用点位,IA模型则假设不同组分的作用机理或作用点位不同。如果混合物的观测毒性与加和参考模型预测毒性一致,则认为该混合物无交互作用,或称加和作用。如果观测毒性明显偏离加和参考模型预测毒性,则认为该混合物产生毒性交互作用,即拮抗(小于预测毒性)或协同作用(大于预测毒性)[19]。尽管这两个参考模型被广泛应用在混合物毒性研究当中,但均只适用于无交互作用的混合物,对于具有交互作用的混合物并不能定量预测其毒性,且无法被用来直接解读混合物毒性作用机理[19-20]。实际环境混合物的各组分之间的交互作用复杂多样,其联合作用效应不仅与组分种类有关[21],也与组分浓度比及效应水平有关。利用加和参考模型对水中有关铜、镉、锌的二元或三元复合污染毒性研究(160组数据)进行元分析发现,存在拮抗或协同作用的情形占80%左右[22]。如何进一步定量地评估混合物联合毒性是亟待解决的关键问题,而明晰混合物交互作用的程度及机制并将其纳入机理性的毒性预测模型中加以考虑则是准确评估混合物毒性的必要条件。
国内外在加和参考模型预测结果的基础上,尝试通过对参考模型进行数学拓展或结合生物有效性分析来定量预测水环境体系中金属混合物的联合毒性[23-25],并取得一定进展,整体上提高了模型的预测能力。生物配体模型(Biotic Ligand Model,BLM)整合了影响生物有效性的三大因素:浓度、络合和竞争[26]。假设单一金属毒性主要取决于溶液(土壤溶液)中自由金属离子活度,而自由金属离子活度受有机、无机配体络合的影响;其他共存阳离子(如Ca2+、H+等)能够和自由金属离子竞争生物配体的结合位点从而缓解金属的毒性[27]。由于该模型充分考虑了生物有效性的重要性,在预测和评价单一重金属的水生或陆生毒性效应方面得到了迅速的发展和应用[28-30]。实践中,竞争性共存阳离子可通过影响上述反应过程而对单一金属毒性产生影响。将这种竞争机制拓展到重金属复合污染的情形下,考虑混合物组分在前述两个反应过程中的交互作用及主要影响因子,同时假定最终结合在生物配体上的各金属的浓度加和代表有效致毒剂量,那么就可以改进并拓展BLM理论来预测混合物毒性,该设想在简单水溶液体系和土壤体系中已得到初步验证[29-30],但该理论是否适用于含氧阴离子型金属混合物的毒性预测尚缺乏研究。
本研究以小麦(Triticum aestivum L.)作为模式植物,溶液体系为毒性测试介质,开展两种典型阴离子型类金属元素(As和Se)的室内毒性暴露试验,系统研究模式植物对含氧阴离子型类金属单一及混合物的毒性响应,阐明As、Se及其交互作用产生的毒性机制,探索构建基于生物有效性的机理模型来预测As、Se及其混合物毒性效应,以期为含氧阴离子型类金属污染土壤风险评估提供有力支撑。
1 材料与方法
1.1 实验设计
供试小麦品种为NAU 9918,购买于南京农业大学。小麦种子预发芽后选取根长度为1.0~1.5 cm的小麦幼苗进行植株毒性试验。实验设计如表1所示。
1.2 测试溶液
采用水培法研究As、Se及其二元混合物的毒性。营养液由0.2 mmol·L-1CaCl2和5 μmol·L-1H3BO3组成。通过添加不同含量的含氧阴离子型类金属(Na2HAsO4·7H2O、Na2SeO3·5H2O,分析纯试剂)至营养液中制备测试溶液。配制好不同浓度的测试溶液后,在小麦短期急性暴露实验开始前24 h内进行各测试溶液pH值的调节。利用0.75 g·L-1的MES缓冲溶液和0.01 mol·L-1的NaOH溶液将每组测试溶液的pH值调至6.0±0.1。
1.3 供试仪器
顶置光源人工气候箱:浙江省宁波市新江南仪器有限公司,RXZ-1000F-4型;数显鼓风干燥箱:上海博迅实业有限公司医疗设备厂,GZX-9140 MBE型;实验室pH计:上海安莱立思仪器科技有限公司,pH510型;ICP-OES:上海赛默飞世尔科技有限公司,iCAP7600型;电子天平:北京赛多利斯科学仪器有限公司,SQP型。
1.4 毒性测试
参照ISO标准(11269-1)进行植物根伸长毒性试验[31]。作为生物毒性(植物、微生物和动物)的一种手段,植物毒性试验因操作简便、试验条件要求低而广泛应用于生态毒理学领域,其作为生态风险评估的常规方法已经得到普遍认可[32-37]。根据实验内容,设计不同浓度的As、Se测试溶液,每个浓度设置2个平行,对照组设置4个平行,每个平行中有4株幼苗。实验时,挑选根长一致的幼芽移植到装有250 mL测试溶液的烧杯中。随后将其移入培养箱中,在设定的暴露条件(温度20℃,湿度75%,光照强度52 000 lx,16 h光照,8 h黑暗)下培养4 d。在实验过程中,每日更新测试溶液,以降低植物生长对溶液pH和金属浓度的潜在影响。暴露4 d后,将幼苗从烧杯中取出,记录每株幼苗最长的根长值。计算相对根伸长(RRE,%),作为小麦暴露于As、Se及其二元混合物的毒性终点。
1.5 化学分析
在毒性测试前后分别测定每个处理组的pH值,pH平均值用于化学形态计算。采用ICP-OES对测试液的As、Se进行测定,每测20个样品会加入1个5 mg·L-1的多元素标准试剂(MultiElement Calibration Std.#1,J&K Scientific Ltd.)和1个空白样品进行质量控制,As和Se的回收率均在90%以上。利用WHAMⅦ软件计算As、Se的自由离子活度,输入的模型参数包括As、Se浓度、测试溶液pH值、温度、CO2分压等。
1.6 数据分析与建模
1.6.1 剂量响应曲线拟合
综合每组小麦根伸长数据,得到平均相对根伸长与平均相对偏差,其中相对根伸长是实验测量小麦根伸长与该组对照组小麦根伸长之比,公式为:
式中:LA表示暴露于测试溶液中的小麦根伸长,cm;LC表示对照组中小麦的根伸长,cm。
依据log-logistic公式[38]拟合,得到对应的剂量-响应曲线。

式中:Ci表示化合物i在体系中的浓度;溶解浓度表示为{M}diss,自由离子活度表示为{M}free;βi表示剂量响应曲线的斜率;EC50为半数有效浓度,是指当小麦根伸长达到50%抑制时对应的浓度。在本实验中,EC50值越大代表含氧阴离子型金属在该条件下的毒性越小,反之则越大。
1.6.2 CA模型
在CA模型中,混合体系中的a、b组分都通过同一毒性作用模式产生毒性效应,可表述为:

式中:xi表示化合物i在混合物体系中产生的毒性效应;Ci表示化合物i在体系中的浓度;ECxi表示该化合物单独作用并产生xi(%)毒性效应时对应的单组分浓度。
1.6.3 IA模型
与CA不同的是,IA模型假设混合体系内的组分通过不同毒性作用模式产生毒性效应。公式可描述为:
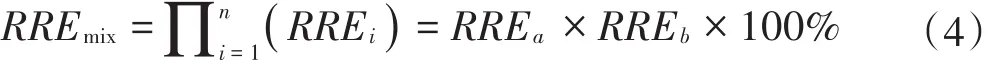
式中:RREi表示化合物i在单一暴露时产生的毒性效应。
1.6.4 BLM模型
BLM将生物膜表面活性位点视为配位体(生物配体,BL),根据BLM理论[26],金属毒性强弱取决于其所结合的生物配体BL占所有配体的比例fMBL,结合其他竞争性阳离子(Ca2+、Mg2+、Na+、K+)与pH值的影响,可表述为:

式中:K表示条件结合常数;{Mn+}和{XZ+}分别表示金属离子和竞争性阳离子的自由离子活度,mol·L-1。
当金属(M)产生50%毒性效应时,公式(5)可改写为:
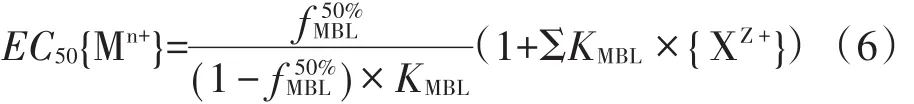
式中:EC50{Mn+}为导致50%毒性效应时金属离子的活度;f50%MBL为导致50%毒性效应时小麦根配体位点被金属离子占据的比例。小麦根长可以表述为:

本研究中,考虑As-Se交互作用,将BLM应用于As-Se联合毒性的预测时,可将公式改写为:

BLM模型所需参数,如条件结合常数K、βi和fM5B0L%等均使用Excel 2010软件通过最优化RRE和fMBL的关系估算得到。
2 结果与讨论
2.1 单一体系下As、Se胁迫对小麦的毒性
如图1所示,As、Se单独作用于小麦时,随着As、Se浓度的增加,小麦根长逐渐减小,表明二者都具有毒性。通过Logistic模型对其剂量响应曲线进行拟合,可求得As和Se的半数有效浓度(表2)。当以溶解态浓度为剂量表达时,As和Se的EC50分别为3.03 μmol·L-1和45.35 μmol·L-1,当以自由离子活度为剂量表达时,二者的EC50分别为2.88μmol·L-1和43.51 μmol·L-1,由剂量响应曲线可知,无论以何种剂量表达形式,As的毒性都远高于Se。从单一毒性测试中获得的剂量响应曲线参数将直接用于CA和IA模型预测As-Se二元混合物毒性。
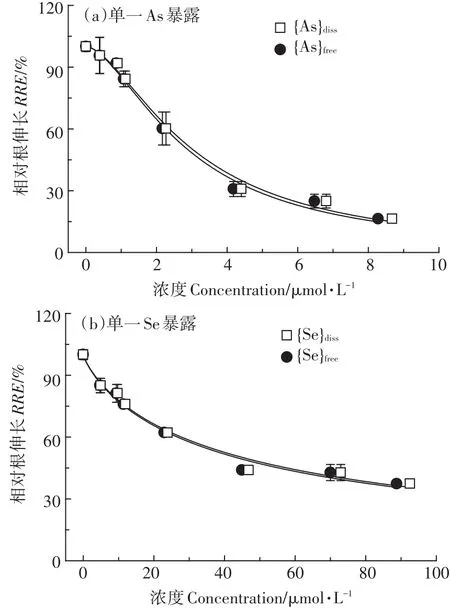
图1 单一体系中小麦相对根伸长与溶解态金属浓度以及自由离子活度之间的剂量响应关系Figure 1 Dose-response relationship between relative root elongation of Triticumaestivum and dissolve metal concentrations/freemetal ion activitiesin single As(a)and Se(b)exposuresystem

表2 As、Se剂量-响应曲线拟合参数输出Table 2 Summary of dose-response parameters(EC50 with standard errors are indicated in brackets,β)for Asand Se
2.2 As胁迫对小麦Se毒性的影响
不同浓度As胁迫对Se生物毒性的影响见图2a和图2b。通过比较两图可以发现,两种剂量表达方法即溶解浓度和自由离子活度在毒性规律上区别不大,基本相似。当Se浓度相同时,随着环境中As浓度的增加(即,溶解浓度从0.40μmol·L-1增加到6.81 μmol·L-1;自由离子活度从0.38 μmol·L-1增加到6.45 μmol·L-1),小麦相对根伸长出现了明显的降低趋势,说明当环境中Se浓度不变时,As浓度的增加会对小麦产生明显的毒害作用,导致小麦受到As-Se的联合毒性作用。
2.3 Se胁迫对小麦As毒性的影响
不同浓度Se胁迫对As生物毒性的影响见图2c和图2d。通过比较两图可以发现,两种剂量表达方法即溶解浓度和自由离子活度在毒性规律上有所区别。由剂量响应曲线可知,当As浓度较低时(即,溶解浓度小于2.27μmol·L-1;自由离子活度小于2.16 μmol·L-1),随着Se浓度的增加(即,溶解浓度从4.94 μmol·L-1增加到 72.95 μmol·L-1;自由离子活度从4.74 μmol·L-1增加到69.97 μmol·L-1),小麦相对根伸长有明显减小的趋势,说明低浓度As条件下,Se浓度的增加,显著加强了其毒性作用。但随着As浓度的增加,这种趋势越来越小,说明高浓度As条件下,Se浓度的增加对其毒性的影响较小。
在As-Se二元混合物中,不论以何种剂量表达形式,一种阴离子金属的存在都会影响另一种阴离子金属的植物毒性(图2)。
2.4 CA/IA模型预测As-Se联合毒性
图3通过采用溶解浓度和自由离子活度剂量两种表达形式来比较CA和IA模型所预测的效应值(相对根伸长值)与实际观测值的差异,从而确定交互作用类型,见表3。结果显示,在CA/IA模型中,无论是基于何种剂量表达形式,模型预测值整体上都小于实际观测值。这表明简单的CA/IA模型高估了含氧阴离子型金属二元混合物对陆地植物小麦的毒性。在CA/IA模型中,当相对根伸长的模型预测值与实际观测值的比值小于1时,说明二元混合污染物之间存在拮抗作用;若相对根伸长的模型预测值与实际观测值的比值大于1,则说明二元混合污染物之间存在协同作用。从图中可以发现,As-Se之间的拮抗作用很明显。当相对根伸长较长时,即As-Se浓度较低时,As-Se之间只存在拮抗作用;随着As-Se浓度和毒性的增加,在关系图的中间部位出现了轻微的加和作用;当As-Se浓度继续增加时,As-Se之间还是表现为拮抗作用。整体来看,As-Se之间的联合毒性还是以拮抗作用为主。Se对As的拮抗效应已被大量报道,陈海珍等[39]认为As与Se结构相似,因而具有相似的吸收机制,二者存在竞争关系,因此Se能缓解As的毒害作用。As-Se之间存在着复杂的相互作用,有研究指出Se拮抗As对水稻的毒害作用是由于二者之间较强的化学亲和力形成了某种稳定且低毒的As-Se复合物,而非Se的存在降低水稻根际对As的吸收量[40]。此外,Se具有较强的抗氧化能力可缓解As污染毒害对植物体内抗氧化系统酶的抑制作用,从而降低了植物体内As的毒性效应[40]。

图2 不同Se(As)浓度下,As(Se)浓度与小麦相对根伸长之间的剂量响应关系Figure 2 Dose-response relationship between the dissolved concentration(a,c)/free ion activity(b,d)and relative root elongation of Triticumaestivum in As-Se mixture

表3 CA/IA模型预测As-Se联合毒性Table 3 Performances of CA/IA for quantifying toxicities of As-Se to wheat roots
2.5 BLM模型预测As-Se联合毒性
CA/IA模型在预测As-Se联合毒性时,其预测值整体上都小于观测值,两种模型都高估了联合毒性,表明As-Se间存在交互作用,主要表现为拮抗作用。对于具有交互作用的混合物CA/IA模型并不能定量预测其毒性,且无法被用来直接解读混合物毒性作用机理,因此进一步尝试使用充分考虑了生物有效性的BLM模型解释As-Se交互作用并预测联合毒性,考虑了混合物交互作用的BLM模型更能反映混合物毒性的实际情况,在实际环境中更具有参考价值和现实意义。将单一As、Se以及As-Se混合的毒性数据一起进行BLM模型拟合,使用Excel 2010软件中的规划求解功能通过获得最小化均方根误差(RMSE)来最优化RRE和fMBL的关系,从而估算As、Se的结合常数K、f50%MBL和βM等模型参数,见表4。
由图4可知,使用BLM模型对As-Se联合胁迫下小麦根长毒性效应进行的预测能力效果很好(R2=0.90),这表明所构建的BLM模型实现了对含氧阴离子型二元金属混合物联合毒性的准确预测,解释了超过90%的毒性变化。在BLM模型中,考虑到As-Se外部竞争作用导致的生物有效性的变化,所有数据点都集中在1∶1线附近,反映出这种拮抗作用主要发生在生物体外部,As-Se整体上呈现浓度加和(无拮抗或协同作用)的趋势,有力地证明了阴离子型金属采用BLM模型是进行环境质量风险评估的有效方式。
3 结论
(1)不论以何种剂量表达形式(溶解浓度和自由离子活度剂量),一种阴离子金属的存在都会影响另一种阴离子金属的植物毒性。

图3 CA/IA模型预测As-Se联合毒性效应与实际观测值的对比Figure 3 The mixed effects were predicted using the reference models(CA and IA)based on the dissolved metal concentration(a)and free ion activity(b)

表4 BLM模型预测As-Se联合毒性参数Table 4 Summary of model fitsassociated with the BLM to As-Se toxicities to wheat roots
(2)根据获得的As、Se单一毒性数据,利用不同剂量表达耦合加和参考模型(CA/IA)预测混合物毒性时,无论是基于何种剂量表达形式,模型预测值整体上都小于实际观测值,表明加和参考模型高估了As-Se二元混合物对陆生植物小麦的毒性,因此判定As-Se之间呈明显拮抗作用。
(3)将As-Se外部竞争作用纳入BLM模型后,实现了对阴离子型类金属As-Se联合毒性的准确预测,由于该模型充分考虑了生物有效性的重要性,更能反映As-Se混合毒性的真实情况,在实际环境中更具参考价值和现实意义。
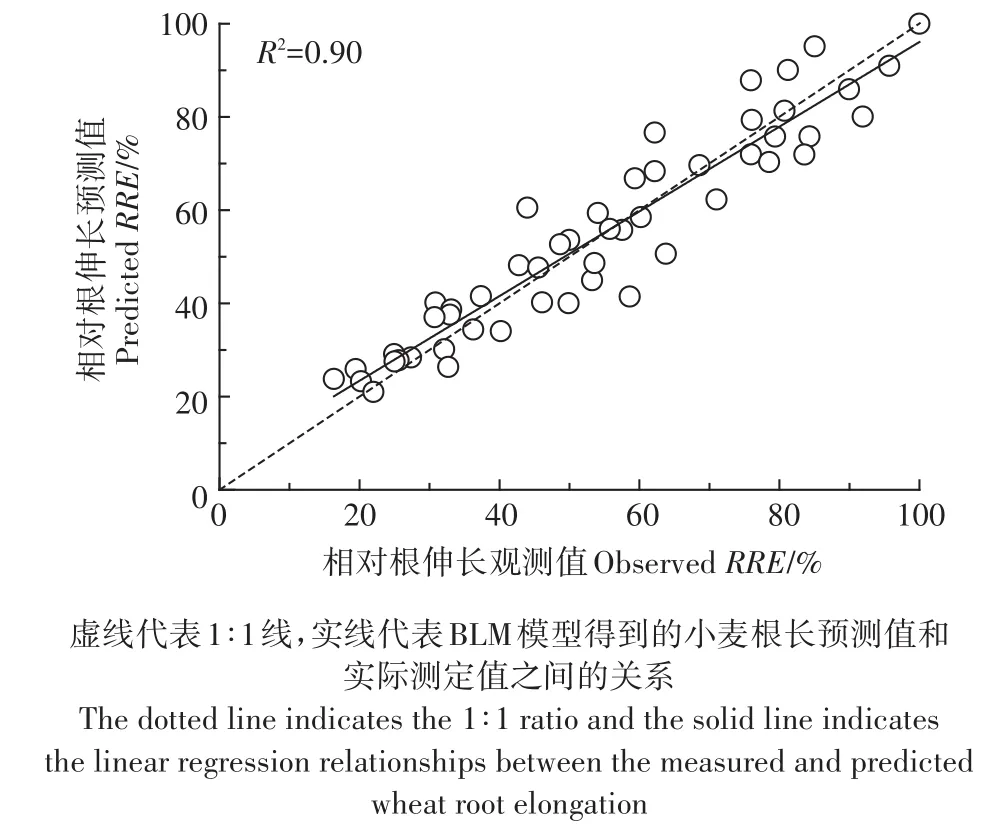
图4 BLM模型预测As-Se联合毒性效应与实际观测值的对比Figure 4 The observed versus predicted relative root elongation of Triticum aestivum exposed to As-Semixture for 4 days based on the BLM

