柔性钯-银纳米线电极用于非酶葡萄糖检测
孟维琛 王清翔 李彦钊 冯凌竹 郎明非 陈宏甡* 孙 晶*
(大连大学环境与化学工程学院1, 附属中山医院2, 医学院3, 大连 116622)
1 引 言
近年来,可穿戴智能电子设备在医疗保健监测[1~3]、身体运动检测[4,5]、电子皮肤应用[6,7]等领域受到广泛关注。然而,因技术及材料原因,现有设备中含有大量刚性电子部件,无法与人体兼容,即无法满足柔软、弹性、可弯曲的条件,因此,柔性材料的开发成为最近的研究热点。Liu等[8]在聚二甲基硅氧烷(PDMS)中掺杂粉末碳,制成拉伸或压缩应变传感器,通过快速拉伸和释放PDMS,记录相对电阻的变化来表征器件的灵敏度,发现拉伸120%时,应变响应快,掺杂了碳的PDMS也表现出了更快的弛豫。Rahimi等[9]研制了一种能实时测量手指运动的柔性传感器,采用激光热解聚酰亚胺产生碳,然后在碳化的聚酰亚胺上浇注未固化的PDMS,待PDMS固化后,碳全部转移和嵌入至PDMS中。此传感器具有高伸缩性(高达200%应变)和高灵敏性(测量系数高达20000)。拉曼光谱分析结果表明,在最佳的激光条件下,可以获得多层纳米碳,且薄层电阻可低至60 Ω/□。Ferrari等[10]制作了一种临时纹身电极,将导电聚合物喷墨印刷到商业贴花转印纸上,然后再转印在皮肤上,其具有超低厚度(<1 μm),保证了极好的不可感知性,且其检测性能与商品电极相当。
近年来,糖尿病患者越来越多,为了检测血糖水平,很多糖尿病患者每天需多次刺破手指,研究者一直在寻找无创检测血糖的简便方法。将柔性材料应用于葡萄糖传感器,制造可穿戴医疗设备,已成为一种新思路。2014年,谷歌公司曾提出制作智能隐形眼镜(Smart contact lens)检测泪液中葡萄糖,进而监测糖尿病人的血糖项目,但是由于技术问题,此项目已宣布暂停。无创葡萄糖检测的另外一种思路是进行唾液中葡萄糖的检测。研究表明,糖尿病患者唾液糖浓度明显高于正常人[11],可能与糖尿病患者腮腺基底膜的通透性增加有关[12]。研发柔性可穿戴唾液葡萄糖传感器,对糖尿病的预防和治疗具有重要意义。
本研究组已建立了用AgNWs(Silver nanowires, AgNWs)和PDMS(Polydimethylsiloxane, PDMS)制备柔性电极的方法,并将其应用于水中Cu2+的检测[13]。这种新型AgNWs/PDMS电极具有可拉伸、弯折、性能稳定、导电性好、检测灵敏度高的特点。本研究以这种AgNWs/PDMS电极为工作电极,利用电化学方法在AgNWs上电沉积一薄层钯纳米粒子,由于AgNWs的纳米尺寸效应,AgNWs表面的钯纳米粒子同样具有较大的比表面积。这种Pd-AgNWs电极对葡萄糖具有良好的电化学响应,以其作为工作电极,可制备出检测性能优异、灵敏度高的柔性葡萄糖传感器。
2 实验部分
2.1 仪器与试剂
CHI660E电化学工作站(上海辰华仪器有限公司); DZF-6050真空烘箱(上海一恒科学仪器); SHZ-Ⅲ循环水真空泵(上海亚荣生化仪器厂); JELIGHT M紫外臭氧清洗机(美国Jelight公司); PC超纯水机(成都品成科技有限公司); GM-0.33B隔膜真空泵(天津津腾实验设备有限公司); S-4800扫描电子显微镜(日本Hitachi公司); BSA224S万分之一分析天平(北京Sartorius公司); EMS-8B加热磁力搅拌器(天津欧若仪器仪表有限公司); Smart R17台式高速冷冻离心机(韩国Hanil公司); K-50HB手动拉力测试仪(福州艾普仪器有限公司); M-3型手持式数字四探针测试仪(苏州晶格电子有限公司)。
AgNWs(直径为90 nm、长度为60 μm)溶液(20 mg/mL,南京先丰纳米材料科技有限公司); RTV615 PDMS(迈图高新材料集团); 丙三醇(Glycerol,Gly)、冰醋酸、乙酸钠(美仑生物技术有限公司); 聚乙烯醇(Polyvinyl alcohol,PVA)、氯化钯、无水乙醇、葡萄糖(国药集团); 尿素(天津市大茂化学试剂厂); 多巴胺、尿酸(萨思化学技术有限公司); 抗坏血酸(天津博迪化工股份有限公司); 除特别标注外,所用试剂均为分析纯,实验用水为超纯水。
2.2 实验过程
2.2.1 柔性纳米Pd-AgNWs电极的制备向放入硅片的表面皿中浇注质量比为10:1的PDMS混合溶液,用真空泵抽尽气泡后,放入烘箱中固化2 h,剥离和切割后得到固体PDMS芯片,用臭氧清洗机清洗PDMS表面。用4%(w/w)PVA和7%(w/w)Gly浸泡PDMS芯片 20 min,对其进行亲水修饰,将表面多余液体刮除后,放入60℃的烘箱中抽真空干燥。将亲水修饰的实验步骤重复两次,再放入80℃的烘箱中固化20 min,得到表面亲水的PDMS芯片。
Pd-AgNWs电极的制作过程如图1所示。取30 μL 0.8 mg/mL AgNWs溶液,均匀涂覆在修饰好的PDMS表面,待AgNWs晾干后,将有AgNWs涂层的PDMS作为工作电极,铂丝电极为对电极,Ag/AgCl电极为参比电极,将三电极体系置于以pH=4的醋酸-醋酸钠为缓冲溶液、 5 mmol/L PdCl2溶液中,采用循环伏安法在AgNWs上沉积纳米钯。制备了8种电极,分别为进行了5、10、15、20、25、30、35、40个循环后的Pd-AgNWs电极,随着循环圈数增加,AgNWs上的钯的含量逐渐增大。
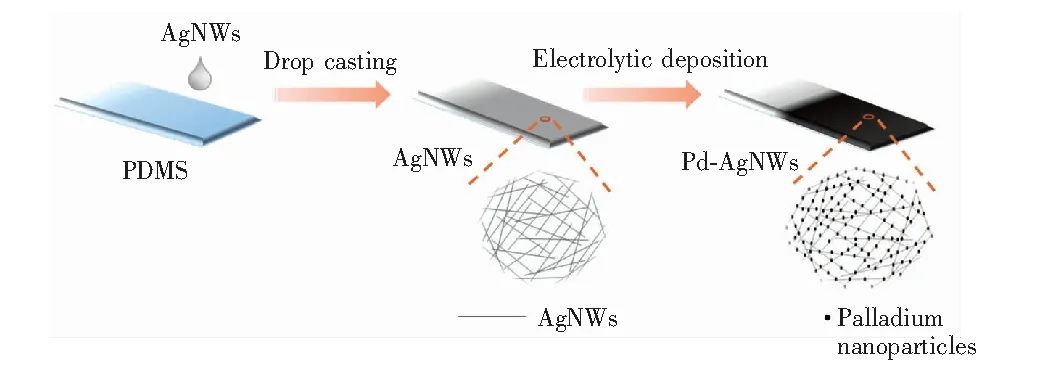
图1 钯-银纳米线(Pd-AgNWs)电极制作过程示意图Fig.1 Diagram of fabrication process of the palladium-silver nanowires (Pd-AgNWs) electrodePDMS, polydimethylsiloxane
2.2.2 电化学测试电化学实验在CHI660E型电化学工作站上进行,采用三电极体系: Pd-AgNWs为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极。采用循环伏安法检测葡萄糖,电位控制范围在-0.7~1.0 V之间。制备电极对葡萄糖的氧化还原反应在0.1 mol/L KOH溶液中进行,实验前对缓冲溶液通高纯氮至少30 min,且在实验过程中一直保持氮气气氛。所有电化学实验在(24±2)℃下进行。
3 结果与讨论
3.1 Pd-AgNWs电极的表征
3.1.1 Pd-AgNWs电极的结构和形貌图2是AgNWs电极(A)和在AgNWs电极上分别进行了5(B)、10(C)、15(D)、20(E)、25(F)、30(G)、35(H)和40(I) 圈钯沉积所制备的Pd-AgNWs电极的扫描电子显微镜(SEM)示意图。如图2所示,随着沉积圈数增加,纳米线的直径逐渐增大,纳米线表面的粗糙度也逐渐增加,纳米钯颗粒的粒径也随之增加。

图2 AgNWs电极(A)和通过循环伏安法制备的Pd-AgNWs电极的SEM图(B~I),B~I分别对应进行了 5、 10、15、20、25、 30、35和40个循环钯沉积; 电压扫描范围: -0.7~1.0 V; 扫速: 50 mV/sFig.2 Scanning electron icroscopy (SEM)images of AgNWs electrode (A) and Pd-AgNWs electrodes (B-I)(Pd deposited by cyclic voltammetry method for 5(B), 10(C), 15(D), 20(E), 25(F), 30(G), 35(H) and 40(I) cycles; scan range: -0.7-1.0 V; scan rate: 50 mV/s)
3.1.2 Pd-AgNWs电极柔性测试Pd-AgNWs电极具有良好的柔韧性,可被多次拉伸和弯折,电极在拉伸和弯折后仍然保持良好的电化学检测性能。图3A是将电极180°弯折25、50、100次后,以其为工作电极,利用循环伏安法检测10 mmol/L葡萄糖的氧化峰电流最大值和电阻的变化图。随着弯折次数的增加,葡萄糖氧化峰电流最大值稍有下降,经过100次弯折,氧化峰电流最大值下降了4.8%,电阻扩大了1.83倍。图3B是将电极分别拉伸为原长的150%、180%、200%后,以其为工作电极,利用循环伏安法检测10 mmol/L葡萄糖溶液的氧化峰电流最大值和电阻的变化图。同样,随着拉伸长度增大,葡萄糖氧化峰电流最大值稍有下降,经过200%拉伸后,氧化峰电流最大值下降2.1%,电阻扩大了1.92倍。以上结果说明Pd-AgNWs电极在弯折和拉伸后仍具有良好的电化学性能,和传统的硬质电极相比,具有更广阔的应用范围。
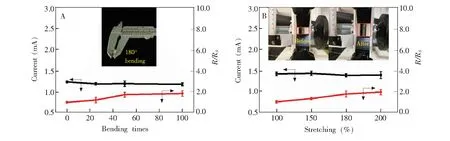
图3 (A) Pd-AgNWs电极180°弯折25、50、100次后电阻的变化,及用于检测10 mmol/L葡萄糖溶液的循环伏安氧化峰电流最大值变化情况,内插图为电极弯折180°的实物图; (B) Pd-AgNWs电极拉伸至原长的150%、180%、200%后电阻的变化,及用于检测10 mmol/L葡萄糖溶液的循环伏安氧化峰电流的最大值变化情况,内插图为电极未拉伸和拉伸200%的实物图Fig.3 (A)The resistance change of Pd-AgNWs electrodes with 180°bending for 25, 50 and 100 times, and variation of oxidative peak current of cyclic voltammogram on detection of 10 mmol/L glucose. Inset shows the picture of the real electrode after bending; (B) The change of resistance of the Pd-AgNWs electrodes after 150%, 180%, and 200% stretching, and variation of oxidative peak current of cyclic voltammogram on detection of 10 mmol/L glucose. Inset shows the pictures of electrode before and after 200% stretching
3.1.3 Pd-AgNWs的精密度、重现性与稳定性测试为了测定所制备柔性Pd-AgNWs电极的精密度,在优化的实验条件下,使用同一支Pd-AgNWs电极对10 mmol/L葡萄糖溶液重复测定20次,得到的曲线基本重合,葡萄糖氧化峰电流的相对标准偏差(RSD)为1.4%,表明此传感器具有较好的精密度。
为了检测所制备柔性Pd-AgNWs电极的重现性。在相同条件下,使用同批次制得的5支Pd-AgNWs电极检测10 mmol/L葡萄糖溶液,氧化峰电流的RSD值为2.3%,说明不同电极之间具有较好的重现性。
测定了柔性Pd-AgNWs电极的稳定性。将电极储存于室温空气中,对10 mmol/L葡萄糖溶液每周测试一次,在测量之前,用0.1 mol/L KOH溶液清洗电极表面,储存30天后,葡萄糖传感器的响应信号仅降低了8%,说明电极在空气和室温条件下具有长期稳定性。
3.2 葡萄糖的电催化氧化
3.2.1 Pd沉积圈数对葡萄糖检测的影响在电沉积过程中,钯纳米粒子的沉积量和颗粒大小与沉积圈数密切相关,对所制得的电极的电活性影响较大。将不同钯沉积圈数制备出的Pd-AgNWs电极用于10 mmol/L葡萄糖溶液的循环伏安检测,发现沉积圈数对葡萄糖氧化峰电流最大值具有较大影响。当沉积圈数小于25圈时,响应电流随着沉积圈数的增加而增大,这可能是因为沉积圈数过少,导致在AgNWs电极表面沉积的钯粒子量过少,对葡萄糖的催化效果不佳; 当沉积圈数为25时,响应电流值达到最大; 而当沉积圈数大于25时,响应电流随着圈数的增加而减小。这是因为随着沉积圈数的增加,AgNWs表面沉积钯的量逐渐增多,颗粒直径逐渐增大; 沉积圈数大于25圈时,虽然沉积钯的量增加了,但是纳米钯粒子粒径的增大,减小了钯电极的活性面积,从而影响了葡萄糖的催化效果。因此,选择制备Pd-AgNWs电极的最佳沉积圈数为25圈。
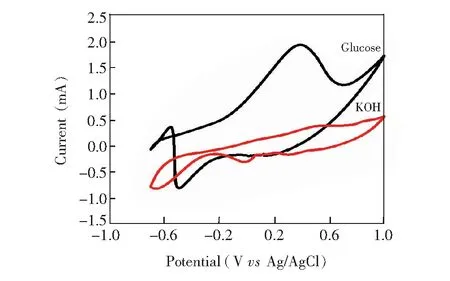
图4 Pd-AgNWs电极在0.1 mol/L的KOH空白溶液和加入10 mmol/L的葡萄糖溶液中的循环伏安曲线Fig.4 Cyclic voltammograms of Pd-AgNWs electrode in 0.1 mol/L KOH solution with or without 10 mmol/L glucose
3.2.2 空白对比采用循环伏安法研究了Pd-AgNWs电极对葡萄糖的催化活性。采用0.1 mol/L KOH溶液为空白溶液,将葡萄糖溶解于空白溶液中得到葡萄糖溶液。电化学响应曲线见图4,正向扫描时,在0.3 V处电流开始增大,根据文献[14,15]报道,这是因为电极表面的钯在碱性溶液中发生氧化反应,失去一个电子氧化为Pd(OH); 在负向扫描时,在0 V处出现了金属氧化物的还原峰,说明形成的Pd(OH)因得到一个电子而被还原为Pd。Pd-AgNWs电极对葡萄糖溶液的响应电流(图4)远高于空白溶液。在外加电场下,循环伏安曲线在-0.6 V和0.4 V附近出现了两个明显的氧化峰。其中,0.4 V处的氧化峰归因于葡萄糖的直接电化学氧化,电位继续增加,金属氧化物积累在活性位点上抑制了葡萄糖的电吸附,从而导致氧化电流减小。在负向扫描时,电极表面的金属氧化物被还原,被占用的金属活性位点被释放,用于进一步反应,所以在-0.6 V出现了葡萄糖的二次氧化峰,对应葡萄糖氧化产物“葡萄糖酸内脂”的进一步氧化[16]。以上结果表明,Pd-AgNWs电极对葡萄糖的电化学氧化具有良好的电催化活性,Pd-AgNWs电极对葡萄糖的催化机理如下:

3.2.3 AgNWs电极和Pd-AgNWs电极对葡萄糖的催化行为制备的AgNWs电极和Pd-AgNWs电极对10 mmol/L葡萄糖的循环伏安曲线如图5所示,AgNWs电极上未出现明显的葡萄糖氧化电流,说明AgNWs电极对葡萄糖没有催化氧化作用; Pd-AgNWs电极对葡萄糖具有明显的伏安响应,表明纳米钯颗粒在无酶葡萄糖柔性传感器的构建中具有电化学氧化还原葡萄糖的活性。
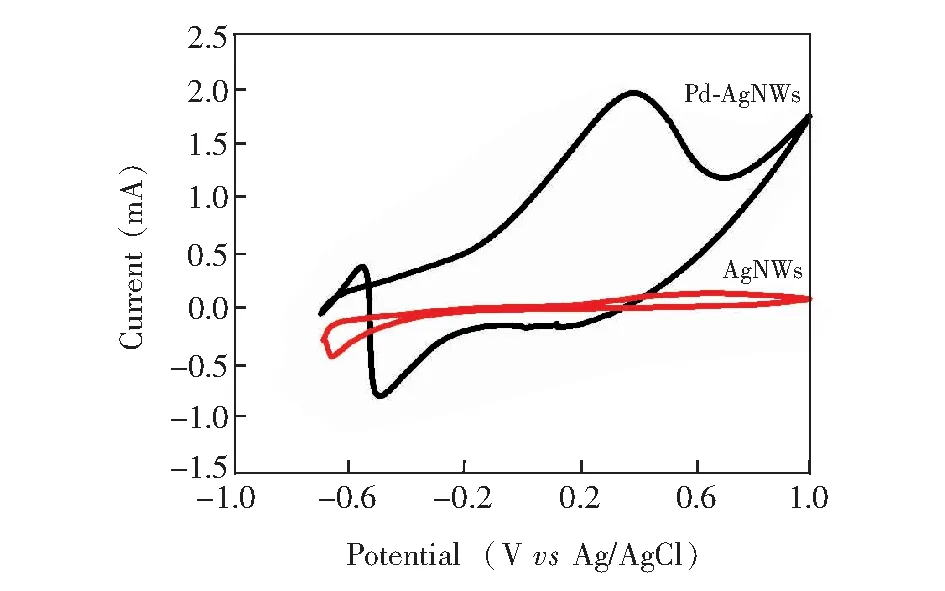
图5 AgNWs电极和Pd-AgNWs电极在10 mmol/L葡萄糖溶液中的循环伏安曲线Fig.5 Cyclic voltammograms of AgNWs electrode and Pd-AgNWs electrode in 10 mmol/L glucose
3.2.4 扫速对葡萄糖检测的影响采用Pd-AgNWs电极对10 mmol/L葡萄糖溶液进行检测。不同扫描速度的循环伏安曲线如图6所示。在20~200 mV/s范围内,随着扫描速度的增加,氧化峰电流随之增大,且氧化峰电位逐渐正移。扫描速率的平方根与峰电流呈良好的线性关系,线性方程为y=0.117x+0.8, 相关系数为0.998,表明葡萄糖在Pd-AgNWs电极上的氧化过程为扩散控制过程。
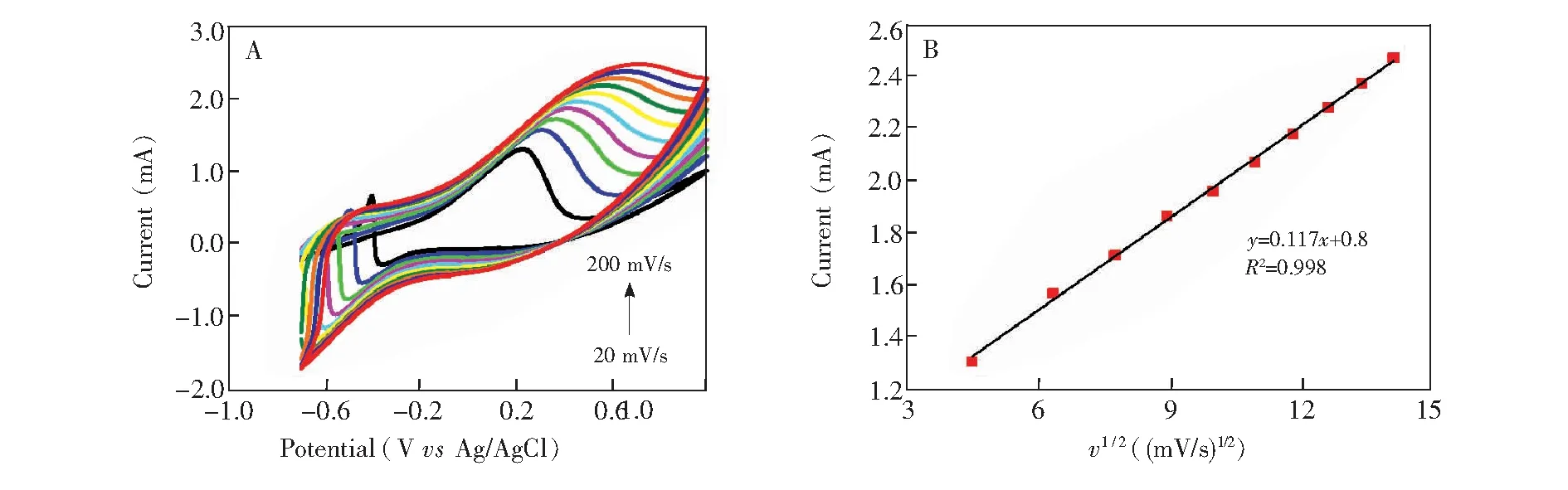
图6 (A) 不同扫速下,Pd-AgNWs电极检测10 mmol/L葡萄糖溶液的循环伏安图; (B) 不同扫速下,Pd-AgNWs电极检测10 mmol/L葡萄糖时扫描速率平方根与氧化峰峰值电流的线性关系Fig.6 (A) Cyclic voltammograms of Pd-AgNWs electrode in 10 mmol/L glucose at different scan rates; (B) Relationship between the oxidization peak current and the square root of scan rate of Pd-AgNWs electrode in 10 mmol/L glucose at different scan rates
3.3 葡萄糖安培传感器
采用电流-时间(i-t)法评估制备的柔性Pd-AgNWs电极对葡萄糖检测的灵敏度。在恒定电位为0.4 V的条件下,从150 s开始,每隔30 s,向不断搅动的0.1 mol/L KOH溶液中依次逐滴加入5次20 μmol/L、4次100 μmol/L和7次500 μmol/L的葡萄糖溶液,检测电极的电流响应。Pd-AgNWs电极对葡萄糖的安培响应曲线如图7所示,当向溶液中加入葡萄糖时,电流急剧增加,并以均匀的增量达到稳定状态,因此在恒电位下显示阶梯式增长。取各个稳态电流值进行线性拟合,结果如图7插图所示,在低浓度区域和高浓度区域分别对应两个线性范围0.02~0.5 mmol/L和1~4 mmol/L,线性方程分别为y=33.181x+7.404和y=25.397x+8.408,线性相关系数分别为0.995和0.996。葡萄糖检测的灵敏度为33.18 μA/(cm2(mmol/L)),检出限为1.0 μmol/L(S/N=3)。与其它葡萄糖传感器(表1)相比,Pd-AgNWs电极检测灵敏度高,线性范围宽。
表1 不同无酶葡萄糖传感器的性能比较
Table 1 Analytical parameters obtained at different glucose sensors
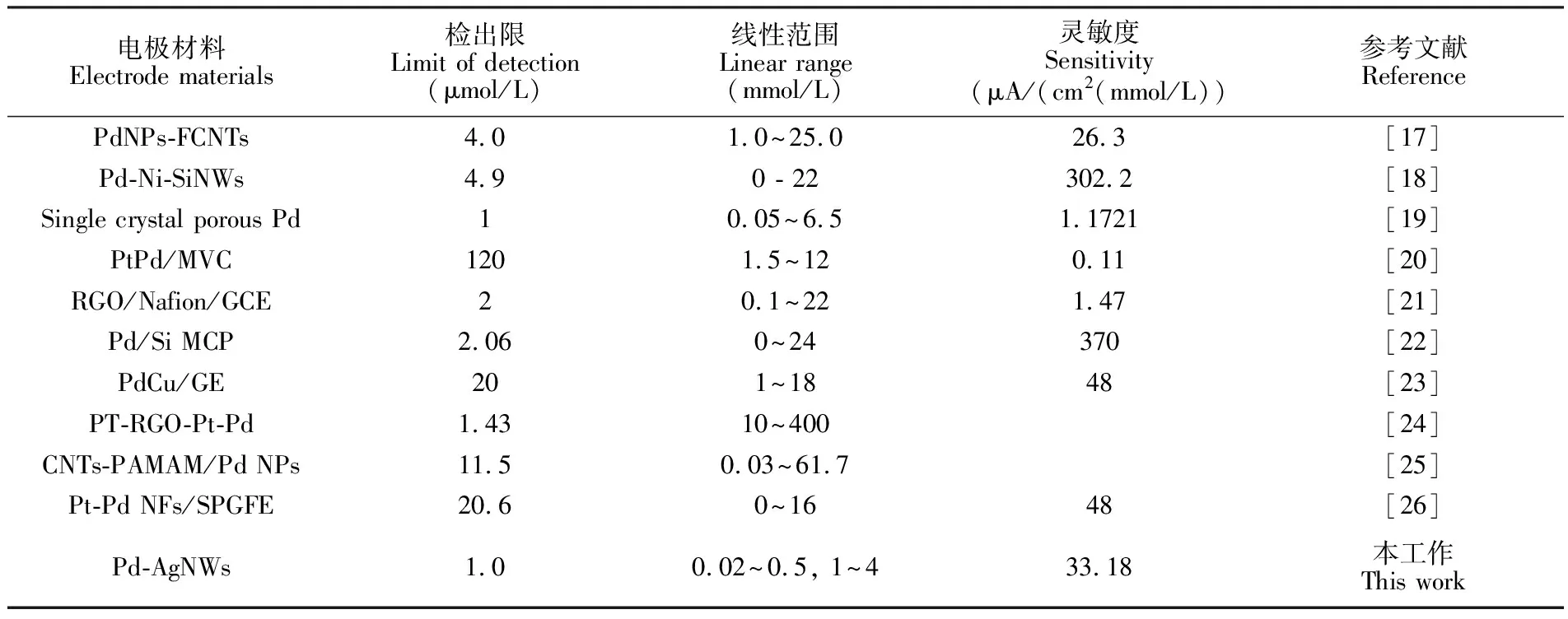
电极材料Electrode materials检出限Limit of detection(μmol/L)线性范围Linear range(mmol/L)灵敏度Sensitivity(μA/(cm2(mmol/L))参考文献ReferencePdNPs-FCNTs4.01.0~25.026.3[17]Pd-Ni-SiNWs4.90 - 22302.2[18]Single crystal porous Pd10.05~6.51.1721[19]PtPd/MVC1201.5~120.11[20]RGO/Nafion/GCE20.1~221.47[21]Pd/Si MCP2.060~24370[22]PdCu/GE201~1848[23]PT-RGO-Pt-Pd1.4310~400[24]CNTs-PAMAM/Pd NPs11.50.03~61.7[25]Pt-Pd NFs/SPGFE20.60~1648[26]Pd-AgNWs1.00.02~0.5, 1~4 33.18本工作This work
3.4 方法的抗干扰性
在实际样品的测定时,非酶葡萄糖检测的主要干扰是抗坏血酸(Ascorbic acid, AA)、尿酸(Purine trione, UA)等易氧化化合物引起的。尽管在正常生理样品中葡萄糖的浓度远高于抗坏血酸、尿酸,但这些干扰物质的电子传递速率比葡萄糖快, 所以产生的氧化电流与葡萄糖相当。考虑唾液成分的复杂性,在恒定电位为0.4 V,不断搅动的条件下,向0.1 mol/L KOH溶液中依次加入0.1 mmol/L UA、 0.1 mmol/L AA、 0.1 mmol/L多巴胺(Dopamine, DA)、 0.1 mmol/L尿素(Urea, UR)、 0.1 mmol/L KCl、 0.1 mmol/L NaCl和1 mmol/L葡萄糖, 测试电极的抗干扰能力。如图8所示,与其它干扰物质相比,葡萄糖产生了明显的信号,表明Pd-AgNWs电极可以克服非酶葡萄糖传感器中存在的干扰问题,具有良好的抗干扰性。
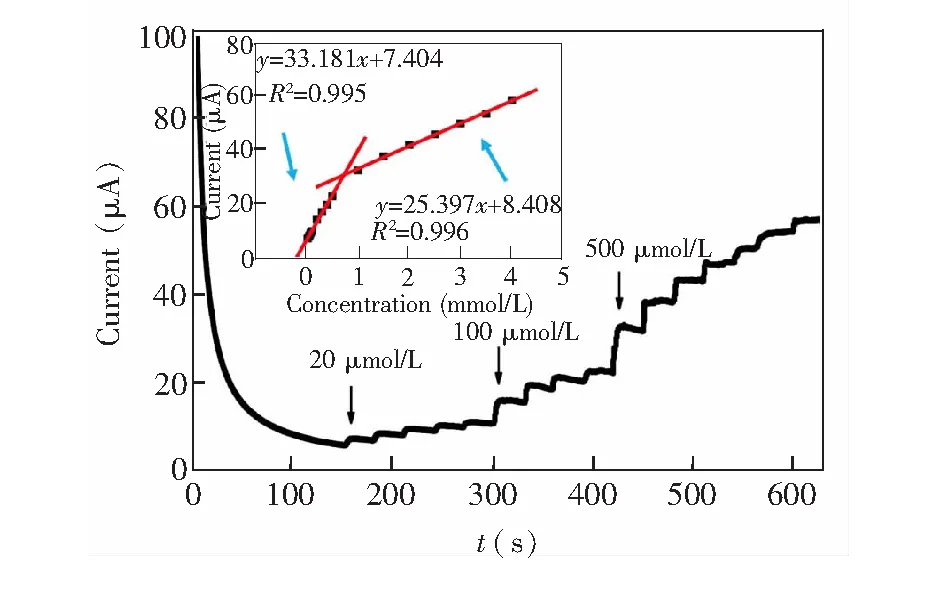
图7 将不同量葡萄糖(20 μmol/L, 100 μmol/L, 500 μmol/L)逐滴注入0.1 mol/L KOH空白溶液中,Pd-AgNWs电极的安培电流响应曲线, 插图为电流密度与葡萄糖浓度的线性关系曲线Fig.7 Typical amperometric current response curve of Pd-AgNWs electrode upon continuously injection of different concentrations of glucose (20 μmol/L, 100 μmol/L, 500 μmol/L)dropwisely in 0.1 mol/L KOH; Inset shows the linear relationship between response current density and glucose concentration
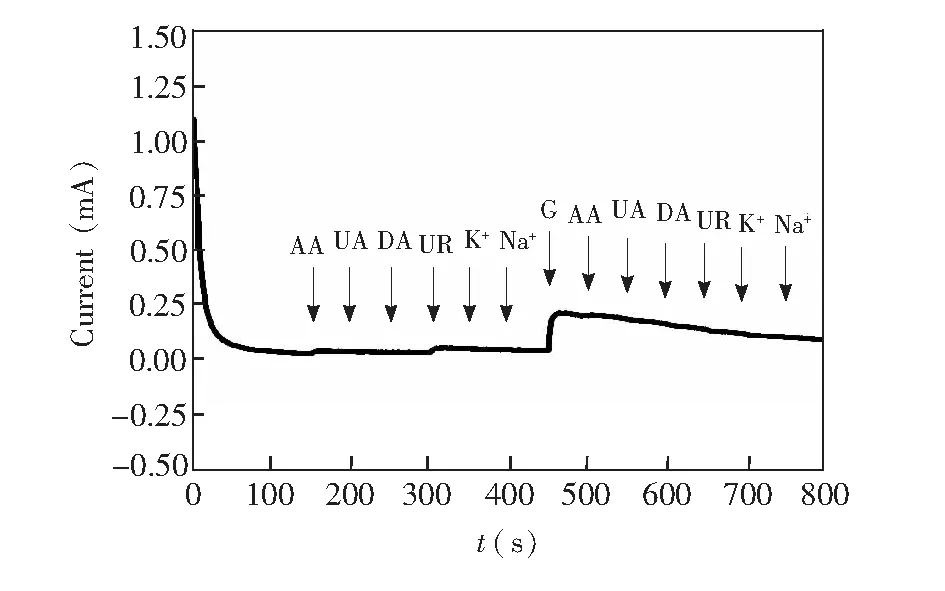
图8 Pd-AgNWs电极在1 mmol/L 葡萄糖溶液中对0.1 mmol/L抗坏血酸、0.1 mmol/L尿酸、0.1 mmol/L多巴胺、0.1 mmol/L尿素、0.1 mmol/L KCl和0.1 mmol/L NaCl电流响应曲线Fig.8 I-t curve of Pd-AgNWs electrode for 1 mmol/L glucose solution in the presence of 0.1 mmol/L ascorbic acid (AA), 0.1 mmol/L uric acid (UA), 0.1 mmol/L dopamine (DA), 0.1 mmol/L urea (UR), 0.1 mmol/L KCl and 0.1 mmol/L NaCl
3.5 唾液样品分析
将Pd-AgNWs电极应用于实际唾液样品中葡萄糖的测定。取3位健康受试者的唾液和3位糖尿病患者的唾液进行平行实验。受试者前一天临睡前均进行口腔清洁,取受试者清晨无刺激状态下自然分泌的混合全唾液100 μL,经3000 r/min离心5 min,取上清液测定,结果见表2。其中样品1、2、3是正常人唾液的测定结果; 样品4,5,6是糖尿病患者的测定结果。结果表明,糖尿病患者唾液中葡萄糖的含量明显高于健康受试者唾液中葡萄糖的含量,可能是因为血糖由唾液腺基底膜渗出,进入唾液导致的,此结果与文献[27]报道一致。回收率在97%~102%之间,说明本方法可用于临床样品的测定。
表2 唾液中葡萄糖的测定和回收率
Table 2 Measurement and recovery of glucose in saliva sample
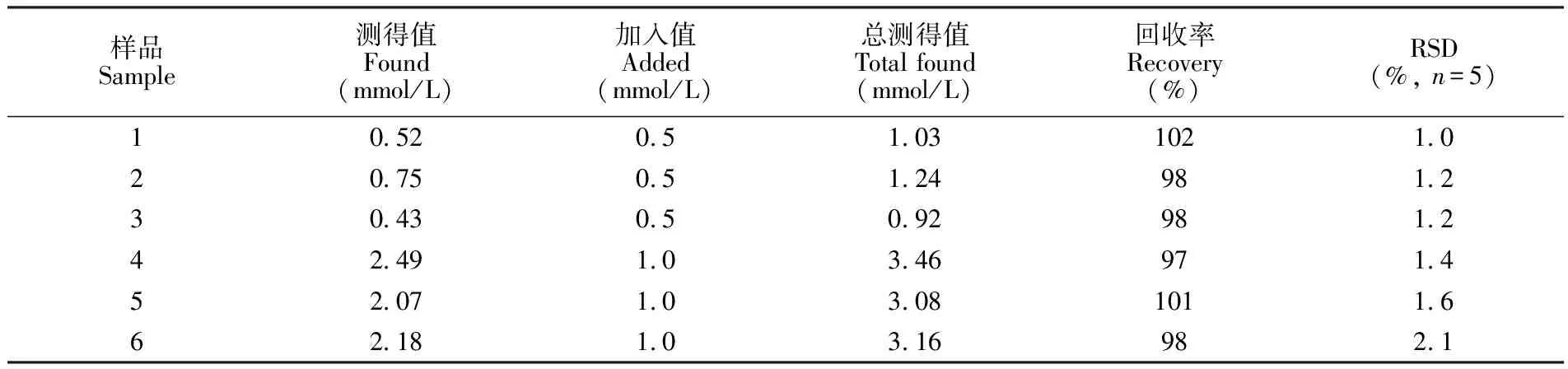
样品Sample测得值Found(mmol/L)加入值Added(mmol/L)总测得值Total found(mmol/L)回收率Recovery(%)RSD(%, n=5)10.520.51.031021.020.750.51.24981.230.430.50.92981.242.491.03.46971.452.071.03.081011.662.181.03.16982.1
4 结 论
制备了具有良好的拉伸和弯折性能的新型柔性Pd-AgNWs电极,并应用于葡萄糖的检测。此传感器具有催化活性好、灵敏度高、稳定性强、重复性好、 选择性好、响应快等优点。用于实际唾液中葡萄糖的检测,发现糖尿病患者唾液中的葡萄糖水平高于健康人唾液中葡萄糖的水平。此电极有望取代传统硬质电极,在可穿戴医疗设备领域具有良好发展前景。

