电子支气管镜检查在可疑恶性孤立性肺结节术前评估中的价值
王辉 陈伟庄 沈世茉 吴宏成
针对可疑恶性孤立性肺结节(solitary pulmonary nodule,SPN)是否常规行电子支气管镜检查评估目前仍存在争议[1-3],Prosch等[4]研究发现各专科医生对可疑恶性SPN的管理存在差异,影像科医生更倾向短期随访或CT引导下肺活检,而呼吸内科和胸外科医生对于可疑恶性SPN更推荐行支气管镜检查。而对可疑恶性SPN术前是否需要行常规支气管镜检查同样存在疑问。美国胸科医师学会(ACCP)指南目前仅推荐有空气支气管征的可疑恶性SPN术前行常规电子支气管镜检查[5],van’t Westeinde等[2]研究认为术前行电子支气管镜检查极少改变原计划手术方案。目前关于可疑恶性SPN患者术前是否常规行支气管镜检查的研究较少,本研究回顾性分析因可疑恶性SPN术前行电子支气管镜检查的502例患者的临床资料,研究术前行支气管镜检查对手术方式选择及手术指征的影响,评估常规电子支气管镜检查在可疑恶性SPN术前评估中的价值及分析相关受益人群(指检查结果使手术取消或术式改变的SPN患者)。
1 对象和方法
1.1 对象 选取2013年2月至2018年11月因可疑恶性SPN在本院行电子支气管镜检查的患者502例,其中男 321 例,女 181 例;年龄 30~83(60.6±8.3)岁。SPN定义:影像学直径≤3cm的边界清楚的单个病灶,无肺不张、肺门增大或胸腔积液。纳入标准:(1)根据SPN的影像学定义,通过胸部CT诊断的SPN患者;(2)参考美国胸科医师协会指南关于SPN的评估方法[5],评估倾向为可疑恶性SPN而拟手术的患者;(3)拟行手术前完成了常规电子支气管镜检查的患者。
1.2 方法 采用Olympus BF-260电子支气管镜(直径4.9mm,钳道 2.0mm),操作根据标准流程进行。电子支气管镜经鼻或经口进入患者气道,操作中观察患者上呼吸道、声带及支气管镜可观察的每级支气管树解剖结构、黏膜。根据CT显示的病变位置,操作者评估可否达到病灶位置,决定是否行经支气管镜活检、刷片和(或)灌洗,送检组织病理和(或)细胞学检查。根据患者支气管镜检查结果、病变特征、心肺功能等评估是否手术及手术方式。收集患者性别、年龄、结节位置、结节所处区域(从肺门到一侧肺野的最外部纵行平均分为内、中、外带3个区域)、结节密度、结节大小、支气管镜病理、支气管镜下管腔情况及手术方式等信息。
1.3 统计学处理 采用SPSS 19.0统计软件。计量资料以表示,组间比较采用两独立样本t检验;计数资料组间比较采用χ2检验。通过logsitic回归分析和ROC曲线分析筛选术前支气管镜检查的受益人群。P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料 502例患者中,SPN病变位于左上叶63例(12.5%),左下叶 81例(16.1%),右上叶153例(30.5%),右中叶83例(16.6%),右下叶122例(24.3%);位于内带 207例(41.2%),中带 173例(34.5%),外带122例(24.3%)。SPN 平均直径(1.95±0.54)cm,其中≤1cm 18例(3.6%),>1cm 且≤2cm 290例(57.8%),>2cm且≤30cm 194例(38.6%)。恶性SPN 461例(91.8%),平均年龄(60.63±8.39)岁,平均直径(1.96±0.54)cm;良性 SPN 41 例(8.2%),平均年龄(60.24±7.76)岁,平均直径(1.83±0.52)cm;两组年龄和直径比较差异均无统计学意义(t=0.282和1.437,均P>0.05)。
2.2 支气管镜检查结果 502例患者中,肉眼可见气道病变57例(11.4%),其中7例见支气管息肉样新生物(支气管镜活检病理均提示黏膜慢性炎)。3例见气道黏膜隆起(支气管镜活检病理均提示黏膜慢性炎)。2例见管腔外压性狭窄(支气管镜细胞学病理提示阴性)。2例见气道黏膜糜烂坏死样改变,支气管镜活检病理提示结核遂取消手术。43例见气道黏膜浸润样改变和(或)气道新生物,其中13例气道病变在原计划手术切除范围内遂维持原手术方案,支气管镜活检病理均提示恶性(9例鳞癌,2例非小细胞低分化癌,2例腺癌);30例因气道病变取消手术或改变原计划手术切除范围,其中5例支气管镜活检病理提示小细胞肺癌遂取消手术,其余25例均改变手术术式(3例支气管镜活检病理提示黏膜慢性炎、术后病理提示鳞癌,16例支气管镜活检病理提示鳞癌,3例提示腺癌,2例提示非小细胞癌,1例提示唾腺源性腺癌)。445例(88.6%)[包括250例纯磨玻璃样结节(ground-glass opacity,GGO)患者]支气管镜检查镜下表现均无异常,其中4例支气管镜毛刷找到抗酸杆菌诊断考虑肺结核予以取消手术,7例支气管镜毛刷找到癌细胞(倾向鳞癌)。
综上,共有11例患者(2.2%)因支气管镜检查结果取消手术,25例(5.0%)改变手术术式加大手术切除范围。
2.3 手术病理检查结果 491例行手术治疗患者中,456例(92.8%)术后病理检查提示恶性,其中42例术前支气管镜病理检查提示恶性,414例术前支气管镜病理检查未提示恶性;35例(7.2%)术后病理检查提示良性,其术前支气管镜检查均未提示恶性,所以支气管镜检查诊断恶性SPN的灵敏度为0.09(42/456),特异度为1.00(35/35),阳性预测值为 1.00(42/42),阴性预测值为 0.08(35/449)。456例术后病理诊断恶性的患者中鳞癌253例,腺癌176例,小细胞癌12例,腺样囊性癌2例,肉瘤样癌5例,腺鳞癌5例,基底细胞样癌1例,神经内分泌肿瘤1例,透明细胞型肾细胞癌转移1例。35例术后病理诊断良性的患者中肺结核11例,肺隐球菌病6例,炎性肌纤维母细胞瘤1例,硬化性血管瘤3例,错构瘤2例,慢性炎症12例。
2.4 术前支气管镜检查受益人群预测因素分析结果 将术前支气管镜检查受益的36例SPN患者纳入Ⅰ组,无受益的466例SPN患者纳入Ⅱ组,结果显示结节所处区域、结节密度和结节大小与SPN患者有导致手术术式改变或取消的支气管镜检查结果有关(均P<0.05),见表1。进一步将结节所处区域、结节密度和结节大小纳入logistic回归分析模型,结果显示结节所处区域、结节大小是术前支气管镜检查受益人群的独立预测因素(均P<0.01),见表2。进一步将502例患者根据结节大小分为结节直径≤2cm组(308例)和2cm<结节直径≤3cm组(194例),两组患者手术取消或术式改变的发生率和支气管镜检查病理恶性的发生率比较差异均有统计学意义(均 P<0.01),见表 3。

表1 术前支气管镜检查受益人群的单因素分析

表2 术前支气管镜检查受益人群的logistic回归分析

表3 结节大小影响术前支气管镜检查的价值[例(%)]
2.5 结节大小、预测概率PRE_1的ROC曲线分析 通过对结节所处区域、结节大小两项指标进行logistic回归分析,产生新变量PRE_1,设x1=结节所处区域,x2=结节大小,得出预测概率PRE_1回归方程:PRE_1=1/{1+e-[-3.978-1.638x1(内=1;中或外=2)+1.673x2]}。ROC 曲线分析显示结节大小预测术前支气管镜检查受益人群的AUC为0.783,95%CI:0.721~0.845,P<0.01,最佳诊断分界点为结节大小在2.35cm时,对应的灵敏度和特异度分别为0.69和0.78;预测概率 PRE_1 AUC 为 0.820,95%CI:0.753~0.887,P<0.01,最佳诊断分界点为PRE_1值在0.076时,对应的灵敏度和特异度分别为0.83和0.77,见图1。提示结节所处区域和结节大小联合预测术前支气管镜检查受益人群的准确性优于单个指标。
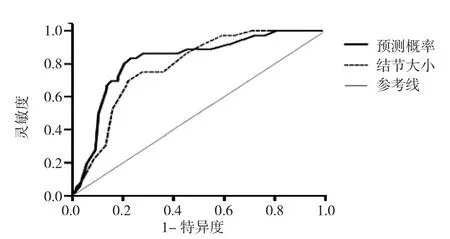
图1 结节大小、PRE_1与术前支气管镜检查受益人群的ROC曲线
3 讨论
随着低剂量胸部CT筛查的广泛开展,SPN患者检出率越来越高[6-7]。在吸烟和既往吸烟人群中使用低剂量胸部CT筛查可减少20%肺癌相关的病死率,手术切除是治疗恶性SPN的主要手段,可以降低肿瘤相关的死亡率[8-9],但对于常规电子支气管镜在可疑恶性SPN诊断及术前评估中的价值一直存在争议,既往研究认为对于可疑恶性SPN术前行常规支气管镜检查极少改变肿瘤分期或发现导致手术禁忌的病变[10-11]。美国Fleischner学会指南推荐对于首次发现的直径>8mm的SPN建议3个月内CT随访或正电子发射计算机断层显像或经皮肺活检但未推荐行常规支气管镜检查[12],ACCP指南目前仅推荐有空气支气管征的可疑恶性SPN术前行常规电子支气管镜检查[5]。Zhang等[3]纳入1 026例可疑恶性SPN患者,80例(7.8%)患者有镜下阳性发现,38例(3.7%)因支气管镜结果取消手术或改变手术术式。Schwarz等[13]纳入225例可疑恶性SPN患者,其中发现10例(4.4%)患者有镜下气道恶性病变,4例患者因支气管镜结果而取消手术,1例患者调整了手术方式。本研究纳入502例因可疑恶性SPN术前行常规电子支气管镜检查的患者,其中57例(11.4%)患者发现气道病变,包括气道黏膜浸润样改变和(或)气道新生物、气道黏膜糜烂坏死样改变、支气管息肉样新生物、气道黏膜隆起、管腔外压性狭窄等表现,其中7例因支气管镜结果取消手术,25例改变手术术式。445例患者(88.6%)支气管镜检查镜下表现均未见明显异常,其中包括全部250例纯GGO患者,但其中4例毛刷找到抗酸杆菌诊断考虑肺结核予以取消手术,所以共11例(2.2%)患者因支气管镜检查结果取消手术,25例(5.0%)改变手术术式加大手术切除范围。
近年来多种高级支气管镜和辅助设备的应用提高了SPN的诊断率,例如荧光支气管镜、支气管镜下针吸活检及超声支气管镜等检查手段的加入明显提高了SPN的诊断率[13-17]。Schwarz等[13]通过荧光支气管镜介导下活检或细胞学检查,SPN病理类型的诊断率可达41%,其中肺癌诊断率可达到46.5%。Chhajed等[18]研究发现联合PET-CT后,支气管镜诊断率可>50%。而Zhang等[3]研究提示常规电子支气管镜对于恶性SPN的灵敏度为0.06,特异度和阳性预测值为1.00,阴性预测值为0.21。van’t Westeinde等[2]研究显示常规电子支气管镜检查诊断恶性SPN的灵敏度为0.14,特异度和阳性预测值均为1.00,阴性预测值为0.48。本研究显示常规电子支气管镜检查诊断恶性SPN的灵敏度为0.09,特异度为1.00,阳性预测值为1.00,阴性预测值为0.08。
本研究将性别、年龄、结节位置、结节所处区域、结节密度、结节大小纳入分析,寻找可疑恶性SPN患者中的哪些人群术前常规电子支气管镜检查受益,logistic回归分析显示,结节所处区域、结节大小是预测术前支气管镜检查受益人群的独立预测因素,结节越大、越靠近肺门,支气管镜检查的价值就越高。而Zhang等[3]研究显示男性及结节直径越大,支气管镜异常发现的可能性就越大。本研究进一步分析将SPN患者根据结节大小分为结节直径≤2cm组和2cm<结节直径≤3cm组,两组患者手术取消或术式改变的发生率和支气管镜病理恶性的发生率比较差异均有统计学意义。
本研究进一步通过对ROC曲线和logistic回归分析的应用,提高了预测的科学性和准确性,首先对相关指标进行logistic回归分析,建立新变量预测概率PRE_1,通过对结节大小和预测概率PRE_1的ROC曲线分析,结果提示结节所处区域和结节大小联合预测术前支气管镜检查受益人群的准确性优于单指标。
综上所述,术前常规电子支气管镜检查的价值与SPN大小及结节所处区域有关,结节越大、越靠近肺门,支气管镜检查的价值就越高,两指标联合能进一步提高预测准确性,可疑恶性SPN患者术前行常规电子支气管镜检查既能协助术前诊治,也有利于制定患者的治疗策略,避免不必要的手术,建议作为术前的常规检查。

