起爆药污染场地土壤中锑的环境风险评估
姜昱聪, 贾晓洋, 夏天翔, 李 宁, 张文毓
1.首都师范大学资源环境与旅游学院, 北京 100048 2.北京市环境保护科学研究院, 污染场地风险模拟与修复北京市重点实验室, 北京 100037 3.北京师范大学水科学研究院, 北京 100875
由于人类活动的影响以及在起爆药、阻燃剂、合金等产品中使用量的增加,Sb(锑)对环境的污染日益加重. Sb因对人体及生物具有强烈的毒性作用而受到越来越多的关注,被许多国家列为优先控制污染物[1]. 研究表明,不同气候及土壤物理化学性质下Sb完全氧化和溶解预计需要30~300 a[2-3],Sb的浸出和迁移存在长期的环境风险.
土壤是Sb累积和迁移的重要介质,相比火山爆发等自然来源,用于炮药、电引火头、延期元件等击发火帽中发火的起爆药造成的Sb污染更为突出. Sb作为起爆药的主要成分(硫化锑占经典混合起爆药组成的33.4%[4]),进行的弹药枪支生产活动是其进入环境的一个重要途径. 起爆药的燃烧残渣会进入土壤孔隙水而导致Sb迁移,对环境和人类健康产生潜在危害[5]. 近年来,国内对土壤中Sb污染的研究主要集中于锑矿开采、矿区冶炼及植物富集等方面[6-8],国外研究主要集中于子弹中Sb对靶场土壤和地下水造成的危害等方面[1-3,5],而对起爆药工业生产场地土壤Sb污染的研究较少. 对起爆药污染土壤中Sb赋存形态及归趋行为了解的缺乏,不利于Sb污染环境风险评估的开展以及修复策略的制定[9].
Sb及其化合物的作用和行为在很大程度上取决于其浓度和化学形态,不同形态会产生不同的环境效应,直接影响到其毒性、在自然界中的迁移循环及生物可给性[1,2,5,10-12]. Johnson等[11]研究表明,自然风化和腐蚀过程中的Sb主要以离子形式〔Sb(OH)6-〕或可溶形态(Sb5+)迁移至地下水中,瑞士某靶场土壤中w(TSb)为500~13 800 mgkg,Sb浸出量为1 mgkg. LI等[12]使用SBET法测试得到湖南省锡矿山土壤中Sb的生物可给性为5.89%~76.44%,且Sb的生物可给性随其总量的增加而增大. 可见,了解Sb在土壤中的存在形态、释放机理和可给性等将有助于开展Sb污染的环境风险评估.
目前,传统的人体健康风险评估过程中在计算暴露剂量时一般以土壤中重金属总量为基准,以经口摄入为主要暴露途径[13],导致评估结果非常保守,造成场地过度修复与资金浪费. 为克服传统方法过于保守的问题,该研究基于不同价态Sb及生物有效态含量开展人体健康风险评估,能更加客观地反映污染物的实际风险.
该研究以某工业场地起爆药生产区实际土壤为研究对象,通过对厂区进行全面系统地采样和分析,选择典型样品测试了土壤中Sb的赋存形态、浸出水平及其生物可给性,并通过人体健康风险评估模型及三相平衡耦合地下水稀释模型分别评估了土壤Sb对人体健康和地下水环境产生的风险,以期为起爆药污染场地土壤重金属Sb的风险评估及环境管理提供科学依据.
1 材料与方法
1.1 供试土壤
供试土壤取自某工业场地起爆药生产区,该区域面积约12.5 hm2,使用硫化锑、氯化钾及雷汞等化合物制造起爆药,用于步枪弹、机枪弹及枪榴弹等多种类型子弹的研制和生产,具有近60年的生产历史. 根据场地环境调查和监测结果,选择9个Sb污染较为显著的表层土壤样品作为研究对象.
1.2 土壤Sb赋存形态分析及浸出测试
采用微波消解原子荧光光度法测定土壤样品中TSb的质量分数及其价态分布[15-16],将土壤样品继续研磨过0.150 mm筛,使用CEM MARS6消解仪(CEM,美国)进行HCL+HNO3消解,然后通过原子荧光光度计AFS-8220(北京吉天仪器有限公司)测定w(TSb);使用柠檬酸钠溶液对Sb5+掩蔽测定w(Sb3+),w(TSb)与w(Sb3+)的差值即为w(Sb5+). 采用美国TCLP毒性浸出法[17]测定Sb的浸出浓度,将土壤样品研磨过0.150 mm尼龙筛,并以20∶1的水土比加入对应体积的浸提剂,在(30±2)rmin下常温振荡18 h,过滤,使用ICP-MS(安捷伦,美国)测定浸出液中Sb的含量. 采用Tessier逐级提取法进行形态分析,将土壤样品研磨过0.250 mm尼龙筛,使用ICP-MS测定各形态Sb的占比,具体操作步骤参照文献[18],该方法按照生物活性的大小,将土壤重金属分为可交换态、碳酸盐结合态、铁锰氧化物结合态、有机结合态和残渣态5种不同的化学形态. 采取三氯化六氨合钴浸提-分光光度法测定土壤CEC(阳离子交换量):将土壤样品研磨至0.250 mm尼龙筛,用三氯化六氨合钴浸提土壤中的Sb,通过UV-1800紫外分光光度仪(岛津,日本)测量浸提液上清液分光度,消除干扰后根据文献[19]计算得到CEC. 土壤pH采用酸度法(水土比为1∶5)测定;w(OM)(OM为有机质)采用重铬酸钾容量法测定[20];w(Fe)和w(Mn)使用Niton XL2-800niton便携式光谱仪(Niton,美国)测定;土壤粒度分布使用Mastersizer 2000粒径分析仪(MALVERN,英国)测定.
1.3 生物的可给性测试
重金属Biog(人体可给性)是指土壤中重金属经口摄入后,生物有效态含量〔w(Sbgb),Sbgb为生物有效态Sb〕与摄入土壤中重金属总量的比值,即溶解于胃液与肠液中Sb与摄入土壤重金属总量的比值. 国内外广泛采用SBET法对污染土壤中Sb的生物可给性进行测试[21-24],具体步骤:取研磨过0.250 mm尼龙筛的土壤1 g,加入提前配置好的0.4 molL的氨基乙酸溶液中,使用盐酸调节pH至1.5±0.2范围内,在摇床上以30 rmin振荡2 h,将提取液在 4 000 rmin下离心10 min,通过0.45 μm的滤纸过滤,将上清液与残渣分离,分别测定上清液和残渣中Sb的含量.
1.4 健康风险评估方法
采用HJ 25.3—2014《污染场地风险评估技术导则》[25]中的方法分别开展敏感用地和非敏感用地土壤Sb污染的健康风险评估. 土壤中非挥发性重金属主要通过经口摄入、呼吸吸入和皮肤接触土壤颗粒这3种暴露途径对人体健康产生危害. 受毒理学发展限制,目前我国健康风险评估所采用的毒性数据主要来源于2018年美国环境保护局区域筛选值RSL(Regional Screening Level) Summary Table[26],其中Sb可对应的暴露途径的毒理学参数值:TSb和Sb5+的经口摄入参考剂量分别为4×10-4和5×10-4mg(kg·d),Sb3+的呼吸吸入参考剂量为2×10-4mg(kg·d). 同时有研究[27]表明,TSb和Sb5+主要通过经口摄入途径进入人体血液,Sb3+主要通过呼吸吸入途径进入人体后积累于红细胞中. 因此,笔者仅考虑经口摄入和呼吸吸入这两种暴露途径下Sb的健康风险,分别以土壤中w(TSb)、w(Sb5+)、w(Sb3+)及w(Sbgb)作为暴露浓度计算起爆药场地土壤中Sb对人体产生的危害商,并进行差异性分析.
Sb仅具有非致癌效应,敏感用地的敏感受体为儿童,非敏感用地的敏感受体为成人. 这两种情景下经口摄入和呼吸吸入暴露导致的危害商计算方法见式(1)~(6)[25],模型参数见表1.
(1)
(2)
(3)
(4)
(5)
(6)
1.5 地下水风险评估方法
土壤中Sb在降雨淋溶作用下会向下迁移并对地下水产生危害,污染物进入地下水的过程一般分为3个阶段[27]:①土壤中Sb解吸至土壤孔隙水中;②土壤孔隙水中Sb在清洁非饱和带经对流弥散、吸附解吸和生物降解等一系列迁移转化过程后到达地下水面处;③孔隙水中Sb进一步向下迁移进入地下水并被混合稀释. 由此,可采用层次化风险评估方法评估土壤污染物对地下水的风险[28]. 该研究基于保守考虑,仅考虑第一阶段,即采用三相平衡耦合地下水稀释模型预测土壤孔隙水中Sb的浓度. 并与GBT 14848—2017《地下水质量标准》中Sb浓度指标及其限值进行对比,以评估Sb迁移对地下水的危害. 三相平衡耦合地下水稀释模型见式(7):
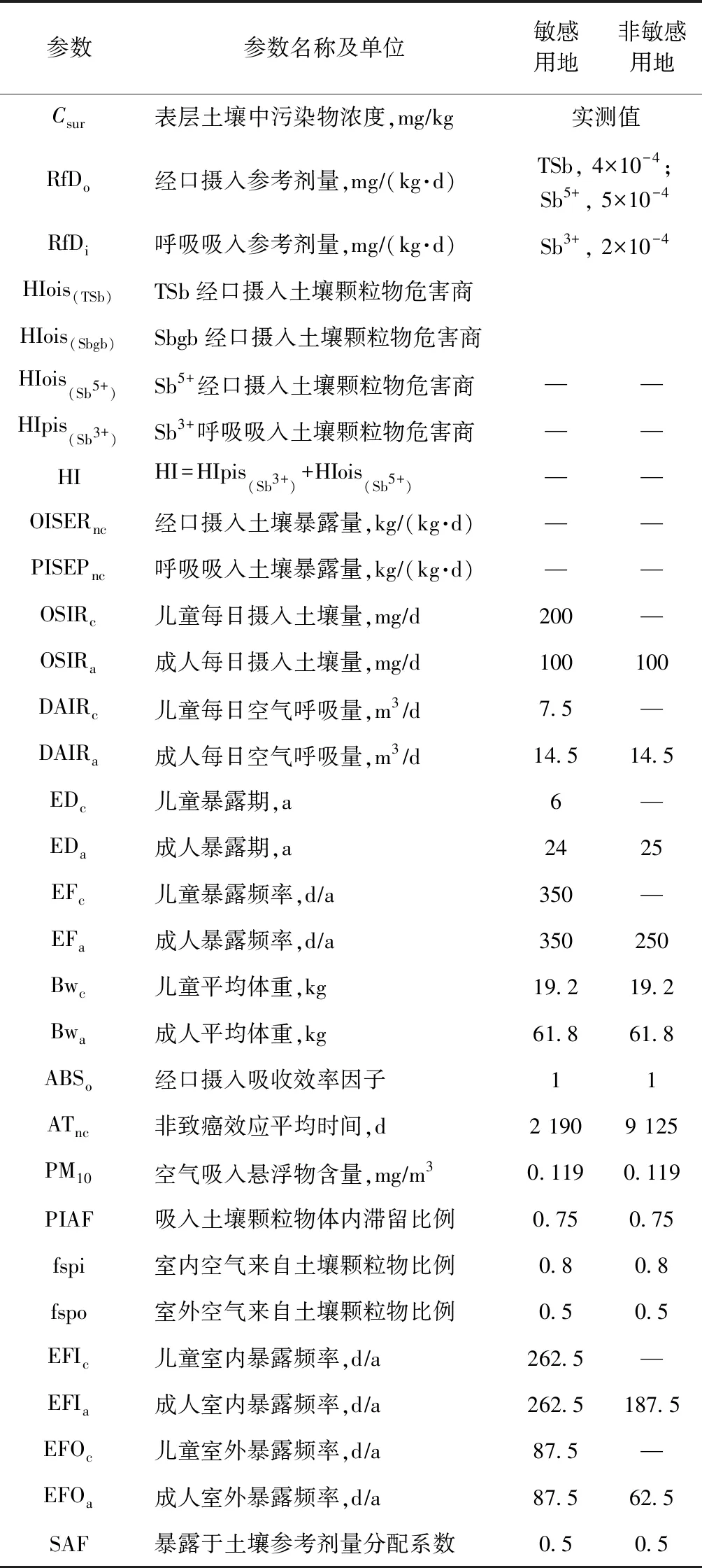
表1 人体健康风险评价模型参数[25]
(7)
式中:Cw土壤孔隙水中污染物浓度,mgcm3;Cs为土壤中污染物总含量,mgkg;ρb为土壤干容重,1.7 gcm3;θw为土壤中水的体积含量,取值0.26;θa为土壤孔隙中空气的体积含量,取值0.17;H为污染物亨利常数,取值0;Kd为污染物土-水分配系数,Sb的Kd为44.67 cm3g.
1.6 数据分析
采用Microsoft Office 2010(Office 14,VOLUME_KMSCLIENT channel)数据处理功能进行数据分析;采用OriginPro 9.5(2018C SR1b 9.5.1.195)进行图形及模型的制作;使用TBM SPSS Statistic 21.0对数据进行回归性分析和皮尔逊相关性(双尾检验)分析.
2 结果与讨论
2.1 土壤理化性质以及锑的含量
供试土壤的理化性质如表2所示. 由表2可见:各土壤样品pH的变化范围为7.69~8.37,差异较小;而w(OM)、w(Fe)、w(Mn)、粒径分布差异较大,土壤CEC为45.82~144.39 cmolkg;w(OM)为12.3~101.0 gkg;w(Fe)为20 000~32 200 mgkg,w(Mn)为396~719 mgkg;w(黏粒)为0.69%~12.47%,w(粉粒)为5.77%~81.77%,w(砂粒)为5.76%~93.53%,土壤粒径分布主要以砂粒和粉粒为主.
土壤中w(TSb)为26.7~4 255.0 mgkg,平均值为791.11 mgkg,是GB 36600—2018《土壤环境质量建设用地土壤污染风险管控标准》[29]中第一类用地筛选值的1.33~212.75倍,最大值超过相应管制值(360 mgkg)的10.82倍. 土壤中Sb污染程度主要与场地用途相关,如李继宁等[7-8]研究表明,锑矿区周边土壤Sb含量分布差异较大,部分采样点高达 16 389 mgkg;Griggs等[1-2]研究的两个不同区域靶场土壤w(TSb)分别为10~123和20~118 mgkg.
由表2可见,土壤样品中Sb主要以Sb3+和Sb5+存在,w(Sb5+)占w(TSb)的65.57%~95.46%,与Griggs等[1-2]的研究结果〔w(Sb5+)占比>70%〕接近. 造成土壤中w(Sb5+)远高于w(Sb3+)的主要原因:①土壤中Sb5+通常被认为主要是Sb3+的氧化态,即便在弱还原状态下,也存在Sb3+向Sb5+的转变;②Sb3+易与腐殖质结合,天然有机物就是其有效吸附剂,而Sb5+很少去结合带负电荷的天然有机物质,更易于在孔隙水和地表水中溶解. 因此,土壤中Sb5+的释放量远高于Sb3+. Okkenhaug等[2]对靶场土壤Sb污染的研究结果显示,土壤中Sb的吸附取决于土壤物理化学性质和Sb的氧化还原状态. 中性和碱性土壤中Sb3+的吸附比Sb5+强烈,Sb主要以Sb(OH)6-存在于土壤水溶液中.
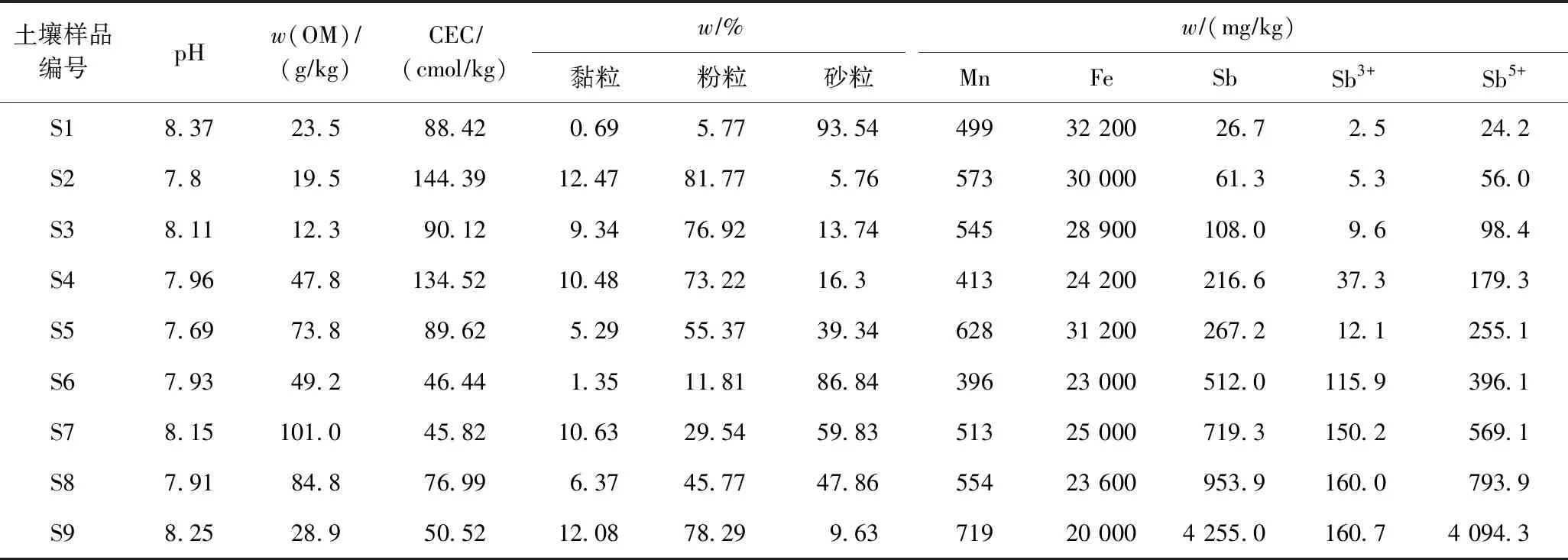
表2 土壤理化性质、粒径分布及部分重金属含量分析
2.2 土壤中锑的化学形态
由图1可见,供试土壤中Sb主要以残渣态(38.05%~94.22%)形式存在,其次为铁锰氧化物结合态(0.01%~31.80%)和有机结合态(0.32%~21.55%),以及碳酸盐结合态(0.01%~11.16%)和可交换态(0.42%~3.70%).
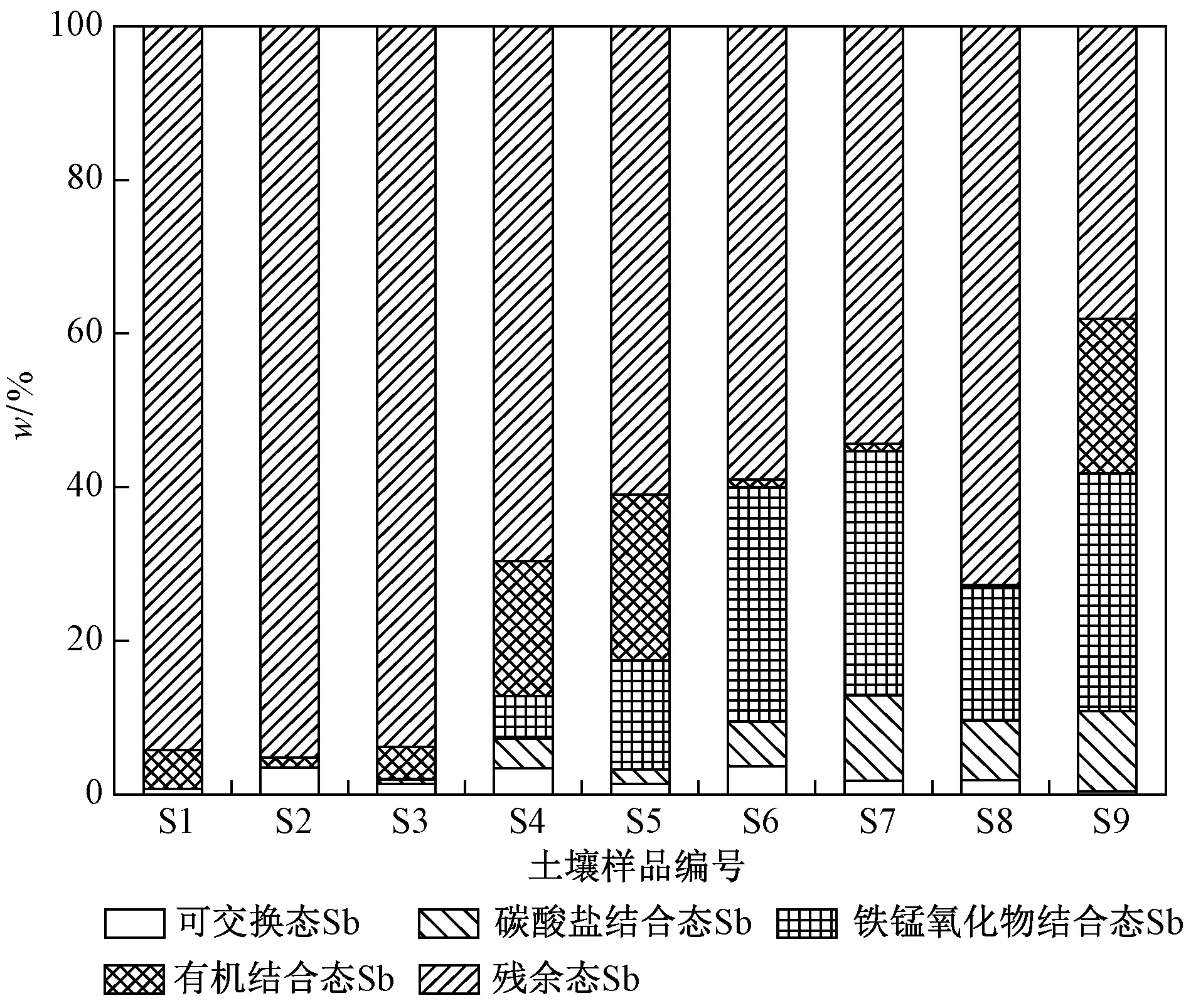
图1 土壤中Sb的化学形态分析Fig.1 Chemical form analysis of soil Sb in the soil
分析土壤CEC、w(Mn)、w(Fe)(见表2)与各形态Sb含量的相关性发现,CEC与w(可交换态Sb)呈负相关(r=-0.681,P<0.05,n=9),w(Fe)、w(Mn)均与w(铁锰氧化物结合态Sb)呈正相关(r分别为0.504、0.631,P均小于0.05,n均为9). 可见,土壤中CEC、w(Mn)、w(Fe)均可影响Sb形态分布. 赖晨焕[30]研究发现,土壤CEC对Sb有钝化能力,土壤中CEC越高,w(可交换态Sb)越低. Okkenhaug等[2,31]研究发现,Fe、Mn的氧化物和氢氧化物具有高亲和力,易吸附Sb形成表面络合物. 因此,土壤CEC、w(Mn)、w(Fe)的变化可改变Sb的存在形态,使可交换态和铁锰氧化物结合态比例发生相对变化.
2.3 Sb的TCLP浸出特征
由表3可见,供试土壤中Sb的浸出浓度在0.22~35.49 μgL之间,浸出率〔土壤中w(SbL)与w(TSb)之比,其中w(SbL)为土壤中Sb的浸出浓度〕在0.006%~0.055%之间,与HU等[32]研究的锑矿区废石中锑的释放规律接近,w(TSb)为2 503 mgkg时,w(SbL)最大(为3.5 mgkg),浸出率为0.011%.

表3 供试土壤中Sb的浸出水平
土壤中Sb的浸出水平与土壤质地及理化性质密切相关. 该起爆药场地土壤中w(砂粒)与Sb浸出率呈显著正相关(r=0.830,P<0.05,n=9). Tack等[33]根据重金属下渗公式计算了砂土和黏土质地下重金属的浸出水平,结果表明,砂土的重金属浸出水平远大于壤土和黏土. Griggs等[1]在研究不同质地土壤(粉土、淤泥、黏土与砂土)重金属Sb的TCLP浸出差异时发现,所有土壤质地中以砂土的浸出浓度(0.59 mgL)为最大. 土壤中w(SbL)与CEC呈显著负相关(r=-0.597,P<0.05,n=9),主要是因为土壤CEC越大,土壤胶体可吸附的Sb含量越高,其活性越低,迁移能力越弱,则w(SbL)也就越低[30].
土壤中w(TSb)与w(SbL)呈显著正相关,为进一步了解二者之间的关系,以土壤中w(TSb)为自变量、w(SbL)为因变量,采用线性回归方法拟合基于土壤w(TSb)的浸出量预测模型,建模结果如式(8)所示.
lg[w(SbL)]=1.080 67 lg[w(TSb)]-4.034 72
(8)
该线性回归拟合方程的R2(决定系数)为0.70(P<0.01,n=9),基于w(TSb)能很好地预测Sb在土壤中的浸出量. 将9个采样点土壤实测w(SbL)分别代入式(8),计算得到表征模型预测精度的平均误差(ME)和均方根误差(RMSE)分别为0.60、0.75,表明该研究构建的上述模型的总体预测精度较高.
由图2可见,S1与S5采样点处土壤实测w(SbL)与式(8)表征的模型预测值存在明显偏差,究其原因:S1采样点处土壤中w(砂粒)最高,因此在w(TSb)较低的情况下仍可能保持较高的浸出量;S5采样点与S4采样点处土壤中w(TSb)相近,但S4采样点的可交换态和碳酸盐结合态Sb含量高于S5采样点,故S4采样点w(SbL)较大,表明土壤中Sb的形态分布会导致其浸出量存在差异.
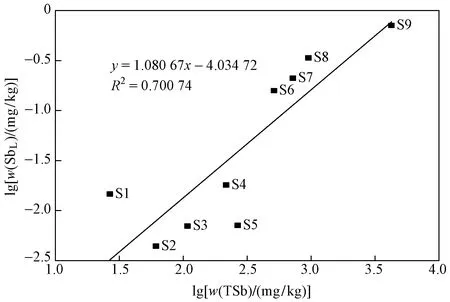
图2 土壤中Sb浸出量模型预测值和实测值的相关性Fig.2 Correlation between predicted and measured values of radon leaching mode
该研究中土壤w(SbL)与不同Sb形态含量的相关性分析结果显示,w(SbL)与w(碳酸盐结合态Sb)及w(可交换态Sb)呈显著正相关,主要是由于酸性浸提剂使碳酸盐结合态在酸性条件下转化成可交换态,部分Sb离子被释放,使得Sb的迁移能力加强.w(SbL)与w(残渣态Sb)呈显著负相关,主要是由于残渣态Sb包裹在矿物晶体中,其活性较低,迁移能力弱,浸出量少[32].w(SbL)与w(铁锰氧化物结合态Sb)、w(有机结合态Sb)均无明显相关性,主要是由于TCLP毒性浸出方法使用浸提剂的pH为4.93±0.05,土壤中铁锰氧化物结合态与有机结合态Sb的化学性质较为稳定,为惰性物质,在强酸、强碱及螯合剂影响下才会转化成其他形态迁移至环境中,在弱酸条件下则较为稳定[34].
2.4 Sb的生物可给性
该起爆药场地土壤样品中Sb在模拟胃阶段释放的w(Sbgb)及w(Sbresidue)(残渣中的Sb含量)如表4所示. 由表4可见,土壤中Sb的Biog为8.03%~67.69%,平均值为25.35%,表明Sb在胃阶段的生物可给性较高. 对土壤中w(Sbgb)与各影响因素的相关性分析表明,影响最为显著的因子是w(TSb)(r=0.979,P<0.01,n=9),其次为w(Fe)(r=-0.602,P<0.05,n=9)和w(OM)(r=-0.202,P<0.05,n=9),表明Sb的生物可给性与w(TSb)呈显著正相关,但与土壤中w(Fe)、w(OM)均呈负相关,这与已有研究结论[12]相一致.

表4 Sb生物可给性测试结果
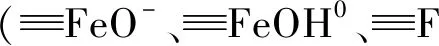
2.5 人体健康风险评估
该研究分别评估了敏感用地和非敏感用地基于w(TSb)、w(Sb5+)、w(Sb3+)及w(Sbgb)的健康风险,结果如表5所示.
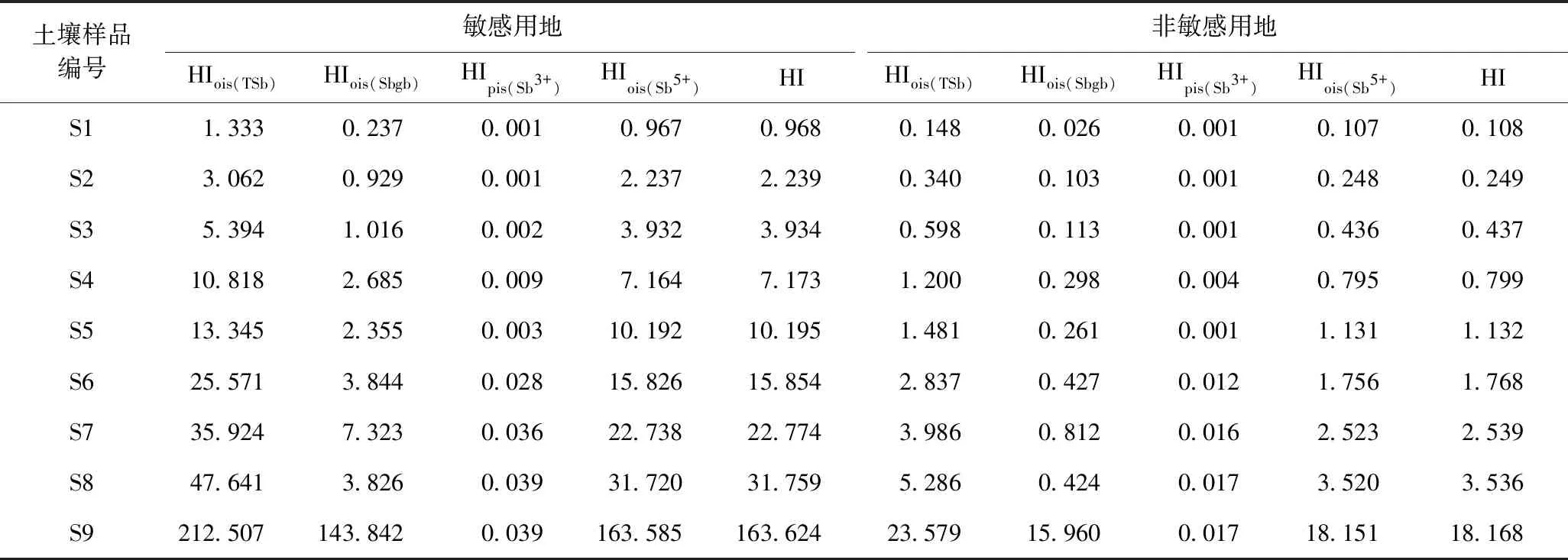
表5 考虑Sb的生物可给性和价态后土壤健康风险评估
使用w(Sbgb)作为暴露浓度调整传统风险评估结果(见表5),结果显示,基于生物有效态浓度计算的HIois(Sbgb)是传统模型预测结果HIois(TSb)的8.00%~67.69%,平均值为24.51%. 使用w(Sb5+)和w(Sb3+)作为暴露浓度调整传统风险评估结果发现,与呼吸吸入的Sb3+相比,经口摄入的Sb5+是对人体健康产生危害的主要来源. Gebel[41]研究指出,虽然Sb3+的毒性大于Sb5+,但土壤中w(Sb3+)远小于w(Sb5+),所以经口摄入的Sb5+是锑进入人体健康的重要暴露途径,是危害人体健康的主要来源.
供试土壤的9个样品中,敏感用地Sb5+经口摄入和Sb3+经呼吸吸入的危害商范围为0.968~163.624,平均值为28.724;非敏感用地下危害指数范围为0.108~18.168,平均值为3.193. 敏感用地和非敏感用地下,基于Sb价态计算的危害指数是传统模型评估结果的62.00%~77.01%,平均值为70.04%. 这表明与传统风险评估结果相比,以重金属生物可给性浓度或以不同价态浓度调整后的危害商显著降低.
综上,与非敏感用地相比,敏感用地对土壤重金属修复要求更高,因此,在未明确土地储备属性时,应按照敏感用地进行人体健康风险评估. 以传统风险评估方法计算危害商并依此制定的修复管理对策过于保守,基于Sb不同价态与生物有效态含量进行的人体健康风险评估能够更加客观地反映污染物的实际风险,可以为场地重金属污染程度的正确评价、污染场地的修复和风险管理提供更为科学的依据.
2.6 地下水风险评估方法
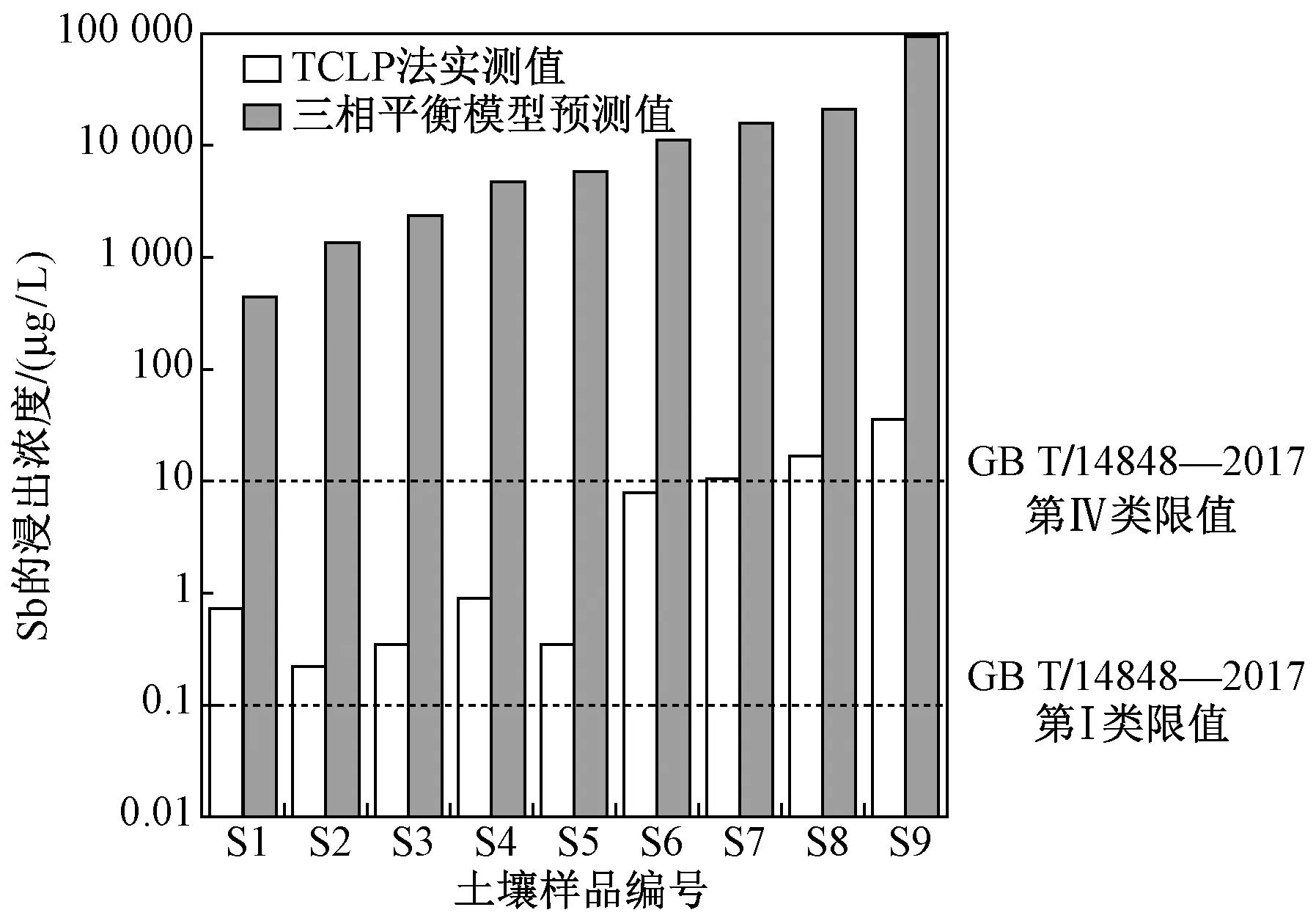
图3 供试土壤中Sb浸出浓度实测值与 三相平衡模型预测结果对比Fig.3 The comparison between measured values of leaching concentration and three-phase equilibrium model prediction in tested soil
传统地下水风险评估通常采用三相平衡耦合地下水稀释模型. 对比供试土壤中Sb浸出浓度实测值与三相平衡模型预测结果(见图3)可以发现,模型预测值均远超过GBT 14848—2017《地下水质量标准》第Ⅳ类用水限值,实测值也均超过第Ⅰ类用水限值[27],其中S7、S8与S9这3个采样点Sb浸出浓度实测值均超过第Ⅳ类用水限值[27],表明该场地周边地区地下水已很有可能被Sb污染,地下水健康存在极大风险. Sb浸出浓度实测值是三相平衡模型预测值的0.01%~0.17%,二者相差3~5个数量级,可见其评估结果足够保守,以此为基础进行污染场地修复可更好地保护场地周边地下水环境.
3 结论
a) 供试土壤中w(TSb)为26.7~4 255.0 mgkg,平均值为791.11 mgkg. 与GB 36600—2018《土壤环境质量建设用地土壤污染风险管控标准》第1类建设用地Sb的筛选值(20 mgkg)进行比较,发现9个采样点处w(TSb)均超标. 进一步对Sb进行价态分析发现,土壤样品中的Sb主要以Sb3+和Sb5+两种价态存在,w(Sb5+)占w(TSb)的65.57%~95.46%.
b) 土壤中不同形态Sb的比例依次为残渣态(38.05%~94.22%)、铁锰氧化物结合态(0.01%~31.80%)、有机结合态(0.32%~21.55%)、碳酸盐结合态(0.01%~11.16%)和可交换态(0.42%~3.70%). 土壤中w(Fe)、w(Mn)均与w(铁锰氧化物结合态Sb)呈正相关,原因在于,Sb易与土壤中的铁、锰氧化物结合形成表面络合物,改变其存在形态. 土壤CEC与w(可交换态Sb)呈负相关,是因为土壤CEC对Sb有钝化能力,土壤中CEC越高,Sb的可交换态含量越少.
c) 供试土壤中Sb的浸出浓度在0.22~35.49 μgL之间.w(SbL)与土壤中w(砂粒)、w(TSb)、w(碳酸盐结合态Sb)、w(可交换态Sb)均呈显著正相关,与w(残渣态Sb)及土壤CEC呈显著负相关. 基于w(TSb)建立的模型能很好地预测土壤在酸性条件下的浸出量.
d) 供试土壤中Sb的生物可给性范围在8.03%~67.69%之间,w(Sbgb)与w(TSb)呈显著正相关,土壤中w(Fe)和w(OM)的增加能够降低Sb的生物可给性.
e) 基于敏感用地和非敏感用地,以w(Sbgb)为暴露浓度计算的健康风险水平是传统风险评估模型预测结果的8.00%~67.69%,平均值为24.51%;基于Sb价态计算的健康风险水平是传统风险评估模型预测结果的62.00%~77.01%,平均值为70.04%;基于TCLP方法测定的Sb浸出浓度是三相平衡模型预测结果的0.01%~0.17%,平均值为0.05%,二者相差3~5个数量级. 可见,充分考虑Sb在污染场地土壤中的赋存特征能够降低常规风险评估方法的保守性.

