对比高考真题探寻命题规律
尉言勋

2019年的考试大纲中对学生的化学实验与探究能力的要求包括2个方面:(1)掌握化学实验的基本方法和技能,并初步实践化学实验的一般过程. (2)在解决化学问题的过程中,运用化学原理和科学方法,能设计合理方案,初步实践科学探究. 化学实验综合题是近年新课标卷的必考题型之一,以化学实验方案的设计与评价为主,主要以物质制备或性质探究为载体,结合实验操作、物质的性质探究、简单计算等命题. 对综合实验中某一环节或某一步骤进行方案设计或探究实验中的有关问题,考查学生发现问题与解决问题的能力. 题目类型主要包括物质制备和性质探究两种,具有较好的区分度. 本文对比近二年新课标Ⅰ卷高考试题,并提出相应的解题策略.
一、真题解析
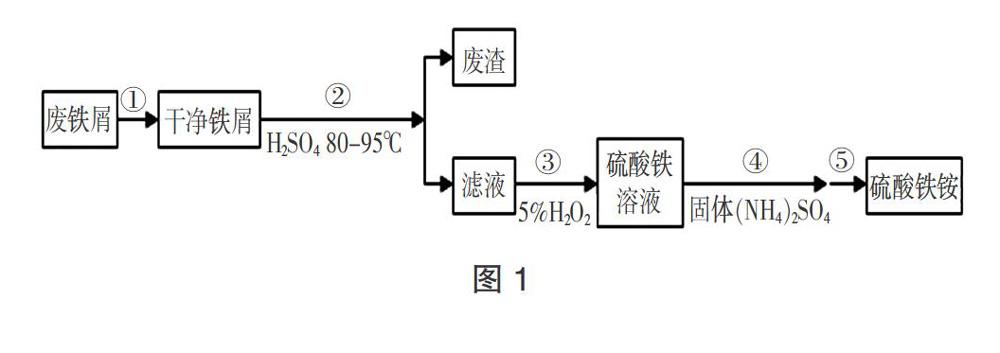
【例1】(2019·新课标Ⅰ卷, 27)(15分)硫酸铁铵[NH4Fe(SO4)2· xH2O]是一种重要铁盐. 为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是 .
(2)步骤②需要加热的目的是 ,温度保持80-95℃,采用的合适加热方式是 . 铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为 (填标号).
(3)步骤③中选用足量的H2O2,理由是 . 分批加入H2O2,同时为了 ,溶液要保持pH小于0.5.
(4)步骤⑤的具体实验操作有 ,经干燥得到硫酸铁铵晶体样品.
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%. 硫酸铁铵晶体的化学式为 .
解析:(1)油污在碱性条件下水解生成羧酸盐和甘油,然后水洗,从而除去油污;(2)温度越高化学反应速率越快,所以加热的目的是加快反应;低于100℃的加热可以采用水浴,采用的合适加热方式为热水浴;硫化物和稀硫酸反应生成H2S,酸性气体应用碱液吸收,且要防止倒吸,B、D不能防止倒吸且A溶解H2S的能力较弱,所以选C;(3)H2O2具有氧化性,能氧化Fe2+生成Fe3+且H2O2被还原生成H2O,不引进杂质,所以选取H2O2作氧化剂;Fe3+水解导致溶液呈酸性,H+能抑制Fe3+水解,为防止Fe3+水解需要溶液的pH保持0.5;(4)从溶液中获取晶体的步骤为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;(5)1.5个结晶水的式量为18×1.5=27,失重5.6%,则该晶体式量为=482,x==12,所以其化学式为NH4Fe(SO4)2·12H2O.
答案:(1)碱煮水洗. (2)加快反应;热水浴;C. (3)将Fe2+全部氧化为Fe3+;不引入杂质;防止Fe3+水解. (4)加热浓缩、冷却结晶、过滤(洗涤). (5)NH4Fe(SO4)2·12H2O.
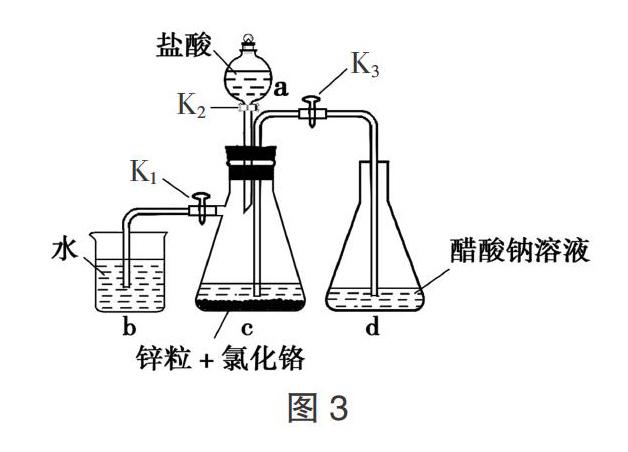
【例2】(2018·新課标Ⅰ卷,26)(14分)醋酸亚铬[(CH3COO)2 Cr·H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂. 一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬. 实验装置如图3所示,回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是__________,仪器a的名称是________.
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3.
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________.
②同时c中有气体产生,该气体的作用是____________.
(3)打开K3,关闭K1和K2. c中亮蓝色溶液流入d,其原因是________ ;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是________ 、_______、洗涤、干燥.
(4)指出装置d可能存在的缺点 ______________.
解析:(1)为避免Cr2+被氧化,应除去水中的溶解氧,则实验中所用蒸馏水均需经煮沸后迅速冷却,由装置图可知a为分液漏斗或滴液漏斗;(2)①c中溶液由绿色逐渐变为亮蓝色,说明生成Cr2+,反应的离子方程式为Zn+2Cr3+=Zn2++2Cr2+;②盐酸与锌反应生成氢气,可将装置内的空气排出,避免Cr2+被氧化;(3)打开K3,关闭K1和K2,由于锌继续与盐酸反应生成氢气,c中压强增大,可将亮蓝色溶液压入d. 由题目给予信息“醋酸亚铬难溶于冷水”,所以为使沉淀充分析出并分离,需采用的操作是冷却(冰浴)、过滤、洗涤,干燥等;(4)由于d装置是敞开体系,因此装置的缺点是可能使醋酸亚铬与空气接触被氧化而使产品不纯,应在密闭容器中制备.
答案:(1)去除水中溶解氧;分液(或滴液)漏斗;(2)①Zn+2Cr3+ = Zn2++2Cr2+;②排除c中空气;(3)c中产生H2使压强大于大气压;(冰浴)冷却;过滤;(4)敞开体系,可能使醋酸亚铬与空气接触.
二、综合分析与对比
实验综合题在知识上考察学生对课程标准规定范围内核心元素及其化合物的性质,比如常考的五大金属(Na、Mg、Al、Fe、Cu)和六大非金属(C、Si、O、S、N、Cl);在能力上考察学生应用元素化合物基础知识、基本原理去分析和选择陌生反应的实验操作步骤、实验装置,预测实验现象、实验结论,以及在陌生情境中解决实际问题的能力;渗透化学学科核心素养中的科学探究与创新意识、证据推理与模型认知,以及科学态度与社会责任,引导教师在教学过程中培养学生的环保意识.
近二年新课标Ⅰ卷实验综合题均考查陌生物质的制备,从设问情况、呈现形式、涉及考点几个角度对比如下:
2019年新课标Ⅰ卷第27题,探究废铁屑制备NH4Fe(SO4)2·xH2O的过程,变废为宝,体现了化学科学实践活动的创造性和价值性,考查原料处理、氧化还原、化学反应速率、水解平衡等方面的知识和实验操作能力及计算能力. 以流程的形式给予制备硫酸铁铵的五个实验步骤,以陌生物质的制备为载体,综合考查实验相关知识和考生分析问题的能力. (1)原料的预处理,涉及两个点①油污在碱性条件下可发生水解;②Fe不具有两性,不可与碱反应,可以用碱性溶液除去废铁屑中的油污. (2)根据反应所需加热的温度高低,①小于100℃水浴加热;②400-500℃酒精灯加热;③1000℃以上酒精喷灯加热;气体的净化既要考虑反应成分,又要防止倒吸;(3)H2O2是绿色氧化剂,把Fe2+被氧化成Fe3+,该考点近年多次出现,比如:2017年新课标Ⅱ卷26题(1)考查加入H2O2代替硝酸氧化二价铁;2016年新课标Ⅱ卷26题(5)考查H2O2氧化Fe2+的离子方程式;(4)步骤4加入固体硫酸铵的目的是为了引入铵根离子,题目没有直接设问;学生可以从流程信息中得知反应物中含 Fe3+、NH4+、SO42-,结合常见的沉淀以及铵盐易溶于水可推理出硫酸铁铵很可能易溶,考查了学生的证据推理素养. (5)步骤5考查从溶液中得到晶体的实验操作方法,加入硫酸铵无沉淀产生,要得到硫酸铁铵晶体则需要蒸发结晶或浓缩再结晶.
2018年新课标Ⅰ卷26题,以醋酸亚铬[(CH3COO)2Cr·H2O]的制备为载体,转换试题呈现方式,重视实验推理,考查学生实验与探究能力,提取信息能力以及逻辑推理能力. 题目有5个空分别涉及操作目的、气体的作用、原因分析、需要采用的操作、存在的缺点等,注重考查学生语言表达、文字表达能力,由装置和现象进行推理的能力,知识间的关联及迁移能力. 题目逻辑性较强,在盐酸溶液中过量的Zn把Cr3+还原为Cr2+,反应产生H2起到保护气的作用,排尽装置中的空气. 生成的H2导致c中压强增大,可以把生成的CrCl2压入d装置发生反應. 第(3)问,打开K3,关闭K1和K2. c中亮蓝色溶液流入d,其原因是________;与2017年新课标Ⅰ卷实验综合题(3)即为相似,均涉及装置中的“压强应用”,由负压造成倒吸.
三、备考策略
1. 命制角度及考查方式.
近年物质制备类实验综合题命题角度变化不大,情景新颖、陌生度高,注重能力考查,渗透核心素养. 其中2019年新课标Ⅰ卷是陌生无机物的制备;Ⅱ卷考查从茶叶中提取咖啡因,Ⅲ卷考查通过水杨酸进行乙酰化制备阿司匹林,天津卷考查环己烯的制备,加大了陌生有机物制备的考查.
2. 思维流程.
①明确实验原理. 实验是根据什么性质和原理设计的?实验的目的是什么?结合实验目的和相关的化学反应原理,进行全面的分析比较和推理,合理选择.
②熟知实验仪器. 选择适宜的装置,掌握仪器性能、使用方法、适用范围、注意事项、仪器规格、是否有替代装置可用等.
③得到产品操作顺序. 蒸发结晶(蒸发溶剂法)和降温结晶(冷却热饱和溶液法)均可得到晶体,前者适合溶解度随温度变化不大的物质,后者适用于溶解度随温度的升高而明显增大的物质.
④产率(纯度)计算:依据题目提供的反应原理和试剂的用量,计算产品的理论产量,产品产率×100%.
3. 仪器连接.
①主要流程
②分类
③仪器选择
4. 把握题目逻辑性,规范答题.
从近年实验综合题比较发现,题目具有整体逻辑性、层次感较强,每一个条件,每一个步骤,都有着紧密的联系. 特别是以流程的形式呈现步骤,要对题目整体分析,关注设问的逻辑关系,前面的小问的答案是否对后面解题具有指导意义. 充分利用题目给予的新信息,新信息表面上看是在随意的叙述,实际上往往隐含着题目的突破口,所给信息一定有用,但有时需分解、重组、迁移到具体情境中. 比如:2018年新课标Ⅰ卷26题题干中给予了醋酸亚铬难溶于冷水,为使沉淀充分析出并分离,需采用的操作是、洗涤,干燥,则需要用冷水浴冷却、过滤、洗涤、干燥.
实验综合题注重考查学生解决问题的能力,要求学生具有较强的书面表达能力. 比如2019年新课标Ⅰ卷27题,8个空中7个考查目的、理由、操作方法等. 考生往往解题思路正确,但所写答案不注意细节,踩不到评分细则的得分点. 书写仪器名称、操作名称、实验方法时,要避免错别字,操作步骤叙述要简洁明了. 例如检验NH4+,取少量试剂放入试管中,加入NaOH溶液,对试管进行加热,取一片湿润的红色石蕊试纸放在试管口,若变蓝,则含有NH4+. 在教学中教师可结合高考真题素材,设置问题情景,训练学生规范答题的能力.
总之,全国卷高考实验综合题以真实的实验情景为载体,重点考查物质性质和反应原理. 实验中反应产物的不确定性、装置操作的陌生化、实验现象的异常化、物质性质的多样化、反应原理的微观化都可能成为制约学生进行问题解决的瓶颈. 因此,备考时要结合化学实验的命制角度、思维流程、反应原理等方面,建构学生的知识体系、提升学生分析问题和解决问题的能力.
责任编辑 李平安

