康莱特注射液联合经肝动脉化疗栓塞术治疗中晚期肝癌效果的Meta分析
孙冬雪, 杨 柱, 龙奉玺, 魏显鳗, 唐东昕
1 贵阳中医学院第一临床附属医院, 贵阳 550002;2 贵州省中医肿瘤传承与科技创新人才基地, 贵阳 550002
原发性肝癌恶性程度高,其发病率在恶性肿瘤中位居第6位,死亡率在恶性肿瘤中位居第3位[1-2]。手术是早期肝癌的主要治疗手段,但肝癌恶性程度高、发病隐匿、病情进展快,多数患者确诊时已是中晚期阶段,错过手术机会,中位生存期只有几个月[3-4]。失去手术机会的中晚期肝癌患者首选一线治疗方案是经肝动脉化疗栓塞术(TACE),可使化疗药集中并隔离在肝癌部位,进而阻断肝癌的血供。TACE具有靶向性高、创伤性小的优势,可显著抑制肝癌的进展,短期疗效显著[5]。中药联合TACE治疗中晚期肝癌具有减毒增效作用[6]。近年来开展了康莱特注射液(KLT)联合TACE治疗中晚期肝癌的研究,表明二者联合可增加疗效,减轻放疗毒副作用,增加机体免疫力。但目前临床研究大多是小样本试验,结果具有不稳定性,缺乏说服力。因此,本研究通过对KLT联合TACE治疗中晚期肝癌的疗效、安全性及不良反应进行系统评价,以期为临床提供安全、有效、合理、可靠的循证医学依据。
1 资料与方法
1.1 文献检索 检索中国知网、万方数据库、维普数据库、中国生物医学数据库、PubMed、Cochrane Library、Embase中有关KLT与TACE治疗中晚期肝癌的临床研究,检索时间自数据库建立至2019年10月。中文检索词为“中晚期肝癌,肝癌,康莱特,薏苡仁油,TACE,肝动脉化疗栓塞术”,英文检索词为“hepatocellular carcinoma、advanced liver cancer、transcatheter arterial chemoembolization、KangLaiTe”。
1.2 文献纳入与排除标准
1.2.1 纳入标准 (1)研究对象为临床对照研究病例,采用随机分配方法或同期对照试验;(2)研究对象需经病理学、临床、影像学检查等证实;(3)试验组为KLT联合TACE,对照组仅用TACE;(4)纳入文献需符合:以论文形式发表,提供原始数据的队列研究。
1.2.2 排除标准 (1)综述、会议论文、摘要、动物实验、个案报道等;(2)文章原始数据不能用于推理计算的;(3)重复发表的会议文章、学位论文及期刊论文;(4)试验组给药剂量、疗程不确定,对照组未行TACE或联合其他中药干预。
1.3 资料提取 整理汇总文献,严格遵循Cochrane协作网相关标准进行筛选与评估,由2名评价员按纳入标准独立排除或纳入文献,核对各自筛选后结果,若遇分歧,采取第三方协助或讨论形式解决。提取资料内容包括:患者基线信息、给药情况、结局指标等。
1.4 文献质量评价 使用Cochrane Handbook5.1.0推荐的“偏倚风险评估”系统[7]对纳入的研究数据进行偏倚风险评估。
1.5 统计学方法 采用Revman5.3软件进行分析。各研究间的异质性采用χ2检验判断,若P≥0.10,I2≤50%,则认为无明显异质性,采用固定效应模型分析;若P<0.10,I2>50%,则认为有明显异质性,采用随机效应模型分析。分析结果以森林图表示,用比值比(OR)和95%可信区间(95%CI)评价结局指标。采用漏斗图分析是否存在发表偏倚。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果与纳入研究基本特征 共检索出相关文献837篇,根据纳入与排除标准进行剔除,最终纳入16篇文献[8-23](图1)。纳入研究的基本特征详见表1,16项研究中肝癌患者1131例,其中试验组558例,对照组573例;单个随机对照试验样本量最少6例,最多60例;均报道了患者的治疗情况。
2.2 纳入研究质量评价 参照Cochrane协作网推荐的风险偏倚评估工具,对纳入的16篇文献进行质量评价。其中10篇[8-11,14,17-21]提及基线具有可比性。1篇[8]采用就诊编号分组,1篇[9]采用就诊日期分组,1篇[10]采用治疗方法分组,1篇[16]未提及分组方法,其余文献为随机分组法。11篇文献[8-10,12-13,16-18,20-22]主要结果报告完整为低风险,5篇[11,14-15,19,23]为高风险,存在风险偏倚(图2)。
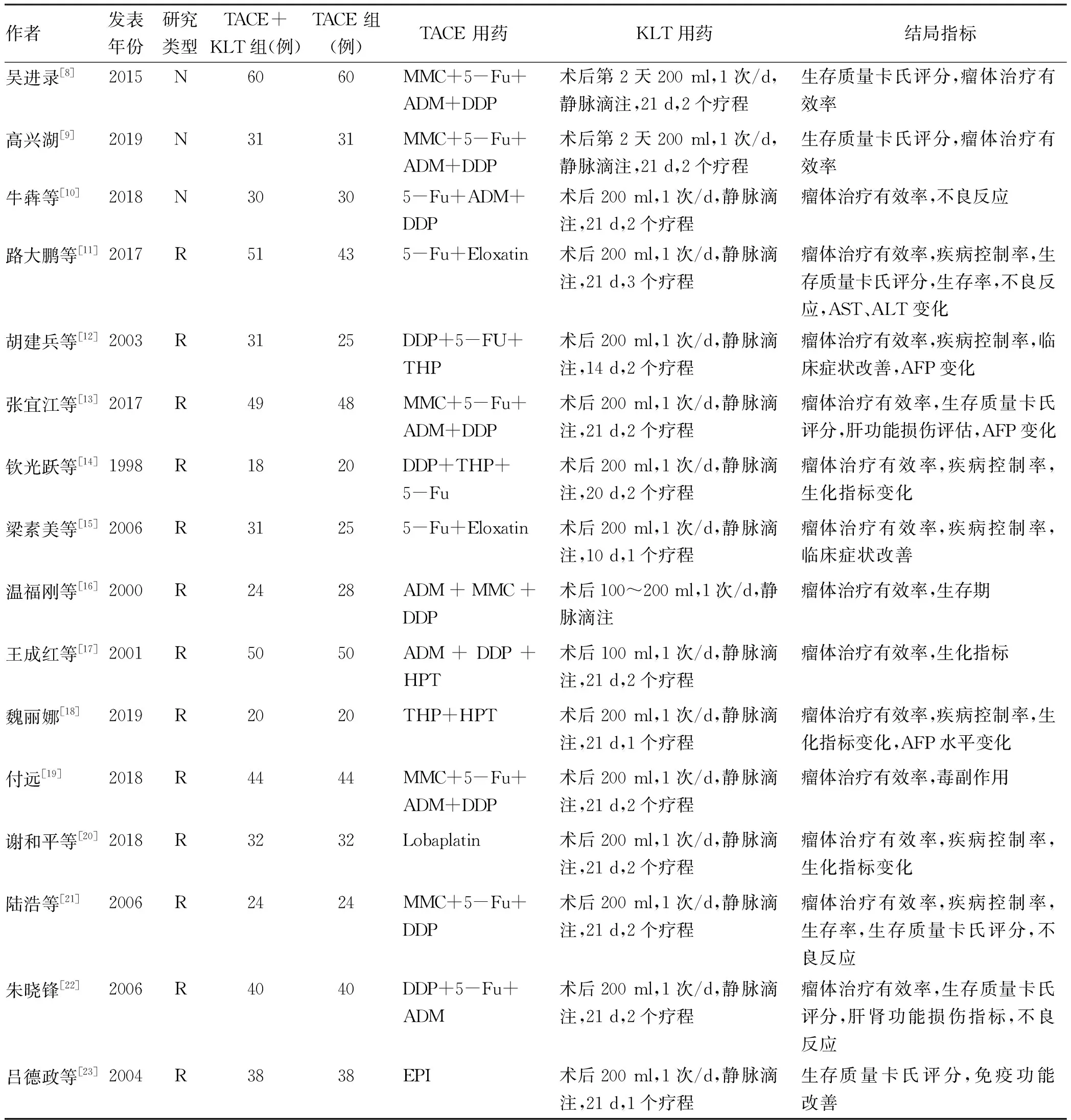
表1 纳入研究的基本特征
注:R,随机对照试验;N,非随机同期对照试验;MMC,丝裂霉素;5-Fu,5-氟尿嘧啶;ADM,表阿霉素;DDP,顺铂;Eloxatin,奥沙利铂;THP,吡柔比星;HPT,羟基喜树碱;Lobaplatin,洛铂;EPI,表柔比星。
2.3 主要结局指标Meta分析
2.3.1 瘤体治疗有效率 15项研究[8-22]报道了瘤体治疗有效率(完全缓解+部分缓解),各项研究间无明显异质性(P=0.99,I2=0),采用固定效应模型分析。结果显示,试验组有效率显著高于对照组(OR=2.85,95%CI: 2.17~3.76,P<0.001)(图3)。
2.3.2 疾病控制率 7项研究[11-12,14-15,18,20-21]报道了疾病控制率(疾病稳定+部分缓解+完全缓解),各项研究间无明显异质性(P=0.52,I2=0),采用固定效应模型分析。结果显示,试验组疾病控制率显著高于对照组(OR=2.58,95%CI:1.57~4.24,P<0.001)(图4)。
2.3.3 生存质量卡氏评分 7项研究[8-9,11,13,21-23]报道了生存质量卡氏评分,各项研究间无明显异质性(P=0.99,I2=0),采用固定效应模型分析。结果显示,试验组生存质量评分显著高于对照组(OR=3.54,95%CI:2.48~5.06,P<0.001)(图5)。
2.4 次要结局指标Meta分析
2.4.1 2年生存率 2项[11,21]报道了2年生存率,两项研究间无明显异质性(P=0.25,I2=24%),采用固定效应模型分析。结果显示两组2年生存率比较,差异无统计学意义(OR=2.37,95%CI:0.93~6.04,P>0.05)(图6)。
2.4.2 临床症状改善情况 2项研究[12,15]报道了临床症状改善情况(明显改善+部分改善),两项研究间无明显异质性(P=0.28,I2=13%),采用固定效应模型分析。结果显示,试验组临床症状改善率显著高于对照组(OR=3.71,95%CI:1.55~8.89,P<0.05)(图7)。
2.4.3 AFP水平改善情况 3项研究[12-13,18]报道了治疗后AFP改善情况(部分缓解+明显缓解),各项研究间无明显异质性(P=0.78,I2=0),采用固定效应模型分析。结果显示,试验组AFP改善率显著高于对照组(OR=2.57,95%CI:1.41~4.68,P<0.05)(图8)。
2.5 安全性分析
2.5.1 一般不良反应 3项研究[10,21-22]报道了恶心呕吐,各项研究间无明显异质性(P=0.99,I2=0),采用固定效应模型分析。结果显示两组恶心呕吐发生率比较,差异无统计学意义(OR=0.76,95%CI:0.40~1.46,P>0.05)(图9a)。3项研究[10-11,22]报道了肝功能损伤,各项研究间无明显异质性(P=0.92,I2=0),采用固定效应模型分析。结果显示两组肝功能损伤发生率比较,差异无统计学意义(OR=0.64,95%CI:0.35~1.18,P>0.05)(图9b)。
2.5.2 化疗引起的骨髓抑制 3项研究[10-11,22]报道了白细胞下降,各项研究间无明显异质性(P=0.80,I2=0),采用固定效应模型分析。结果显示,试验组白细胞下降数显著低于对照组(OR=0.39,95%CI:0.23~0.66,P<0.001)(图10a)。
3项研究[10-11,22]报道了血小板降低,各项研究间无明显异质性(P=0.97,I2=0),采用固定效应模型分析。结果显示,试验组血小板降低指数显著低于对照组(OR=0.22,95%CI:0.12~0.42,P<0.001)(图10b)。
3项研究[10-11,22]报道了血红蛋白下降,各项研究间无明显异质性(P=0.84,I2=0),采用固定效应模型分析。结果显示两组血红蛋白下降数比较差异无统计学意义(OR=0.74,95%CI:0.37~1.47,P>0.05)(图10c)。
2.6 发表偏倚分析 以瘤体治疗有效率为评价指标,对16篇文献进行漏斗图分析,结果显示漏斗图呈不对称分布(图11),提示存在一定的发表偏倚。
3 讨论
KLT的有效成分为薏苡仁油,是双相广谱抗癌药,不仅可抑制恶性肿瘤生长、阻止癌细胞分裂、诱导癌细胞凋亡,还可提高机体免疫力,减轻放化疗引起的毒副反应,进而提高患者生活质量[13]。研究[24-25]表明,薏苡仁油可特异性与血管内皮生长因子结合,退化肿瘤血管,抑制新生血管形成,减轻肿瘤的增殖及转移。KLT可阻断M和G2细胞周期,降低S期细胞百分比,减少有丝分裂及DNA合成,促进肿瘤细胞凋亡[26]。此外,KLT通过激活IL-2及自然杀伤细胞,为吞噬细胞吞噬功能及脾淋巴细胞增殖提供良好条件,进而提升机体免疫功能及非特异性抗病能力[27]。 TACE用于失去手术机会的中晚期肝癌治疗,但在化疗方案上缺乏统一标准,常用药物包括ADM、DDP、5-Fu等,常伴有消化道反应、肝功能损伤、骨髓抑制等毒副反应[28]。国内学者尝试将KLT与TACE联合应用,以期减轻化疗引起的不良反应,但结果不尽一致,本研究将其进行合并分析。
本研究共纳入16项KLT联合TACE治疗中晚期肝癌的试验,Meta分析结果表明,试验组患者瘤体治疗有效率、疾病控制率、生存质量卡氏评分、临床症状改善率、AFP下降水平高于对照组,骨髓抑制(血小板降低、白细胞下降)发生率低于对照组,差异均有统计学意义(P值均<0.05)。提示KLT与TACE联合治疗中晚期肝癌可显著增加瘤体治疗有效率、疾病控制率、生存质量卡氏评分,能够改善患者临床症状,同时可降低化疗引起的骨髓抑制等毒副作用发生率。
本研究存在以下不足之处。第一,本系统评价所纳入的16项研究原始数据均来自中国,其中13项研究对随机方法及细节进行明确说明,3项研究为非随机同期对照试验,其在方法学上存在一定局限性。只有2项研究[11,21]报告无失访,其他均未报道失访情况,削弱了本研究在安全性评估和远期疗效中的证据强度。第二,纳入本研究的TACE治疗方案中化疗药物的差异性会造成临床异质性客观存在;KLT治疗的给药剂量、疗程因素等差异性也会引起临床异质性的发生。第三,纳入研究的样本量较小,具有潜在的选择性偏倚。第四,纳入研究化疗药物方案不尽相同,KLT用药时间和疗程亦有差异,可能会影响本研究的可信度。第五,部分随机对照试验对安全性指标描述不系统,难以作亚组分析明确具体特征。第六,纳入的随机对照试验在质量评估方面存在偏倚风险,提供的细节信息不完善,所得结果证据支撑力度不足。
针对本系统评价纳入研究的局限性,对以后临床研究提出以下建议:(1)详细报道随机分配和随机序列产生方法及实施情况;(2)明确阐明分析方法,如意向性接受治疗、完成治疗、接受治疗分析;(3)统一TACE化疗方案及KLT使用剂量及疗程的标准;(4)统一各种诊断和安全性评价相关标准;(5)加强长期疗效和安全性指标的观察和记录,详细报告失访情况;(6)重视KLT在临床应用中的剂量效应并开展相关研究,使其更加合理有效地应用于肝癌患者。

