婴幼儿先天性心脏病合并肺动脉高压术后延迟拔管的危险因素分析
何思毅,王宪颖,殷小强,卢忠杰,陈 杰,刘敬臻,张近宝
先天性心脏病(congenital heart disease,CHD)已成为我国出生缺陷排名第一的先天畸形,造成巨大的经济和社会负担[1]。目前绝大多数CHD需要进行手术治疗。但是对于婴幼儿患者来讲,其自身器官发育不完善、免疫功能低下,在经过心脏手术的巨大创伤以及心肺转流(cardiopulmonary bypass,CPB)带来的全身炎性反应后,患儿术后容易出现多器官功能不全等并发症,严重影响临床预后[2]。尤其是对于合并肺动脉高压(pulmonary artery hyper⁃tension,PAH)的CHD患儿,长期的左向右分流使得肺血增多、右心负荷加重,呼吸道正常保护屏障的破坏会增加术后肺部感染等并发症的发生率,延长患儿机械通气时间[3]。而一旦出现延迟拔管,将有可能导致肺水肿、肺不张、呼吸机相关性肺炎等,进一步加重患儿病情[4]。因此,明确婴幼儿CHD合并PAH术后机械通气时间延长的主要影响因素,将有助于提高救治成功率。本文拟通过总结本科收治此类患儿的临床资料,分析术后延迟拔管的危险因素及其对临床结局的影响,从而为优化术后监护提供依据。
1 资料与方法
1.1 一般资料及分组 回顾性分析2016年1月至2018年12月在本科行CPB心脏手术的CHD患儿。通过经胸心脏彩超采用三尖瓣返流法对肺动脉压进行估算,肺动脉收缩压大于30 mm Hg,即可诊断为PAH[5]。本文共纳入286例患儿,纳入标准:①术前经心脏彩超检查,诊断为CHD合并PAH;②年龄小于3岁的婴幼儿患者;③在本科行传统正中开胸CPB下心脏手术。排除标准:①介入、侧切口或其他微创心脏手术者;②二次手术者;③术前已合并严重感染或多器官功能不全者;④临床资料收集不全。根据患儿术后机械通气时间长短,包括气管插管及气管切开、大于24 h者纳入延迟组(n=81),反之则纳入非延迟组(n=205)[6]。 年龄 19.1(10.8,27.2)月,最小为出生后21 d。男性138名。体重12.0(9.1,14.5)kg。 再次气管插管者只针对术后第一次机械通气的数据进行分析。
1.2 收集指标 术前基本信息:年龄、性别、体重、肺动脉压力、经皮血氧饱和度(saturation of oxygen,SO2)、肺部感染、左室射血分数(left ventricular ejec⁃tion fraction,LVEF)、气管插管。采用CHD手术风险调整-1(Risk Adjustment for Congenital Heart Sur⁃gery-1,RACHS-1)评分对手术的复杂程度进行分级[7]。术中临床资料:CPB时间、主动脉阻断时间、自动复跳、二次转机。记录术后当天心包纵膈引流量。术后第一天清晨抽取静脉血,送本院检验科进行常规检测,收集白细胞、血红蛋白、血尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine,Cr)、白蛋白(albumin,Alb)、谷草转氨酶(aspartate amin⁃otransferase,AST)、谷丙转氨酶(alanine aminotrans⁃ferase,ALT)、总胆红素(total bilirubin,TBil)、B 型钠尿肽(B-type natriuretic peptide,BNP)、C 反应蛋白(C-reaction protein,CRP)等指标。统计患者术后ICU停留时间、总住院日、死亡率。
1.3 统计分析 采用SPSS 22.0进行统计分析。正态分布计量资料以均值±标准差(±s)表示,组间比较采用独立样本t检验;非正态分布计量资料以中位数(Q1,Q3)表示,组间比较采用Wilcoxon秩和检验;计数资料以例数(百分比)表示,组间比较采用卡方检验。以可能的危险因素作为自变量,进行lo⁃gistic回归分析,计算优势比(odds ratio,OR)及95%置信区间(confidence interval,CI),分析术后延迟拔管的独立危险因素。当P<0.05时认为存在统计学差异。
2 结 果
2.1 一般信息 本组患儿机械通气时间 34.3(21.8,45.2)h,最短为术后 2 h,最长为术后 395 h。 单纯简单CHD(包括室间隔缺损、房间隔缺损、动脉导管未闭)170例,占59.4%,合并二尖瓣关闭不全45例,肺静脉异位引流29例,房室间隔缺损23例,主动脉弓缩窄10例,三尖瓣下移畸形5例,右室双出口2例,大动脉转位2例。
2.2 危险因素 婴幼儿CHD合并PAH术后延迟拔管的危险因素见表1。术前肺动脉压力、术前气管插管、术中CPB转流时间、自动复跳均与延迟拔管的发生显著相关(P<0.05)。术前因素包括年龄、性别、体重、SO2、肺部感染、LVEF;术中因素包括RACHS-1评分、主动脉阻闭时间、二次转机;术后因素包括白细胞、血红蛋白、BUN、Cr、Alb、AST、ALT、TBil、BNP、CRP,均在两组中无显著差异。P<0.1 的相关因素共有9个,分别为肺动脉压力、SO2、肺部感染、术前气管插管、CPB转流时间、主动脉阻闭时间、自动复跳、BNP、CRP,进一步行多因素logistic回归分析显示(表2)。术前肺动脉压力、术前气管插管、术后第一日CRP为延迟拔管的独立危险因素。
2.3 临床结局 婴幼儿CHD合并PAH术后出现延迟拔管,其ICU停留时间(P=0.007)、总住院日(P=0.039)均显著高于非延迟拔管患者,而两组的死亡率未有显著性差异(P=0.463)。见表3。
3 讨 论
PAH为CHD的常见合并症,其发病率及病死率均较高。当心内畸形存在时,会造成血液左向右流动,肺动脉血流量的长期增加引起肺血管内膜纤维增生、管腔狭窄,造成肺血管重建、肺阻力进行性升高,临床常表现为反复的肺部感染以及低氧血症。若心内畸形得不到有效纠正,当肺动脉压力超过体循环压力时则形成艾森曼格综合征,患者失去手术机会[8]。因此,在临床上绝大多数的CHD患儿需在婴幼儿期就行心脏手术矫治。婴幼儿CHD患者在经历CPB手术后,由于炎性介质的大量释放,会对全身各个系统造成一定的损伤,并且血管通透性增加、细胞内液外渗,能够加重肺间质水肿,使肺表面活性物质减少,肺血管阻力增加,肺顺应性降低。缺血再灌注引起的氧自由基蓄积也会进一步加重肺损伤[9-10]。此外,PAH患儿往往会出现肺血管扩张,进而压迫临近气管导致气体输送异常,增加气道阻力。因此,肺功能异常是婴幼儿CHD合并PAH术后常见的并发症。
表1 术后延迟拔管的单因素分析项目(±s)
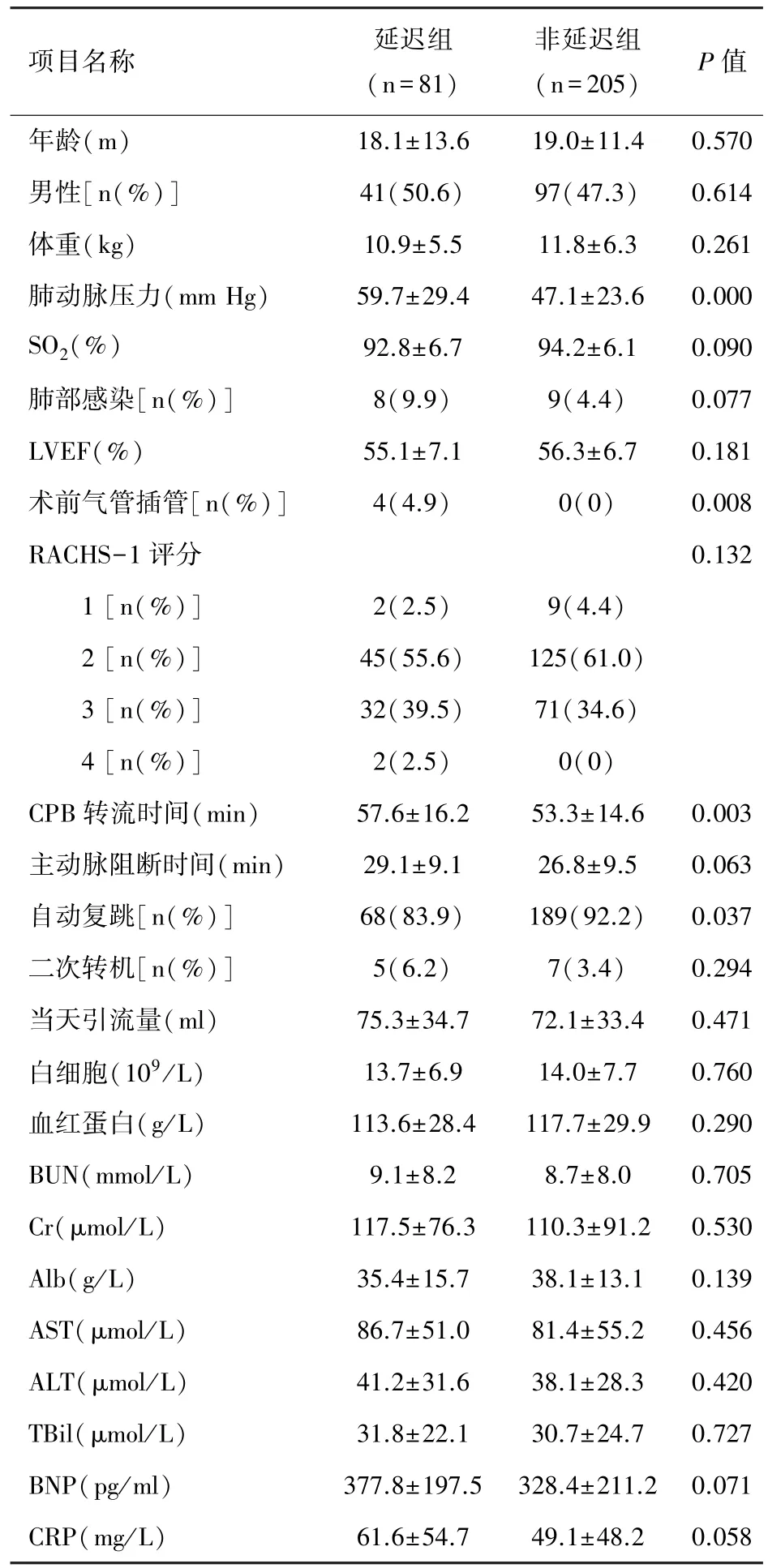
表1 术后延迟拔管的单因素分析项目(±s)
项目名称 延迟组(n=81)非延迟组(n=205) P 值年龄(m) 18.1±13.6 19.0±11.4 0.570男性[n(%)]41(50.6) 97(47.3) 0.614体重(kg) 10.9±5.5 11.8±6.3 0.261肺动脉压力(mm Hg) 59.7±29.4 47.1±23.6 0.000 SO2(%) 92.8±6.7 94.2±6.1 0.090肺部感染[n(%)]8(9.9) 9(4.4) 0.077 LVEF(%) 55.1±7.1 56.3±6.7 0.181术前气管插管[n(%)]4(4.9) 0(0) 0.008 RACHS-1 评分 0.132 1 [n(%)]2(2.5) 9(4.4)2 [n(%)]45(55.6) 125(61.0)3 [n(%)]32(39.5) 71(34.6)4 [n(%)]2(2.5) 0(0)CPB 转流时间(min) 57.6±16.2 53.3±14.6 0.003主动脉阻断时间(min) 29.1±9.1 26.8±9.5 0.063自动复跳[n(%)]68(83.9) 189(92.2) 0.037二次转机[n(%)]5(6.2) 7(3.4) 0.294当天引流量(ml) 75.3±34.7 72.1±33.4 0.471白细胞(109/L) 13.7±6.9 14.0±7.7 0.760血红蛋白(g/L) 113.6±28.4 117.7±29.9 0.290 BUN(mmol/L) 9.1±8.2 8.7±8.0 0.705 Cr(μmol/L) 117.5±76.3 110.3±91.2 0.530 Alb(g/L) 35.4±15.7 38.1±13.1 0.139 AST(μmol/L) 86.7±51.0 81.4±55.2 0.456 ALT(μmol/L) 41.2±31.6 38.1±28.3 0.420 TBil(μmol/L) 31.8±22.1 30.7±24.7 0.727 BNP(pg/ml) 377.8±197.5 328.4±211.2 0.071 CRP(mg/L) 61.6±54.7 49.1±48.2 0.058
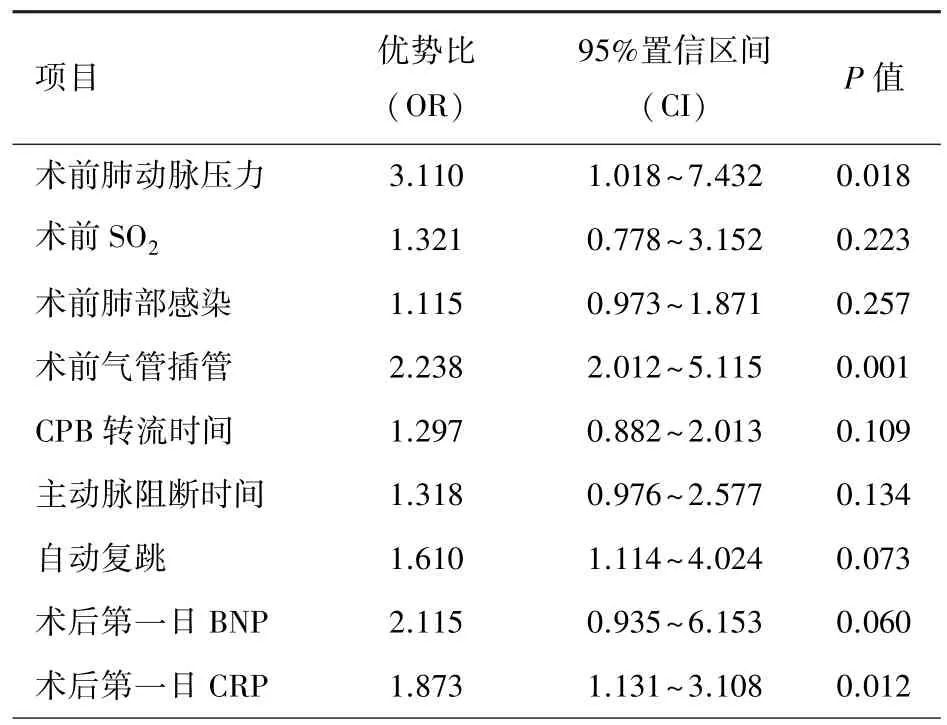
表2 术后延迟拔管的logistic回归多因素分析
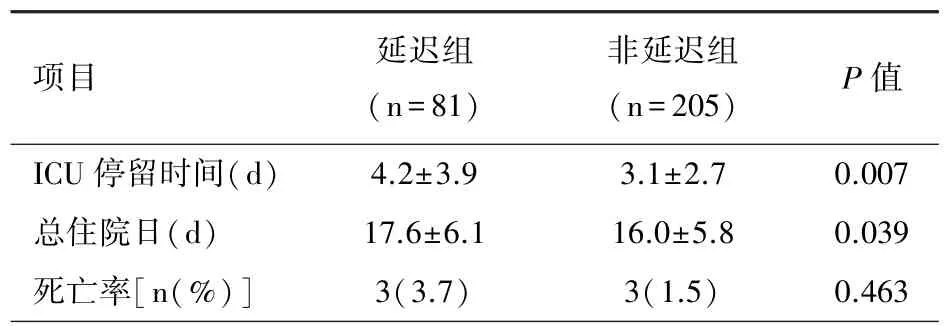
表3 延迟拔管对临床结局的影响
CPB心脏手术的患者术后均需行机械通气治疗,通过维持较高的血氧饱和度,保证组织及器官供氧,降低心脏的后负荷,并较少呼吸做功,改善患者的心肺功能,维持血流动力学稳定。然而,过度延长的机械通气会增加患儿院内感染的风险,以及肺不张、肺水肿、气道损伤等并发症,增加住院时间及费用,与不良预后密切相关[11-12]。本文的结果也提示术后延迟拔管会增加患儿的ICU停留时间及总住院日。针对婴幼儿CHD合并PAH患者,笔者前期研究了影响其术后机械通气时间的主要因素,结果证实CPB时间、术后低心排血量综合征、呼吸机相关性肺炎、肺动脉压力等与机械通气时间有关[13]。本研究进一步对术后延迟拔管的危险因素进行分析,发现术前肺动脉压力、术前气管插管、术后第一日CRP是延迟拔管的独立危险因素。合并重度PAH的患儿围术期肺损伤也较重,术后会因缺氧、容量控制、酸碱失衡等诱因出现肺高压危象,术后早期常需深度镇静镇痛,并且需要使用多种药物联合治疗,这就决定了此类患儿术后会接受长时间的机械通气。术前就已行气管插管提示患儿肺功能较差,可能合并有严重的肺部感染或支气管狭窄等,也可能与重度PAH引起的低氧血症有关。因此,术后往往需要延长呼吸机治疗时间来改善心肺功能及低氧血症。虽然CRP是一种急性期的炎性标志物,但是其也可作为心脏术后不良事件的独立预测因子[14-15],术后早期的CRP升高提示患儿全身损伤重,有可能会造成对呼吸机的过度依赖。因此,通过对延迟拔管的危险因素进行分析,可以进行针对性的干预和治疗,来改善患者的临床结局。比如,在术前可以加强患儿肺功能的改善,充分纠正肺部感染,积极采用靶向药物降肺动脉压治疗,术中注重加强心肌及多器官保护等。
综上所述,婴幼儿CHD合并PAH术后延迟拔管会显著影响患儿的临床预后,通过对其发生的危险因素进行分析及干预,将会有助于术后恢复。然而,对于重度PAH患儿,术后过早撤机也同样会诱发肺高压危象,导致再次插管,对患儿造成更大的损伤,而适当地延长机械通气时间、合理使用呼气末正压、应用肺保护性通气,维持足够的氧合也会对患儿产生有利效应[11]。因此,如何进一步改进机械通气策略、把握撤机指征、明确机械通气维持时间,仍是未来需研究的内容。

