原位肝移植术后慢性肾功能损伤的危险因素
方浩然,郭文治
(1.郑州大学第一附属医院 肝移植科,河南 郑州 450000;2.河南省器官移植医学工程技术中心,河南 郑州 450000;3.郑州市器官移植技术与应用工程重点实验室,河南 郑州 450000)
肝移植是治疗终末期肝病的最有效治疗手段。近年来,随着外科手术技术的进步及新型免疫抑制药物的开发,肝移植患者数量不断增加,生存期也不断延长,肝移植术后远期并发症已成为临床关注的焦点。慢性肾功能损伤(chronic renal dysfunction,CRD)是肝移植术后常见的远期并发症,发生率为17.6%~80.0%[1-5]。CRD可影响患者预后,部分CRD患者可转变为慢性肾功能衰竭,严重影响患者的生存。目前国内外对于肝移植术后肾损伤的研究主要聚焦于急性肾功能损伤(acute kidney injury,AKI),对CRD研究较少,不利于临床早期预防和治疗。本研究回顾性分析135例同种异体原位肝移植患者的临床资料,分析CRD的危险因素,以期为临床预防及治疗提供更多参考依据。
1 资料与方法
1.1 一般资料回顾性分析2014年1月至2016年8月郑州大学第一附属医院肝移植科收治的135例患者的临床资料。男110例,女25例;年龄16~71岁,平均(47.6±8.8)岁;49例原发病为肝癌,82例为肝硬化,2例为爆发性肝衰竭,1例为药物性肝衰竭,1例为肝豆状核变性。所有患者均接受非体外转流的同种异体原位肝移植术,术后均接受以他克莫司为主的免疫抑制方案治疗,患者均签署知情同意书。本研究由郑州大学第一附属医院医学伦理委员会批准,伦理审批号为2019-KY-019。
1.2 纳入及排除标准(1)纳入标准:①年龄≥12岁;②首次接受同种异体原位肝移植;③供肝来源为心脏死亡或脑死亡器官捐献;④术后生存时间长于3 a且临床资料完整。(2)排除标准:①合并其他器官移植;②术前存在肾病综合征等基础肾脏疾病。
1.3 诊断标准及分组根据慢性肾脏病评价及管理临床实践指南[6]诊断CRD,即肾损害>3个月,伴或不伴肾小球滤过率降低,同时表现为以下异常之一:有肾损伤指标,表现为血、尿检查或影像学检查异常;有组织病理学检查异常;肾小球滤过率(glomerular filtration rate,GFR)<60 mL·min-1。根据患者术后是否出现CRD分为CRD组和非CRD组。
1.4 观察指标收集患者一般资料及术前、术中、术后早期相关资料,包括性别、年龄、体质量指数(body mass index,BMI)、糖尿病患病情况、高血压患病情况、HBV感染情况,是否为肝细胞癌患者、Child评分、终末期肝病模型(model for end-stage liver disease, MELD)评分、国际标准化比值(international normalized ratio,INR)、凝血酶原时间(protothrombin time,PT)、血红蛋白(hemoglobin,Hb)、白蛋白(albumin,ALB)、GFR、肌酐(creatinine,Cr)、血尿素氮(blood urea nitrogen,BUN)、尿酸(uric acid,UA)、血钾、血钠、血糖、冷缺血时间、热缺血时间、无肝期及术后1周血糖、BUN、GFR、他克莫司浓度。

2 结果
患者术前GFR为(115.6±21.3)mL·min-1,术后3 a内共20例患者出现CRD,发生率为14.80%。单因素分析显示高血压、年龄、Hb、BUN、GFR、UA、MELD评分、术后1周血糖、术后1周他克莫司浓度、术后1周BUN、术后1周GFR为肝移植术后CRD发生的相关因素,见表1。Logistic回归分析显示年龄、MELD评分、UA、术后1周他克莫司浓度、术后1周血糖是CRD发生的独立危险因素,见表2。分别以上述指标建立预测CRD发生的ROC曲线模型,各因素预测价值见表3。

表1 影响肝移植术后CRD的相关因素(单因素分析)
注:HBV—乙型肝炎病毒,Hb—血红蛋白,INR—国际标准化比值,PT—凝血酶原时间,ALB—白蛋白,BUN—血尿素氮,Cr—肌酐,GFR—肾小球滤过率,UA—尿酸,MELD—终末期肝病模型。
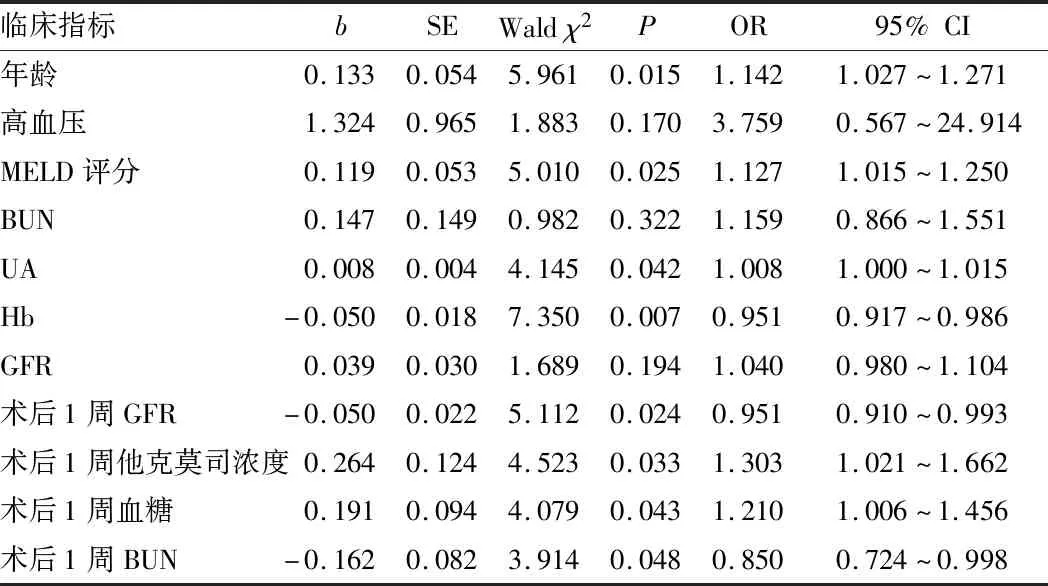
表2 影响肝移植术后CRD的多因素Logistic回归分析
注:MELD—终末期肝病模型,BUN—血尿素氮,UA—尿酸,Hb—血红蛋白,GFR—肾小球滤过率。
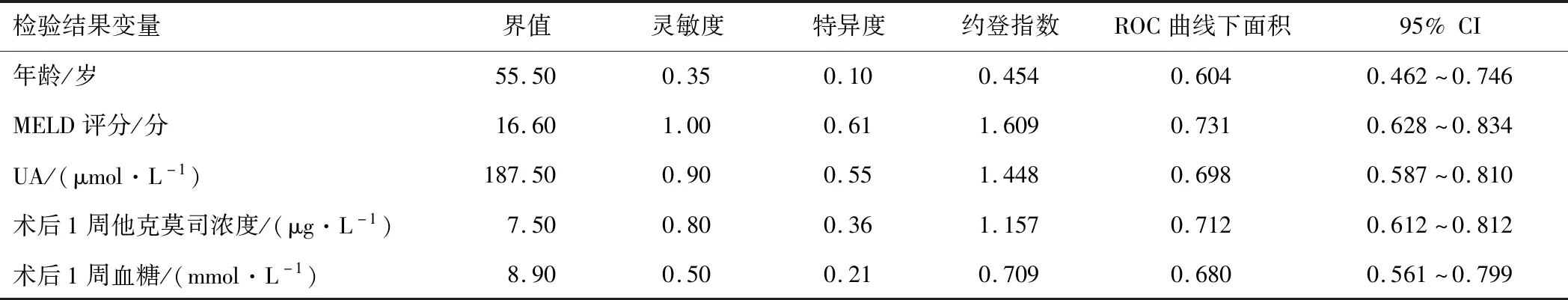
表3 影响肝移植术后CRD的危险因素预测价值
注:MELD—终末期肝病模型,UA—尿酸。
3 讨论
肝移植术后CRD的发生是多因素共同作用的结果,病因和发病机制尚不完全清楚,明确病因、早期预防和治疗对改善患者预后有积极作用。本研究结果显示:高血压、年龄、Hb、BUN、UA、GFR、MELD评分、术后1周血糖、术后1周他克莫司浓度、术后1周BUN、术后1周GFR为CRD发生的相关因素,其中年龄、UA、MELD评分、术后1周他克莫司浓度、术后1周血糖是CRD发生的独立危险因素,对CRD的发生有一定的预测作用,各指标界值可为移植者的健康管理提供依据。
随着年龄增长,GFR不断下降。Ojo等[7]在一项针对69 321例非肾脏移植患者的研究中发现,术后3 a共有16.5%的患者出现慢性肾功能衰竭,且年龄每增加10岁,慢性肾功能衰竭的相对风险增加1.36倍[7],这与本研究相符。
血Cr水平并不能完全反映肾脏功能,其受许多肾外因素的影响,如年龄、性别、肌肉质量、膳食蛋白质和肌酸摄入量等[8],同时其变化也往往滞后于肾功能的变化[9]。由于终末期肝病患者术前往往会出现蛋白质缺乏、肌肉萎缩、水肿和管状Cr排泄增加等,导致肌酸合成Cr显著受损(高达50%)[10],这可能是本研究未发现Cr是CRD危险因素的原因之一。UA也是反映肾功能的指标之一,高尿酸血症可加剧肾功能恶化。Ryoo等[11]在一项针对18 778例个体的前瞻性研究中发现,UA水平与CRD的发生独立相关。术后1周GFR反映患者经过手术“打击”后短期内肾脏状态。肝移植术中血流低灌注、术后移植肝无功能、感染及药物性肾损害等均可导致术后GFR降低[12]。Velidedeoglu等[13]研究发现,肝移植术后发生急性肾损伤可预测慢性肾脏病的发生,并把术后1周血Cr值是否大于2 mg·dL-1作为术后是否发生慢性肾脏病的“压力测试点”。Fisher等[2]证实术后3个月血Cr水平与术后慢性肾功能衰竭密切相关。因此,术后早期肾功能对CRD的发生有一定的预测价值。
本研究显示Child评分不是CRD发生的危险因素,而MELD评分是CRD的独立危险因素,这是由于MELD评分把肾功能考虑在内。与Child评分比,MELD评分更能反映患者的综合状态,更好地反映预后。王小明等[14]研究也发现MELD评分与肝移植术后慢性肾功能衰竭的发生密切相关。
本研究示术后1周他克莫司浓度是CRD发生的独立危险因素。钙调磷酸酶抑制剂(calcineurin inhibitor,CNI)的肾脏毒性可使肾脏发生急性功能性和慢性结构性改变[15]。CNI导致肾素-血管紧张素和内皮素系统的激活及交感神经活动的增加[16]。此外,CNI抑制一氧化氮合成和一氧化氮介导的血管舒张,且可通过血管收缩相关的缺氧增加自由基和超氧化物的产生,从而导致肾脏血管收缩,肾小管坏死,间质纤维化,空泡化,细胞外基质沉积,最终使肾功能受损。研究证实CNI造成肾小动脉病变,加剧糖尿病肾病的进展[17]。Nashan等[18]发现肝移植术后接受依维莫司与减量他克莫司二联免疫抑制剂治疗的患者,肾功能优于单纯接受他克莫司治疗的患者。
本研究结果未显示糖尿病、高血压是肝移植术后CRD发生的独立危险因素,可能与样本量较少及研究为回顾性研究有关。但研究发现术后1周血糖水平是CRD发生的独立危险因素。移植术后大量使用激素,导致患者术后血糖升高,糖尿病发病率上升。Schmitz等[19]研究发现肝移植术后CRD组糖尿病发病率由术前的17.5%增加至20.4%。术后糖尿病发病率的上升使糖尿病相关肾病增多,增加CRD的发生。
本研究发现Hb也是肝移植术后CRD发生的相关因素,术前低Hb状态可导致术后CRD发生风险增加。这可能是由于肾脏是一个高血流灌注器官,对缺血缺氧极为敏感,Hb水平下降致使氧气运输减少,肾脏受到缺氧损伤,导致细胞发生凋亡或上皮-间充质转化,形成恶性循环,导致肾功能持续下降[20]。同时术前低Hb的患者术中往往需要输血,王万里等[21]研究表明术中大量输血可导致术后肾损伤的发生。
积极采取各种预防措施有助于减少肝移植术后CRD的发生。术前应避免Hb过低,术后适当减少糖皮质激素的使用,同时根据术后早期GFR采取预防措施,必要时进行替代治疗,使患者平稳度过术后危险期,避免肾功能恶化。维持他克莫司等CNI类药物浓度处于较低水平。总之,对于肝移植术后CRD,重在预防,应尽量避免各种危险因素,这对改善患者预后有积极作用。

