2-取代苯并噻唑类化合物的合成研究进展
杨志勇, 成园园, 周 亮
(贵州理工学院 化学工程学院,贵州 贵阳 550003)
苯并噻唑及其衍生物作为生物二级代谢产物中常见的结构单元具有良好的生物活性,被广泛应用于农药、医药和材料等领域。由于苯并噻唑及其衍生物在应用领域的广泛性,使得药物学和有机化学研究人员对其产生了浓厚的研究兴趣,并且一直持续到现在。早在1887年,Hantzsch[1]就提出利用α-卤代酮与硫脲反应合成2-取代噻唑类化合物(Scheme 1)。该方法作为合成2-取代噻唑类化合物的有效方法之一,被命名为Hantzsch法。在此后的一个多世纪里,该方法作为合成2-取代噻唑类化合物的经典方法被广泛应用。Wipf[2]与Buchanan[3]等分别在1996年和1999年对该方法进行了改进,使反应条件更温和,应用范围更广。除以上传统合成方法外,本文还将对其他合成方法进行综述。

Scheme 1
1 以邻氨基苯硫酚为原料合成2-苯基苯并噻唑类化合物
1.1 邻氨基苯硫酚与苯甲醛反应
由邻氨基苯硫酚与芳香醛及其衍生物缩合反应生成苯并噻唑衍生物是一类被广泛应用的方法。该方法原料来源丰富,反应条件简单。1990年,Deligeorgiev[4]报道了邻氨基苯硫酚与苯甲醛或苯甲酸在氧化剂作用下,DMSO为溶剂,以90%产率获得2-苯基苯并噻唑(Scheme 2)。该方法最大的优点在能够使邻胺基苯硫酚与苯甲酸反应生成预期产物,而不再限制于与苯甲醛反应。
2008年,Bahrami[5]报道了以H2O2与CAN(硝酸铈铵)作为混合氧化剂,在50 ℃条件下,实现苯甲醛与邻氨基苯硫酚反应生成2-苯基苯并噻唑(Scheme 3)。该方法中仅使用了相对廉价易得的氧化剂H2O2与CAN,而且在该反应中无需要用到任何溶剂,简单易行,而且对环境污染较小。同年,Al-Qalaf等以甲醇为溶剂,在室温条件下只利用硝酸铈铵,使邻氨基苯硫酚和芳香醛在温和的条件下反应以较高产率合成了2-芳基苯并噻唑类衍生物。

Scheme 3
2009年,Bahrami等[6]以邻氨基苯硫酚与醛为原料,在Fe(NO3)3·9H2O和H2O2的作用下反应快速高效地生成了苯并噻唑类衍生物(Scheme 4)。通过实验证实Fe(NO3)3·9H2O是起催化氧化关键作用的催化剂,而H2O2是协助硝酸铁完成催化循环的氧化剂。该方法的反应条件温和、催化效率高、产率高、对环境友好以及使用廉价的催化剂,是合成苯并噻唑类衍生物不可替代的新方法。Cao与Prabal等[7-9]在此基础上又报道了以FeCl3或物Al2O3-Fe2O3等作催化剂合成2-取代苯并噻唑类化合物。

Scheme 4
2009年,Pratap等[10]以二氯甲烷为溶剂,在室温条件下利用酵母催化邻氨基苯硫酚与芳香醛反应生成苯并噻唑类衍生物(Scheme 5)。该法首次以酵母为催化剂在有机溶剂中高效地合成了苯并噻唑类化合物,为苯并噻唑类化合物的合成提供了新方法。

Scheme 5
随着现代有机合成化学的发展,由邻氨基苯硫酚与苯甲醛反应生成2-苯基苯并噻唑的方法也在不断得到改进和更新。尤其是在最近几年,光催化合成化学快速发展的前景下,传统合成2-苯基苯并噻唑的方法也开始与光催化反应相结合。
2013年,Biswas[11]分别报道了邻氨基苯硫酚与苯甲醛在有机光催化剂pytz(3,6-diphenyl-1,2,4,5-tetrazine)催化下反应合成2-苯基苯并噻唑(Scheme 6)。该方法首次将传统合成方法与有机光催化相结合,体现了巨大的应用前景。

Scheme 6
2013年,Biswas[11]报道了邻氨基苯硫酚与苯甲醛在有机光催化剂CdSNS(CdSnS4)的催化下反应合成2-苯基苯并噻唑(Scheme 7)。该方法在可见光、常温条件下就能完成,具有巨大的应用前景。

Scheme 7

Scheme 8
2014年,Hemant Sharma[12]等采用球磨法制备了一种方便、无溶剂的苯并噻唑、苯并咪唑和苯并恶唑衍生物(Scheme 8)。该方法过程非常高效,并且提供了简单的产品隔离。
此类反应机理假设已经基本成熟,主要过程分为两步:第一步邻氨基苯硫酚中的氨基与苯甲醛发生缩合反应生成席夫碱,第二步席夫碱与邻位的巯基发生环化反应生成苯并噻唑啉,该中间体在氧化剂的作用下脱氢生成目标产物2-取代的苯并噻(Scheme 9)。
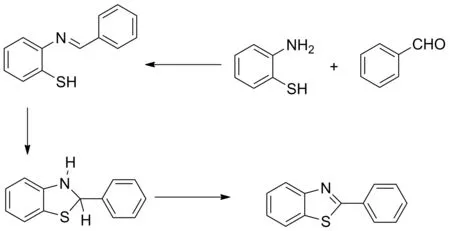
Scheme 9
1.2 邻氨基苯硫酚与苯甲酰氯反应
相对于苯甲醛与邻氨基苯硫酚反应生成2-苯基苯并噻唑通常需要氧化剂的存在,利用苯甲酰氯与邻氨基苯硫酚反应生成2-苯基苯并噻唑则无需添加任何氧化剂。
2001年,Barlos等[13]报道了苯甲酰氯与邻氨基苯硫酚在室温下,使用N,N-二异丙基乙胺(DIPEA)作为催化剂,生成2-苯基苯并噻唑(Scheme 10)。该方法简单易行,在基本不需要溶剂的条件下就能够完成预期反应。2013年,Lee等[14]对Barlos方法进行改进,苯甲酰氯与邻氨基硫酚在不添加任何催化剂和氧化剂,且无溶剂条件下反应生成2-取代的苯并噻唑。
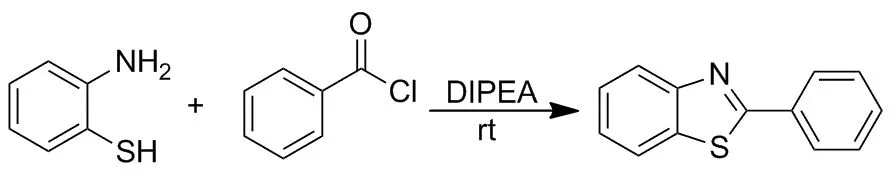
Scheme 10
1.3 邻氨基苯硫酚与苄醇反应
2004年,Taylor等[15]报道了苄醇与邻氨基苯硫酚在MnO2作为氧化剂,甲苯作为溶剂的条件下,反应生成2-苯基苯并噻唑。2011年,Kanchugarakoppal等[16]实现了将邻氨基苯胺与苄醇加入T3P(丙基磷酸酐)的乙酸乙酯溶液中,在室温下反应4个小时生成咪唑,产率最高达到90%。他同时还指出此方法也适用于邻氨基苯硫酚与苄醇反应生成2-苯基苯并噻唑(Scheme 11),而且乙醇和丙烯醇也可以与2-氨基苯胺反应生成预期产物。
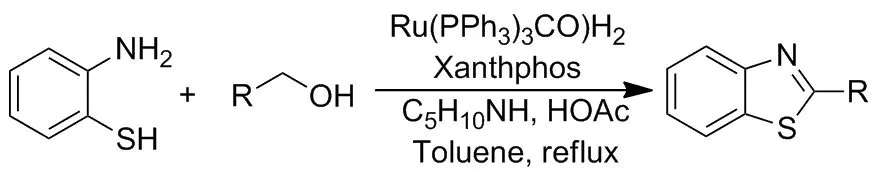
Scheme 11
1.4 邻氨基苯硫酚与其他化合物反应生成2-取代苯并噻唑
1957年, Leavitt课题组[17]报道了多聚磷酸催化的2-氨基苯硫酚直接与酰胺、腈等发生缩合反应,合成一系列的2-取代苯并噻唑衍生物(Scheme 12),相比用醛的缩合反应,多聚磷酸是一种良好的催化剂,该反应需要在高温下反应,反应时间较长。
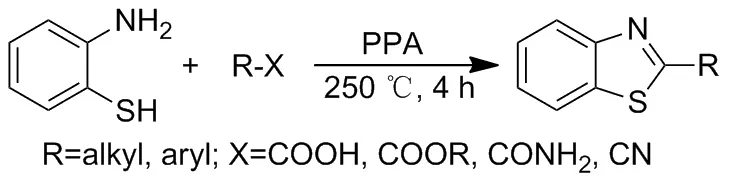
Scheme 12
2007年,Mohammadpoor等[18]在无溶剂的条件下,以ZrOCl2·8H2O为催化剂,使邻氨基苯硫酚与原酸酯反应快速高效地合成了苯并噻唑类衍生物(Scheme 13)。该法所使用的催化剂无毒、高效、价廉易得,催化剂还可循环利用,并且此法具有不需要溶剂、操作简单、反应时间短、反应条件温和、产率高等特点。2011年,Liu等[19]将催化剂ZrOCl2·8H2O换为Ga(OTf)3后在同样的条件下发现反应效果更好。这是一种很好的绿色合成方法,该反应的缺点就是原酸酯原料的种类比较少,合成方法的应用受到一定的局限。

Scheme 13
2007年,Gupta等[20]在碘的作用下,使邻氨基苯硫酚与芳香酸在固态下研磨反应10 min合成了苯并噻唑类衍生物(Scheme 14)。这种方法不需要有机溶剂,成本低、无污染,是一种合成苯并噻唑类衍生物的好方法。
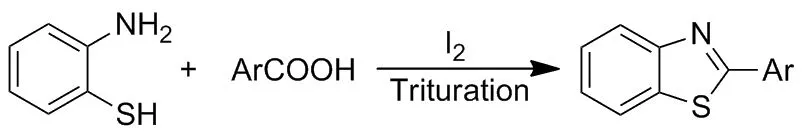
Scheme 14
Yu等[21]在浓硫酸的作用下使邻氨基苯硫酚和硫代羰基酸酯进行缩合反应生成了2-芳基取代的苯并噻唑类衍生物(Scheme 15)。该合成方法首先进行胺解反应(胺-酯交换形成酰胺),然后环化脱硫化氢即得苯并噻唑类衍生物。

Scheme 15
2008年,Lim等[22]利用联接在树脂上的酯基团与邻氨基苯硫酚在微波辅助的条件下进行缩合反应合成了苯并噻唑类化合物(Scheme 16),这是一种利用固相法快速高效合成苯并噻唑类衍生物的新方法。

Scheme 16

Scheme 17
2014年,Bao等[23]报道了一种相对简便新颖的合成2-芳基苯并噻唑化合物的方法。以邻氨基苯硫酚和乙酸乙酯等作为原料,甲苯磺酸为催化剂进行缩合,亲核加成环化和C—C键断裂得到目标产物,在这个反应中不仅可以得到2-芳基苯并噻唑也能得到2-烷基苯并噻唑(Scheme 17),但有副产物生成,经济性低。
2015年,Liu等认为构筑C—S键时以二氧化碳作为C1原料,是一种比较绿色的合成含硫化合物的路线。他们报告了通过环合邻氨基苯硫酚与二氧化碳在温和的条件下合成苯并噻唑(Scheme 18)。研究发现,1-丁基-3-甲基咪唑乙酸酯可以作为一种多功能催化剂,活化CO2和氢硅烷形成中间体,同时通过氢键活化2-氨基噻吩,获得了一系列高收率的苯并噻唑。
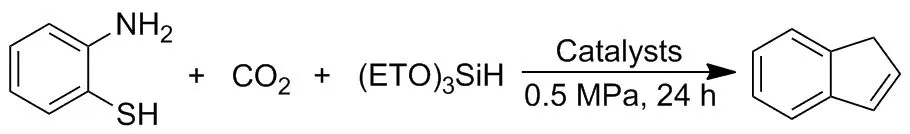
Scheme 18
2016年Muhammad等[25]报道了B(C6F5)3与大气CO2相结合可高效环化DMF的邻取代苯胺衍生物(Scheme 19),并得到一系列含N的杂环,包括苯并噻唑、苯并咪唑、喹唑啉酮和苯并恶唑,产率良好,产率优良。
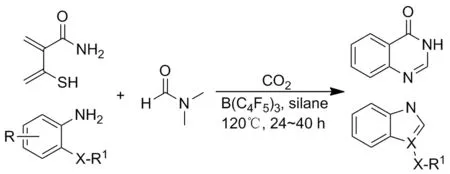
Scheme 19
2016年Kalidas等[26]以DMF为溶剂,2-氨基苯腈为环化反应,制备了新型高效、可伸缩的CO2介导的喹唑啉-2,4(1H,3H)-二酮。以邻苯二胺(OPD)和2-氨基苯硫醇酚为原料,在最佳条件下合成了苯并咪唑、苯并噻唑、苯并咪唑及其衍生物(Scheme 20),具有很好的转化率和选择性。
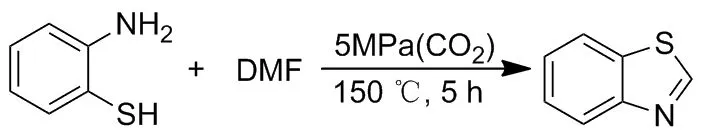
Scheme 20
2 以酰胺为原料合成噻唑及2-取代苯并噻唑类化合物
随着邻氨基苯硫酚为原料合成苯并噻唑类衍生物的方法不断发展成熟, 产率也一般较高。但是由于含有取代基的邻氨基苯硫酚不稳定,影响了其进一步发展,因此又提出了过渡金属催化酰胺类化合物环化脱氢合成苯并噻唑的方法, 该方法主要利用过渡金属使邻位苯环上的C—H键活化,然后再环化形成C—S键获得目标产物。
1997年,Jayanthi等[27]报道了光催化合成苯并噻唑类化合物的方法(Scheme 21)。用光照催化是一个开拓性的发现,经济消耗低,同时他们也通过量子产率和光解中间体的研究探讨光催化反应的机理。
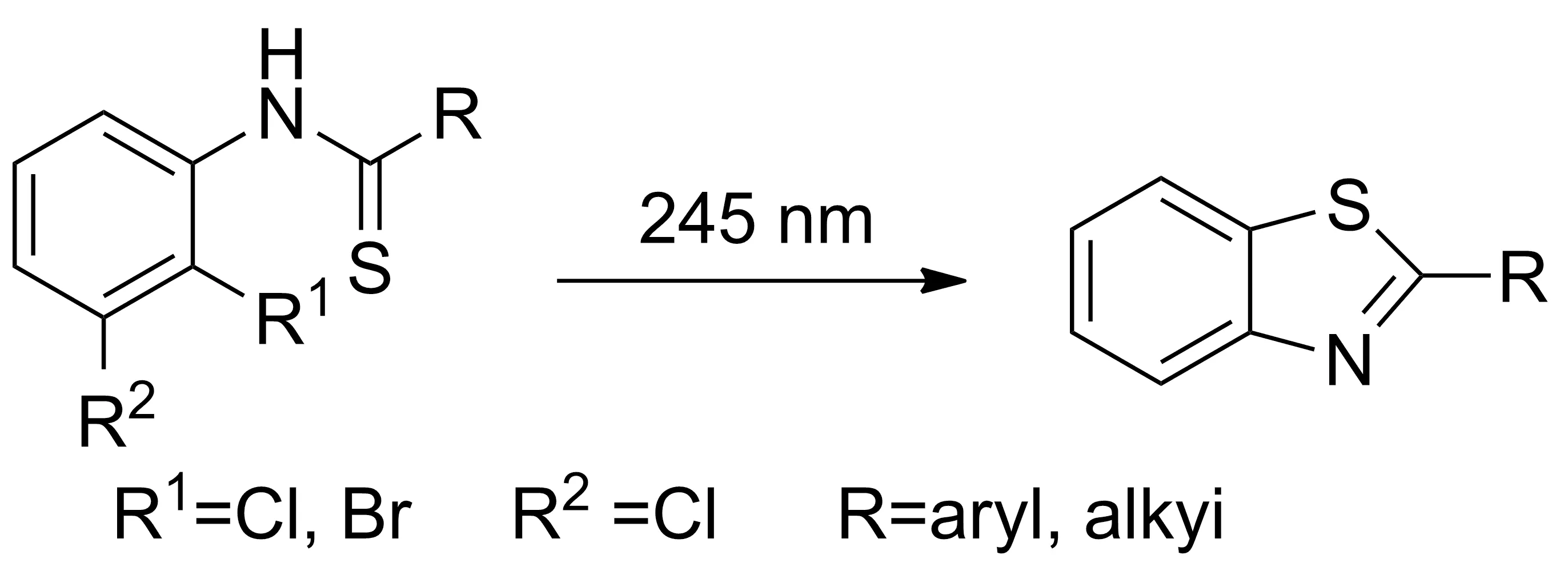
Scheme 21
Scheme 22

Scheme 23
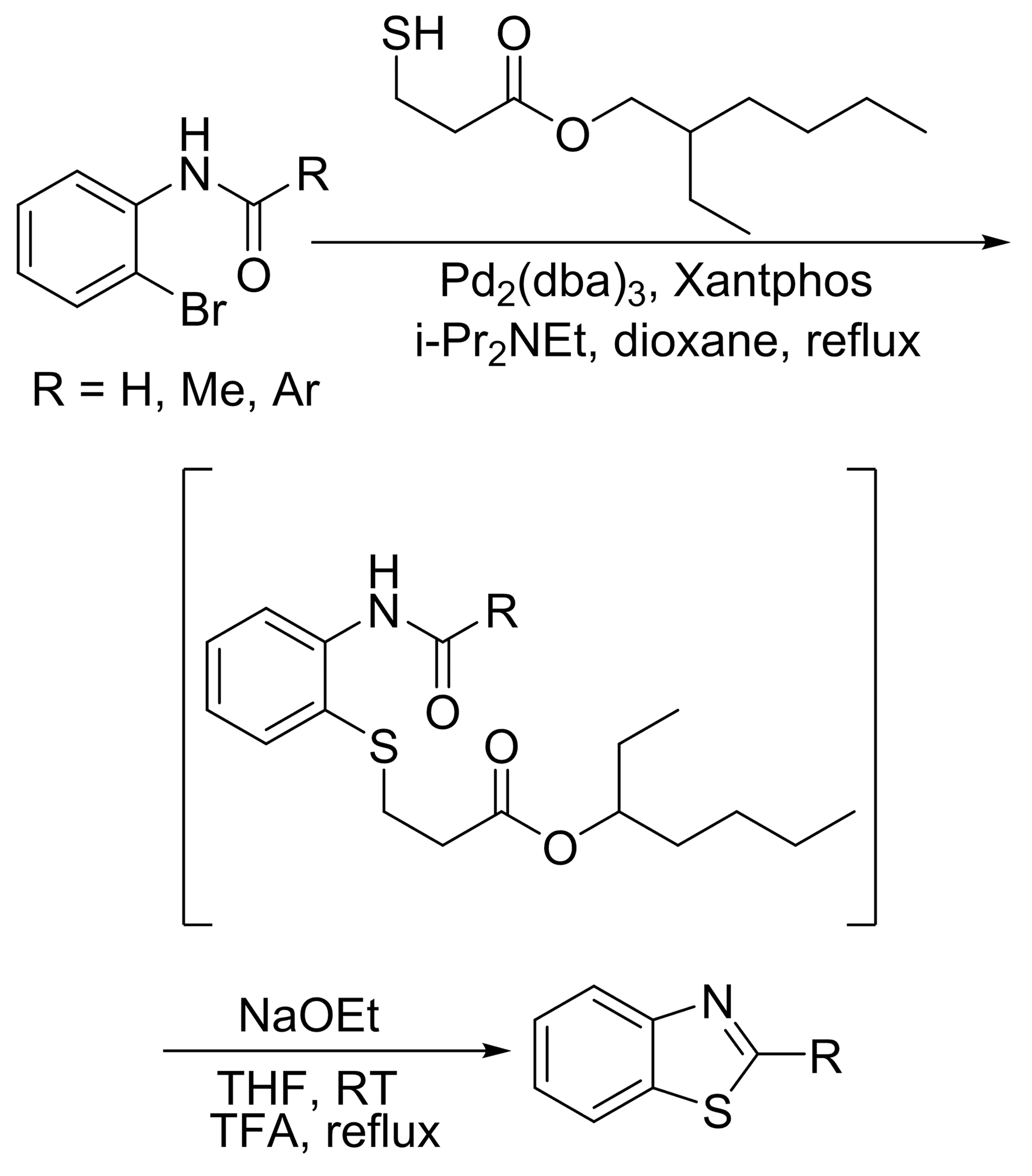
2000年,Itoh等[28]报道了邻溴取代酰基苯胺与硫化物在Pd2(dba)3作为催化剂,Xantphos(4,5-双二苯基膦-9,9-二甲基氧杂蒽)作为配体,iPr2NEt和NaOEt作为碱,二氧六环作为溶剂回流的条件下生成C2位取代的苯并噻唑。该方法不仅能合成2-烷基苯并噻唑和2-芳基苯并噻唑,而且能够使邻溴取代的甲酰苯胺环化生成苯并噻唑(Scheme 22),具有较好的适应性。
2007年,Bernardi等[29]报道了以邻卤素苯甲酰苯胺做底物、Cs2CO3作为碱,二甲苯为溶剂,通过劳森试剂一锅反应制取苯并噻唑类化合物(Scheme 23)。
2008年,Nagasawa等[30]在Itoh报道的方法的基础上,提出了苯甲酰苯胺或硫代苯甲酰苯基胺在氧气条件下,Cu(OTf)2作为催化剂,邻二甲苯作为溶剂,发生环化反应生成2-苯基苯并噻唑或2-苯基苯并噁唑(Scheme 24)。该方法在环化的过程中不需要将苯胺邻位卤代,而且仅仅需要用到Cu(OTf)2作为催化剂就可实现苯甲酰苯胺或硫代苯甲酰苯基胺环化生成预期产物,更加简单可行。

Scheme 24
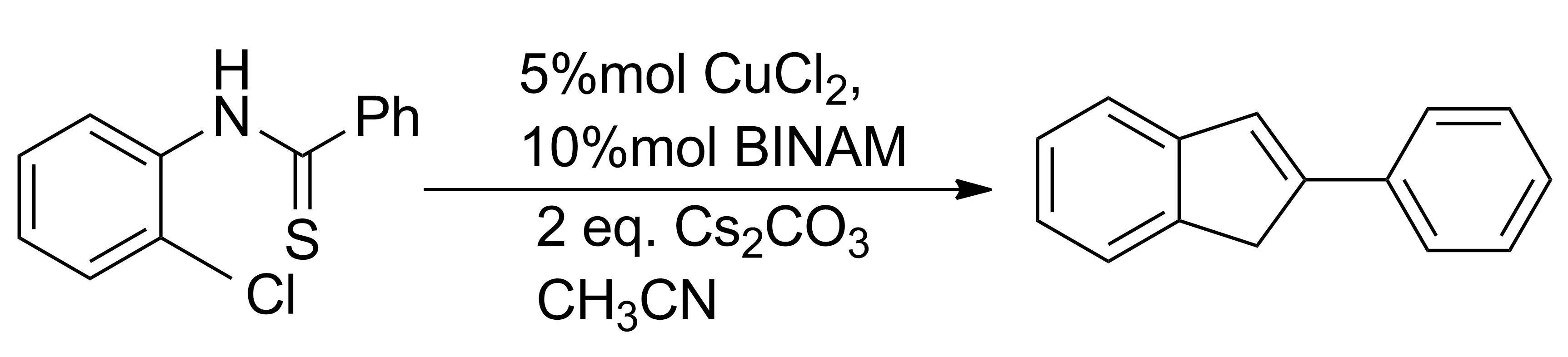
Scheme 25
2010年,Sekar等[31]也报道了2-氯硫代苯甲酰苯基胺在CuCl2作催化剂,BINAM((S)-(-)-1,1′-联-2-萘胺)作为配体,Cs2CO3作为碱,乙腈作为反应溶剂的条件下,于82 ℃反应生成2-苯基苯并噻唑(Scheme 25)。
3 结语
随着苯并噻唑衍生物的抗菌、抗肿瘤等生理活性以及作为功能材料方面的应用的研究与发展,苯并噻唑衍生物的合成势必会有更大的市场需求。近年来,在除传统合成方法外,过渡金属催化、光催化、苯并噻唑与苯甲醛缩合等新方法都成为合成2-取代苯并噻唑的有效方法,尤其是苯并噻唑与苯甲醛等化合物直接缩合反应的合成方法条件简单温和,副产物只有CO2,符合绿色化学的要求。随着苯并噻唑类衍生物在医药、农业以及材料等方面的深入研究与开发,笔者相信在将来会诞生更高效、更绿色合成苯并噻唑类衍生物的新方法。

