吡喃糖氧化酶法检测血清1,5-脱水葡萄糖醇的方法学性能评价
陈颖,李莎,索明环,王伟佳
中山大学附属中山医院检验医学中心,广东 中山 528403
1,5-脱水葡萄糖醇又称1,5-脱水-D-山梨醇(1,5-anhydroglucitol,1,5-AG),是自然界存在的多元醇,可反映检测前1~2周内的平均血糖水平。机体在高糖状态下,葡萄糖会竞争性地抑制1,5-AG在肾小管的重吸收,从而使血清1,5-AG的含量显著降低[1-2]。近年来,1,5-AG反映餐后高血糖和短期血糖波动的优势受到广泛的关注[3-4]。1,5-AG可作为糖尿病患者诊断和预测常见并发症的必要补充,其准确测定有着重要意义。本研究参考CLSIEP文件和相关文献[5-8],评价吡喃糖氧化酶法检测血清1,5-AG的主要分析性能,使其更好地应用于临床,现将结果报道如下:
1 材料与方法
1.1 实验样本 选取2019年4~6月来自广东省中山大学附属中山医院就诊人员样本,无溶血、乳糜、黄疸等干扰物;其中生物参考区间验证样本,男性10例,年龄20~62岁;女性10例,年龄19~62岁,均无任何疾病史。
1.2 试剂与仪器 1,5-AG测定试剂盒、校准品及质控品均由北京九强生物技术股份有限公司提供。仪器为德国西门子ADVIA2400生化分析仪。
1.3 方法
1.3.1 精密度实验 参考EP5-A2文件进行确认。批内精密度:选取低值、高值新鲜血清1,5-AG样本,重复检测20次。批间精密度:选取低值、高值质控品,分成5份,每天测4次,连续测5 d,分别计算其平均值()、标准偏差(SD)和变异系数(CV)。
1.3.2 正确度验证 测定另一个批号1,5-AG校准品低值(7.0µg/mL)和高值(25µg/mL)三次,计算测定均值与配套校准品标示值的相对偏倚。
1.3.3 抗干扰实验 参考EP7-A2文件进行确认,选择低高值1,5-AG新鲜血清样品作为基础样本。干扰物试剂盒和空白对照由北京九强公司提供,以添加不同浓度干扰物之后的血清1,5-AG测定均值超过同一浓度下空白对照管的±5%为产生干扰作用。
1.3.4 分析测量范围(AMR)实验 即线性范围,参考EP6-A文件,分别收集血清1,5-AG浓度接近厂家声明的分析测量范围下限和上限的低值样本(L)和高值样本(H),将L和H样本按:7L、6L+1H、5L+2H、4L+3H、3L+4H、2L+5H、1L+6H、7H混合,配置成1,5-AG系列浓度血清,每个浓度重复测量两次,在一个分析批次内完成。
1.3.5 临床可报告范围(CRR)实验 选择分析范围内高浓度标本3份,配套稀释液做2、4、8、16、32倍稀释,计算稀释回收率,确定可靠测量低限及最大稀释倍数,以回收率(100±10)%为可接受范围;CRR上限=AMR上限×最大稀释倍数。
1.3.6 生物参考区间验证 参考C28-A2文件,对20个参考个体测定血清1,5-AG浓度,与厂家给定的参考区间比较(>14µg/mL)。
1.4 统计学方法 所有资料应用Microsoft Excel 2003及SPSS16.0软件进行统计学分析。精密度、正确度和抗干扰分析采用x-、SD和CV表示;分析测量和临床可报告范围的评价应用多项式回归分析;生物参考区间验证应用“1/3”规则进行离群值检验。以P<0.05为差异有统计学意义。
2 结果
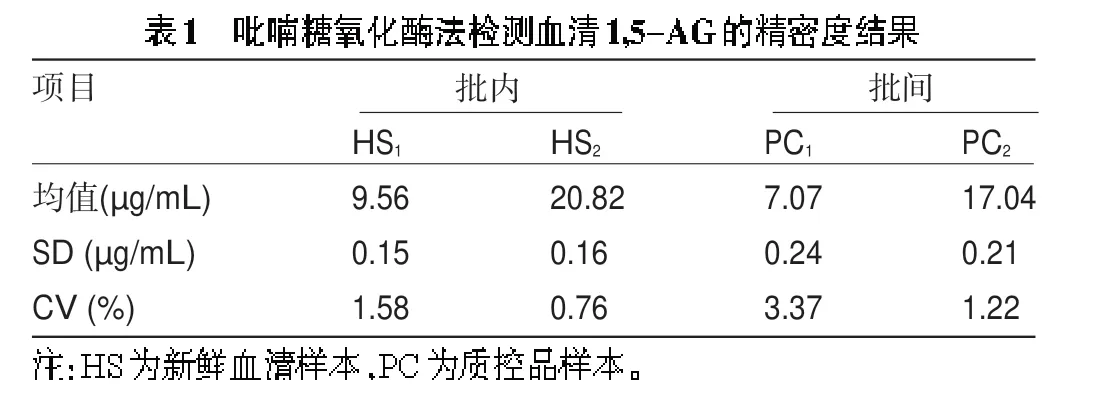
2.1 精密度 吡喃糖氧化酶法检测血清1,5-AG的批内精密度为1.58和0.76%,批间精密度为3.37%和1.22%,见表1。
2.2 正确度 另一个批号校准品测定均值分别是7.1µg/mL和25.32µg/mL,与配套校准品标示值相对偏倚分别为1.42%和1.27%。
2.3 抗干扰评价 低值和高值血清1,5-AG浓度基础样本重复10次测定,均值为7.1µg/mL和25.2µg/mL。当TG≤500 mg/dL、Bil≤50 mg/dL、Hb≤20 mg/dL、VitC≤50 mg/dL时,吡喃糖氧化酶法检测血清1,5-AG基本无干扰,见表2。
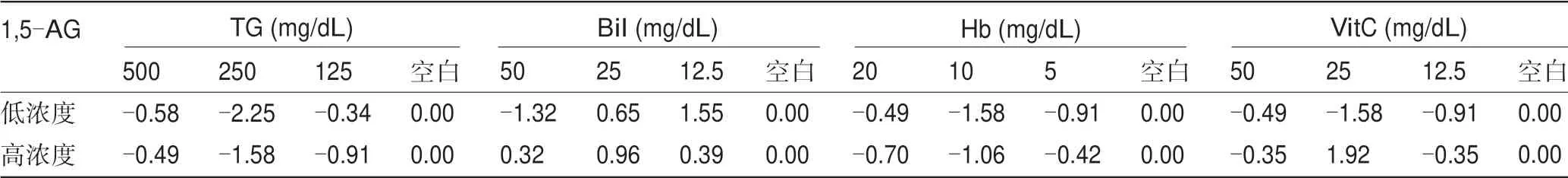
表2 吡喃糖氧化酶法检测血清1,5-AG干扰评价结果
2.4 AMR评价 8个系类浓度血清1,5-AG样本的重复测量结果的均值分别为49.82µg/mL、42.99µg/mL、35.99µg/mL、28.86µg/mL、21.71µg/mL、14.75µg/mL、7.23µg/mL、0.16µg/mL,重复测量误差变异系数<2.0%,小于设定的允许误差目标5%。以理论值为X轴,测定均值为Y轴,进行多项式回归分析,结果见表3。二次多项回归式中非线性系数b2(-3.391)具有显著性,三次回归中的非线性系数b2(0.090)、b3(-0.660)均不具显著性,二次多项式有较小的回归标准误,所以最合适多项式为二次,最佳拟合方程为二元一次多项式,则认为存在线性关系。本项目在0.16~49.82µg/mL的线性范围内,为临床可接受线性范围。
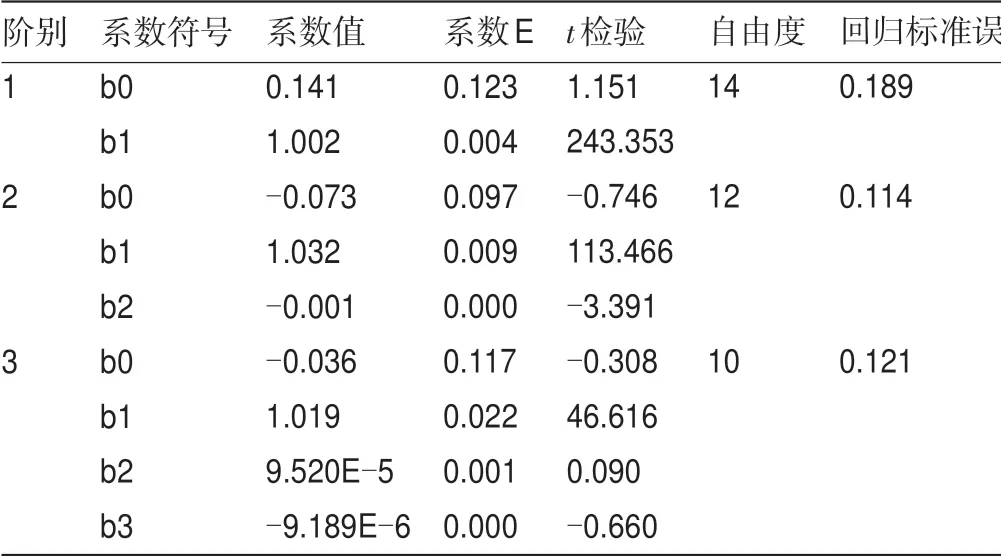
表3 吡喃糖氧化酶法检测血清1,5-AG多项式回归分析结果
2.5 CRR评价 标本经2~32倍稀释后,确定样本最大稀释倍数是32倍及确定稀释后的可靠低限是0.35µg/mL。回收率均落在90%~110%的最大稀释倍数值,故其可报告的临床范围为0.35~1 594.24µg/mL,可以满足临床的需求,见表4。
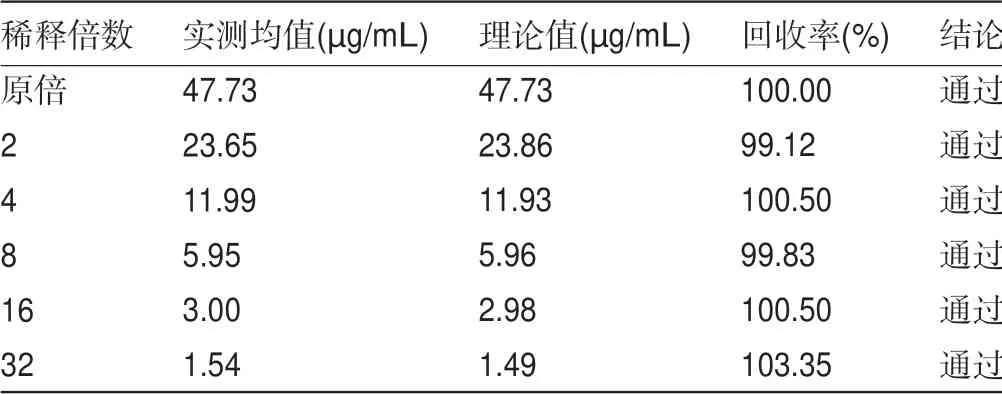
表4 吡喃糖氧化酶法检测血清1,5-AG稀释回收率测定结果
2.6 生物参考区间验证 20名健康个体血清1,5-AG浓度除了一个检测值(12.68µg/mL)低于商家提供的参考区间外,其余均在厂家提供的参考区间内。
3 讨论
血清1,5-AG作为一个新的糖尿病诊断指标,其刷查糖尿病的临床价值初露端倪,适于临床推广。1,5-AG测定方法有很多种,如质谱分析法、高效液相色谱法、微柱层析法等,这些方法虽然较灵敏,但是操作繁琐、费时、设备要求高。吡喃糖氧化酶法检测血清1,5-AG可在生化分析仪上实现全自动化操作,微量简单快速,符合临床检测的要求[4,9]。实验室在使用新的仪器设备或检测方法时,应对其方法学主要性能参数进行初步评估。结合本实验室具体实际,本研究评价国内常用生化分析仪德国西门子ADVIA2400采用吡喃糖氧化酶法检测血清1,5-AG的主要分析性能。
本研究参照EP5-A2文件,验证厂商声明的精密度性能。结果显示批内和批间的精密度均低于厂商的声明和基于生物学变异的精密度质量规范,说明吡喃糖氧化酶法检测血清1,5-AG重复性好、结果稳定,能够满足临床检测的要求。正确度验证采用北京九强公司提供另一个批号校准物,其校准物具有可靠的溯源性,结果显示相对偏倚分别为1.42%和1.27%,均小于基于生物学变异设定质量规范中的允许误差,正确度性能得到验证,说明吡喃糖氧化酶法检测血清1,5-AG正确度高可满足质量要求。抗干扰评估显示吡喃糖氧化酶法检测血清1,5-AG具有良好的抗脂血、黄疸和溶血等干扰能力。AMR验证对数据进行多项式回归分析,则认为血清1,5-AG浓度在0.16~49.82µg/mL范围内存在线性关系,该范围在厂家提供的范围内并且涵盖了临床医学决定水平。CRR范围为0.35~1 594.24µg/mL,最大稀释倍数为32倍,能够满足临床的要求。厂家提供的参考区间得到验证,说明该范围有效,适合本实验室所在地区。
综上所述,吡喃糖氧化酶法检测血清1,5-AG的各项性能均符合临床检测要求。目前1,5-AG在国内外未有标准参考方法和参考物质可供选择,其检测方法的标准化和质量评价没有建立统一的标准,各生产厂商试剂盒的检测标准各异,实验室间的结果差异仍将存在。1,5-AG的检测仍有其局限性和诸多方面需要更多的研究。1,5-AG作为近年来开始在临床逐步推广应用的新项目,本室将继续参考相关评价文件进行后续方法学和临床应用的研究,为实现1,5-AG标准化和一致性提供必要的基础。

