阿奇霉素固体分散体制备工艺研究*
王腾飞,张先华,王 丽
(1.重庆健能医药开发有限公司,重庆 401121; 2.重庆市公共卫生医疗救治中心,重庆 400036)
阿奇霉素(AZM)为大环内酯类抗生素,是第一个结构为氮杂内酯类的抗生素,是用化学方法在红霉素A内酯环上插入1个氮原子而衍生所得。阿奇霉素为结晶性粉末状,易溶于无水乙醇、丙酮、稀盐酸、甲醇等,一般呈类白色或白色,味苦,无臭[1-3]。阿奇霉素水溶性差,会影响其在体内的溶出和吸收,药理学研究发现,其生物利用率为37%[4]。为了提高其生物利用度,龙涛等[5]采用了超声乳化溶剂扩散法技术,廖九中等[6]研制了阿奇霉素的β-环糊精包合工艺,王建松等[7]制备了阿奇霉素脂质体,均在一定程度上提高了生物利用度。固体分散体技术是指将难溶性药物以无定形、微晶、分子、胶态等形式均匀分散在一种或多种载体物质中,形成高度分散体系的技术,常用来提高难溶性药物的溶解度和溶出度。固体分散体技术有很多优点,如可供选择的制备方法多样、载体类型多、增溶效果明显[8]。目前的制备方法主要有溶剂和熔融2种,前者的实际应用是喷雾干燥或冷冻干燥,后者的主要代表应用是热熔挤出技术[9-10]。本研究中考察了热熔挤出法及喷雾干燥技术制备阿奇霉素固体分散体,并与气流粉碎技术制备的样品从饱和溶解度、累积溶出度等方面进行比较。现报道如下。
1 仪器与试药
1.1 仪器
1260型高效液相色谱系统(美国Agilent科技有限公司);Mini-ME型热熔挤出仪(深圳市信宜特科技有限公司);ADL311S型喷雾干燥器(重庆雅马拓科技有限公司);YQ50型超音速气流粉碎机(上海赛山粉体机械制造有限公司);Bettersize2000型智能激光粒度仪(丹东百特仪器有限公司);D8 Advance型X射线衍射仪(美国布鲁克道尔顿公司);RC12AD型智能溶出试验仪(天津天大天发科技有限公司);DP30型单冲压片机(上海天凡制药机械制造厂)。
1.2 试药
阿奇霉素原料药(浙江永宁药业股份有限公司);阿奇霉素对照品(中国食品药品检定研究院,批号为130593-201303,纯度为94.5%);聚乙烯吡咯烷酮(ISP,K30),羟丙基纤维素(LF,亚什兰),羟丙甲纤维素(陶氏化学,E5);乙腈为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 制备方法
2.1.1 原料药微粉化处理
将阿奇霉素原料药置气流粉碎机中,调节工作压力为4~6 kg,调节加料压力为4~5 kg,加料速度为155~165 V,粉碎压力为3.5~4.5 kg,进行粉碎,作为与固体分散体的对照样品。
2.1.2 固体分散体制备
热熔挤出法:分别以羟丙纤维素(LF)、聚乙烯吡咯烷酮(K30)和羟丙甲纤维素(E5)为载体,称取混合好的阿奇霉素-载体不同比例的物理混合物适量。投于热熔挤出仪的料斗内,设定热熔温度为140~180℃,挤出转速为20~50 r/min进行热熔挤出,得到的条状挤出物,经研磨粉碎后过筛,即得阿奇霉素-载体固体分散体,备用。
喷雾干燥法:分别称取羟丙纤维素(LF)、聚乙烯吡咯烷酮(K30)和羟丙甲纤维素(E5)为载体,并将载体和原料依次溶于50%乙醇溶液中。设置喷雾干燥器的进风温度为130℃、风量为0.5 m3/min、供液频率为10 Hz和雾化压力为0.05 MPa,待进风温度上升至120℃左右开始喷液,物料温度全程控制在55~65℃;喷液完成后,关闭供液3~5 min,依次关闭进风温度、物化压力及风量,收集固体分散体,备用。
2.1.3 片剂制备
按以上2种方法制备的固体分散体,通过饱和溶解度选择较优的载体和适当比例,分别按相同处方和工艺制备普通口服片剂;同时按2.1项下选择气流粉碎后的原料药,制备成品。3种样品通过体外累积溶出度进行比较。片剂处方及主要工艺描述见表1,其中2种固体分散体处方一致;使用气流粉碎后的原料制备样品,使用乳糖代替载体用量。片剂制备工艺为粉末直接压片工艺:将各原辅料混合均匀,使用12 mm圆形冲压片,片重控制为500 mg,压片硬度为7~12 kgf。
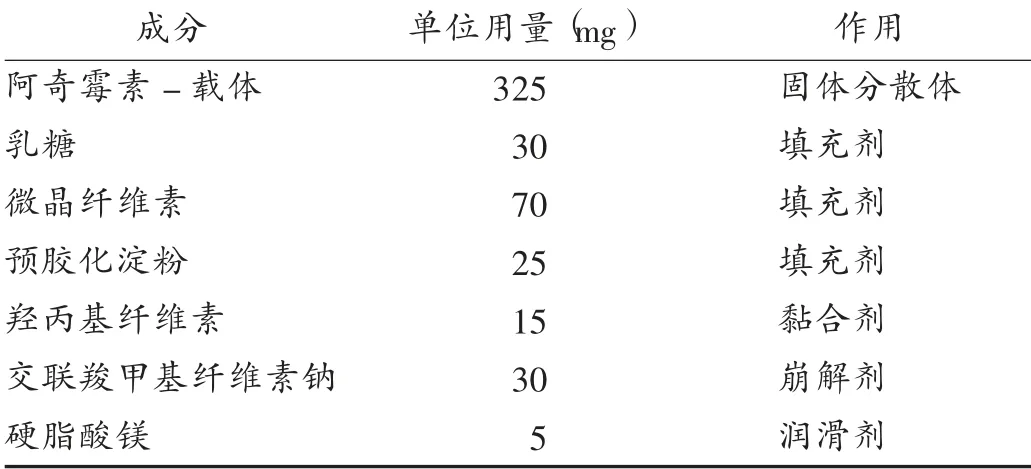
表1 片剂处方成分用量及主要作用
2.2 工艺评价
2.2.1 粒径检测
介质和样品折射率分别为1.400和1.636。向样品槽加入约500 mL饱和氯化钠水溶液,开泵,泵速为2 000 r/min,待系统稳定后,对光并测量背景。取本品适量,加入30 mL分散剂中,超声搅拌,使其分散均匀,缓缓均匀地加入样品槽,至遮光度为10%~20%,连续测量3次,取平均值。取热熔挤出及喷雾干燥技术制备的固体分散体的最优处方分别进行粒径检测,即热熔挤出制备的阿奇霉素-羟丙纤维素(1∶0.5)及喷雾干燥制备的阿奇霉素-羟丙纤维素(1∶0.5)固体分散体,粒径见表2。可见,喷雾干燥制备的固体分散体粒径较小,可达到与气流粉碎基本一致的粒径。热熔挤出制备的固体分散体再次粉碎后粒径较大。

表2 固体分散体粒径(μm)
2.2.2 含量测定
色谱条件:色谱柱为Agilent HC-C18柱(250 mm×4.6 mm,5μm);流动相为磷酸盐缓冲液(取0.05 mol/L磷酸氢二钾溶液,用20%磷酸溶液调节pH至8.2)-乙腈(45∶55,V/V);检测波长为210 nm;柱温为30℃;流速为1.0 mL/min;进样量为50μL。取本品适量,加乙腈溶解并定量稀释成每1 mL中约含0.2 mg的溶液,作为供试品溶液。精密量取50μL,注入液相色谱仪,记录色谱图(见图1)。另取阿奇霉素对照品适量,同法测定,按外标法以峰面积计算含量。
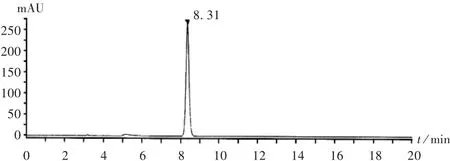
图1 高效液相色谱图
2.2.3 饱和溶解度测定
取阿奇霉素原料药、阿奇霉素-载体固体分散体适量,以水为溶剂,于37℃恒温水浴中搅拌,制成过饱和溶液,用0.45μm水系滤膜过滤,取续滤液作为样品溶液,经适当稀释后照含量检测方法测定其饱和溶解度。结果见表2和表3。通过饱和溶解度检测,经气流粉碎后,不同粒径的原料饱和溶解度变化趋势较小,说明该气流粉碎对此晶型无影响,在晶型一致的情况下,饱和溶解度不会发生变化;相较于气流粉碎的原料药,热熔挤出法和喷雾干燥法制备的固体分散体饱和溶解度显著提高,相较于气流粉碎的原料药提高了约10倍,且喷雾干燥工艺制备的固体分散体溶解性整体优于热熔挤出工艺。
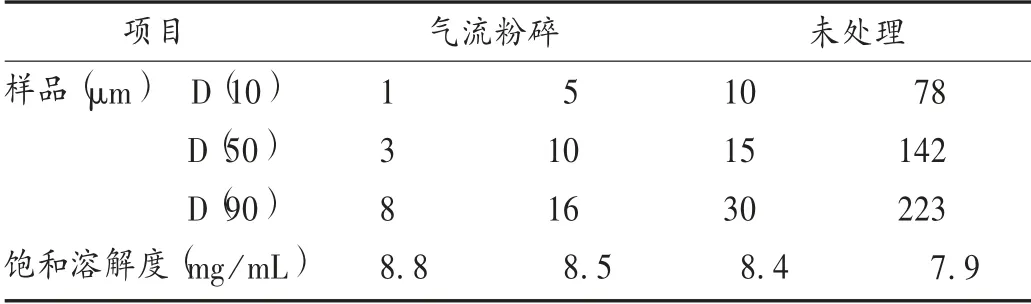
表2 原料药饱和溶解度

表3 制备方法不同载体及不同比例固体分散体饱和溶解度(mg/mL)
2.2.4 体外累积溶出度测定
阿奇霉素在酸性溶液中较易溶解,随着pH的升高,溶解度降低很快;在水中难溶[11]。为了使溶出条件更具区分力,选择水作为溶出介质。将3种口服片剂分别进行溶出度试验。参照2015年版《中国药典(四部)》通则第二法,转速为50 r/min,温度为(37±0.5)℃,在5,10,15,30,45,60,120,180 min时间点分别取样,并补充同温度下等体积的溶出介质。取气流粉碎处理的原料药、热熔挤出及喷雾干燥技术制备的固体分散体的最优处方分别进行口服片剂的制备。片剂累积溶出度结果见表4和图2。可见,喷雾干燥法制成片剂后累积溶出度较高,与前者饱和溶解度的趋势一致。
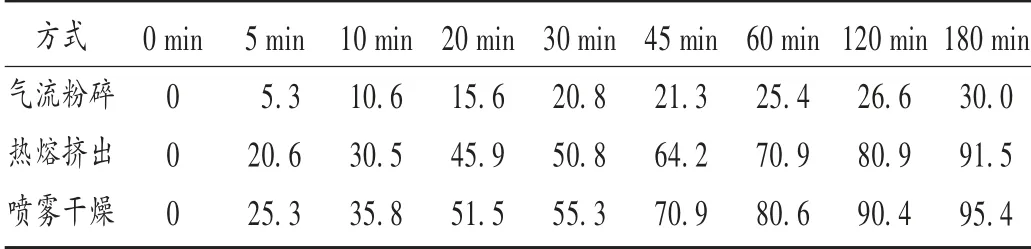
表4 不同成品不同时间体外累积溶出度比较(%)
2.2.5 晶型分析(X射线衍射法)
CuKa靶石墨单色器衍射束单色比,管压40 kV,管流30 mA,扫描2θ角度5°~50°。以4°/min扫描速率对阿奇霉素固体分散体进行粉末X射线衍射扫描。通过饱和溶解度及成品的累积溶出度可见,喷雾干燥法制备的阿奇霉素-羟丙纤维素(1∶0.5)固体分散体质量最优,故将初始原料药和该固体分散体进行粉末X射线衍射分析。结果见图2。可见,初始原料药有明显的晶型特征峰,固体分散体已无原料药的晶型特征峰,表明固体分散体中阿奇霉素已转变成无定形态。
3 讨论
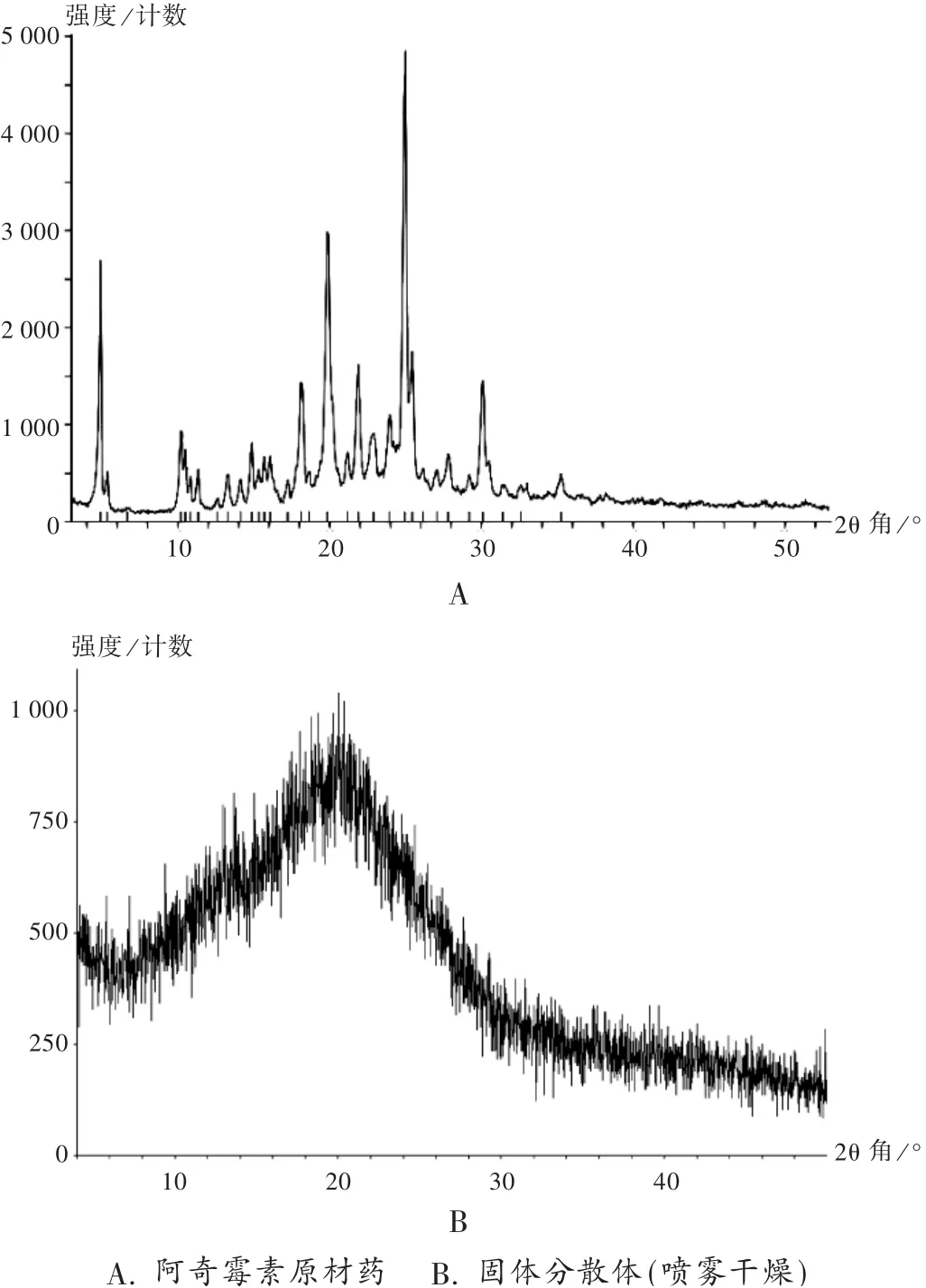
图2 X射线衍射图
热熔挤出法和喷雾干燥法制备阿奇霉素分散体均可大幅度提高原料的饱和溶解度和片剂的累积溶出度。2种工艺制备的固体分散体均能增加物料的亲水性,同时喷雾干燥制备的固体分散体工艺较热熔挤出简单,无需再进行粉碎处理,该工艺更符合商业化生产。
喷雾干燥工艺制备的固体分散体优于热熔挤出工艺。由粒径分布可见,前者的粒径较小,这可能与喷雾干燥过程中物料的高度分散化有关,同时形成的固体分散体脆性较小;后者经热熔挤出后,固体分散体存在老化现象,且制备过程原料均匀性较差。粉末衍射图谱显示,喷雾干燥制备的固体分散体中阿奇霉素已转变成无定形态。采用喷雾干燥工艺制备固体分散体,原料药和载体溶解在溶剂中后能形成均一分散体系,并极度分散,其分散程度大于热熔挤出工艺;喷雾干燥形成的固体分散体疏松多孔,比表面积大,亲水性也增大,提高了原料药的饱和溶解度,同时溶出时固体分散体能快速均匀地分散在溶出介质中。
基于喷雾干燥法制备阿奇霉素的固体分散体可提高溶出度,后续研究应继续对该固体分散体的工艺参数进行优化,同时考察固体分散体的稳定性,并进行体内药物代谢动力学研究。

