N-乙酰半胱氨酸的快速卫生技术评估*
李少强,赵紫楠,王其琼,李可欣,薛 薇,胡 欣△
(1.北京医院药学部·国家老年医学中心·药物临床风险与个体化应用评价北京市重点实验室·北京医院临床试验研究中心,北京 100730; 2.北京大学药学院药事管理与临床药学系,北京 100083)
慢性阻塞性肺疾病(COPD)是一种以持续气流受限为特征的可预防和治疗的常见疾病,气流受限多呈进行性发展,与气道和肺对有毒颗粒或气体的慢性炎性反应增强有关[1]。COPD的发病机制与肺部炎性反应、氧化应激、蛋白酶和抗蛋白酶失衡有关,氧化应激可能是COPD重要的炎症放大机制[2]。慢性支气管炎是指除外慢性咳嗽的其他已知病因后,患者每年咳嗽、咳痰3个月以上,并连续2年以上者,吸烟、感染、环境等均是重要的影响因素,其发病机制不仅受肺部炎症影响,还与氧化/抗氧化系统的失衡相关[3]。特发性肺纤维化(IPF)是指原因不明并以普通型间质性肺炎为特征病理性改变的慢性炎症性间质性肺部疾病,主要表现为弥漫性肺泡炎、肺泡单位结构紊乱和肺纤维化[4]。IPF患者肺泡灌洗液中的抗氧化剂如谷胱甘肽显著低于正常值[5]。
N-乙酰半胱氨酸(NAC)属体内氧自由基清除剂,为还原型谷胱甘肽(GSH)的前体,其分子中所含的巯基(—SH)可使痰液中糖蛋白多肽链的二硫键(—S—S—)断裂,且可通过分解核糖核酸酶,使脓性痰液中的DNA纤维断裂,不仅可溶解白色黏痰,还可溶解脓性痰。N-乙酰半胱氨酸在《慢性阻塞性肺疾病基层诊疗指南》中推荐用于化痰和抗氧化治疗。其最早在1994于美国上市,美国及欧盟目前剂型有泡腾片、颗粒剂、吸入溶液剂及注射剂4种,国外主流口服剂型为泡腾片,无普通片剂。1997年其在中国上市,现有泡腾片、普通片剂、颗粒剂、胶囊、吸入溶液、注射剂多种剂型。由于其自身的结构影响,NAC原料药呈酸性(pH约为2),使用时可能会对有胃溃疡病史的患者产生刺激。外加制剂类型如泡腾片因添加碱性发泡剂碳酸氢钠,调整其pH,解决了强酸对胃黏膜的刺激,相对片剂和胶囊而言,具有更好的稳定性和更低的不良反应发生率。作为COPD等慢性疾病长期用药,更需兼顾安全性及依从性,这可能也是国际上选择泡腾片作为主流口服剂型的原因。雷霆等[6]的研究显示,NAC可显著改善COPD患者肺功能第1秒用力呼吸容积(FEV1)水平,而也有研究表明[7],NAC并不能改善FEV1及其恶化的速度。
卫生技术评估(HTA)是指对卫生技术的内容、效果和(或)影响的系统性评价,是对卫生干预措施或卫生技术的社会、经济、组织和伦理问题的多学科交叉评价,主要目的是为政策决策提供建议。快速卫生技术评估作为一种快速决策工具,通过简化卫生技术评估/系统评价方法和流程,快速评估药物的有效性、安全性和经济性。基于目前NAC研究相互矛盾的结果,本研究中对NAC治疗COPD、慢性支气管炎和IPF的安全性,有效性和经济性开展快速卫生技术评估,以期为临床提供循证医学证据。现报道如下。
1 资料与方法
1.1 文献纳入与排除标准
纳入标准:研究对象均诊断为COPD、慢性支气管炎或IPF;干预措施为,干预组患者在服用NAC(600 mg,每日1次;1 200 mg,每日1次;1 800 mg,每日1次)的同时接受相应的常规治疗,对照组患者仅接受常规治疗或加用安慰剂;结局指标为临床症状改善率;急性加重频率;肺功能[动脉血气氧分压(PaO2)、动脉血气二氧化碳 分 压(PaCO2)、FEV1、肺 活 量(VC),用 力 肺 活 量(FVC)、一氧化碳弥散量(DLco)];研究类型为HTA报告、系统评价(SR)/Meta分析、经济学评价;来自各个国家或地区的研究者发表的NAC的经济学研究。
排除标准:会议摘要。
1.2 检索策略
计算机检索PubMed,Embase,the Cochrane Library,Web of Science等英文数据库,CNKI、万方和维普等中文数据库,同时检索国内外HTA机构官方网站及相关数据库。为全面获取有关研究,只用“乙酰半胱氨酸”“NAcetylcysteine”作为关键词进行全文检索或主题检索。检索时限均从建库至2019年5月;同时,手工检索纳入研究的参考文献列表。
1.3 文献资料提取和质量评价
由2位评价者独立筛选文献并提取资料和数据,共同决定纳入的文献,如遇分歧通过讨论或咨询第3位评价者解决。按预先设计的资料提取表提取资料和数据,内容包括纳入研究的基本特征及研究结果,如检索时间、纳入人群、样本量、干预措施、结局指标和结论等。评价研究质量时,对HTA报告采用国际卫生技术评估组织协会(INAHTA)制订的HTA检查表;对SR/Meta分析采用多系统评价评估问卷(AMSTAR)量表;对经济学研究采用卫生经济学评价报告标准共识(CHEERS)量表。
1.4 证据的合成和分析
由于本研究为快速卫生技术评估,方法学上对纳入的HTA报告和SR/Meta分析这类二次研究及经济学研究进行描述性的评价和分析。在定性描述时主要呈现纳入研究的研究目的、主要研究方法,主要研究结果和研究结论。若现有研究不能覆盖此次评估的问题,则考虑进一步开展SR/Meta分析。
2 结果
2.1 文献检索结果
对数据库检索共纳入文献1 032篇,除重后阅读文献标题和摘要进行初筛,初筛得到795篇文献。进一步获取全文进行复筛,最终纳入20篇文献,其中系统评价/Meta分析17篇,经济学研究3篇。文献筛选流程及结果见图1。
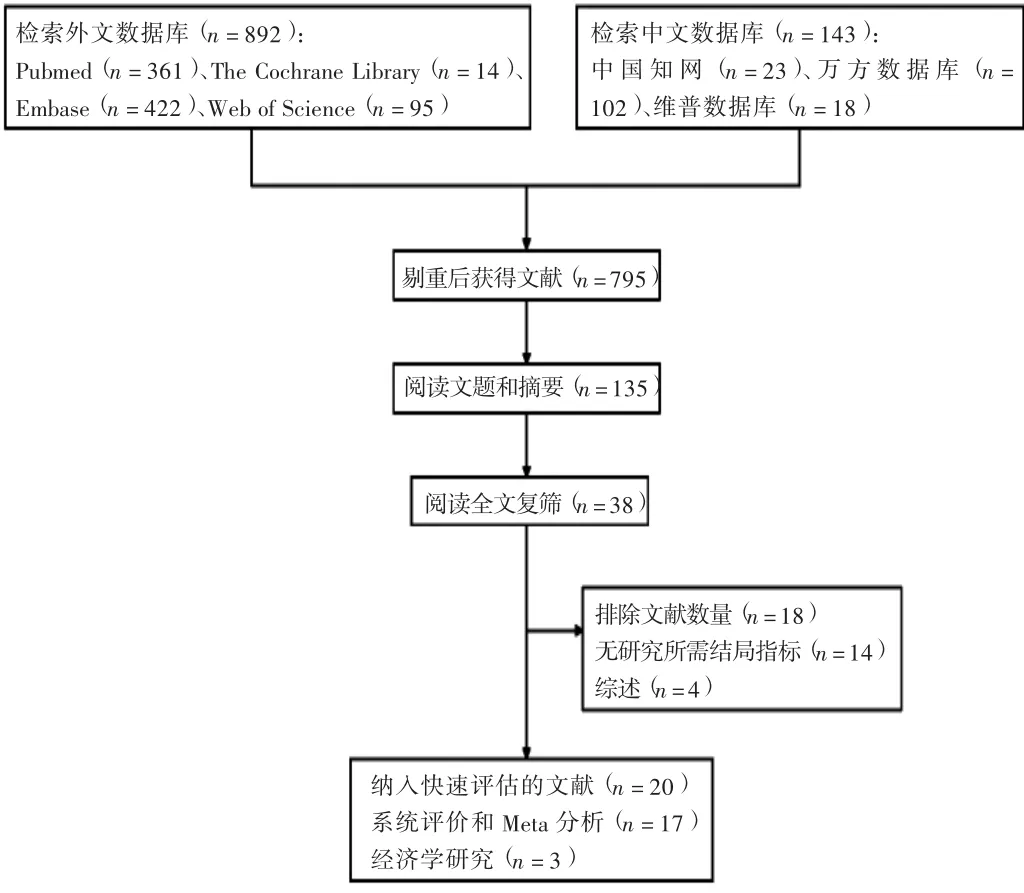
图1 快速HTA分析文献筛选流程及结果
2.2 纳入文献的基本特征及其质量评价
所有研究的基本特征见表1和表2。文献总体质量良好。
2.3 有效性评价
2.3.1 IPF
临床症状改善率:3篇Meta分析[18,20-21]显示,与联用安慰剂相比,激素如泼尼松、环磷酰胺等联用NAC时可显著提高临床症状改善率。
DLco:3篇Meta分析[18-19,21]显示,NAC与安慰剂相比,激素联用NAC和吡非尼酮联用NAC均存在显著差异;其中1篇[22]显示,联用NAC与联用其他类药物相比无显著差异。

表1 纳入Meta分析研究的基本特征

表2 纳入经济学研究的基本特征
VC:3篇Meta分析[18-19,22]显示,治疗后NAC组IPF患者VC高于对照组,其差异有统计学意义。
2.3.2 COPD与慢性支气管炎
临床症状改善率:5篇Meta分析[6,10,14,16-17]显示,与联用安慰剂相比,β受体激动剂、激素及氨溴索、孟鲁司特等联用NAC时可显著提高临床症状改善率。
急性加重频率:7篇Meta分析[8,11-13,15-17]显示,治疗后NAC组COPD患者急性加重频率低于对照组,且差异有统计学意义(P<0.05)。
FEV1:4篇Meta分析[3,6,10,14]显示,NAC与安慰剂相比,NAC可显著改善FEV1水平;另有4篇[9,11-13]显示,联用NAC与联用安慰剂相比无显著差异。
PaCO2:1篇Meta分析[8]显示,NAC与安慰剂相比,NAC可显著改善PaCO2水平;另有1篇[14]显示,联用NAC与联用安慰剂相比无显著差异。
PaO2:2篇Meta分析[8,10]显示,NAC与安慰剂相比,NAC可显著改善PaO2水平;另有1篇[14]显示,联用NAC与联用安慰剂相比无显著差异。
FVC:2篇Meta分析[3,10]显示,NAC与安慰剂相比,NAC可显著改善PaO2水平;另有2篇[11,13]显示,联用NAC与联用安慰剂相比无显著差异。
2.4 安全性评价
NAC常见的不良反应为胃肠紊乱、皮肤病、口干、关节疼痛。纳入的20篇文献均未显示出NAC和对照组存在显著性差异。针对泡腾片是否会比其他剂型对胃部刺激更强或不良反应更多,尚未检索到相关的SR/Meta分析。《欧洲药典》通则中已明确阐明口服片剂可代指泡腾片[25]。暂可认为NAC的泡腾片不良反应治疗时与常规剂型相比无明显差异。NAC有很好的耐受性,且其不良反应无剂量依赖性[17]。
2.5 经济性评价
GRANDJEANA等[24]的研究表明,NAC在冬季使用能显著降低慢性支气管炎发作的例数、降低患病天数和住院率。直接成本:未NAC的为869瑞士法郎,NAC的为700瑞士法郎;间接成本:未NAC的为1 324瑞士法郎,NAC的为779瑞士法郎。有报道指出,600 mg NAC每日1次,对于肺功能FEV1及VC无明显改善,但使用1 200 mg或1 800 mg NAC后可能会减少肺气肿的发生,从而改善生活质量,减少医疗成本[7,23]。NAC长期使用是获益的。SUN等[26]发现静脉注射或肠内注射可能比口服给药成本效益更佳。
3 讨论
由于本研究为快速HTA,对纳入的研究仅作定性分析,且纳入的文献数量较少,结果具有一定的局限性。有条件时仍需系统检索随机对照研究进行Meta分析对乙酰半胱氨酸进行全面的卫生技术评估。
分析上述结论所产生的差异。首先,由于文献质量参差不齐,导致得出的结论有一定误差;其次,纳入文献给予NAC的剂量有差别,分600 mg每日1次和1 200 mg每日1次不等,纳入文献中的低剂量为≤600 mg,大剂量为≥600 mg;再次,由于观察时限的差异导致结果的出入,雷霆等[6]纳入的研究观察时限只有15 d,而SHEN等[12]纳入的研究时间为4个月至3年,2项研究最后针对NAC的使用是否能显著改善FEV1的水平有差异。
对于不同的给药剂量,6篇Meta分析[8,11-13,15,17]显示,高剂量对于急性加重率的控制和临床症状缓解率的改善都强于低剂量组,且NAC的不良反应无剂量依赖性。故针对COPD可使用1 200 mg每日1次进行治疗与维持,对于慢性支气管炎可以给予NAC 600 mg[17]。
综上所述,根据本研究的评估,NAC具有良好的有效性,虽然胃肠道不良反应发生率较高,但仍认为具有较好的安全性,在我国应用具有良好的经济性。

