甲襞微循环检查在抗着丝点抗体阳性原发性干燥综合征的临床价值
俞秋霞,刘伟丽,王晓东,施清怡,丁健,张瑾
原发性干燥综合征(primary Sjögren’s syndrome, pSS)是一种主要累及外分泌腺体的自身免疫性疾病。抗干燥综合征A抗体(抗SSA抗体)和抗干燥综合征B抗体(抗SSB抗体)是诊断pSS的重要血清标志物[1-3]。研究发现,部分pSS患者抗SSA/SSB阴性而抗着丝点抗体(anticentromere antibodies, ACA)阳性[4-7],使其成为pSS的独特亚组。
甲襞微循环(nailfold videocapillaroscopy, NVC)检查近年来已被广泛地应用于结缔组织病的诊断与随访。NVC异常已被纳入2013年系统性硬化症(systemic sclerosis,SSc)分类标准[8],但其在pSS患者等其他自身免疫性疾病中的作用及特征性表现却鲜被关注。本研究拟探讨NVC在pSS患者,尤其是ACA阳性pSS患者的特点及临床意义。
1 对象与方法
1.1 研究对象
收集本院2016年7月至2019年7月pSS患者53例,所有患者均行唇腺活检,诊断符合2002年pSS国际分类标准[2]。其中ACA阳性组患者22例,来自风湿科门诊及住院的所有初诊患者;ACA阴性组患者31例,来自于第一作者及通信作者门诊的初诊患者。ACA阳性组除外SSc[8]。入组患者均除外高血压、糖尿病、慢性肾脏病,均无吸烟史。所有患者均行NVC检查。
1.2 NVC检查方法
患者在室温20~25 ℃下,安静休息10~20 min,坐位,左手放置与心脏同一水平,均取左手环指进行检查。采用甲襞微循环镜(江苏徐州同人医疗电子科技有限公司, 型号: TR-8000)进行检查(低倍镜扩大20倍,高倍镜扩大50倍),拍摄典型图片,并录制图像,记录包括管袢数目、管袢直径(包括输入袢直径、输出袢直径、袢顶直径)、管袢长度、管袢畸形比例、血色、袢周渗出、出血等16项观测指标。其中(1)管袢数目:正常毛细血管管袢数量7~9条/mm。若每5毫米视野下毛细血管管袢数量少于30条(即<6条/mm)定义为“毛细血管袢缺失”,这是SSc的特征性NVC改变之一[9]。(2)管袢直径:输入袢管径正常值为 9~13 μm,输出袢管径正常值为11~17 μm,袢顶直径正常值为12~18 μm。(3)巨大毛细血管袢:毛细血管管径>50 μm。巨大毛细血管袢的出现也是SSc的另一特征性NVC表现[9]。(4)管袢长度:正常管袢长度为150~250 μm。(5)管袢形态分为交叉和畸形2项:交叉管袢数正常值应<30%,畸形管袢数正常值应<10%。(6)袢周包括渗出、出血、乳头下静脉丛、皮下乳头和汗腺导管等指标。(7)出血:毛细血管附近出现点状或斑片状含铁血黄素沉积。出血并不是SSc的特有表现,也可出现在其他结缔组织病中[9]。
积分采用“田牛加权积分法”[10]:观察1 mm线性长度内毛细血管改变:0分:未观察到毛细血管异常改变;1分:上述观测指标出现异常改变<33%;2分:上述观测指标出现异常改变33%~66%;3分:上述观测指标出现异常改变>66%。所有入组患者的NVC由第一作者独立完成,并由通信作者质控核实。
1.3 血清学及影像学检查
抗核抗体、抗SSA/SSB抗体、ACA采用间接免疫荧光法(欧蒙公司试剂盒)。肺间质纤维化依据肺部高分辨CT(HRCT)确定,以肺一氧化碳弥散量(diffusion capacity for carbon monoxide of lung,DLCO)<80%作为弥散功能下降。肺动脉高压通过彩色多普勒超声心动图,采用肺动脉收缩压(pulmonary artery systolic pressure, PASP)≥40 mm Hg作为临界值。
1.4 统计学处理
2 结果
2.1 一般资料与临床资料
两组患者性别、口干、眼干、猖獗龋齿、干燥性角膜炎、唇腺活检阳性率无显著统计学差异,但ACA阳性组患者发病年龄较ACA阴性组更大,差异具有统计学意义(P<0.05)(表1)。
两组患者手指肿胀、乏力、胃食管反流、毛细血管扩张、肺间质纤维化、用力肺活量(forced vital capacity, FVC)占预计值百分比、一秒用力呼气容积(forced expiratory volume in one second, FEV1)/用力呼气量(forced vital capacity,FVC)比较无显著差异;但ACA阳性组患者更易出现雷诺现象,且更易出现肺功能DLCO下降及PASP升高(P<0.05)(表2)。
22例ACA阳性组中,抗SSA抗体阳性3例,抗SSB抗体0例;31例ACA阴性组中,抗SSA抗体阳性31例,抗SSB抗体13例(表1)。
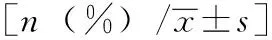
表1 两组患者一般资料比较Table 1 Demographic and general clinical characteristics according to the presence of ACA in patients
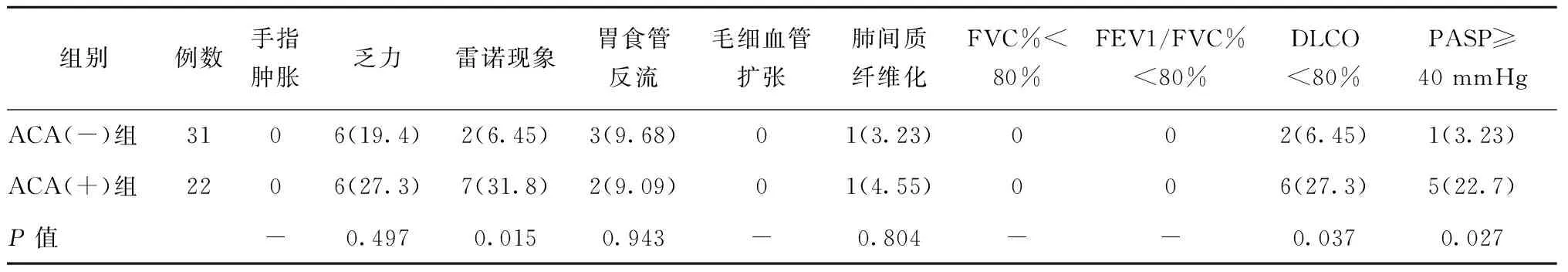
表2 两组患者临床资料比较[n(%)]Table 2 Clinical characteristics according to the presence of ACA in patients with pSS[n(%)]
2.2 NVC特点
毛细血管管袢数目上两组差异无统计学意义。其中,两组各有1例患者出现毛细血管袢数<6条/mm的“SSc样”NVC改变(表3)。但ACA阳性组此例患者临床上无雷诺现象、肿胀指、皮肤硬化、毛细血管扩张等表现,因此诊断不符合2013年SSc分类标准。
ACA阳性组毛细血管管袢直径(输入袢管径、输出袢管径、袢顶管径)分别较ACA阴性组增宽(P≤0.001)。ACA阳性组甲襞袢周渗出比例及出血管袢数比例均高于ACA阴性组(P<0.05)。两组患者的畸形管袢数比例与血色呈暗红的比例,差异无统计学意义(P均>0.05)。同时,两组患者均未见巨大毛细血管袢的“SSc样”NVC改变(表3)。
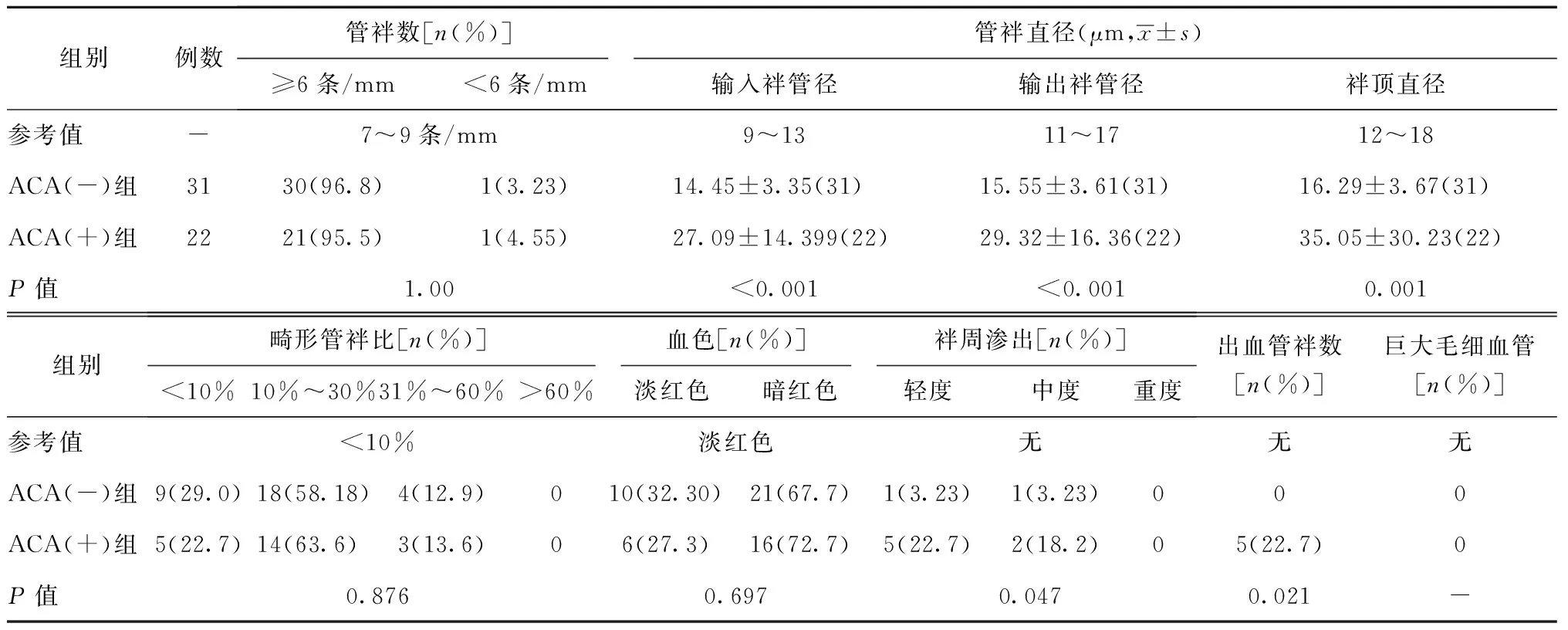
表3 两组患者NVC结果比较Table 3 NVC parameters according to the presence of ACA in patients with pSS
两组患者的甲襞血管形态、血液流态、以及乳头下静脉丛等指标比较,差异无统计学意义(P均>0.05)。
2.3 NVC指标的临床相关性
将两组患者的甲襞管袢数、管袢直径(输入袢管径、输出袢管径、袢顶直径)、袢周渗出、管袢出血与病程、出现雷诺现象、DLCO<80%及PSAP≥40 mmHg进行相关性分析显示:管袢数量与疾病病程、雷诺现象、DLCO<80%、PASP≥40 mmHg 无显著相关;管袢直径(输入袢管径、输出袢管径、袢顶直径)、袢周渗出、管袢出血与病程、出现雷诺现象、PASP≥40 mmHg呈正相关,与DLCO<80%呈负相关,差异均具有统计学意义(P均<0.01)(表4)。
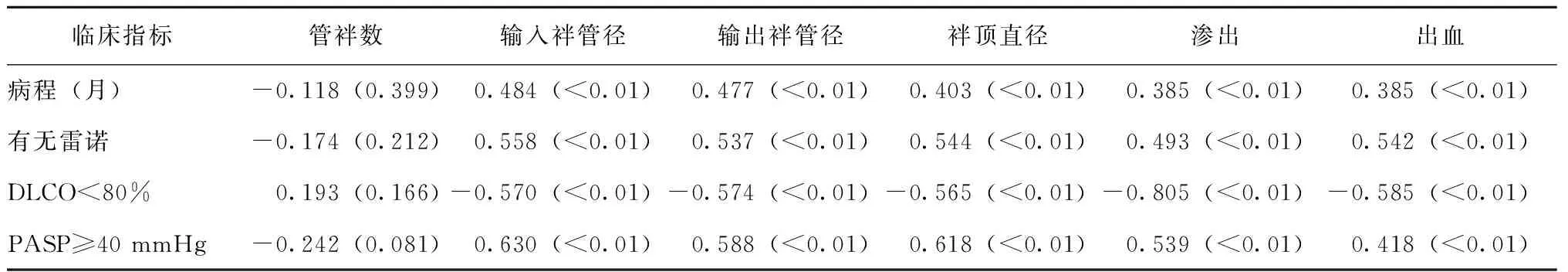
表4 NVC指标与临床指标的关系[r(P)]Table 4 Relationship of NVC parameters and clinical features in patients with pSS[r(P)]
3 讨论
ACA自发现以来,长期被认为是SSc尤其是CREST综合征(即钙质沉积、雷诺现象、食管运动功能障碍、指端硬化、毛细血管扩张)的特异性抗体[11]。近年来国内外研究指出,ACA也是一种与pSS相关的抗体[12-13]。与传统抗SSA /抗SSB阳性pSS患者相比,ACA阳性pSS患者虽在口眼干燥症及唇腺活检组织学等并无明显差别,但更容易出现雷诺现象、肝功能异常及吞咽困难[7,13]。本研究通过对53例pSS患者分析发现,ACA阳性组与阴性组比较,口眼干、猖獗龋齿及唇腺活检阳性率上无显著差异,但雷诺现象发生率显著增加,与文献报道基本一致。
已有研究证实,在SSc患者中ACA阳性者更容易出现肺脏受累,并认为ACA阳性与肺功能下降(如用力肺活量FVC及DLCO)显著相关,ACA是SS肺间质纤维化及肺动脉高压的危险因素[14-16]。本研究发现,ACA阳性pSS患者更容易出现DLCO下降及PASP升高,提示ACA可能也与pSS脏器受累相关。
NVC已广泛应用于SSc的诊断及预后随访,巨大毛细血管袢和/或毛细血管袢缺失被认为是SSc的特征性NVC表现[8]。NVC严重改变的SSc患者更容易出现肢端溃疡、食道受累,且易出现肺功能DLCO下降及PASP升高[17-21]。同时,NVC越来越广泛应用于其他结缔组织病的评估[22]。研究证实,轻度毛细血管扩张、管袢数量减少以及出血并不是SSc的特有表现,亦可出现在其他结缔组织病中[8-9]。2016年,Corominas等[23]对150例pSS患者进行NVC检查发现,伴有雷诺现象的pSS患者更易出现甲周毛细血管扩张。本研究发现,与传统pSS患者相比,ACA阳性pSS患者更易出现管袢轻度扩张及不同程度渗出与出血等“非特异性SSc样”NVC改变,提示ACA阳性pSS可能存在更明显的微循环障碍,NVC可作为ACA阳性pSS患者评价微血管病的重要手段。
早在1999年,Tektonidou等[24]即提出:ACA阳性且伴有雷诺现象的pSS患者可出现巨大毛细血管袢等“SSc样”NVC改变,且逐渐出现局限性硬皮病的临床特征,少数病例最终可演变为局限性硬皮病。因此,此类患者即使尚无SSc临床表现或未满足SSc分类标准,仍需密切随访至少10年。另外文献报道,ACA阳性pSS患者的NVC易出现管袢数量减少、毛细血管扩张甚至出现巨大毛细血管袢,考虑与长期雷诺现象密切相关[25-26]。但是本研究中:两组患者虽均未出现巨大毛细血管袢,在毛细血管袢数目上差异也无统计学意义,而以“非特异性SSc样”NVC改变为主。这种“非特异性SSc样”的NVC改变考虑为微血管病变的早期表现,随着病程的进展,管袢的扩张可能不断加重,尤其在ACA阳性pSS患者中,是否出现“巨大毛细血管袢”等“SSc样”NVC改变,值得进一步的随访与观察。值得一提的是,两组各有1例患者出现毛细血管袢缺失的“SSc样”NVC改变,既无统计学差异,也不符合SSc诊断,且均年龄较大(60岁以上),不排除动脉粥样硬化等其他血管因素所致。但是随着病程的进展,在ACA阳性pSS患者中是否出现进行性的“毛细血管袢缺失”,有待长期随访及扩大样本量。
同时,本研究还发现两组患者的NVC参数中,管袢直径(输入袢管径、输出袢管径、袢顶直径)、渗出与出血的异常程度与病程、出现雷诺现象、DLCO下降及PASP升高显著相关,这证实NVC在pSS病情评估中的临床价值。雷诺现象的本质是微血管病变,DLCO与肺部血管病变紧密相连,PASP升高也是由于血管阻力增加引起的并发症。而甲襞毛细血管袢增粗正是组织缺血缺氧后血管代偿性调节的反映。随着疾病的进展,缺血/再灌注损伤导致微血管通透性增加,管袢渗出与出血是毛细血管壁完整性破坏的体现。
综上所述,ACA阳性pSS是pSS的一种特殊亚型,其发病年龄更晚,更易出现雷诺现象,DLCO下降及PASP升高,且其“非特异性SSc样”NVC改变的程度显著高于传统抗SSA/抗SSB阳性的pSS患者。同时,NVC可作为一项有效的临床工具,有利于对pSS患者进行病情严重性与预后评估。 ACA阳性pSS患者如果出现NVC异常,更应积极干预及早期治疗,密切随访评估脏器受累情况,警惕其转变为SSc的可能。当然,本研究仍然存在若干不足之处,首先这是1项包含少量数据的单中心研究,因此某些结论可能并不适用于所有医疗机构;同时,本研究样本量较小,随访时间尚短,仍存在不足,有待进一步扩大样本量及随访。

