MgO NPs及其析出的Mg2+对细叶蜈蚣草(Egeria najas)光合作用的影响
郑博文,徐长山,何惠敏,程亮,郭佳昕,刘晓男
东北师范大学紫外光发射材料与技术教育部重点实验室,长春130024
纳米材料因其特殊的理化性质而在医学、化学纤维、电子工业和催化等许多领域具有重要的应用价值[1-3]。随着纳米材料进入生态系统的几率大大增加,其生物安全性也越来越引起人们的重视。金属氧化物纳米粒子作为纳米材料中重要的一种,在现代生活中发挥着不可或缺的作用,其生物安全性的研究也同样倍受关注。氧化镁纳米粒子(MgO NPs)由于其比表面积大、表面活性高和吸附性强等优点,可用作催化剂催化裂解生物质材料,包括草本植物、藻类及有机废弃物[4]。MgO NPs拥有强抗菌能力,对葡萄球菌和大肠杆菌等表现出完美的抗菌杀菌效果[5]。MgO NPs吸波效果好、抗冲击能力强,被认为是良好的吸波材料[6]和陶瓷材料[7]。目前,已有关于MgO NPs毒性研究的报道。Ghobadian等[8]报道了高剂量MgO NPs对斑马鱼胚胎孵化有显著抑制作用,Ali等[9]在研究中发现,MgO NPs对淡水壳菜有毒性效应。
笔者研究MgO NPs对水生植物细叶蜈蚣草(Egerianajas)光合作用的影响。细叶蜈蚣草是属于水蟹科蜈蚣草属的沉水植物,具有净化水质的作用,是水生态系统重要初级生产者。因此,研究MgO NPs对细叶蜈蚣草的影响具有很重要的意义。细叶蜈蚣草的光合作用过程采用叶绿素a荧光检测法进行测量。叶绿素荧光现象是叶绿素分子吸收光能后,处于激发态的叶绿素分子通过跃迁又恢复到稳定态的过程中产生的发光现象。叶绿素a荧光检测通过测量光系统Ⅱ(photosystem Ⅱ, PS Ⅱ)发出的荧光的变化来分析植物光合作用的变化[10]。测量叶绿素a荧光的方法有2种:一种是植物经过暗适应处理并用短饱和脉冲光激发后,测量快速荧光动力学曲线;另外一种是经几分钟光化光适应处理使叶绿素a荧光恢复稳态,再加饱和脉冲光测荧光产量,进一步分析稳态下的光合作用情况[11]。这2种方法使PS Ⅱ供体侧和受体侧电子传递的研究更加深入。快速叶绿素荧光诱导动力学曲线也称为OJIP曲线[12-13],它反映了PS Ⅱ受体侧电子从微秒级到秒级的电子传递状况,如PS Ⅱ的电子传递、能量捕获、能量利用率和天线复合体上的激发能依靠质子梯度的热能耗散等[14]。
为了深入研究MgO NPs及其析出的Mg2+对细叶蜈蚣草光合作用的影响,采用离子选择性微电极对MgO NPs悬浮液中析出的Mg2+浓度进行了原位实时动态检测。离子选择性微电极(ISEM)[15]是一种电化学传感器,它利用具有离子选择性的液体离子交换剂(liquid ion exchanger, LIX)将待测离子的活度转化为膜电位进行测量。与以往对上清液进行电感耦合等离子体原子发射光谱(ICP-AES)测量相比,微电极法避免了上清液中纳米粒子残留及检测的非实时性带来的问题,具有操作方便、速度快、灵敏度高和无损伤等优点,能够在MgO NPs与细叶蜈蚣草相互作用的全过程中,对悬浮液中Mg2+的浓度进行测量。
1 材料与方法(Materials and methods)
1.1 实验材料
MgO NPs和MgCl2(分析纯)购自Macklin生化科技有限公司(中国)。MgO NPs粒径<50 nm,纯度>99.9%。细叶蜈蚣草(Egerianajas)购自水族养殖场,用去离子水(UPH-1V-10T,四川优普超纯科技有限公司,中国)洗净并放置在容积10 L的玻璃水缸中,室温下培养待用。
1.2 MgO NPs悬浮液和Mg2+溶液的配制
用分析天平(XS205DU,梅特勒-托利多公司,瑞士)称取1、2、3、4、5、6、8和10 mg MgO NPs分别加入到50 mL去离子水中,超声(KQ-250DB,350 W,昆山市超声仪器有限公司,中国)分散30 min,得到浓度分别为20、40、60、80、100、120、160和200 mg·L-1的悬浊液。称取0.375 mg的MgCl2加入到150 mL去离子水中,得到150 mL浓度为2.5 mg·L-1的MgCl2溶液,将溶液按照1∶2∶3∶4∶5的比例分成5份,加离子水制成体积50 mL浓度分别为0.5、1.0、1.5、2.0和2.5 mg·L-1的Mg2+溶液。
1.3 细叶蜈蚣草培养
随机选取3根生长状况一致的细叶蜈蚣草切掉根部与顶部,中间部分均匀分成10段,每段长约2 cm。将共30段细叶蜈蚣草随机抽取,每2段为1份,共分为15份。将这15份分为2组,一组9份、另一组6份,分别处理。处理一,将一组(9份)细叶蜈蚣草分别暴露在浓度为0、20、40、60、80、100、120、160和200 mg·L-1的MgO NPs悬浮液中(0 mg·L-1为50 mL的去离子水)。处理二,另一组(6份)分别暴露在浓度为0、0.5、1.0、1.5、2.0和2.5 mg·L-1的Mg2+溶液中。室温下用植物灯(SY-ZWD-1200W,广西三熠照明电器有限公司,中国)每天光照8 h,光强约为80 μmol·(m2·s)-1,培养2 d。然后从每一烧杯中2段蜈蚣草上各取3片叶片,每2片一组,共3组,进行叶绿素a荧光检测。测试前在叶夹内暗适应15 min。
1.4 离子选择性微电极的性能
使用的离子选择性微电极是通过将硼硅酸盐玻璃管(B150-110-10,Sutter Instrument公司,美国)加热拉制而成,LIX购自北京旭月公司。Mg2+选择性微电极在标定液浓度10-1~10-5mol·L-1范围内都有良好的响应,线性回归系数为0.99984,其检测下限可达约10-5mol·L-1,检测精度为1.4%。
1.5 叶绿素a荧光检测
1.5.1 快速荧光动力学曲线测量
用叶绿素荧光仪(Yaxin-1161G,北京雅欣理仪科技有限公司,中国)在室温下测量细叶蜈蚣草快速叶绿素荧光诱导动力学曲线(OJIP曲线)。470 nm蓝光LED激发,探测波长685 nm,激发光强3 500 μmol·(m2·s)-1。20 μs、2 ms和30 ms的荧光强度分别记为O(Fo)、J(FJ)、I(FI)点,饱和光照下最大荧光强度记为P(Fm)点。
1.5.2 脉冲瞬态荧光动力学曲线测量
用饱和光与光化光脉冲交替激发叶绿素荧光。饱和脉冲宽度为1 s,光强3 500 μmol·(m2·s)-1。光化光脉冲宽度9 s,强度为100 μmol·(m2·s)-1。饱和光照射期间,记录OJIP曲线,可得到叶片的最大叶绿素荧光(Fm)。光化光照射期间,可测得稳态荧光(FS)。实际最大叶绿素荧光(F’m)在达到稳态荧光后通过照射饱和脉冲测量。
1.6 统计方法
本实验中,每组叶绿素a荧光检测均重复3次以上,数据处理采用SSPS 23.0软件进行方差分析,采用ANOVA方法对实验数据进行差异显著性分析(检验标准为P<0.05)。*表示P<0.05,**表示P<0.01。实验结果表示方式为平均值±标准差。
2 结果(Results)
2.1 MgO NPs悬浮液中析出的Mg2+浓度的变化
图1(a)为培养细叶蜈蚣草时不同浓度MgO NPs悬浮液在48 h内析出Mg2+的情况。在前4 h内不同浓度MgO NPs悬浮液中析出的Mg2+浓度基本不随时间变化。4 h之后Mg2+浓度逐渐升高,24 h后达到饱和值,范围在0.7~2.4 mg·L-1之间。当MgO NPs悬浮液浓度达到160 mg·L-1时,析出Mg2+饱和浓度达到2.4 mg·L-1且不再随MgO NPs浓度的增加而升高。图1(b)给出了未培养细叶蜈蚣草时,MgO NPs悬浮液在相同时间内析出Mg2+的情况。
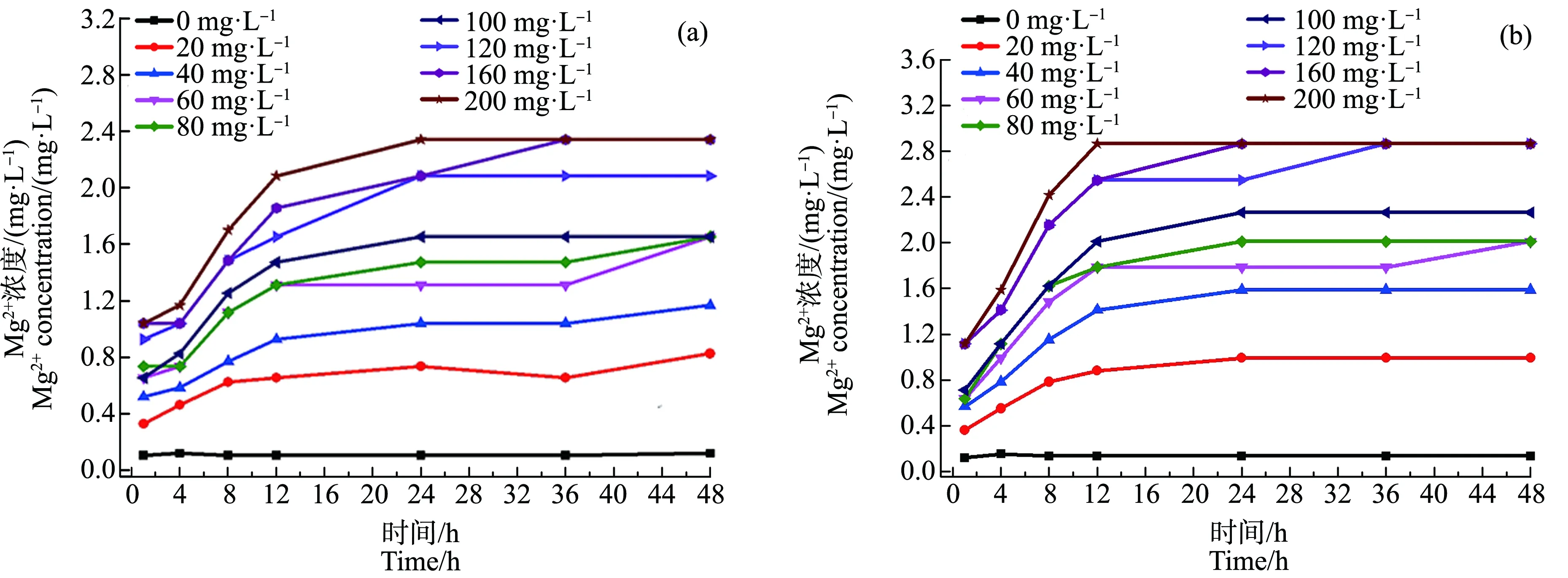
图1 培养(a)与未培养(b)细叶蜈蚣草时不同浓度MgO NPs悬浮液48 h内析出的Mg2+浓度变化Fig. 1 Changes of the concentrations of Mg2+ released in the suspensions of different concentrations of MgO NPs with (a) and without (b) Egeria najas cultivated in them within 48 h
Mg2+浓度随时间不断升高,24 h后达到饱和值,范围在0.9~2.8 mg·L-1之间。比较而言,未培养细叶蜈蚣草的悬浮液中Mg2+浓度较高。
2.2 MgCl2溶液中Mg2+浓度的变化
在初始浓度分别为0.5、1.0、1.5、2.0和2.5 mg·L-1的MgCl2溶液中培养细叶蜈蚣草时,溶液中Mg2+浓度在48 h内的变化情况如图2所示,随着时间的推移,Mg2+浓度都在不断降低。Mg2+浓度下降的速度也随时间而改变,在0~4 h内,Mg2+浓度下降较快,4 h后Mg2+浓度的变化逐渐趋缓。
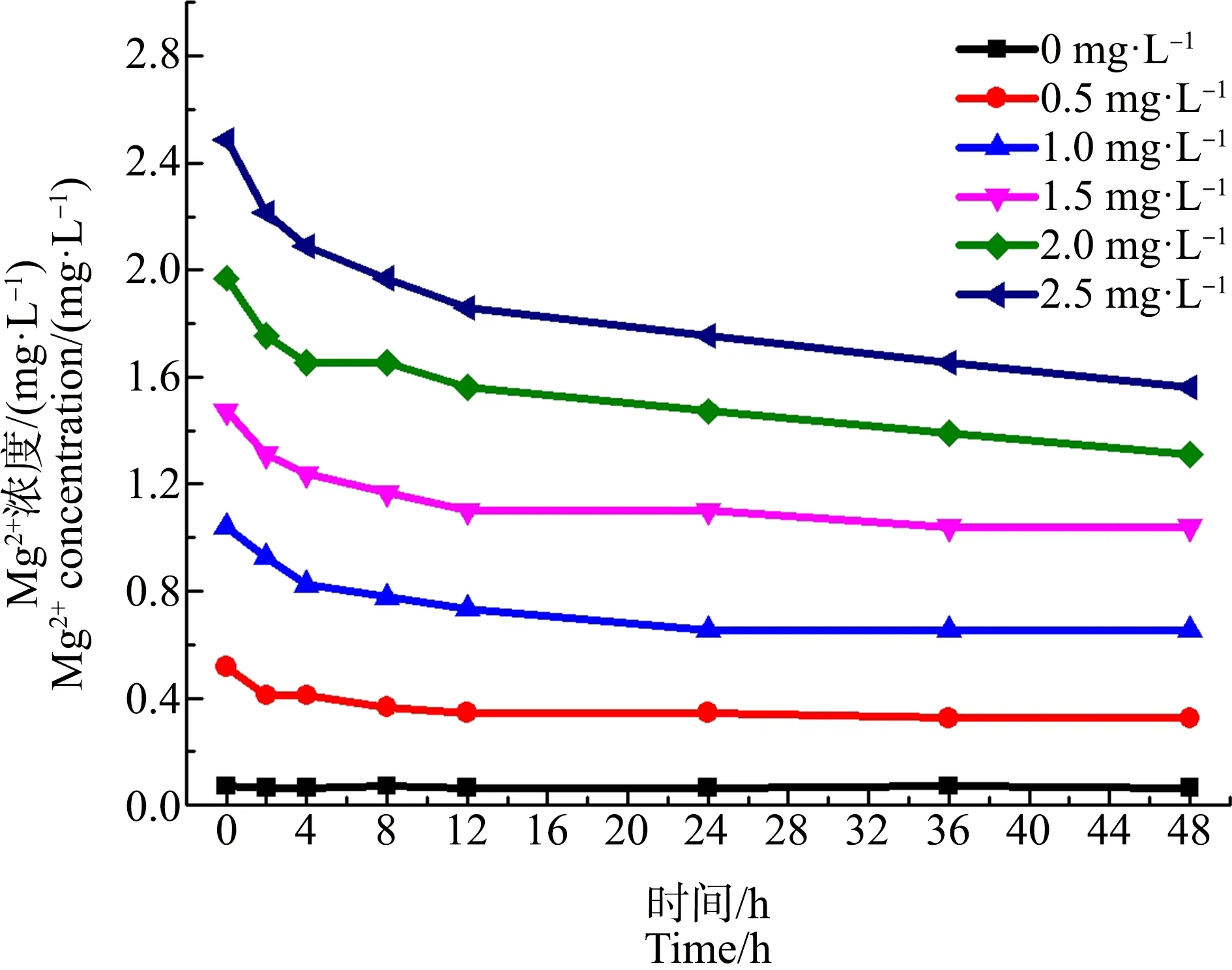
图2 培养细叶蜈蚣草时,不同浓度MgCl2溶液48 h内的Mg2+浓度的变化Fig. 2 Changes of Mg2+ concentrations in different concentrations of MgCl2 solution within 48 h when cultivating Egeria najas
2.3 MgO NPs处理后细叶蜈蚣草荧光动力学曲线参数的变化
快速叶绿素荧光诱导动力学曲线,又称OJIP曲线,其中,O、J、I和P点大致在20 μs、2 ms、30 ms和400 ms处,Fo、FJ、FI和FP分别代表O、J、I和P这4点荧光强度。图3(a)是细叶蜈蚣草经去离子水培养2 d的OJIP曲线,它反映了光合作用中PS Ⅱ电子传递状态。由图3(b)中可知,细叶蜈蚣草经MgO NPs处理2 d,初始荧光的斜率和J点相对荧光强度发生了改变。荧光强度在浓度为80 mg·L-1之前有随着浓度的增加而增大的趋势。而浓度超过80 mg·L-1时,初始荧光的斜率和J点的相对可变荧光强度随着浓度的增加有减小的趋势。
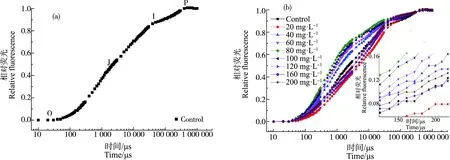
图3 经过去离子水(a)与MgO NPs(b)处理后的细叶蜈蚣草的快速叶绿素a荧光诱导动力学曲线(OJIP)注:在O和P之间将叶绿素a荧光强度做归一化处理,V=(Ft-Fo)/(Fm-Fo),(b)中插图为100~200 μs的OJIP曲线局部放大图。Fig. 3 The fast chlorophyll a fluorescence induction kinetics curve (OJIP) of Egeria najas after treatment with deionized water (a) and MgO NPs (b)Note: Normalized the fluorescence intensity of chlorophyll a between O and P, V=(Ft-Fo)/(Fm-Fo); the illustration in (b) is a partial enlargement of the OJIP curve of 100~200 μs.
通过JIP测定计算出相应的荧光参数来分析MgO NPs对PS Ⅱ的影响。由图4(a)可知,MgO NPs浓度为40~100 mg·L-1时,PS Ⅱ反应中心关闭的净速率(M0)和相对可变荧光强度(VJ)有明显上升趋势(P<0.05)。浓度分别为40、60、80和100 mg·L-1时,M0分别上升了37.4%、67.9%、69.5%和47.6%,VJ分别上升25.7%、45.3%、43.2%和32.5%。当MgO NPs浓度为120~200 mg·L-1时,M0和VJ的上升趋势并不明显。图4(b)为细叶蜈蚣草经不同浓度MgO NPs处理后能量利用率的变化。随着MgO NPs浓度的增加,捕获激子中用来推动电子传递的效率(Ψ0)、最大光化学量子效率(ΦP0)以及电子传递的量子产额(ΦE0)呈下降趋势。当MgO NPs浓度为40~100 mg·L-1时,Ψ0和ΦE0有明显的下降趋势(P<0.01)。在浓度为40、60、80和100 mg·L-1时,Ψ0分别下降了20.3%、35.7%、34.0%和25.7%,ΦE0分别下降22.2%、42.3%、44.2%和38.5%。MgO NPs浓度为60~100 mg·L-1时,ΦP0有明显下降趋势(P<0.01)。在浓度为60、80和100 mg·L-1时,ΦP0分别下降10.4%、16.1%和17.5%。当MgO NPs为120~200 mg·L-1时,ΦP0下降趋势不明显。
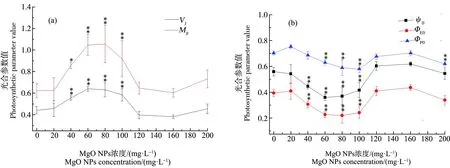
图4 经MgO NPs处理后,细叶蜈蚣草PS Ⅱ关闭的净速率和J点的叶绿素a相对可变荧光强度的变化(a)与PS Ⅱ能量利用率的变化(b)注:VJ为相对可变荧光强度,M0为PS Ⅱ反应中心关闭的净速率,Ψ0为电子传递的效率,ΦE0为电子传递的量子产额,ΦP0为最大光化学量子效率。Fig. 4 The net rate of PS Ⅱ closure and the relative variable fluorescence intensity of chlorophyll a at point J (a) and PS Ⅱ energy utilization (b) in Egeria najas after treatment with MgO NPsNote: VJ is the relative variable fluorescence; M0 is the net rate of the closure of the reaction center of PS Ⅱ; Ψ0 is efficiency of electron transport; ΦE0 is quantum yield of electron transport; ΦP0 is the maximum quantum yield of photochemistry.
图5(a)为经不同浓度MgO NPs悬浮液处理后,细叶蜈蚣草PS Ⅱ的能量流的变化。从图中可看出,单位反应中心吸收的光能(ABS/RC)、捕获的光能(TR0/RC)、用于电子传递的能量(ET0/RC)和用于热耗散的能量(DI0/RC)均有不同程度的变化。MgO NPs浓度为60~100 mg·L-1时,ABS/RC、TR0/RC和DI0/RC随着MgO NPs浓度增加而明显升高(P<0.05),ET0/RC明显降低(P<0.05)。MgO NPs浓度为80 mg·L-1时变化最为明显,ABS/RC升高了42.1%,TR0/RC升高17.9%,DI0/RC升高99.5%,ET0/RC降低22.8%。MgO NPs浓度为120~200 mg·L-1时,各参数呈降低趋势,在200 mg·L-1时,降低趋势不明显。图5(b)为细叶蜈蚣草PS Ⅱ吸收能量耗散过程的变化。随着MgO NPs浓度增加,PS Ⅱ实际光量子效率(ΦPS Ⅱ)呈下降趋势,非调节性能量耗散(ΦNO)和调节性能量耗散(ΦNPQ)呈升高趋势。当MgO NPs浓度为40~200 mg·L-1时,ΦPS Ⅱ下降趋势明显(P<0.05),浓度为120 mg·L-1和160 mg·L-1时,下降趋势减弱。当MgO NPs浓度为60~120 mg·L-1时,ΦNO升高趋势非常明显(P<0.01)。浓度为120 mg·L-1和160 mg·L-1时,升高趋势减弱。当MgO NPs浓度为40~80 mg·L-1时,ΦNPQ升高趋势明显(P<0.05),而当浓度再升高时,ΦNPQ升高趋势并不明显。

图5 经MgO NPs处理后,细叶蜈蚣草PS Ⅱ能量流的变化(a)和PS Ⅱ吸收能量的耗散过程的变化(b)注:ABS/RC为单位反应中心吸收的光能Fig. 5 Changes in the energy flow of PS Ⅱ (a) and changes in the dissipation process of PS Ⅱ absorbed energy (b) in Egeria najas after treatment with MgO NPsNote: ABS/RC is the absorption flux per reaction center (RC).
2.4 Mg2+处理下细叶蜈蚣草荧光动力学曲线参数的变化
经过不同浓度Mg2+溶液处理后,细叶蜈蚣草各个光合作用参数变化如图6所示。图6(a)中M0和VJ呈下降的趋势,当Mg2+浓度为1 mg·L-1和2.5 mg·L-1时下降明显(P<0.05)。由图6(b)可知,捕获的激子中Ψ0、ΦP0以及ΦE0呈上升趋势,在Mg2+浓度为1 mg·L-1和2.5 mg·L-1时上升明显(P<0.05)。由图6(c)和图6(d)可知,ABS/RC、TR0/RC、ET0/RC、DI0/RC以及ΦPS Ⅱ、ΦNO、ΦNPQ各个参数均基本不变。

图6 经不同浓度的Mg2+溶液处理后,细叶蜈蚣草各个光合作用参数变化Fig. 6 Changes in photosynthesis parameters of Egeria najas after treatment with different concentrations of Mg2+ solution
3 讨论(Discussion)
根据测得的JIP参数进行分析,发现经不同浓度的MgO NPs处理后,细叶蜈蚣草PS Ⅱ受体侧的电子传递发生了不同的变化。M0为PS Ⅱ反应中心关闭的净速率,VJ反映了经光照2 s活性反应中心关闭的程度。由图4(a)可知,细叶蜈蚣草经过低浓度MgO NPs处理后,PS Ⅱ受体侧的电子传递和PS Ⅱ反应中心之间的连通性受到抑制。ΦP0表示细叶蜈蚣草经暗适应后PS Ⅱ的最大光化学量子效率,由图4(b)可知,Ψ0和ΦE0都有所下降,说明MgO NPs抑制了PS Ⅱ对吸收光能的利用。由图5(a)中可知,经MgO NPs处理后,ABS/RC和DI0/RC都有明显升高的趋势。由于TR0/RC没有ABS/RC和DI0/RC升高明显,且ET0/RC降低,因此,细叶蜈蚣草叶绿素含量降低,说明MgO NPs抑制了叶绿素合成。这一点与吴明珠等[16]的结果相一致,在他们的报道中,100 mg·L-1的MgO NPs悬液,几乎完全抑制了叶绿素的合成。由图5(b)可知,ΦPS Ⅱ随着MgO NPs浓度增加而降低,说明MgO NPs抑制了PS Ⅱ反应中心吸收的光能用于光合电子传递的效率。ΦNPQ和ΦNO有不同程度升高,反映了调节性能量耗散这种保护机制不能抵抗MgO NPs的毒性,PS Ⅱ反应中心受到了损伤。以上结果说明,MgO NPs从多个方面对细叶蜈蚣草光合作用产生了抑制。但当MgO NPs处于高浓度时,大多数荧光参数没有发生明显变化。这可能是由于MgO NPs在高浓度时发生团聚,减低了对细叶蜈蚣草的毒性[17]。
由图6可知,用不同浓度的MgCl2溶液处理的细叶蜈蚣草M0和VJ有下降的趋势,说明Mg2+促进了PS Ⅱ反应中心之间的连通性。Ψ0、ΦP0和ΦE0呈上升趋势,说明Mg2+对光能利用率也有促进作用。这种促进作用并不难理解,一方面Mg2+是叶绿素的中心离子,对维持叶绿体的结构和功能起着重要作用,是光合作用中不可或缺的重要元素;另一方面Portis和Heldt[18]曾报道Mg2+能够从类囊体腔进入基质从而起到优化光合酶活性的作用。
金属氧化物纳米粒子自身与其所释放的金属离子各自毒性的大小,一直存在着分歧[19-21]。吴明珠等[16]在研究MgO NPs对斜生栅藻(Scenedesmusobliquus)的毒性效应及致毒机理时,对培养至对数期的(3 d)的藻液取样离心后,发现当MgO NPs的浓度为100 mg·L-1时,上清液中的Mg2+浓度为2.14 mg·L-1,与本文在培养细叶蜈蚣草的MgO NPs悬液中测得的数值1.65 mg·L-1大体相当。由于该文中没有给出未培养藻类的MgO NPs悬液中的Mg2+浓度及培养过程中藻液中Mg2+浓度变化的相关结果,因此,无法判断斜生栅藻(Scenedesmusobliquus)对Mg2+的吸收情况。由本文的结果可知,100 mg·L-1的MgO NPs悬液配制完成后,如不加入细叶蜈蚣草,其Mg2+的浓度的饱和值为2.26 mg·L-1。当加入细叶蜈蚣草时,Mg2+的饱和浓度有所减小,为1.65 mg·L-1。MgCl2溶液在培养细叶蜈蚣草的过程中,其Mg2+的浓度也会逐渐下降。Mg2+浓度的下降可能来自于细叶蜈蚣草自身的吸收,也可能来自于Mg2+在细叶蜈蚣草表面的直接吸附或通过吸附于纳米颗粒而间接地在细叶蜈蚣草表面聚集[22]。但如果只有单纯的表面吸附或聚集,则很难解释MgCl2溶液中细叶蜈蚣草光合作用的增强,因此,可以认为细叶蜈蚣草对Mg2+有吸收。
由于初始浓度为0.5、1.0、1.5、2.0和2.5 mg·L-1的MgCl2溶液对细叶蜈蚣草的光合作用均起促进作用,因此,尽管MgO NPs悬液中确有Mg2+析出,但其对细叶蜈蚣草光合作用的毒性并非来自Mg2+,而应与MgO NPs自身特殊的物理化学性质有关。
如果把未培养和培养有细叶蜈蚣草的MgO NPs悬液(或MgCl2溶液)中Mg2+浓度的饱和值之差视为细叶蜈蚣草对Mg2+的表观吸收量,可以发现,当MgO NPs的浓度为80 mg·L-1时,其饱和Mg2+浓度为2.01 mg·L-1,表观吸收量约为0.36 mg·L-1;而对于初始浓度为2.0 mg·L-1的MgCl2溶液,其表观吸收量则为0.69 mg·L-1,高出47.8%。这表明,MgO NPs抑制了细叶蜈蚣草对Mg2+的吸收。这种抑制作用可能来自2个方面,一是MgO NPs的存在降低了细叶蜈蚣草自身对Mg2+的吸收能力。二是在高浓度下,纳米粒子在细叶蜈蚣草表面沉积形成阻挡层,阻碍了细叶蜈蚣草表对Mg2+的吸收。由于MgO NPs悬液在作用于细叶蜈蚣草之前其游离Mg2+浓度已经达到稳定值,故MgO NPs对Mg2+的吸附应该已经达到饱和,其对表观吸收量的影响略去不计。Perreault等[20]曾报道CuO NPs对膨胀浮萍(LemnagibbaL.)的毒性主要源于其颗粒释放的Cu2+。CuO NPs与MgO NPs致毒机理不同的原因可能和Mg2+在叶绿素中处于弱结合点位有关[23],过量的Cu2+会代替Mg2+点位导致植物缺镁。
综上所述,经MgO NPs处理后,细叶蜈蚣草的M0和VJ上升,表明MgO NPs减弱了PS Ⅱ反应中心之间的连通性并抑制了PS Ⅱ受体侧的电子传递;ABS/RC和TR0/RC升高以及ΦNPQ和ΦNO降低,说明部分PS Ⅱ反应中心失活;DI0/RC的升高以及ET0/RC、ΦPS Ⅱ、Ψ0、ΦE0和ΦP0的降低则表明MgO NPs抑制了PS Ⅱ对吸收光能的利用。而经MgCl2溶液处理后,细叶蜈蚣草的M0和VJ降低、Ψ0、ΦE0和ΦP0升高,表明Mg2+促进反应中心之间的连通性及对吸收光能的利用,即Mg2+促进了细叶蜈蚣草光合作用。尽管MgO NPs悬浮液的确会释放出Mg2+,但其对细叶蜈蚣草光合作用的毒性来源于MgO NPs本身而非其析出的Mg2+。实验中还发现,MgO NPs悬浮液中析出的Mg2+浓度并非常数,随时间推移Mg2+浓度不断增高并在大约24 h后达到饱和值。加入细叶蜈蚣草后,饱和值的数值有所下降。MgCl2溶液中加入细叶蜈蚣草后,其中的Mg2+浓度也会下降。这一发现弥补了常用的对离心后的上清液进行测量的不足,同时也说明细叶蜈蚣草会吸收MgO NPs悬浮液和MgCl2溶液中的Mg2+。但比较2种情况下的表观吸收量会发现,MgO NPs抑制了细叶蜈蚣草对Mg2+的吸收能力。

